PÉPTIDOS MODULADORES DE PGC-1Alfa.
Péptidos de fórmula general (I):
****IMAGEN****
sus estereoisómeros,
mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, un procedimiento de preparación, composiciones cosméticas o farmacéuticas que los contienen y su uso para el tratamiento y/o cuidado de condiciones, desórdenes y/o enfermedades que mejoran o son prevenidos por la modulación de PGC-1α.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201130439.
Solicitante: LIPOTEC, S.A..
Nacionalidad solicitante: España.
Inventor/es: GARCIA ANTON,JOSE MARIA, CEBRIAN PUCHE,JUAN, FERRER MONTIEL,ANTONIO VICENTE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/04 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen hasta 20 aminoácidos en una secuencia totalmente determinada; Sus derivados (gastrinas A61K 38/16, somatostatinas A61K 38/31, melanotropinas A61K 38/34).
- C07K7/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 5 a 11 aminoácidos.
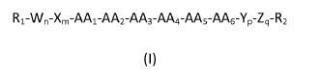
Fragmento de la descripción:
PÉPTIDOS MODULADORES DE PGC-la CAMPO DE LA INVENCiÓN
La presente invención se refiere a péptidos capaces de modular PGC-1a y a composiciones cosméticas o farmacéuticas que contienen dichos péptidos de utilidad en el tratamiento y/o cuidado de aquellas condiciones, desórdenes y/o enfermedades que mejoran o son prevenidos por la modulación de PGC-1a.
ANTECEDENTES DE LA INVENCiÓN
El tejido adiposo o tejido graso es un tejido conjuntivo de origen mesenquimal conformado por la asociación de células que acumulan lípidos en su citoplasma: los adipocitos. El tejido adiposo de los mamíferos se puede clasificar en dos tipos: tejido adiposo blanco y tejido adiposo marrón o pardo. El tejido adiposo blanco es el predominante, está formado por adipocitos monoloculares que acumulan todo su contenido lipídico en una sola gota, y tiene como función principal la acumulación de reservas energéticas en forma de triglicéridos. El tejido adiposo marrón, por su parte, está formado por adipocitos multiloculares, es menos frecuente, y suele desaparecer poco tiempo después del nacimiento, siendo especialmente relevante en mamíferos hibernadores. En humanos, el feto y el recién nacido presentan tejido adiposo marrón en los depósitos cervical, axilar, perirrenal y periadrenal; en adultos, en cambio, no hay depósitos de grasa marrón pero existen poblaciones de adipocitos multiloculares intercaladas entre tejido adiposo blanco. El tejido adiposo marrón es altamente termogénico, posee gran número de mitocondrias en su citoplasma y elevados niveles de expresión de genes mitocondriales, y su función consiste en la disipación de energía en forma de calor.
Una de las particularidades del tejido adiposo es su plasticidad. Esta plasticidad es sobre todo consecuencia de la capacidad del tejido adiposo de variar su volumen bien sea por variación de la cantidad de los lípidos intracelulares (aumento de tamaño de los adipocitos) o bien por variación del número de adipocitos. Los adipocitos maduros acumulan grasa como fuente de energía (i.e. exceso de ingesta de calorías) y son capaces de liberarla en caso de requerimiento de energía (i.e. periodos de ayuno, exposición a frío, etc.) . El número de adipocitos maduros se mantiene más o menos constante desde la etapa adulta. Sin embargo, las células precursoras de los adipocitos o
preadipocitos, constantemente se multiplican y se diferencian en adipocitos maduros capaces de acumular grasa. Este mecanismo se denomina diferenciación o adipogénesis.
La adipogénesis se caracteriza principalmente por una modificación morfológica de las células precursoras, un cambio fenotípico y la aparición de los marcadores específicos de los adipocitos. En el momento de entrar en la diferenciación, la mayoría de los genes se activan, entre ellos PPARy (receptor activado por el proliferador de peroxisomas-y) . PPARy, un miembro de la familia de receptores nucleares PPAR que se expresa en tejido adiposo, es un regulador maestro de la diferenciación de adipocitos [Tontonoz P. et 01., "Regulotion of odipocyte gene expression ond differentiotion by peroxisome proliferator octivoted receptor gommo", (1995) , Curro Opino Genet. Dev., 5 (5) , 571-576]. Estos receptores actúan como factores de transcripción y regulan la expresión génica en los procesos de diferenciación celular. PPARy es esencial en el tejido adiposo y forma heterodímeros con los receptores retinoides X que se unen a regiones específicas en el DNA de los genes diana y regulan su expresión. Los genes activados por PPARy estimulan la captación de lípidos por las células grasas e inducen fuertemente la diferenciación del tejido adiposo blanco. Los ratones transgénicos sin el gen de PPARy (PPARy knockout) son incapaces de producir tejido adiposo cuando son alimentados con una dieta alta en grasas [Jones J.R. et 01., "Deletion of PPARgommo in odipose tissues of mice protects ogoinst high fot diet-induced obesity ond insulin resistonce'~ (2005) , Proc. Not!. Acod. Sci. U.S.A., 102 (17) , 6207-6212].
PPARy tiene función en la diferenciación de preadipocitos a adipocitos maduros a nivel transcripcional, ya que se ha visto que la activación de PPARy por unión de ligando da lugar a la acumulación de lípidos, cambios morfológicos y promueve la expresión de genes específicos de tejido adiposo [Tontonoz P. et 01., "Stimulotion of odipogenesis in fibroblosts by PPARV2, o lipidoctivoted transcription foctor", (1994) , Cel/, 79, 7355-7359]. Adicionalmente, hay datos que demuestran que la estimulación de la adipogénesis debida a la activación de PPARy por unión de ligando sucede también in vivo [Okuno A. et 01., 'Troglitozone increoses the number of smoll odipocytes without the chonge of white odipose tissue moss in obese Zucker rats", (1998) , J. Clin. Invest., 101, 1354-1361]. La implicación de PPARy en adipogénesis también queda refrendada por el hecho que pacientes con una mutación en PPARy que hace que este receptor esté constantemente activado presentan mayor diferenciación adipocitaria y obesidad [Ristow M. et 01., "Obesity ossocioted with o mutotion in o genetic regulotor of odipocyte differentiotion", (1998) , N. Engl. J. Med., 339, 953-959]. El mecanismo por el que PPARy estimula la adipogénesis parece estar relacionado con su efecto mediador del arresto del ciclo celular [Closson M. et 01., "Opposing roles of pRB ond p107 in odipocyte differentiotion", (2000) , P.N.A.S., 97, 10826-108311, ya que, en general se considera que división celular y diferenciación celular son procesos mutuamente excluyentes.El sector farmacéutico ha realizado grandes esfuerzos encaminados a desarrollar nuevos compuestos moduladores de PPARy con el objetivo de frenar el avance de la obesidad y la diabetes de tipo 2 en la población de los países desarrollados. También se han descrito agonistas de PPARy para el tratamiento y/o prevención de desórdenes o enfermedades de la piel tales como transtornos debidos a hiperproliferación de queratinocitos como por ejemplo psoriasis, liquen plano, lesiones de la piel asociadas a lupus, dermatitis tales como la ató pica, seborreica o solar, queratosis tales como la seborreica, senil, actínica, fotoinducida o folicular, acné vulgar, nevi, queloides o arrugas entre otros [WO 95/535108 Al; EP 1041977 B1; WO 2009/153373 A2; Krentz A.l. et al., NType 2 diabetes, psoriasis and thiazolidinediones", (2006) , Int. J. elin. Proct., 60, 362-3631, transtornos de la queratinización como por ejemplo acné común, comedones, polimorfos, rosácea, acné noduloquístico, acné conglobata, acné senil, ictiosis, enfermedad de Darier, queratodermia palmatoplantar, leucoplaquia, liquen mucoso o liquen cutáneo; condiciones con un componente inflamatorio como psoriasis cutánea, mucosa o ungueal, reumatismo psoriático, atopia cutánea incluyendo eczema; proliferaciones dérmicas como verrugas comunes, verrugas planas, epidermodisplasia verruciforme, papilomatosis orales; dermatosis inmunes como lupus eritematoso, enfermedades bullosas, esclerodermia, envejecimiento de la piel, queratosis actínicas, y transtornos de pigmentación [EP 1781297 B11, alopecia areata o vitiligo [EP 1331934 Bl], desórdenes del metabolismo lipídico cutáneo como por ejemplo hiperseborrea del acné y seborrea simple [EP 1781297 Bl], regulación de la función de los fibroblastos o miofibroblastos, exceso de producción de matriz extracelular, procesos de cicatrización o reepitelización, fascitis modular o contractura de Dupuytren rUS 2004/0152746 Al; US 2008/0182780 Al] entre otros.
Los receptores PPAR son factores de transcripción que regulan la expresión de genes específicos de tejido adiposo, pero existe otro nivel de regulación formado por un conjunto de proteínas que modulan estos factores de transcripción: los coactivadores transcripcionales. Un coactivador de la transcripción es un complejo proteico que aumenta la tasa de transcripción de su diana mediante interacciones con factores de transcripción pero no reconoce ni se une a secuencias específicas de DNA. Estos complejos constan de proteínas que median el anclaje en los factores de transcripción y de proteínas que ejercen funciones específicas, tales como la modificación de histonas por actividad acetiltransferasa, por fosforilación y por metilación, el desenrollado y remodelado dependientes de ATP de la cromatina, y otras. Los coactivadores son reclutados a los genes diana mediante interacciones proteína-proteína con factores de transcripción que se unen a DNA. Éstos modifican la
estructura de la cromatina del gen diana por asociación a la maquinaria RNA polimerasa, dando lugara un incremento de la transcripción de los genes diana. Las interacciones entre coactivadores V factores de unión a DNA son específicas,...
Reivindicaciones:
1. Un péptido de fórmula general (1)
sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, caracterizado porque: AA, se selecciona del grupo formado por -His-y -Ser-; AA, se selecciona del grupo formado por -lIe-y -Val-; AA3 se selecciona del grupo formado por -Tyr-y -Va 1-; AA4 es -Val-; AAs se selecciona del grupo formado por -Ala-, -Arg-y -Gly-; AA6 se selecciona del grupo formado por -Thr-y -Va 1-; w, X, Y Y Z son aminoácidos y se seleccionan independientemente entre sí; n, m, p y q se seleccionan independientemente entre sí y tienen un valor de Oó 1;
n+m+p+q es menor o igual a 2 R, se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido y Rs-CO-, donde Rs se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido, heterociclilo sustituido o no sustituido y heteroarilalquilo sustituido o no sustituido;
R, se selecciona del grupo formado por -NR3R4, -OR3 Y -SR3, donde R3 y R4 se seleccionan independientemente del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido, y aralquilo sustituido o no sustituido; y con la condición de que R, y R, no son a-aminoácidos.
2. Péptido según la reivindicación 1, caracterizado porque R, se selecciona del grupo formado H
o Rs-eO-, donde Rs se selecciona del grupo formado por radical alquilo e, -e'4 sustituido o no sustituido, alquenilo e, -e'4 sustituido o no sustituido, alquinilo e, -e'4 sustituido o no sustituido, cicloalquilo er e'4 sustituido o no sustituido, cicloalquenilo eS-e'4 sustituido o no sustituido, cicloalquinilo eS-e'4 sustituido o no sustituido, arilo e6-e30 sustituido o no sustituido, aralquilo er e'4 sustituido o no sustituido, heterociclilo de 3-10 miembros de anillo sustituido o no sustituido, y heteroarilalquilo sustituido o no sustituido de 2 a 24 átomos de carbono y de 1 a 3 átomos diferentes al carbono y una cadena alquílica de 1 a 6 átomos de carbono.
3. Péptido según la reivindicación 2, caracterizado porque R, se selecciona del grupo formado por H, acetilo, terc-butanoilo, hexanoilo, 2-metilhexanoilo, ciclohexancarboxilo, octanoilo, decanoilo, lauroilo, miristoilo, palmitoilo, estearoilo, oleoilo y linoleoilo.
4. Péptido según cualquiera de las reivindicaciones anteriores, caracterizado porque R, es -NR3R4 o -OR3, donde R3 y R4 se seleccionan independientemente del grupo formado por H, alquilo e, -e'4 sustituido o no sustituido, alquenilo e, -e'4 sustituido o no sustituido, alquinilo e, -e'4 sustituido o no sustituido, cicloalquilo er e'4 sustituido o no sustituido, cicloalquenilo eS-e'4 sustituido o no sustituido, cicloalquinilo eS-e'4 sustituido o no sustituido, arilo e6-e30 sustituido o no sustituido, aralquilo er e'4 sustituido o no sustituido, heterociclilo de 3-10 miembros de anillo sustituido o no sustituido, y heteroarilalquilo sustituido o no sustituido de 2 a 24 átomos de carbono y de 1 a 3 átomos diferentes al carbono donde la cadena alquílica es de 1 a 6 átomos de carbono.
5. Péptido según la reivindicación 4, caracterizado porque R3 y R. se seleccionan independientemente del grupo formado por H, metilo, etilo, hexilo, dodecilo y hexadecilo.
6. Péptido según cualquiera de las reivindicaciones anteriores, caracterizado porque R, se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo o palmitoilo, AA, es -l-Ser-, AA, es -L-lIe -, AA3 es -L-Tyr-, AA4 es -l-Val-, AAs es -l-Ala -, AA6 es -L-Thr-y R, es -NR3R. o -OR3 donde R3 y R4 se seleccionan independientemente de H, metilo, etilo, hexilo, dodecilo y hexadecilo.
7. Péptido según cualquiera de las reivindicaciones 1 a 5, caracterizado porque R, se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo o palmitoilo, AA, es -l-Ser-, AA, es
- l-Val-, AA3 es -L-Tyr-, AA, ¡ es -l-Val-, AAs es -l-Ala -, AA6 es -L-Thr-y R, es -NR3R" o -OR3
donde R3 y R4 se seleccionan independientemente de H, metilo, etilo, hexilo, dodecilo y
hexadecilo.
8. Péptido según cualquiera de las reivindicaciones 1 a 5, caracterizado porque R, se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo o palmitoilo, AA, es -l-Ser-, AA, es -L-lIe-, AA3 es -l-Val-, AA, ¡ es -l-Val-, AAs es -L-Gly -, AA6 es -L-Thr-y R, es -NR3R" o -OR3donde R3 y R" se seleccionan independientemente de H, metilo, etilo, hexilo, dodecilo y hexadecilo.
9. Péptido según cualquiera de las reivindicaciones 1 a 5, caracterizado porque R, se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo o palmitoilo, AA, es -l-Ser-, AA, es -l-Val-, AA3 es -l-Val-, AA4 es -l-Val-, AAs es -L-Arg -, AA6 es -L-Thr-y R, es -NR3R4 o -OR3 donde R3 y R4 se seleccionan independientemente de H, metilo, etilo, hexilo, dodecilo y hexadecilo.
10. Péptido según cualquiera de las reivindicaciones 1 a 5, caracterizado porque R, se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo o palmitoilo, AA, es -L-His-, AA, es -L-lIe-, AA3 es -l-Val-, AA4 es -l-Val-, AAs es -L-Gly -, AA6 es -L-Thr-y R, es -NR3R4 o -OR3donde R3 y R4 se seleccionan independientemente de H, metilo, etilo, hexilo, dodecilo y hexadecilo.
11. Péptido según cualquiera de las reivindicaciones anteriores, caracterizado porque R, se selecciona del grupo formado por H, acetilo y palmitoilo y R, se selecciona del grupo formado por -OH y -N H, .
12. Péptido según la reivindicación 1, caracterizado porque n, m, p y s son O.
13. Péptido según cualquiera de las reivindicaciones anteriores para su uso en la modulación de PGC-la.
14. Péptido según la reivindicación 13 para su uso en la modulación de PPARy.
15. Péptido según cualquiera de las reivindicaciones 1 a 12 para su uso en el tratamiento y/o cuidado de las condiciones, desórdenes o enfermedades seleccionadas del grupo formado por enfermedades y/o desórdenes metabólicos, enfermedades relacionadas con el metabolismo lipídico, alteraciones en la gluconeogénesis, obesidad, diabetes tipo2, celulitis, ginecomastia, pseudoginecomastia, lipoatrofia, lipoatrofia semicircular, lipodistrofia, envejecimiento, fotoenvejecimiento, traumas cutáneos, reepitelización de heridas, deshidratación de la piel, xerosis, transtornos de la queratinización, callos, durezas, psoriasis,
liquen plano, lesiones de la piel por lupus, dermatitis, dermatitits atópica, dermatitis seborreica, dermatitis senil, caspa, costra láctea del bebé, seborrea, hiperseborrea del acné, dermatitis solar, queratosis seborreica, queratosis senil, queratosis actínica, queratosis fotoinducida, queratosis folicular, acné vulgar, nevi, queloides, alteración de la función de los fibroblastos, fascitis nodular, escleroderma, contractura de Dupuytren, formación de cicatrices fibrosas, transtornos de las glándulas sebáceas, acné rosa cea, acné polimorfo, comedones, polimorfos, rosácea, acné noduloquístico, acné conglobata, acné senil, ictiosis, enfermedad de Darier, queratodermia palmatoplantar, leucoplaquia, liquen mucoso, liquen cutáneo, psoriasis cutánea, psoriasis mucosa, psoriasis ungueal, reumatismo psoriático, eczema, verrugas comunes, verrugas planas, epidermodisplasia verruciforme, papilomatosis orales, lupus eritematoso, enfermedades bullosas, pémfigo bulloso, esclerodermia, queratosis actínicas, trastornos de la pigmentación, vitiligo, alopecia areata, enfermedad de Alzheimer, enfermedad de Parkinson, enfermedad de Huntington, enfermedad de Pick, enfermedad Kuf, enfermedad con cuerpos de Lewy, ovillos neurofibrilares, fibras de Rosenthal, hialina de Mallor y , demencia senil, miastenia gravis, síndrome de Gilles de la Tourette, esclerosis múltiple, esclerosis lateral amiotrófica, parálisis supra nuclear progresiva, epilepsia, enfermedad de Creutzfeldt-Jakob, síndrome sordera-distonía, síndrome de Leigh, neuropatía óptica hereditaria de Leber, parkinsonismo, distonía, enfermedad de la neurona motora, síndrome de neuropatía, ataxia y retinitis pigmentosa, síndrome de Leigh heredado por vía materna, ataxia de Friedreich, paraplejía espástica hereditaria, síndrome de MohrTranebjaerg, enfermedad de Wilson, enfermedad de Alzheimer esporádica, esclerosis lateral amiotrófica esporádica, enfermedad de Parkinson esporádica, alteraciones de la función autonómica, hipertensión, trastornos del sueño, trastornos neuropsiquiátricos, depresión, esquizofrenia, trastorno esquizoafectivo, psicosis de Korsakoff, manía, trastornos de ansiedad, trastorno fóbico, trastornos del aprendizaje o memoria, amnesia o pérdida de la memoria relacionada con la edad, trastorno por déficit de atención, trastorno distímico, trastorno depresivo mayor, trastorno obsesivo-compulsivo, trastornos por consumo de sustancias psicoactivas, trastorno de pánico, trastorno afectivo bipolar, migrañas, trastornos de hiperactividad y trastornos del movimiento.
16. Péptido de fórmula general (1) , sus este reo isómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 12, para su uso en el tratamiento y/o cuidado de la piel.
17. Péptido de fórmula general (1) , sus estero isómeros, mezclas de los mismos y/o sus sales
cosmética o farmacéuticamente aceptables según cualquiera de las reivindicaciones 13, 14 ó
16, que incrementa o reduce el volumen del tejido adiposo.
18. Péptido de fórmula general (1) , sus estero isómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables según cualquiera de las reivindicaciones 13, 14, ó 16, que incrementa o reduce el contenido de triglicéridos del tejido adiposo.
19. Péptido de fórmula general (1) , sus estero isómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables según cualquiera de las reivindicaciones 17 ó 18, donde el tejido adiposo es el tejido adiposo subcutáneo.
20. Péptido según la reivindicación 19 donde el tejido adiposo subcutáneo es el tejido adiposo subcutáneo de los muslos, senos, parte baja del cuello, escote, nalgas, cara, labios, mejillas, párpados y/o manos.
21. Péptido de fórmula general (1) , sus estero isómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables según cualquiera de las reivindicaciones 13 a 20 que reduce, previene o retrasa la aparición de la celulitis.
22. Péptido de fórmula general (1) , sus este reo isómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables según la reivindicación 16 donde el tratamiento y/o cuidado disminuye, retrasa, y/o previene los signos del envejecimiento y/o del fotoenvejecimiento.
23. Péptido de fórmula (1) , sus esteroisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables según la reivindicación 13 que aumenta la temperatura de la piel.
24. Péptido según cualquiera de las reivindicaciones 13 a 23 en el que el uso se realiza mediante aplicación tópica, transdérmica, oral o parenteral de dicho péptido.
25. Péptido según la reivindicación 24 en el que la aplicación tópica o transdérmica se realiza mediante iontoforesis, sonoforesis, electroporación, presión mecánica, gradiente de presión osmótica, cura oclusiva, microinyecciones, mediante inyecciones sin agujas mediante presión, mediante parches microeléctricos, mascarillas faciales o cualquier combinación de ellas.
26. Procedimiento de preparación de un péptido de fórmula general (1) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéutica mente aceptables según
cualquiera de las reivindicaciones 1 a 12, caracterizado porque se realiza en fase sólida o en solución.
27. Procedimiento según la reivindicación 26, caracterizado porque los grupos protectores de los grupos amino libre se seleccionan del grupo formado por Boc, Fmoc, Trt, Troc, Teoc, Alloc, Mtt, Z, CIZ, Dnp, Dde, ivDde y Adpoc, los grupos protectores de los grupos carboxilo libre se seleccionan del grupo formado por ésteres de tBu, Bzl, Chx, AII, Dmab, 2-fenilisopropilo, Fm y Trt, la cadena lateral de arginina se protege con el grupo 2, 2, 4, 6, 7 -penta metildihidrobenzofuran-5-sulfonilo (Pbf) o 2, 2, 5, 7, 8-penta metilcroma n-6sulfonilo (Pmc) , la cadena lateral de histidina se protege con el grupo Trt y las cadenas laterales de treonina y serina se protegen con un grupo tBu.
28. Composición cosmética o farmacéutica que comprende una cantidad cosmética o farmacéuticamente eficaz de al menos un péptido de fórmula general (1) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 12, y al menos un excipiente o adyuvante cosmética o farmacéutica mente aceptable.
29. Composición según la reivindicación 28, caracterizada porque el péptido de fórmula general
(1) se encuentra a una concentración comprendida entre el 0, 000001% y el 20% en peso, con respecto al peso total de la composición.
30. Composición según la reivindicación 29, caracterizada porque el péptido de fórmula general
(1) se encuentra a una concentración comprendida entre el 0, 0001% y el 5% en peso, con respecto al peso total de la composición.
31. Composición según cualquiera de las reivindicaciones 28 a 30, caracterizada porque el péptido de fórmula general (1) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado a un sistema de vehiculización o a un sistema de liberación sostenida cosmética o farmacéuticamente aceptable seleccionado del grupo formado por liposomas, liposomas mixtos, oleosomas, niosomas, etosomas, milicápsulas, microcápsulas, nanocápsulas, soportes lipídicos nanoestructurados, esponjas, ciclodextrinas, vesículas, micelas, micelas mixtas de tensioactivos, micelas mixtas fosfolípido-tensioactivo, miliesferas, microesferas, nanoesferas, lipoesferas, microemulsiones, nanoemulsiones, minipartículas, milipartículas, micropartículas, nanopartículas y nanopartículas sólidas lipídicas.
32. Composición según la reivindicación 31, caracterizada porque las nanocápsulas son nanocápsulas conteniendo microemulsiones.
33. Composición según cualquiera de las reivindicaciones 28 a 32, caracterizada porque el péptido de fórmula general (1) , sus estereoisómeros, mezclas de los mismos V/o sus sales cosmética o farmacéutica mente aceptables, se encuentra adsorbido sobre un polímero orgánico sólido o soporte mineral sólido cosmética o farmacéuticamente aceptable seleccionado del grupo formado por talco, bentonita, sílice, almidón V maltodextrina.
34. Composición según cualquiera de las reivindicaciones 28 a 32, caracterizada porque se presenta en una formulación seleccionada del grupo formado por cremas, emulsiones múltiples, composiciones anhidras, dispersiones acuosas, aceites, leches, bálsamos, espumas, lociones, geles, geles crema, soluciones hidroalcohólicas, soluciones hidroglicólicas, hidrogeles, linimentos, sueros, jabones, champús, acondicionadores, serums, ungüentos, mousses, pomadas, polvos, barras, lápices, vaporizadores, aerosoles, cápsulas, cápsulas de gelatina, cápsulas blandas, cápsulas duras, comprimidos, comprimidos recubiertos de azúcar, formas granuladas, gomas de mascar, soluciones, suspensiones, emulsiones, jarabes, elixires, films de polisacáridos, jaleas V gelatina.
35. Composición según cualquiera de las reivindicaciones 28 a 34, caracterizada porque se encuentra incorporada a un producto seleccionado del grupo formado por correctores de ojeras, fondos de maquillaje, lociones desmaquillantes, leches desmaquillantes, sombras de ojos, barras de labios, brillos labiales, protectores labiales V polvos.
36. Composición según cualquiera de las reivindicaciones 28 a 34, caracterizada porque el péptido de fórmula general (1) , sus estereoisómeros, mezclas de los mismos V/o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado en un tejido, un tejido-no-tejido o un producto sanitario.
37. Composición según la reivindicación 36, caracterizada porque el tejido, tejido-no-tejido o producto sanitario se selecciona del grupo formado por vendas, gasas, camisetas, medias, calcetines, ropa interior, fajas, guantes, pañales, compresas, apósitos, cubrecamas, toallitas, parches adhesivos, parches no adhesivos, parches oclusivos, parches microeléctricos V mascarillas faciales.
38. Composición según cualquiera de las reivindicaciones 28 a 37, caracterizada porque
comprende adicionalmente una cantidad cosmética o farmacéuticamente eficaz de al menos un adyuvante seleccionado del grupo formado por otros agentes moduladores de PGC-la, otros agentes moduladores de PPARy, otros agentes que incrementan o reducen el contenido de triglicéridos de los adipocitos, agentes aceleradores o retrasadores de la diferenciación de los adipocitos, agentes lipolíticos o estimuladores de la lipólisis, agentes anticelulíticos, agentes adipogénicos, agentes estimuladores de la proliferación de adipocitos, inhibidores de la agregación de los receptores de acetilcolina, agentes inhibidores de la contracción muscular, agentes anticolinérgicos, agentes inhibidores de elastasa, agentes inhibidores de las metaloproteasas de matriz, agentes estimuladores o inhibidores de la síntesis de melanina, agentes blanqueantes o despigmentantes, agentes propigmentantes, agentes autobronceantes, agentes antienvejecimiento, agentes inhibidores de la NO-sintasa, agentes inhibido res de l.
5. reductasa, agentes inhibido res de lisil-y/o prolil-hidroxilasa, agentes antioxidantes, agentes capturadores de radicales libres y/o anticontaminación atmosférica, agentes capturadores de especies reactivas carbonilo, agentes antiglicación, agentes antihistamínicos, agentes antivirales, agentes antiparasitarios, agentes emulsionantes, emolientes, disolventes orgánicos, propelentes líquidos, acondicionadores de la piel, humectantes, sustancias que retienen la humedad, alfahidroxiácidos, betahidroxiácidos, hidratantes, enzimas epidérmicas hidrolíticas, vitaminas, aminoácidos, proteínas, pigmentos o colorantes, tintes, biopolímeros, polímeros gelificantes, agentes espesantes, tensioactivos, agentes suavizantes, emulgentes, agentes aglutinantes, conservantes, agentes antiarrugas, agentes capaces de disminuir o tratar las bolsas bajo los ojos, agentes exfoliantes, agentes descamantes, agentes que rato líticos, agentes antimicrobianos, agentes antifúngicos, agentes fungistáticos, agentes bactericidas, agentes bacteriostáticos, agentes estimuladores de la síntesis de macromoléculas dérmicas o epidérmicas y/o capaces de inhibir o prevenir su degradación, agentes estimuladores de la síntesis de colágeno, agentes estimuladores de la síntesis de elastina, agentes estimuladores de la síntesis de decorina, agentes estimuladores de la síntesis de la minina, agentes estimuladores de la síntesis de defensinas, agentes estimuladores de la síntesis de chaperonas, agentes estimuladores de la síntesis de cAMP, proteínas de choque térmico, agentes estimuladores de la síntesis de HSP70, agentes estimuladores de la síntesis de proteínas de choque térmico, agentes estimuladores de la síntesis de aquaporinas, agentes estimuladores de la síntesis de ácido hialurónico, agentes estimuladores de la síntesis de fibronectina, agentes estimuladores de la síntesis de sirtuínas, agentes estimuladores de la síntesis de lípidos y componentes del estrato córneo, ceramidas, ácidos grasos, agentes inhibidores de la degradación de colágeno, agentes inhibido res de la degradación de elastina, agentes inhibidores de proteasas de serina, agentes estimuladores de la proliferación de fibroblastos, agentes estimuladores de la proliferación de queratinocitos, agentes estimuladores de la proliferación de melanocitos, agentes estimuladores de la diferenciación de queratinocitos, agentes inhibidores de la acetilcolinesterasa, agentes dermorelajantes, agentes estimuladores de la síntesis de glicosaminoglicanos, agentes antihiperqueratosis, agentes comedo líticos, agentes antipsoriasis, agentes reparadores del DNA, agentes protectores del DNA, estabilizantes, agentes antiprurito, agentes para el tratamiento y/o cuidado de pieles sensibles, agentes reafirmantes, agentes redensificantes, agentes reestructurantes, agentes antiestrías, agentes astringentes, agentes reguladores de la producción de sebo, agentes antiperspirantes, agentes estimuladores de la cicatrización, agentes coadyuvantes de la cicatrización, agentes estimuladores de la reepitelización, agentes coadyuvantes de la reepitelización, factores de crecimiento de citoquinas, agentes calmantes, agentes antiinflamatorios, agentes anestésicos, agentes que actúen sobre la circulación capilar y/o la microcirculación, agentes estimuladores de la angiogénesis, agentes inhibidores de la permeabilidad vascular, agentes venotónicos, agentes que actúen sobre el metabolismo de las células, agentes destinados a mejorar la unión dermis-epidermis, agentes inductores del crecimiento del cabello, agentes inhibidores o retardadores del crecimiento del cabello, perfumes, agentes quelantes, extractos vegetales, aceites esenciales, extractos marinos, agentes provenientes de un procedimiento de biofermentación, sales minerales, extractos celulares, filtros solares y agentes fotoprotectores de naturaleza orgánica o mineral activos contra los rayos ultravioleta A y/o B, o mezclas de ellos.
39. Composición según la reivindicación 38 caracterizada porque el agente activo es de origen sintético o es un extracto vegetal o proviene de un procedimiento biotecnológico o de una combinación de un procedimiento sintético y un procedimiento biotecnológico.
40. Composición según cualquiera de las reivindicaciones 28 a 39, caracterizada porque comprende adicionalmente una cantidad farmacéutica mente eficaz de al menos un agente antidiabético.
41. Composición según cualquiera de las reivindicaciones 38 a 39, caracterizada porque el adyuvante se selecciona del grupo formado por agentes que incrementan o reducen el contenido de triglicéridos de los adipocitos, agentes aceleradores o retrasadores de la diferenciación de los adipocitos, agentes anticelulíticos, agentes lipolíticos y/o agentes venotónicos.
42. Composición cosmética o farmacéutica según la reivindicación 41, caracterizada porque el agente que incrementa o reduce el contenido de triglicéridos de los adipocitos, agente acelerador o retrasador de la diferenciación de los adipocitos, agente anticelulítico, agente lipolítico y/o agentes venotónico se selecciona del grupo formado por forscolina, cafeína, escina, carnitina, coenzima A, lipasa, glaucina, esculina, visnadina, sarsasapogenina, extracto de Coffea arabica, extracto de Coleus forskohlii, extracto de Anemarrhena apshodeloides, y la mezcla de Agua, Glicerina, Lecitina, Cafeína, Extracto de raíz de Brusco (Ruscus Aculeatus) , Maltodextrina, Silica, Hidroyoduro de Trietanolamina, Propilenglicol, Extracto de Hiedra (Hedera Helix) , Carnitina, Escina, Tripéptido-l, Goma Xantana, Carragenina (Chondrus Crispus) y EDTA Disódico.
43. Composición según cualquiera de las reivindicaciones 38 a 39, caracterizada porque el adyuvante se selecciona del grupo formado por agentes reafirmantes, redensificantes y reestructurantes.
44. Composición cosmética o farmacéutica según la reivindicación 43, caracterizada porque el agente reafirmante, redensificante o reestructurante se selecciona del grupo formado por Extracto de Fermento de Pseudoalteromonas, Tripéptido-l0 Citrulina, Acetilarginiltriptofil Difenilglicina, Hexapeptido-l0 y la mezcla de Extracto de Fermento de Pseudoalteromonas, Proteína de Trigo Hidrolizada, Proteína de Soja Hidrolizada, Tripéptido-l0 Citrulina y Tripéptido-1.
45. Composición según cualquiera de las reivindicaciones 38 a 39, caracterizada porque el adyuvante se selecciona del grupo formado por agentes antiestrías.
46. Composición cosmética o farmacéutica según la reivindicación 45, caracterizada porque el agente anti-estrías se selecciona del grupo formado por extracto de Centella Asiatica, extracto de Rosa canina, extracto de Rosa moschata, extracto de Rosa rubiginosa, y la mezcla de Agua, CaprililjCapril Glucósido, Lecitina, Glicerina, Extracto de Fermento de Pseudoalteromonas, Acetil Tripéptido-30 Citrulina, Pentapéptido-18, Goma Xantana y Caprilil Glicol.
47. Composición según cualquiera de las reivindicaciones 38 a 39, caracterizada porque el adyuvante se selecciona del grupo formado por agentes antiarrugas y agentes antienvejecimiento.
48. Composición cosmética o farmacéutica según la reivindicación 47, caracterizada porque el
agente antiarrugas y agente antienvejecimiento se selecciona del grupo formado por Acetil Hexapéptido-8, Acetil Heptapéptido-4, Acetil Octapéptido-3, Pentapéptido-18, Acetil Hexapéptido-30, la mezcla de Proteína de Trigo Hidrolizada, Proteína de Soja Hidrolizada, y Tripéptido-l, Diaminopropionoil Tripéptido-33, Tripéptido-l0 Citrulina, la mezcla de Extracto 5 de Fermento de Pseudoalteromonas, Proteína de Trigo Hidrolizada, Proteína de Soja Hidrolizada, Tripéptido-l0 Citrulina y Tripéptido-l, Acetil Tetrapéptido-5, Acetil Tripéptido-30 Citrulina, Acetilarginiltriptofil Difenilglicina, Acetil Tetrapéptido-22, Dimetilmetoxi Cromanol, Dimetilmetoxi Cromanil Palmitato, Extracto de Fermento de Pseudoalteromonas, la mezcla de Lisina HCI, Lecitina y Tripéptido-9 Citrulina y la mezcla de Lisina HCI, Lecitina y
Tripéptido-l0 Citrulina.
<llO>
<120>
<130>
<140>
<141>
<160>
<170>
<210> <2ll> <212> <213>
<220>
<223>
<400>
Ser rle Tyr val Ala Thr
<210> <2ll>
<212>
<213>
<220>
<223>
<400>
ser val val val Arg Thr
<210>
<211>
<212>
<213>
<220>
<223>
<400>
His rle Tyr val Ala Thr
<210>
<211>
<212>
<213>
<220>
<223>
<400>
His Val 5
PRT
Artificial Sequence synthetic peptide 6 PRT
Artificial Sequence synthetic peptide
Lipotec, S.A. PEPTIDOS MODULADORES DE
JJ
ES p20ll-30439 20ll-03-25
Patentrn version 3.5
6 PRT Artificial Sequence synthetic peptide 1
PRT
Artificial Sequence synthetic peptide Tyr val Ala Thr PGC-1alfa <210>
<211>
<212>
<213>
<220>
<223>
<400>
ser val
<210>
<211>
<212>
<213>
<220>
<223>
<400>
His 11 e <210>
<211>
<212>
<213>
<220>
<223>
<400>
Ser 11 e <210>
<211>
<212>
<213>
<220>
<223>
<400>
His val
<210>
<211>
<212>
<213>
<220>
<223>
<400>
PRT Artificial Sequence
synthetic peptide Tyr val Ala Thr
6
PRT Artificial Sequence
synthetic peptide Val val Ala Thr
PRT Artificial Sequence
synthetic peptide Val val Ala Thr
PRT Artificial Sequence
synthetic peptide val val Ala Thr
6
PRT Artificial Sequence
synthetic peptide Ser val val val Ala Thr 1 5
<210> 10
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 10
His rle Tyr Val Arg Thr 1 5
<210> 11
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 11
Ser rle Tyr Val Arg Thr 1 5
<210> 12
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 12
His Val Tyr val Arg Thr 1 5
<210> 13
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 13
Ser Val Tyr val Arg Thr 1 5
<210> 14
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 14
His rle Val val Arg Thr
5
<210> 15
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 15
Ser rl e val val Arg Thr
5
<210> 16
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 16
His val val val Arg Thr
5
<210> 17
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 17
His rle Tyr val Gly Thr
5
<210> 18
<211> 6
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 18
Ser rle Tyr val Gly Thr
5
<210> 19
<211> 6
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 19
His Val Tyr val Gly Thr 1 5
<210> 20
<211> 6
<212> PRT <2l3> Artificial Sequence <220>
<223> synthetic peptide <400> 20
Ser val Tyr val Gly Thr 1 5
<210> 21
<211> 6
<212> PRT <2l3> Artificial sequence <220>
<223> synthetic peptide <400> 21
His 11 e val val Gly Thr 1 5
<210> 22
<211> 6
<212> PRT <2l3> Artificial sequence <220>
<223> synthetic peptide <400> 22
Ser 11 e val val Gly Thr 1 5
<210> 23
<211> 6
<212> PRT <2l3> Artificial sequence <220>
<223> synthetic peptide <400> 23
His val val val Gly Thr 1 5
<210> 24
<211> 6
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 24
Ser val val val Gly Thr 1 5
<210> 25
<211> 6
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 25
His rle Tyr val Ala val 1 5
<210> 26
<211> 6
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 26
Ser rle Tyr val Ala val 1 5
<210> 27
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 27
His val Tyr val Ala val 1 5
<210> 28
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 28
Ser val Tyr val Ala val 1 5
<210> 29
<211> 6
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide
<400> 29
His rle val val Ala val
1 5
<210> 30
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 30
Ser rl e val val Ala Val 1 5
<210> 31
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 31
His val val val Ala val 1 5
<210> 32
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 32
Ser val val val Ala val 1 5
<210> 33
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 33
His rle Tyr val Arg val 1 5
<210> 34
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 34
Ser rle Tyr val Arg val 1 5
<210> 35
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 35
His val Tyr val Arg val 1 5
<210> 36
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 36
ser val Tyr val Arg val 1 5
<210> 37
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 37
His rle val val Arg val 1 5
<210> 38
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 38
Ser rl e val val Arg val
5
<210> 39
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 39
His val val val Arg val 1 5
<210> 40
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 40
Ser Val val val Arg val 1 5
<210> 41
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 41
His Ile Tyr Val Gly val 1 5
<210> 42
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 42
Ser Ile Tyr val Gly val 1 5
<210> 43
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 43
His val Tyr val Gly val
5
<210> 44
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 44
Ser val Tyr val Gly val
5
<210> 45
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 45
His 11 e Val val Gly val
5
<210> 46
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 46
Ser 11 e Val val Gly val
5
<210> 47
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 47
His val val val Gly val
5
<210> 48
<211> 6
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 48
Ser val val val Gly val 1 5
<210> 49
<211> 7
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 49
Gly Ser rle Tyr val Ala Thr 1 5
<210> 50
<211> 7
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 50
Ser rle Tyr val Ala Thr Ala 1 5
<210> 51
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 51
Gly Gly Ser rl e Tyr val Ala Thr 1 5
<210> 52
<211> 8
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 52
Ala Ser rle Tyr val Ala Thr Ala 1 5
<210> 53
<211> 8
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 53
Gly Gly Ser Val Tyr val Ala Thr 1 5
<210> 54
<211> 7
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 54
Ala Ser val Tyr val Ala Thr 1 5
<210> 55
<211> 7
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 55
Gly Ser val Tyr val Ala Thr 1 5
<210> 56
<211> 8
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 56
Ser val Tyr val Ala Thr Ala Ala 1 5
<210> 57
<211> 8
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 57
Gly Ser val 1 Tyr val 5 Ala Thr Ala
<210> 58
<211> 7
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 58
Tyr Ser rle val val Gly Thr 1 5
<210> 59
<211> 8
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 59
Thr Gly Ser rle val val Gly Thr 1 5
<210> 60
<211> 8
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 60
Gly Ser rle val val Gly Thr His 1 5
<210> 61
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 61
Ser rle val val Gly Thr Ala Gly1 5
<210> 62
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 62
Gly Ser rle val val Gly Thr Gly1 5
<210> 63
<211> 7
<212> PRT
<213> Artificial sequence <220>
<223> synthetic peptide <400> 63
Ser val val val Arg Thr rle 1 5
<210> 64
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 64
Ser val val val Arg Thr rle val 1 5
<210> 65
<211> 7
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 65
Gly Ser val val val Arg Thr 1 5
<210> 66
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 66
Gly Gly Ser val val val Arg Thr 1 5
<210> 67
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 67
Gly ser val val val Arg Thr Gly1 5
<210> 68
<211> 7
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 68
Ala His rle val val Gly Thr 1 5
<210> 69
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 69
Gly His rle val val Gly Thr Ala 1 5
<210> 70
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 70
His rle val val Gly Thr Leu Ala 1 5
<210> 71
<211> 8
<212> PRT
<213> Artificial Sequence <220>
<223> synthetic peptide <400> 71
Ala Leu His rle val val Gly Thr 1 5
Patentes similares o relacionadas:
Uso del péptido qbp1 para la prevención o el tratamiento del trastorno del estrés postraumático, el síndrome de estrés agudo y/o el síndrome de adaptación general, del 8 de Abril de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Una composición que comprende un péptido que consiste en una secuencia de aminoácidos con al menos un 70% de identidad con la SEQ ID NO: 1, o que […]
Péptidos capaces de reactivar mutantes de p53, del 18 de Marzo de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Un péptido recombinante o sintético que comprende una secuencia de aminoácidos expuesta en la SEQ ID NO: 314, en donde dicho péptido reactiva […]
Péptidos de diseño corto que poseen acciones selectivas contra bacterias y células cancerosas, del 26 de Febrero de 2020, de THE UNIVERSITY OF MANCHESTER: Un péptido con la fórmula I o II que se muestra a continuación **(Ver fórmula)** en donde: A1v se selecciona de G, GKI o GIK […]
Compuestos para su uso en el tratamiento y/o prevención de una infección de mycoplasma sp., del 31 de Enero de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Compuestos para su uso en el tratamiento y/o prevención de una infección de mycoplasma sp. La presente invención hace referencia a compuestos con […]
Composiciones para unir módulos de dedos de cinc, del 15 de Enero de 2020, de Sangamo Therapeutics, Inc: Una proteína de dedos de cinc de múltiples dedos que se une específicamente a un sitio diana, comprendiendo la proteína de dedos de cinc de […]
Análogos de compstatina de acción prolongada y composiciones y métodos relacionados, del 8 de Enero de 2020, de Apellis Pharmaceuticals, Inc: Un análogo de compstatina de acción prolongada que comprende un resto reductor de la eliminación unido con dos restos análogos de compstatina, en donde cada resto […]
Terapias de antibióticos peptídicos derivados del búfalo de agua, del 20 de Noviembre de 2019, de Centaur, Inc: Una composición antibiótica que comprende un péptido antibiótico, en donde el péptido comprende una secuencia aminoacídica sintética que tiene la […]
Péptidos, dispositivos y procedimientos para la detección de anticuerpos de Anaplasma, del 20 de Noviembre de 2019, de Abaxis, Inc: Una composición que comprende una población de péptidos aislados, comprendiendo dicha población tres o más péptidos diferentes, en la que cada péptido en la población […]