Procedimiento para la preparación de l-3,4-dihidroxi-6-[18f]fluoro-fenilalanina y de 2-[18f]fluoro-l-tirosina y de sus derivados metilados en posición alfa a partir de un compuesto precursor.
Procedimiento para la preparación de un compuesto de acuerdo con las Fórmulas (1) y (2)
con X ≥
H o CH3
caracterizado por que
el compuesto según la Fórmula (3) i
con X ≥ H o CH3 y R5 ≥ grupo lábil nucleófilo, ≥ F; R2 ≥ bencilo (Bn) y R4 ≥ (S)-BOC-BMI: (S)-1-(terc.-butoxicarbonil)-2-terc.-butil-3-metil-4-imidazolidinona,
mediando utilización de hidrógenocarbonato de tetrabutil-amonio o de Kryptofix-oxalato de potasio como catalizadorde transferencia de fases, se fluorura con 18F,
se separa en una etapa adicional y en el caso de la preparación del compuesto según la Fórmula (1) se oxida y en elcaso de la preparación del compuesto según la Fórmula (2) se descarbonila, el producto resultante se hidroliza y sesepara.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11001114.
Solicitante: FORSCHUNGSZENTRUM JULICH GMBH.
Nacionalidad solicitante: Alemania.
Dirección: 52425 Jülich ALEMANIA.
Inventor/es: WAGNER,FRANZISKA, ERMERT,JOHANNES, COENEN,HEINRICH HUBERT.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C229/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › Compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada.
- C07D233/32 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 233/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, no condensados con otros ciclos. › Un átomo de oxígeno.
PDF original: ES-2420629_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de l-3, 4-dihidroxi-6-[18f]fluoro-fenilalanina y de 2-[18f]fluoro-l-tirosina y de sus derivados metilados en posición alfa a partir de un compuesto precursor
El invento se refiere a un procedimiento para la preparación de L-3, 4-dihidroxi-6-[18F]fluoro-fenilalanina y de 2-[18F]fluoro-L-tirosina y de sus derivados metilados en posición α a partir de un respectivo compuesto precursor.
Desde hace veinte años, es conocido el potencial de la PET (tomografía por emisión de positrones) de aminoácidos aromáticos, en particular de la L-3, 4-dihidroxi-6-[18F]fluoro-fenilalanina (= [18F]FDOPA) , y éste se ha consagrado internacionalmente también en el sector clínico sobre todo para la investigación de pacientes de Parkinson así como adicionalmente en los últimos años para el diagnóstico de tumores (transporte de aminoácidos) . En conjunto, existe inalteradamente, para usos tanto neurológicos como oncológicos, un gran interés en desarrollar procedimientos sencillos para la síntesis de [18F]FDOPA por reacción con el [18F]fluoruro, que se puede preparar con facilidad.
A partir del año 2001 se conoce una publicación de T. Tierling, K. Hamacher y H.H. Coenen con el título “A new nucleophilic asymetric synthesis of 6-[18F]Fluoro-DOPA” [Una nueva síntesis asimétrica nucleofílica de 6-[18F]fluoro-DOPA], que ha aparecido en J. Label. Compds. Radiopharm. 44, suplemento 1, y en la que se describe un procedimiento para la preparación de un compuesto precursor de [18F]FDOPA y su conversión química en L-6-[18F]fluoro-DOPA. De acuerdo con este procedimiento, un compuesto precursor se hace reaccionar mediante una sustitución nucleófila con un criptando K18F para formar en primer lugar unos compuestos precursores y a continuación para formar el [18F]FDOPA. El producto es obtenido en una pureza enantiomérica de 85 %.
Las actuales vías de síntesis nucleófilas de múltiples etapas presuponen un alto gasto en tiempo y aparatos. En el procedimiento de marcación nucleófila directa, conocido hasta ahora, se podían obtener solamente unas purezas enantioméricas de 85 %, como en el caso de la síntesis de Tierling, Hamacher y Coenen. Unos enfoques electrófilos de reacción permiten solamente unas síntesis radiológicas con unas cantidades de actividad aproximadamente diez más pequeñas junto con un gasto en costos relativamente alto para la preparación de los radionúclidos, puesto que las tasas de producción del [18F]F2 elemental necesario para la fluoración radiológica electrófila son esencialmente más pequeñas con iguales costos para la irradiación.
La publicación “Fluorination of aromatic compounds from 1-ar y l-3, 3-dimethyltriazenes and fluoride anions in acidic medium 2. Synthesis of (S) -[18F]-3-fluoro-α-methyl-phenylalanine” [La fluoración de compuestos aromáticos a partir de 1-aril-3-dimetiltriazenos y aniones de fluoruro en un medio ácido 2. Síntesis de (S) -[18F]-3-fluoro-α-metilfenilalanina] de Thierr y Pages y colaboradores en el Journal of Fluorine Chemistr y 107 (2001) páginas 329-335, divulga unos compuestos precursores y unos procedimientos para la preparación de L-aminoácidos aromáticos marcados con [18F]fluoro.
Los procedimientos nucleófilos de múltiples etapas son malamente automatizables y susceptibles de perturbaciones. Los procedimientos conocidos según el estado de la técnica para la preparación de compuestos precursores de [18F]FDOPA y de [18F]FTyr conducen a unos rendimientos radioquímicos relativamente pequeños y están vinculados con un alto gasto en costos.
La publicación "Synthesis of a Chiral Precursor for No-Carrier-Added (NCA) PET Tracer 6-[18F]Fluoro-L-dopa Based on Regio- and Enantioselective Alkylation of 2, 4-Bis (chloromethyl) -5-iodoanisole" [Síntesis de un compuesto precursor quiral para un compuesto trazador de PET sin vehículo añadido (NCA) basado en una alquilación regio-y enantioselectiva de 2, 4-bis (clorometil) -5-yodoanisol] de Chiaki Kuroda y colaboradores en la revista Bull. Chem. Soc. Jpn. 73, 417-422 del año 2002, divulga una síntesis de compuestos precursores cíclicos para fármacos radiológicos que tienen un sustituyente yodado como grupo lábil (saliente) .
La publicación de Bin Shen y colaboradores “Decarbonylation of multi-substituted [18F]benzaldehy des for modelling syntheses of 18F-labelled aromatic amino acids” [Descarbonilación de [18F]benzaldehídos múltiplemente sustituidos para síntesis de modelación de aminoácidos aromáticos marcados con 18F] de Applied Radiation and Isotopes, Elsevier, Oxford, Gran Bretaña, tomo 65 nº 11, 17 de Octubre de 2007 (2007-10-17) páginas 1227-1231 muestra la utilización de un catalizador de transferencia de fases en el caso de la fluoruración con 18F.
Por lo tanto, la misión del invento es la de poner a disposición un procedimiento para la preparación de [18F]FDOPA, de [18F]FTyr y de sus derivados metilados en posición α así como de sus compuestos precursores y un procedimiento para la preparación de sus compuestos precursores, que conduzca a mayores rendimientos radioquímicos y a una mayor pureza enantiomérica. Además de esto, el procedimiento debe de ser apropiado para un funcionamiento automático de la síntesis.
El problema planteado por esta misión se resuelve conforme al invento con las características de la reivindicación 1.
Con los procedimientos conformes al invento y los compuestos precursores, se ha hecho posible ahora preparar [18F]FDOPA, [18F]FTyr y sus derivados metilados en posición α en solamente tres etapas radiactivas, en un estado enantioméricamente puro. La síntesis se puede llevar a cabo de una manera automática y conduce a unas purezas enantioméricas de ≥ 98 %.
Las Figuras muestran unos esquemas de reacciones para la preparación de los compuestos precursores conformes al invento, así como para la preparación de los compuestos diana [18F]FDOPA y [18F]FTyr y de sus derivados metilados en posición α.
Muestran:
La Fig.1: Un esquema general de reacciones para la preparación del compuesto precursor.
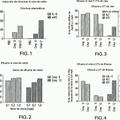
La Fig. 2: Un esquema de reacciones para la síntesis del compuesto precursor con etapas individuales de reacción. La Fig.2a: Un ejemplo especial de realización para la síntesis del compuesto precursor. La Fig.3: Las etapas generales para la preparación de [18F]FDOPA y del derivado metilado en posición α. La Fig.3a: La preparación dada a modo de ejemplo de [18F]FDOPA y del derivado metilado en posición α.
La Fig.3b: Las etapas para la preparación de [18F]FDOPA (Ejemplo) La Fig.4: Las etapas generales para la preparación de [18F]FTyr y del derivado metilado en posición α. La Fig.4a: La preparación dada a modo de ejemplo de [18F]FTyr y del derivado metilado en posición α. La Fig.4b: Las etapas para la preparación de L-[18F]FTyr (Ejemplo) .
La Fórmula (1) muestra la estructura de [ 18F]FDOPA y del derivado metilado en posición α. En ella X = H o CH3.
Fórmula (1)
La Fórmula (2) muestra la estructura de [18F]FTyr del derivado en posición α. En ella X es = H o CH3.
Fórmula (2) 25 La Fórmula (3) muestra la estructura del compuesto precursor. En ella X es = H o CH3.
Fórmula (3) En lo sucesivo se debe de describir el invento en su forma general.
En las Fórmulas así como en las Figuras se pueden indicar como sustituyentes Rn y X los siguientes grupos:
R1 = Br, I R2 = bencilo (Bn) , R3 = tetrahidropiranilo (THP) , metiltiometilo (MTM) , metoximetilo (MOM) , TBDMS, TBDPS, grupos protectores generales del tipo de sililo R4 = (S) -BOC-BMI: (S) -1- (terc. butoxicarbonil) -2-terc. butil-3-metil-4-imidazolidinona, nomenclatura de fórmula:
R4 =
R5 = grupo lábil nucleófilo, p.ej. F, con R = alquilo p.ej. CH3, C2H5 X = H o CH3. En la Figura 1 se indica un esquema general de reacciones, de acuerdo con el cual se puede preparar el compuesto precursor para [18F]FDOPA y [18F] FTyr según la fórmula 3. Como preparación previa para la síntesis del compuesto precursor conforme al invento, un compuesto según la fórmula a según la etapa I de reacción es halogenado para dar el producto b.
Como halógenos se pueden emplear en particular bromo o yodo. La halogenación se puede llevar a cabo en un intervalo de temperaturas comprendidas entre -20ºC y -80ºC, de
manera preferida entre -50ºC y -80ºC, de manera especialmente preferida a -78ºC, es decir a la temperatura del hielo seco. De manera preferida, la halogenación se efectúa mediando adición de un tampón. Como tampón entra en consideración por ejemplo acetato de sodio. Como disolvente se puede... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de un compuesto de acuerdo con las Fórmulas (1) y (2)
con X = H o CH3 caracterizado por que
el compuesto según la Fórmula (3) i con X = H o CH3 y R5 = grupo lábil nucleófilo, = F; R2 = bencilo (Bn) y R4 = (S) -BOC-BMI: (S) -1- (terc. butoxicarbonil) 2-terc. butil-3-metil-4-imidazolidinona,
mediando utilización de hidrógenocarbonato de tetrabutil-amonio o de Kr y ptofix-oxalato de potasio como catalizador de transferencia de fases, se fluorura con 18F, se separa en una etapa adicional y en el caso de la preparación del compuesto según la Fórmula (1) se oxida y en el caso de la preparación del compuesto según la Fórmula (2) se descarbonila, el producto resultante se hidroliza y se separa.
2. Procedimiento de acuerdo con la reivindicación 1,
caracterizado por que la separación del producto de fluoruración con 18F se efectúa mediante una extracción en fase sólida.
3. Procedimiento de acuerdo con una de las reivindicaciones 1 ó 2,
caracterizado por que el grupo formilo, en el caso de la preparación del compuesto según la Fórmula (1) se oxida para dar un éster.
4. Procedimiento de acuerdo con la reivindicación 3,
caracterizado por que la oxidación se lleva a cabo con MCPBA, o con ácido peracético o con un perborato.
5. Procedimiento de acuerdo con una de las reivindicaciones 1 ó 2,
caracterizado por que 18F
el compuesto precursor fluorurado con se descarbonila mediante un catalizador para la preparación del compuesto según la Fórmula (2) .
6. Procedimiento de acuerdo con una de las reivindicaciones 1 hasta 5,
caracterizado por que el éster o el producto de descarbonilación se hidroliza.
7. Procedimiento de acuerdo con una de las reivindicaciones 1 hasta 5,
caracterizado por que el producto según la Fórmula (1) o (2) se separa mediante una HPLC.
Fig.2a
Patentes similares o relacionadas:
Formulaciones de liberación controlada de levodopa y usos de las mismas, del 8 de Abril de 2020, de Impax Laboratories, LLC: Formulación sólida oral multiparticulada de liberación controlada que comprende 50 a 600 mg de levodopa y 10 a 80 mg de carbidopa, donde los multiparticulados están en una cápsula […]
Inhibidores de la arginasa y métodos de uso, del 8 de Mayo de 2019, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un compuesto de fórmula IA o fórmula IB:**Fórmula** o uno de sus estereoisómeros o sales farmacéuticamente aceptables; en donde: dicha línea discontinua […]
Esteraminas y derivados de la metátesis del aceite natural, del 5 de Diciembre de 2018, de STEPAN COMPANY: Una esteramina que comprende un producto de reacción de un ácido monoinsaturado C10-C17 derivado de metátesis, ácido octadeceno-1,18-dioico o sus derivados éster con una alcanolamina […]
Compuestos que son agentes moduladores de S1P y/o agentes moduladores de ATX, del 3 de Enero de 2018, de Biogen MA Inc: Un compuesto representado por la fórmula (IIa):**Fórmula** o una sal farmacéuticamente aceptable del mismo, en la que: A3c y A5c son N o […]
Disolución de almacenamiento para estabilizar una proteína hemo, del 30 de Noviembre de 2016, de Eiken Chemical Co., Ltd: Una disolución de almacenamiento para la estabilización de hemoglobina que comprende hemoglobina y ácido 3- hidroxi-2,2'-iminodisuccínico de fórmula , o una sal del mismo:**Fórmula** […]
Conjugados de GABA y métodos de utilización de los mismos, del 8 de Junio de 2016, de Xgene Pharmaceutical Inc: Un compuesto que comprende un fármaco analgésico unido por enlace covalente a un primer resto mediante un enlazador covalente fisiológicamente […]
 Nuevos lípidos catiónicos con diversos grupos de cabeza para el suministro oligonucleotídico, del 30 de Marzo de 2016, de SIRNA THERAPEUTICS, INC: Un lípido catiónico de Fórmula A:**Fórmula**
en la que:
p es 1 a 8;
R1 y R2 se seleccionan independientemente de H, alquilo (C1-C10), heterociclilo, y […]
Nuevos lípidos catiónicos con diversos grupos de cabeza para el suministro oligonucleotídico, del 30 de Marzo de 2016, de SIRNA THERAPEUTICS, INC: Un lípido catiónico de Fórmula A:**Fórmula**
en la que:
p es 1 a 8;
R1 y R2 se seleccionan independientemente de H, alquilo (C1-C10), heterociclilo, y […]
Uso de un suplemento de metal en alimentación animal, del 23 de Diciembre de 2015, de AKZO NOBEL CHEMICALS INTERNATIONAL B.V: Uso de un suplemento para preparar metal (nutricionalmente) disponible para animales, comprendiendo dicho suplemento al menos un compuesto seleccionado del grupo que consiste […]