Procedimiento para la preparación de bromuro de tri-terc-butilfosfina paladio(I) dímero.
Procedimiento para la preparación de un complejo de fórmula (I):
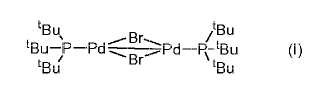
**Fórmula**
que comprende las etapas de:
(a) mezclar Pd(diolefina)Br2 y tBu3P en un disolvente; y
(b) añadir un hidróxido alcalino para formar el complejo de fórmula (I).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2010/051232.
Solicitante: JOHNSON MATTHEY PUBLIC LIMITED COMPANY.
Nacionalidad solicitante: Reino Unido.
Dirección: 5th Floor 25 Farringdon Street London EC4A 4AB REINO UNIDO.
Inventor/es: GRASA,Gabriela,Alexandra, COLACOT,THOMAS JOHN, HOOPER,MARK WILLIAM.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07F15/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › Compuestos que contienen elementos de los grupos 8, 9, 10 o 18 del sistema periódico.
PDF original: ES-2433600_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de bromuro de tri-terc-butilfosfina paladio (I) dímero.
La presente invención se refiere a la preparación de complejos de metal precioso, en particular un complejo de fosfina paladio.
El bromuro de tri-terc-butilfosfina paladio (I) dímero {[Pd (PtBu3) ( !-Br) ]2} es un catalizador activo para reacciones de acoplamiento cruzado. El bromuro de tri-terc-butilfosfina paladio (I) dímero ha sido preparado por Mingos et al empleando o bien Pd2dba3.C6H6 o bien una combinación Pd2dba3.C6H6 y Pd (COD) Br2 (J. Chem. Soc. Dalton Trans. (1996) 4313 y J. Organomet. Chem. 600 (2000) 198) . El propio Pd2dba3.C6H6 se prepara por cristalización de Pd (dba) 2 en un volumen grande de C6H6. El Pd2dba3.C6H6 es un catalizador altamente sensible al aire que requiere condiciones de alto vacío y baja temperatura para la cristalización.
Un objeto de la presente invención consiste en proporcionar un procedimiento alternativo para la preparación de complejos de metal precioso, en particular bromuro de tri-terc-butilfosfina paladio (I) dímero.
Por tanto, la presente invención proporciona un procedimiento para la preparación de un complejo de fórmula (I) :
que comprende las etapas de:
(a) mezclar Pd (diolefina) Br2 y tBu3P en un disolvente; y
(b) añadir un hidróxido alcalino para formar el complejo de fórmula (I) .
El procedimiento de la presente invención no utiliza Pd2dba3.C6H6 como material de partida. Por tanto, se puede evitar la cristalización de Pd (dba) 2. Además, se facilita la preparación de [Pd (PtBu3) (μ-B) ]2 ya que el complejo no llega a contaminarse con ligando dba. El procedimiento de la presente invención resulta por tanto más adecuado para la producción a gran escala.
Con preferencia, el compuesto de Pd (diolefina) Br2 contiene una diolefina cíclica, más preferentemente 2, 5norbornadieno (NBD) o 1, 5-ciclooctadieno (COD) . Compuestos adecuados de Pd (diolefina) Br2 incluyen por tanto Pd (COD) Br2 y Pd (NBD) Br2. En particular se prefiere Pd (COD) Br2.
Alternativamente, la diolefina puede ser reemplazada por dos moléculas de una monoolefina. En este caso, la monoolefina puede ser seleccionada del grupo consistente en un alqueno C2-10 de cadena lineal, un alqueno C2-10 de cadena ramificada, un cicloalqueno C5-10 y combinaciones de los mismos. Más preferentemente, la monoolefina es etileno o cicloocteno.
El compuesto de Pd (diolefina) Br2 y el ligando tBu3P se mezclan entre sí en un disolvente. El disolvente se puede seleccionar del grupo consistente en alcanol C1-10 de cadena lineal, ramificada o cíclico, un hidrocarburo aromático C6-10 y combinaciones de los mismos. Con preferencia, el disolvente se elige del grupo consistente en metanol, etanol, 2-propanol, 1-butanol, 2-butanol, 3-metil-2-butanol, 2-metil-2-butanol, 3-metil-1-butanol, benceno, tolueno y combinaciones de los mismos. Disolventes particularmente preferidos son metanol y tolueno. La concentración de Pd (diolefina) Br2 en el disolvente es con preferencia de 0, 05 mol/l a 2, 5 mol/l aproximadamente y más preferentemente de 0, 2 mol/l a 2 mol/l aproximadamente.
El ligando tBu3P se puede emplear como un sólido o, más preferentemente, como una solución en un disolvente tal como tolueno o tetrahidrofurano (THF) . Se puede emplear cualquier concentración adecuada de tBu3P en el disolvente, aunque es preferible que la relación molar de Pd (diolefina) Br2:tBu3P sea de 1:1 aproximadamente. Si se desea, la relación molar de tBu3P puede encontrarse en un ligero exceso con respecto a la cantidad molar de Pd (diolefina) Br2. Por ejemplo, la cantidad de tBu3P en la mezcla de reacción puede ser calculada para proporcionar un exceso molar de hasta 10% aproximadamente con respecto a la cantidad requerida para la reacción estequiométrica.
En la combinación de Pd (diolefina) Br2 y tBu3P en el disolvente, los componentes se pueden mezclar en cualquier orden adecuado, aunque preferentemente se añade primero el Pd (diolefina) Br2 al disolvente, seguido por tBu3P.
En una modalidad particularmente preferida de la invención, los disolventes que pueden ser empleados en la etapa (a) pueden comprender al menos una proporción de tolueno. Los presentes inventores han comprobado que la inclusión de una cantidad adecuada de tolueno se traduce en la obtención del complejo de fórmula (I) en una forma más cristalina. A este respecto, el disolvente como el descrito anteriormente para la etapa (a) puede comprender tolueno, o bien el ligando tBu3P puede ser añadido a la mezcla de reacción como una solución en tolueno.
Una vez que el compuesto Pd (diolefina) Br2 y el ligando tBu3P se mezclan entre sí en el disolvente, con preferencia la mezcla de reacción se agita a una temperatura del orden de -10º C a 35º C aproximadamente, preferentemente de 5º C a 30º C aproximadamente. La mezcla puede ser agitada durante un periodo, por ejemplo, preferentemente de 1 min a 3 horas aproximadamente, más preferentemente de 5 min a 2 horas aproximadamente y con suma preferencia de 10 min a 1 hora aproximadamente.
Se añade un hidróxido alcalino a la mezcla de Pd (diolefina) Br2 y tBu3P. Preferentemente, la relación molar de Pd (diolefina) Br2:hidróxido alcalino es de 1:1 aproximadamente. Si se desea, la cantidad molar del hidróxido alcalino puede encontrarse en un ligero exceso con respecto a la cantidad molar de Pd (diolefina) Br2. Por ejemplo, la cantidad de hidróxido alcalino a la mezcla de reacción puede ser calculada para proporcionar un exceso molar de hasta 10% aproximadamente con respecto a la cantidad requerida para la reacción estequiométrica.
El hidróxido alcalino puede ser hidróxido potásico o hidróxido sódico, con preferencia hidróxido sódico. Según una modalidad, el hidróxido alcalino se añade a la mezcla de reacción como un sólido. Alternativamente, el hidróxido alcalino puede ser disuelto en un alcanol C1-10 de cadena lineal, ramificada o cíclico y se añade entonces a la mezcla de reacción como una solución. Alcanoles adecuados metanol, etanol, 2-propanol, 1-butanol, 2-butanol, 3-metil-2butanol, 2-metil-2-butanol, 3-metil-1-butanol o una combinación de los mismos. Con preferencia, el alcanol es metanol. La solución de hidróxido alcalino/alcanol se puede emplear en cualquier concentración adecuada, por ejemplo, del orden de 0, 05 mol/l a 3 mol/l aproximadamente, con preferencia de 0, 1 mol/l a 2, 5 mol/l aproximadamente.
Después de la adición del hidróxido alcalino, preferentemente la mezcla de reacción se agita a una temperatura del orden de -10º C a 35º C aproximadamente, con preferencia de -5º C a 30º C aproximadamente. La mezcla se puede agitar durante un periodo, por ejemplo preferentemente de 1 min a 4 horas aproximadamente, más preferentemente de 5 min a 3, 5 horas aproximadamente y con suma preferencia de 10 min a 3 horas aproximadamente.
Una vez terminada la reacción, el complejo de fórmula (I) se separa de la mezcla de reacción por cualquier método adecuado que sea dependiente de la forma física del producto. Por ejemplo, cuando se desea recuperar el complejo de fórmula (I) como un sólido, el complejo puede ser precipitado en la mezcla de reacción por la adición de un disolvente adecuado (por ejemplo, metanol) . El complejo puede ser entonces aislado por filtración, decantación o centrifugado. El complejo separado se lava preferentemente con más disolvente y luego se seca. El secado puede ser efectuado empleando métodos adecuados, por ejemplo, a temperaturas del orden de 10-60º C aproximadamente y con preferencia 20-40º C aproximadamente bajo un vacío de 1-30 mbar aproximadamente durante 1 hora aproximadamente a 5 días aproximadamente.
Es preferible que todas las etapas en la preparación y aislamiento del complejo de fórmula (I) se lleven a cabo bajo una atmósfera inerte (por ejemplo, nitrógeno o argón) . Además, dado que el complejo de fórmula (I) no es estable en agua, es preferible controlar la cantidad de agua que puede estar presente en cualquiera de los disolventes utilizados. En una modalidad de la invención, por tanto, los disolventes son anhidros.
El procedimiento de la presente invención da lugar a un alto rendimiento y el catalizado obtenido es puro. En consecuencia, según otro aspecto, la presente invención proporciona un complejo de fórmula (I) obtenible de acuerdo con el procedimiento como se ha descrito anteriormente.
La invención será ilustrada adicionalmente con referencia a los siguientes ejemplos no limitativos.
EJEMPLOS
Ejemplo 1
Después de desgasificar tres veces bajo vacío/N2, se hizo reaccionar Pd (COD) Br2 (4, 4 mol, 1, 66 kg) en suspensión en tolueno (2, 3 litros) con un equivalente molar... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de un complejo de fórmula (I) :
que comprende las etapas de:
(a) mezclar Pd (diolefina) Br2 y tBu3P en un disolvente; y
(b) añadir un hidróxido alcalino para formar el complejo de fórmula (I) .
2. Procedimiento según la reivindicación 1, en donde la diolefina es una diolefina cíclica.
3. Procedimiento según la reivindicación 2, en donde la diolefina cíclica es 2, 5-norbornadieno (NBD) o 1, 5ciclooctadieno (COD) .
4. Procedimiento según la reivindicación 1, en donde la diolefina comprende dos moléculas de una monoolefina.
5. Procedimiento según la reivindicación 4, en donde la monoolefina se elige del grupo consistente en un alqueno C2-10 de cadena lineal, un alqueno C2-10 de cadena ramificada, un cicloalqueno C5-10 y combinaciones de los mismos.
6. Procedimiento según la reivindicación 4, en donde la monoolefina es etileno o cicloocteno.
7. Procedimiento según la reivindicación 1, en donde el disolvente se elige del grupo consistente en un alcanol C115 10 de cadena lineal, de cadena ramificada o cíclico, un hidrocarburo aromático C6-10 y combinaciones de los mismos.
8. Procedimiento según la reivindicación 1, en donde el disolvente se elige del grupo consiste en metanol, etanol, 2-propanol, 1-butanol, 2-butanol-3-metil-2-butanol, 2-metil-2-butanol, 3-metil-1-butanol, benceno, tolueno y combinaciones de los mismos.
9. Procedimiento según la reivindicación 1, en donde el hidróxido alcalino es hidróxido potásico o hidróxido 20 sódico.
10. Procedimiento según la reivindicación 1, en donde la concentración de Pd (diolefina) Br2 en el disolvente es de 0, 05 mol/l a 2, 5 mol/l aproximadamente.
11. Procedimiento según la reivindicación 1, en donde la relación molar de Pd (diolefina) Br2:tBu3P es de 1:1 aproximadamente.
12. Procedimiento según la reivindicación 1, en donde la relación molar de Pd (diolefina) Br2:hidróxido alcalino es de 1:1 aproximadamente.
13. Procedimiento según la reivindicación 1, en donde la etapa (a) y la etapa (b) se llevan a cabo independientemente a una o más temperaturas entre -10º C y 35º C aproximadamente.
Patentes similares o relacionadas:
Procedimiento para la preparación diastereoselectiva de complejos de rutenio, del 13 de Mayo de 2020, de SYNGENTA PARTICIPATIONS AG: Un procedimiento para la preparación de un compuesto de fórmula I **(Ver fórmula)** en donde X es -CH2-, -CH2-CH2-, -CH2-CH2-CH2- o -CH2-CH2-CH2-CH2-; […]
Sistema catalítico para la preparación de alcano altamente ramificado a partir de olefinas, del 19 de Febrero de 2020, de Shanghai ChemRun Co. Ltd: Un compuesto de fórmula I, **(Ver fórmula)** en la que, Z es hidrógeno, alquilo C1-C4 o haloalquilo C1-C4, fenilo sin sustituir o sustituido; […]
Complejos a base de rutenio, del 29 de Enero de 2020, de FIRMENICH SA: Un procedimiento para la elaboración de un compuesto de fórmula {[(dieno)Ru(OOCR1)2]n(S)v} (I') en la que n es 1 o 2; v es 0,1 o 2; S es una molécula […]
Catalizadores de polimerización para producir polímeros con bajos niveles de ramificación de cadena larga, del 29 de Enero de 2020, de CHEVRON PHILLIPS CHEMICAL COMPANY LP: Una composición catalítica que comprende el producto de contacto de: 1) al menos un ansa-metaloceno; 2) al menos un compuesto de organoaluminio; y 3) al menos un activador, […]
Complejos de wolframio oxo alquilideno para la metátesis de olefinas selectiva de Z, del 3 de Enero de 2020, de MASSACHUSETTS INSTITUTE OF TECHNOLOGY: Un compuesto de fórmula I:**Fórmula** en donde: cada uno de R1 y R2 es independientemente R, -OR, -SR, -N(R)2, -OC(O)R, -SOR, -SO2R,-SO2N(R)2, […]
METALODENDRÍMEROS DE NATURALEZA CARBOSILANO CONTENIENDO RUTENIO Y COBRE COORDINADOS A LIGANDOS BASE DE SCHIFF, SU PREPARACIÓN Y SUS USOS, del 19 de Diciembre de 2019, de UNIVERSIDAD DE ALCALA.: La presente invención se refiere a metalodendrímeros de naturaleza carbosilanoque contienen complejos metálicos coordinados a ligandos bases de Schiff. Además, […]
Bisfosfitos con unidades 2,4-dimetilfenilo y su empleo como ligandos en la hidroformilación, del 18 de Diciembre de 2019, de Evonik Operations GmbH: Procedimiento para la producción de 2-propil-1-heptanol con los siguientes pasos: a) puesta a disposición de una mezcla de sustancias de empleo […]
Metalodendrímeros de naturaleza carbosilano conteniendo rutenio y cobre coordinados a ligandos base de Schiff, su preparación y sus usos, del 17 de Diciembre de 2019, de UNIVERSIDAD DE ALCALA.: La presente invención se refiere a metalodendrimeros de naturaleza carbosilano que contienen complejos metálicos coordinados a ligandos bases de Schiff. Además, la invención […]