Análogos de 2-fenoxipirimidinona.
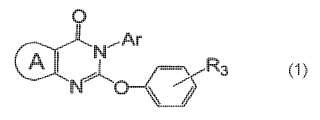
Un compuesto de la fórmula
o una sal farmacéuticamente aceptable o hidrato del mismo,
en la que:
representa un heteroarilo de 5 ó 6 miembros condensado que contiene 1, 2 ó 3 heteroátomos seleccionadosindependientemente de O, N y S, siendo los átomos anulares restantes carbono, en el que el heteroarilocondensado está opcionalmente sustituido con de 0 a 3 sustituyentes seleccionados independientemente deamino, hidroxi, alquilo de C1-C6, hidroxialquilo de C1-C6, (cicloalquil C3-C7)-alquilo de C0-C2, haloalquilo de C1-C6, alcoxi de C1-C6, alquil C2-C6-éter, alcanoil C1-C6 oxi, alquil C1-C6-sulfonilamino, alcanoil C1-C6-amino, ymono- o di-(alquil C1-C6)amino;
Ar es fenilo o un heteroarilo de 5 ó 6 miembros, cada uno de los cuales está sustituido con de 0 a 4sustituyentes que se seleccionan independientemente de halógeno, ciano, amino, nitro, alquilo de C1-C6,alquenilo de C2-C6, alquinilo de C2-C6, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6,haloalcoxi de C1-C6, (cicloalquil C3-C7)-alquilo de C0-C4, y mono- o di-(alquil C1-C6)amino; y
R3 representa de 0 a 4 sustituyentes, los cuales se seleccionan de forma independiente de halógeno, hidroxi,ciano, amino, nitro, alquilo de C1-C6, alquenilo de C2-C6, alquinilo de C2-C6, haloalquilo de C1-C6,hidroxialquilo de C1-C6, alcoxi de C1-C6, haloalcoxi de C1-C6, (cicloalquil C3-C7)-alquilo de C0-C4, mono- o di-(alquil C1-C6)amino, y mono- o di-(alquil C1-C6)aminosulfonilo, en el que el compuestso está opcionalmenteradiomarcado.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/018654.
Solicitante: NEUROGEN CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 35 NORTHEAST INDUSTRIAL ROAD BRANFORD, CT 06405 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GHOSH, MANUKA, BAKTHAVATCHALAM, RAJAGOPAL, BLUM, CHARLES, A., CHENARD, BERTRAND, L., XU,Jianjun, CAPITOSTI,SCOTT MICHAEL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/519 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensadas en orto o en peri con heterociclos.
- A61K31/522 A61K 31/00 […] › teniendo grupos oxo unidos directamente al heterociclo, p. ej. hipoxantina, guanina, aciclovir.
- A61P11/14 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Agentes antitusígenos.
- A61P25/02 A61P […] › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › para neuropatías periféricas.
- A61P25/06 A61P 25/00 […] › Agentes contra la migraña.
- A61P3/04 A61P […] › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › Anorexiantes; Medicamentos para el tratamiento de la obesidad.
- A61P35/04 A61P […] › A61P 35/00 Agentes antineoplásicos. › específicos para la metástasis.
- C07D471/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas condensados en orto.
- C07D473/30 C07D […] › C07D 473/00 Compuestos heterocíclicos que contienen sistemas cíclicos de purina. › unido en posición 6, p. ej. hipoxantina.
- C07D513/04 C07D […] › C07D 513/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tiene átomos de nitrógeno y azufre como únicos heteroátomos del ciclo, no previstos por los grupos C07D 463/00, C07D 477/00 ó C07D 499/00 - C07D 507/00. › Sistemas orto-condensados.
PDF original: ES-2399928_T3.pdf
Fragmento de la descripción:
Análogos de 2-fenoxipirimidinona
CAMPO DE LA INVENCIÓN
Esta invención se refiere en general a análogos de 2-fenoxipirimidinona que tienen propiedades farmacológicas útiles. La invención se refiere además al uso de tales compuestos para tratar afecciones relacionadas con la activación de los receptores de capsaicina, para detectar otros agentes que se unen al receptor de capsaicina, y como sondas para sondas para detectar y localizar receptores de capsaicina.
ANTECEDENTES DE LA INVENCIÓN
La percepción del dolor, o nocirrecepción, está mediada por los terminales periféricos de un grupo de neuronas sensoras especializadas, denominadas “nocirreceptores”. Una gran diversidad de estímulos físicos y químicos inducen la activación de tales neuronas en los mamíferos, conduciendo al reconocimiento de un estímulo potencialmente dañino. Sin embargo, la activación inadecuada o excesiva de nocirreceptores puede dar como resultado un dolor agudo o crónico debilitante.
El dolor neuropático implica transmisión de señales de dolor en ausencia de estímulo, y típicamente es el resultado del daño al sistema nervioso. En la mayoría de los casos, se cree que dicho dolor ocurre debido a la sensibilización en los sistemas nerviosos periférico y central después de un daño inicial al sistema periférico (v.g., por lesión directa o enfermedad sistémica) . El dolor neuropático es típicamente ardiente, punzante e implacable en su intensidad, y a veces puede ser más debilitante que el proceso inicial de lesión o enfermedad que lo indujo.
Los tratamientos existentes para el dolor neuropático son en gran medida ineficaces. Los opiáceos, tales como la morfina, son analgésicos potentes, pero su utilidad es limitada debido a efectos secundarios adversos, tales como adictividad física y propiedades de retirada, así como depresión respiratoria, cambios de humor, y motilidad intestinal reducida con estreñimiento, náusea, vómitos, y alteraciones concomitantes en los sistemas endocrino y nervioso autónomo. Adicionalmente, el dolor neuropático es frecuentemente insensible o sólo parcialmente sensible a los regímenes analgésicos convencionales con opioides. Los tratamientos que emplean el antagonista de N–metil–D– aspartato quetamina o el agonista alfa (2) –adrenérgico clonidina pueden reducir el dolor agudo o crónico, y permiten una reducción en el consumo de opioides, pero estos agentes son a menudo mal tolerados debido a efectos secundarios.
El tratamiento tópico con capsaicina ha sido utilizado para tratar el dolor crónico y agudo, incluyendo dolor neuropático. La capsaicina es una sustancia picante derivada de las plantas de la familia de las solanáceas (que incluye los pimientos picantes chili) , y parece actuar selectivamente sobre las fibras nerviosas aferentes de pequeño diámetro (fibras A–delta y C) que se cree median el dolor. La respuesta a la capsaicina se caracteriza por la activación persistente de nocirreceptores en los tejidos periféricos, seguida de desensibilización eventual de los nocirreceptores periféricos a uno o más estímulos. Como resultado de estudios en animales, parece ser que la capsaicina desencadena la despolarización de la membrana de las fibras C por apertura de canales catiónicos selectivos para calcio y sodio.
Respuestas similares son también provocadas por análogos estructurales de capsaicina que comparten un resto vainilloide común. Un análogo de este tipo es la resiniferatoxina (RTX) , un producto natural de las plantas Euphorbia. El término receptor vainilloide (VR) fue acuñado para describir el sitio de reconocimiento de la membrana neuronal para capsaicina y compuestos irritantes afines de este tipo. La respuesta a la capsaicina es inhibida competitivamente (y de ese modo antagonizada) por otro análogo de capsaicina, la capsazepina, y es inhibida también por el bloqueador de los canales catiónicos no selectivos rojo de rutenio, que se fija a VR con afinidad sólo moderada (típicamente con valores Ki no menores que 140 !M) .
Receptores vainilloides de rata y humanos han sido clonados a partir de células ganglionales de raíz dorsal. El primer tipo de receptor vainilloide que ha sido identificado se conoce como receptor vainilloide tipo 1 (VR1) , utilizándose los términos “VR1” y “receptor de capsaicina” de forma intercambiable en esta memoria para hacer referencia a receptores de rata y/o humanos de este tipo, así como homólogos de mamífero. El papel de VR1 en la sensación del dolor se ha confirma utilizando ratones que carecen de este receptor, que no exhiben comportamiento alguno de dolor provocado por vainilloides, ni respuestas alteradas al calor y la inflamación. VR1 es un canal catiónico no selectivo con un umbral para la apertura que está reducido en respuesta a temperaturas elevadas, pH bajo y agonistas de receptores de capsaicina. La apertura del canal del receptor de capsaicina va seguida generalmente de la liberación de péptidos inflamatorios a partir de neuronas que expresan el receptor y otras neuronas próximas, con aumento de la respuesta de dolor. Después de la activación inicial por capsaicina, el receptor de capsaicina sufre una desensibilización rápida vía fosforilación por una proteína cinasa dependiente de cAMP.
Debido a su aptitud para desensibilizar los nocirreceptores en los tejidos periféricos, los compuestos vainilloides agonistas de VR1 han sido utilizados como anestésicos tópicos. Sin embargo, la aplicación de agonistas puede causar por sí misma dolor ardiente, lo cual limita su uso terapéutico. Recientemente, se ha dado a conocer que los antagonistas de VR1, incluyendo compuestos no vainilloides, son útiles también para el tratamiento del dolor (véanse, v.g., las Publicaciones de Solicitudes de Patentes Internacionales PCT Números WO 02/08221, WO 03/062209, WO04/054582, WO 04/055003, WO 04/055004, WO 04/056774, WO 05/007646, WO 05/007648, WO 05/007652, WO 05/009977, WO 05/009980, WO 05/009982, WO 05/049601, WO 05/049613, WO 06/122200 y WO
06/120481) .
Así pues, los compuestos que interaccionan con VR1, pero no provocan la sensación dolorosa inicial de los compuestos vainilloides agonistas de VR1, son deseables para el tratamiento del dolor agudo y crónico, incluyendo el dolor neuropático, así como otras afecciones que son sensibles a la modulación del receptor de capsaicina. La presente invención satisface esta necesidad, y proporciona otras ventajas afines.
SUMARIO DE LA INVENCIÓN
La presente invención proporciona análogos de 2-fenoxipirimidinona de Fórmula A:
Fórmula A
así como sales farmacéuticamente aceptables, solvatos (por ejemplo hidratos) y ésteres de tales compuestos. En la fórmula A:
representa un heteroarilo de 5 ó 6 miembros condensado que contiene 1, 2 ó 3 heteroátomos en el anillo, seleccionándose dichos heteroátmos independientemente de O, N y S, siendo los átomos anulares restantes carbono, en el que el heteroarilo condensado está opcionalmente sustituido; preferiblemente, el heteroarilo condensado está sustituido con de 0 a 3, o de 0 a 2, sustituyentes seleccionados independientemente de amino, hidroxi, alquilo de C1-C6, hidroxialquilo de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C2, haloalquilo de C1-C6, alcoxi de C1-C6, alquil C2-C6-éter, alcanoil C1-C6-oxi, alquil C1-C6-sulfonilamino, alcanolil C1-C6-amino, y mono- o di- (alquil C1-C6) amino;
Ar es fenilo o un heteroarilo de 5 ó 6 miembros, cada uno de los cuales está opcionalmente sustituido, y cada uno de los cuales está preferiblemente sustituido con de 0 a 4 o de 0 a 3 sustituyentes que se seleccionan independientemente de halógeno, ciano, amino, nitro, alquilo de C1-C6, alquenilo de C2-C6, alquinilo de C2-C6, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6, haloalcoxi de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C4, y mono- o di- (alquil C1-C6) amino; y
R3 representa de 0 a 4, o de 0 a 3, sustituyentes, los cuales se seleccionan preferiblemente de forma independiente de halógeno, hidroxi, ciano, amino, nitro, alquilo de C1-C6, alquenilo de C2-C6, alquinilo de C130 C6, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6, haloalcoxi de C1-C6, (cicloalquil C3-C7)
alquilo de C0-C4, mono- o di- (alquil C1-C6) amino, y mono- o di- (alquil C1-C6) aminosulfonilo.
La presente invención proporciona además análogos de 2-fenoxipirimidinona de Fórmula I:
Fórmula I
así como sales farmacéuticamente aceptables, solvatos (por ejemplo hidratos) y ésteres de tales compuestos. En la 35 fórmula I:
y R3 son como se describen para la Fórmula A; 10
X
es N o CH, que está opcionalmente... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de la fórmula o una sal farmacéuticamente aceptable o hidrato del mismo, en la que:
representa un heteroarilo de 5 ó 6 miembros condensado que contiene 1, 2 ó 3 heteroátomos seleccionados independientemente de O, N y S, siendo los átomos anulares restantes carbono, en el que el heteroarilo condensado está opcionalmente sustituido con de 0 a 3 sustituyentes seleccionados independientemente de amino, hidroxi, alquilo de C1-C6, hidroxialquilo de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C2, haloalquilo de C1-C6, alcoxi de C1-C6, alquil C2-C6-éter, alcanoil C1-C6-oxi, alquil C1-C6-sulfonilamino, alcanoil C1-C6-amino, y mono- o di- (alquil C1-C6) amino;
Ar es fenilo o un heteroarilo de 5 ó 6 miembros, cada uno de los cuales está sustituido con de 0 a 4 sustituyentes que se seleccionan independientemente de halógeno, ciano, amino, nitro, alquilo de C1-C6, alquenilo de C2-C6, alquinilo de C2-C6, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6, haloalcoxi de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C4, y mono- o di- (alquil C1-C6) amino; y
R3 representa de 0 a 4 sustituyentes, los cuales se seleccionan de forma independiente de halógeno, hidroxi, ciano, amino, nitro, alquilo de C1-C6, alquenilo de C2-C6, alquinilo de C2-C6, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6, haloalcoxi de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C4, mono- o di (alquil C1-C6) amino, y mono- o di- (alquil C1-C6) aminosulfonilo, en el que el compuestso está opcionalmente radiomarcado.
2. Un compuesto o sal o hidrato del mismo según la reivindicación 1, en el que el compuesto tiene la fórmula:
en la que:
representa un heteroarilo de 5 ó 6 miembros condensado que contiene 1, 2 ó 3 heteroátomos seleccionado independientemente de O, N y S, y está sustituido con de 0 a 2 sustituyentes seleccionados independientemente de amino, hidroxi, alquilo de C1-C6, hidroxialquilo de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C2, haloalquilo de C1-C6, alcoxi de C1-C6, alquil C2-C6-éter, alcanoil C1-C6-oxi, alquil C1-C6-sulfonilamino, alcanolil C1-C6-amino, y mono-o di- (alquil C1-C6) amino;
X es N o CH, que está opcionalmente sustituido con un sustituyente representado por R1;
R1 representa de 0 a 3 sustituyentes seleccionados de forma independiente de halógeno, ciano, amino, nitro, alquilo de C1-C6, alquenilo de C2-C6, alquinilo de C2-C6, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6, haloalcoxi de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C4, y mono- o di- (alquil C1-C6) amino; y
R3 representa de 0 a 3, sustituyentes seleccionados de forma independiente de halógeno, hidroxi, ciano, amino, nitro, alquilo de C1-C6, alquenilo de C2-C6, alquinilo de C1-C6, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6, haloalcoxi de C1-C6, (cicloalquil C3-C7) -alquilo de C0-C4, mono- o di- (alquil C1C6) amino, y mono- o di- (alquil C1-C6) aminosulfonilo.
3. Un compuesto o sal o hidrato del mismo según la reivindicación 1 o la reivindicación 2, en el que
es un heteroarilo de 5 miembros que está sustituido con de 0 a 2 sustituyentes seleccionados independientemente de alquilo de C1-C4, (cicloalquilo de C3-C5) alquilo de C0-C2 y haloalquilo de C1-C4.
4. Un compuesto o sal o hidrato del mismo según la reivindicación 3, en el que
es o en las que R2 es hidrógeno, alquilo de C1-C4, haloalquilo de C1-C4 o cicloalquilo de C3-C5.
5. Un compuesto o sal o hidrato del mismo según la reivindicación 1 o la reivindicación 2, en el que
es un heteroarilo de 6 miembros que está sustituido con de 0 a 3 sustituyentes seleccionados independientemente de hidroxi, alquilo de C1-C6, (cicloalquilo de C3-C7) alquilo de C0-C2, haloalquilo de C1-C6, hidroxialquilo de C1-C6, alcoxi de C1-C6, mono (alquilo de C1-C6) amino, alcanoilamino de C1-C6 o alquilsulfonilamino de C1-C6.
6. Un compuesto o sal o hidrato del mismo según la reivindicación 5, en el que
es en el que R4 representa de 1 a 3 sustituyentes seleccionados independientemente de hidroxi, alquilo de C1-C4, (cicloalquilo de C3-C5) alquilo de C0-C2, haloalquilo de C1-C4, hidroxialquilo de C1-C4, alcoxi de C1-C4, mono (alquilo de C1-C4) amino, alcanoilamino de C1-C4 o alquilsulfonilamino de C1-C4.
7. Un compuesto o sal o hidrato del mismo según una cualquiera de las reivindicaciones 2-6, en el que R1 representa de 1 a 3 sustituyentes seleccionados independientemente de halógeno, ciano, alquilo de C1-C4 y haloalquilo de C1-C4.
8. Un compuesto o sal o hidrato del mismo según la reivindicación 7, en el que un sustituyente representado por R1 es un halógeno o un ciano en la posición para.
9. Un compuesto o sal o hidrato del mismo según la reivindicación 7 o reivindicación 8, en el que R1 representa 30 exactamente un sustituyente.
10. Un compuesto o sal o hidrato del mismo según una cualquiera de las reivindicaciones 1-9, en el que R3 representa de 1 a 3 sustituyentes seleccionados independientemente de halógeno, ciano, alquilo de C1-C6, haloalquilo de C1-C6 y alcoxi de C1-C6.
11. Un compuesto o sal o hidrato del mismo según la reivindicación 2, en el que el compuesto tiene la fórmula:
o en las que: R2 es hidrógeno, alquilo de C1-C4, haloalquilo de C1-C4 o cicloalquilo de C3-C5; R3 representa de 1 a 3 sustituyentes seleccionados independientemente de halógeno, ciano, alquilo de C1-C4,
haloalquilo de C1-C4 y alcoxi de C1-C4; 10 y R5 es halógeno o CN,
o en el que el compuesto tiene la fórmula:
o en las que: R3 representa de 1 a 3 sustituyentes seleccionados independientemente de halógeno, ciano, alquilo de C1-C4,
haloalquilo de C1-C4 y alcoxi de C1-C4; y R5 es halógeno o CN,
o en el que el compuesto tiene la fórmula:
o en las que: R2 es hidrógeno, alquilo de C1-C4, haloalquilo de C1-C4 o cicloalquilo de C3-C5; R3 representa de 1 a 3 sustituyentes seleccionados independientemente de halógeno, ciano, alquilo de C1-C4,
haloalquilo de C1-C4 y alcoxi de C1-C4; y R5 es halógeno o CN,
o en el que el compuesto tiene la fórmula:
o en las que: R3 representa de 1 a 3 sustituyentes seleccionados independientemente de halógeno, ciano, alquilo de C1-C4,
haloalquilo de C1-C4 y alcoxi de C1-C4; R4 representa de 0 a 2 sustituyentes seleccionados independientemente de hidroxi, alquilo de C1-C4, (cicloalquil C3
C5) -alquilo de C0-C2, haloalquilo de C1-C4, hidroxialquilo de C1-C4, alcoxi de C1-C4, mono- (alquil C1-C4) amino, alcanoil C1-C4-amino o alquil C1-C4-sulfonilamino; y R5 es halógeno o CN.
12. Un compuesto o sal o hidrato del mismo según la reivindicación 1, en el que el compuesto es: 1- (4-bromofenil) -9-metil-2- (2, 3, 4-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -2- (2, 3-difluorofenoxi) -9-metil-1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -2- (2, 4-difluorofenoxi) -9-metil-1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -2-[2-fluoro-3- (trifluorometil) fenoxi]-9-metil-1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -9-metil-2- (2, 3, 4-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -9-metil-2- (2, 3, 5-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -9-metil-2- (2, 3, 6-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -9-metil-2- (2, 4, 5-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -9-metil-2- (2, 4, 6-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-clorofenil) -9-metil-2- (3, 4, 5-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-fluorofenil) -2-[2-fluoro-3- (trifluorometil) fenoxi]-9-metil-1, 9-dihidro-6H-pufin-6-ona; 1- (4-fluorofenil) -2-[3-fluoro-5- (trifluorometil) fenoxi) -9-metil-1, 9-dihidro-6H-purin-6-ona; 1- (4-fluorofenil) -9-metil-2- (2, 3, 4-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-fluorofenil) -9-metil-2- (2, 3, 5-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-fluorofenil) -9-metil-2- (2, 3, 6-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-fluorofenil) -9-metil-2- (2, 4, 5-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-fluorofenil) -9-metil-2- (2, 4, 6-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; 1- (4-fluorofenil) -9-metil-2-[3- (trifluorometil) fenoxi]-1, 9-dihidro-6H-purin-6-ona; 1- (6-cloropiridin-3-il) -9-metil-2- (3, 4, 5-trifluorofenoxi) -1H-purin-6 (9H) -ona; 2- (2, 3-difluoro-4-metoxifenoxi) -1- (4-fluorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona; 2- (2, 3-difluoro-4-metoxifenoxi) -9-etil-1- (4-fluorofenil) -1, 9-dihidro-6H-purin-6-ona; 2- (2, 3-difluorofenoxi) -1- (4-fluorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona; 2- (2, 3-difluorofenoxi) -9-etil-1- (4-fluorofenil) -1, 9-dihidro-6H-purin-6-ona; 2- (2, 3-dimetoxifenoxi) -3- (4-fluorofenil) -7-metiltieno[3, 2-d]pirimidin-4 (3H) -ona; 2- (2, 3-dimetilfenoxi) -1- (4-fluorofenil) -9-metil-1, 9-dihidro-6H-purin-ona; 2- (2, 4-difluorofenoxi) -1- (4-fluorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona; 2- (2, 4-difluorofenoxi) -3- (4-fluorofenil) pirido[3, 2-d]pirimidin-4 (3H) -ona; 2- (2, 4-difluorofenoxi) -9-etil-1- (4-fluorofenil) -1, 9-dihidro-6H-purin-6-ona; 2- (2, 6-dimetilfenoxi) -1- (4-fluorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona; 2- (2-cloro-4-fluorofenoxi) -1- (4-clorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona;
2- (2-cloro-4-fluorofenoxi) -1- (4-fluorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona; 2- (2-etilfenoxi) -3- (4-fluorofenil) -7-metiltieno[3, 2-d]pirimidin-4 (3H) -ona; 2- (4-cloro-2-fluorofenoxi) -1- (4-clorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona; 2- (4-cloro-2-fluorofenoxi) -1- (4-fluorofenil) -9-metil-1, 9-dihidro-6H-purin-6-ona; 2- (4-cloro-2-fluorofenoxi) -3- (4-clorofenil) -7-metiltieno[3, 2-d]pirimidin-4 (3H) -ona;
2- (4-cloro-2-fluorofenoxi) -3- (4-fluorofenil) -7-metiltieno[3, 2-d]pirimidin-4 (3H) -ona; 2- (4-cloro-2-fluorofenoxi) -9-etil-1- (4-fluorofenil) -1, 9-dihidro-6H-purin-6-ona; 2, 3-difluoro-4-{[1- (4-fluorofenil) -9-metil-6-oxo-6, 9-dihidro-1H-purin-2-il]oxi}benzonitrilo; 2-[2-cloro-3- (trifluorometil) fenoxi]-3- (4-fluorofenil) pirido[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-clorofenil) -2- (2, 4-difluorofenoxi) -7-metiltieno[3, 2-d]pirimidin-4 (3H) -ona;
3- (4-clorofenil) -7-metil-2- (2, 3, 4-trifluorofenoxi) tieno[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-fluorofenil) -2- (2, 3, 4-trifluorofenoxi) pirido[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-fluorofenil) -2- (2-isopropilfenoxi) -7-metiltieno[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-fluorofenil) -2- (2-metoxifenoxi) -7-metiltieno[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-fluorofenil) -2-[3- (trifluorometil) fenoxi]pirido[3, 2-d]pirimidin-4 (3H) -ona;
3- (4-fluorofenil) -2-[3-fluoro-5- (trifluorometil) fenoxi]pirido[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-fluorofenil) -4-oxo-2- (2, 3, 4-trifluorofenoxi) -3, 4-dihidrotieno[3, 2-d]pirimidin-7-carbonitrilo; 3- (4-fluorofenil) -7-metil-2- (2, 3, 4-trifluorofenoxi) tieno[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-fluorofenil) -7-metil-2- (2, 3, 6-trifluorofenoxi) tieno[3, 2-d]pirimidin-4 (3H) -ona; 3- (4-fluorofenil) -7-metil-2- (2-metilfenoxi) tieno[3, 2-d]pirimidin-4 (3H) -ona;
4-{[1-4-clorofenil) -9-metil-6-oxo-6, 9-dihidro-1H-purin-2-il]oxi}-2, 3-difluorobenzonitrilo; 5- (2, 3-difluorofenoxi) -6- (4-fluorofenil) [1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 5- (4-cloro-2-fluorofenoxi) -6- (4-fluorofenil) [1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 5- (9-Metil-6-oxo-2- (3, 4, 5-trifluorofenoxi) -6H-purin-1 (9H) -il) picolinonitrilo; 5-[2-cloro-3- (trifluorometil) fenoxi]-6- (4-fluorofenil) [1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona;
6- (4-fluorofenil) -5- (2, 3, 4-trifluorofenoxi) [1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 6- (4-fluorofenil) -5- (2, 3, 5-trifluorofenoxi) [1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 6- (4-fluorofenil) -5- (2, 4, 5-trifluorofenoxi) [1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 6- (4-fluorofenil) -5- (3- (trifluorometil) fenoxi) tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 6- (4-fluorofenil) -5- (3, 4, 5-trifluorofenoxi) [1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona;
6- (4-fluorofenil) -5-[2-fluoro-3- (trifluorometil) fenoxi][1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 6- (4-fluorofenil) -5-[3-fluoro-5- (trifluorometil) fenoxi][1, 3]tiazolo[5, 4-d]pirimidin-7 (6H) -ona; 9-etil-1- (4-fluorofenil) -2- (2, 3, 4-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona;
9. etil-1- (4-fluorofenil) -2- (2, 3, 5-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona;
9. etil-1- (4-fluorofenil) -2- (2, 4, 5-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona; o 9-etil-1- (4-fluorofenil) -2- (2, 4, 6-trifluorofenoxi) -1, 9-dihidro-6H-purin-6-ona.
13. Una composición farmacéutica, que comprende al menos un compuesto o sal o hidrato del mismo según una cualquiera de las reivindicaciones 1–12, en combinación con un vehículo o excipiente fisiológicamente aceptable.
14. Un método in vitro para reducir la conductancia del calcio de un receptor de capsaicina celular, que comprende poner en contacto una célula que expresa un receptor de capsaicina con al menos un compuesto o sal o hidrato del mismo según una cualquiera de las reivindicaciones 1–12, y reducir de ese modo la conductancia del calcio del receptor de capsaicina.
15. Un método para inhibir la unión de un ligando vainilloide a un receptor de capsaicina in vitro, comprendiendo el método poner en contacto el receptor de capsaicina con al menos un compuesto o sal o hidrato del mismo según cualquiera de las reivindicacionas 1-12, , en condiciones y en cantidad suficientes para inhibir detectablemente la unión del ligando vainilloide al receptor de capsaicina.
16. Una preparación farmacéutica empaquetada, que comprende:
(a) una composición farmacéutica según la reivindicación 13 en un recipiente; y
(b) instrucciones para utilizar la composición a fin de tratar dolor, tos o hipo, obesidad, o incontinencia urinaria, o vejiga hiperactiva.
17. El uso de un compuesto o sal o hidrato del mismo según cualquiera de las reivindicacionas 1-12 para la fabricación de un medicamento para tratar una afección sensible a la modulación del receptor de capsaicina, en el que la afección es asma, enfermedad pulmonar obstructiva crónica, prurito, tos, hipo, obesidad, síntomas de la menopausia, incontinencia urinaria, vejiga hiperactiva, exposición a capsaicina, quemadura o irritación debida a exposición a calor, quemadura o irritación debida a exposición a luz, quemadura, broncoconstricción o irritación debida a exposición a gas lacrimógeno, agentes infecciosos, contaminantes del aire o espray de pimienta, quemadura o irritación debida a exposición a ácido; dolor, en el que el dolor está asociado opcionalmente a una afección seleccionada de: síndrome de dolor tras mastectomía, dolor de muñón, dolor de miembro fantasma, dolor neuropático oral, dolor de muelas, neuralgia post–herpética, neuropatía diabética, distrofia simpática refleja, neuralgia del trigémino, osteoartritis, artritis reumatoide, fibromialgia, síndrome de Guillain–Barre, meralgia parestésica, síndrome de boca ardiente, neuropatía periférica bilateral, causalgia, neuritis, neuronitis, neuralgia, neuropatía relacionada con SIDA, neuropatía relacionada con MS, dolor relacionado con lesión en la médula espinal, dolor relacionado con cirugía, dolor músculoesquelético, dorsalgia, cefalea, migraña, angina, parto, hemorroides, dispepsia, dolores de Charcot, gases intestinales, menstruación, cáncer, exposición a venenos, síndrome de intestino irritable, enfermedad intestinal inflamatoria y traumatismo; o dolor neuropático.
Patentes similares o relacionadas:
NANOPARTÍCULAS TERAPÉUTICAS QUE ENCAPSULAN TERPENOIDES Y/O CANNABINOIDES, del 14 de Mayo de 2020, de GBS GLOBAL BIOPHARMA: En el presente documento se proporcionan nanopartículas de PEGA que encapsulan terpenoides y cannabinoides y composiciones farmacéuticas que comprenden […]
Compuestos o-quinónicos como agentes neutralizantes del óxido nítrico, del 29 de Abril de 2020, de INSTITUT DES SUBSTANCES VEGETALES: Compuesto de fórmula (I) **(Ver fórmula)** en la que R1 se selecciona entre el grupo que constituido por: • -CH=CH-COOR2 […]
Composición para el tratamiento de la cavidad de la garganta/orofaringe, del 25 de Marzo de 2020, de MARIA CLEMENTINE MARTIN KLOSTERFRAU VERTRIEBSGESELLSCHAFT MBH: Composición en forma de una dosificación líquida para su utilización en el tratamiento profiláctico o terapéutico de enfermedades inflamatorias de la cavidad oral y/o […]
Composición basada en plantas para su utilización en el tratamiento de la tos, del 3 de Julio de 2019, de ABOCA S.P.A. SOCIETA'' AGRICOLA: Composición para su utilización en el tratamiento de la tos que consiste en: azúcar de caña, miel, agua desionizada, zumo de limón, extracto de Plantago […]
Orvepitant para el tratamiento de la tos crónica, del 26 de Junio de 2019, de NeRRe Therapeutics Limited: El ácido 2-(R)-(4-fluoro-2-metil-fenil)-4-(S)-((8aS)-6-oxo-hexahidro-pirrolo[1,2-α]-pirazin-2-il)-piperidin-1- carboxílico [1-(R)-(3,5-bis-trifluorometil-fenil)-etil]-metilamida…
DROPROPIZINA EN COMBINACIÓN CON AMBROXOL EN LA FORMA FARMACÉUTICA DE JARABE Y TABLETAS, del 23 de Mayo de 2019, de PRODUCTOS FARMACÉUTICOS, S.A. DE C.V: La presente invención se refiere a una combinación farmacéutica de ambroxol o una sal farmacéuticamente aceptable del mismo y dropropizina. Asimismo, se refiere a una […]
Composición farmacéutica que contiene flurbiprofeno, del 15 de Mayo de 2019, de Reckitt Benckiser Healthcare International Limited: Un AINE o una sal farmacéuticamente aceptable del mismo para su uso en el tratamiento tópico de la tos en la membrana mucosa de la garganta de una persona que necesita tratamiento […]
Compuestos de quinina e isómeros ópticos, procedimiento de preparación y uso médico de los mismos, del 27 de Febrero de 2019, de Beijing Shuobai Pharmaceutical Co., Ltd: Compuesto de fórmula I:**Fórmula** o una sal, solvato o isómero óptico de la misma farmacéuticamente aceptables, en donde en la fórmula I: n se selecciona entre […]