SISTEMA PARA LA MEDICIÓN, REGISTRO Y MONITORIZACIÓN CONTINUA DE LA PERFUSIÓN TISULAR ESPLÁCNICA Y EL ESPACIO MUERTO FISIOLÓGICO PULMONAR, Y SU USO.
Sistema para la medición, registro y monitorización continua de la perfusión tisular esplácnica y el espacio muerto fisiológico pulmonar,
y su uso.
La presente invención hace referencia a un nuevo sistema para medir, registrar y monitorizar la perfusión tisular esplácnica y el espacio muerto fisiológico pulmonar de forma automatizada, tanto continua como intermitente y en tiempo real, que es fácilmente manejable y genera información fácilmente interpretable. Dicho sistema comprende al menos cuatro dispositivos de medida de parámetros médicos, conectados a un dispositivo que recibe, convierte, almacena, integra, procesa, y permite el manejo y visualización de los datos registrados en las mediciones y de los parámetros estimados mediante el mismo. Para ello, dicho dispositivo comprende un programa informático específico de estimación de parámetros relacionados con la medida de la perfusión tisular esplácnica y el espacio muerto fisiológico pulmonar, a partir de los datos procedentes de los dispositivos de medida. Asimismo, la presente invención se refiere al uso del dispositivo para medir, registrar y monitorizar la perfusión tisular esplácnica y el espacio muerto fisiológico pulmonar.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200901119.
Solicitante: MUÑOZ BONET, JUAN IGNACIO.
Nacionalidad solicitante: España.
Inventor/es: MUÑOZ BONET,JUAN IGNACIO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B5/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › Medidas encaminadas a establecer un diagnóstico (diagnóstico por medio de radiaciones A61B 6/00; diagnóstico por ondas ultrasónicas, sónicas o infrasónicas A61B 8/00 ); Identificación de individuos.
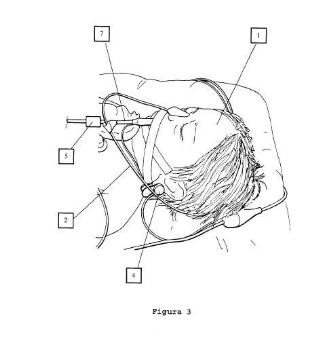
Fragmento de la descripción:
Sistema para la medición, registro y monitorización continua de la perfusión tisular esplácnica y el espacio fisiológico pulmonar, y su uso.
Campo de la invención
La presente invención se engloba en el campo de la medicina, concretamente del cuidado médico intensivo y la cirugía mayor, específicamente para el diagnóstico de shock oculto.
Antecedentes de la invención
Ante un inadecuado aporte de oxígeno, la célula utiliza la glucólisis anaerobia en un intento por mantener la función celular normal, lo que ocasiona un acumulo de ácido láctico y la liberación de hidrogeniones provenientes de la hidrólisis del ATP, provocando una disminución del pH tisular (referencia bibliográfica (1)). De este modo, los cambios tempranos en el pH tisular son útiles para evaluar la oxigenación de ese tejido y el estado de su microcirculación (2).
En el paciente grave, cuando se agotan los mecanismos de compensación para mantener una adecuada oxigenación en todos los tejidos, la respuesta neurohumoral del organismo provoca una redistribución del flujo sanguíneo encaminada a preservar la función de "órganos nobles" como cerebro y corazón, a expensas de disminuir la perfusión de "órganos no vitales" como la piel y el territorio esplácnico (3). A diferencia de la piel, el territorio esplácnico y especialmente la mucosa intestinal posee unas necesidades metabólicas elevadas, que junto a determinadas características anatómicas que la hacen especialmente susceptible a la hipoxia, explican que el intestino sea el primer órgano en afectarse ante situaciones de hipoperfusión/hipoxia y el último en recuperarse (2, 4). Por ello, la valoración de la oxigenación tisular a este nivel, mediante la monitorización del pH intramucoso gástrico (pHi), nos permitirá detectar precozmente estas situaciones y prevenir su agravamiento posterior, así como asegurar una recuperación completa tras un episodio de shock manifiesto (2, 4, 5).
El pHi puede ser medido con un microelectrodo insertado en la mucosa gástrica, pero la invasividad del método, la imposibilidad de recalibración in vivo y la frecuente desinserción del electrodo, lo hacen impracticable en la clínica (6). Por ello, recurrimos a la medición indirecta del pHi, basándonos en el principio de la tonometría, por el que los gases difunden libremente a través de los tejidos. Así, en 1959 Boda y Murányi (7) realizaron una estimación de la PCO2 arterial en más de 4 00 niños ventilados mecánicamente por poliomielitis, utilizando una sonda de tonometría similar a las actuales e insertada en el estómago a través de la nariz. Su experiencia clínica les llevó a concluir que: 1) La tensión de CO2 arterial puede ser estimada con razonable exactitud con el método gastrotonométrico. 2) En pacientes en situación de shock severo la PCO2 del tonómetro puede ser engañosamente elevada. Sin embargo, no interpretan el porqué de este último hecho. Estos resultados fueron confirmados posteriormente por Bergofsky (8) al demostrar que el fluido en la luz de un órgano hueco (vejiga urinaria, vesícula biliar, estómago), equilibra la tensión de los gases (PO2 y PCO2) con la de las células y tejidos que lo contienen, y estos a su vez con los de la sangre que los irriga. Y simultáneamente también por Dawson (9) que observó en animales de experimentación como la PO2 y la PCO2 medida en el suero salino instilado en bolsas de intestino experimentaban cambios proporcionales a los de la sangre. Por tanto, la medición de la Presión de CO2 en el gas de la luz del intestino es equivalente a la Presión de CO2 en la mucosa intestinal (10).
En 1982 Fiddian-Green et al (11) utilizan estas observaciones para postular que el pH de la mucosa intestinal puede ser calculado de modo indirecto. Esta hipótesis se basa en dos asunciones: 1) La PCO2 medida tonométricamente se aproxima a la de la mucosa intestinal, ya que el CO2, por su alta capacidad de difusión, alcanza con rapidez el equilibrio entre el tejido y la luz intraluminal. 2) La concentración de bicarbonato en la mucosa intestinal está en equilibrio con la del lecho capilar intestinal, y ésta a su vez, con la de la sangre arterial (1). De este modo, el cálculo del pHi puede realizarse mediante una modificación de la ecuación de Henderson-Hasselbalch:
Donde 6,1 es el pK del sistema HCO3-/CO2 en plasma a 37ºC; [HCO3-] es la concentración arterial de bicarbonato (mM/L); PgCO2 es la PCO2 de la sonda de tonometría ajustada al tiempo de equilibrio; 0,03 la constante de solubilidad del CO2 en plasma a 37ºC.
Así pues, las engañosas elevaciones de la PCO2 del estómago en relación con la PCO2 arterial, observadas por Boda y Murányi en pacientes en situación de shock grave, se corresponderían con caídas del pHi a consecuencia de la hipoperfusión regional tisular. Grum et al, en 1984 desarrollan una sonda de tonometría que constituye la base de los actuales equipos comerciales. Utilizando este equipo en perros, observaron como el pHi permanecía constante mientras el flujo sanguíneo se mantuviera por encima de un valor crítico. Por debajo de éste el pHi disminuía. Además, estos descensos del pHi se acompañaron de descensos en el consumo de O2. En 1990 Antonsson et al (6) validan la técnica en un modelo experimental, mediante la comparación del pHi calculado tonométricamente con el obtenido desde microelectrodos implantados directamente en la mucosa del estómago.
Clásicamente, se han utilizado otros 2 parámetros derivados. Para su cálculo se utilizan los valores de pH arterial (pHa), obtenido con el análisis de una muestra de sangre arterial y el pHi, calculado mediante la ecuación 1.
Según el lugar en que se realice la medición del CO2 de la luz del tubo digestivo (PgCO2) se diferencian 2 tipos de medición:
1) Tonometría con análisis del CO2 fuera del organismo: la técnica consiste en la colocación de una sonda nasogástrica que dispone de un balón de silicona terminal permeable al CO2 que se deja alojado en estómago. Es radiopaco para facilitar su correcta ubicación por Rx. Es por tanto, una técnica mínimamente invasiva. El análisis requiere la extracción de las muestras para ser analizadas. Existen dos modalidades según el medio con que se rellene el balón:
Reivindicaciones:
1. Sistema para medir, registrar y monitorizar la perfusión tisular esplácnica y el espacio muerto fisiológico pulmonar, que comprende al menos:
caracterizado porque dicho sistema comprende además:
2. Sistema según la reivindicación 1, caracterizado porque la sonda del dispositivo (a) puede ser colocada en el estómago o en el colon recto-sigmoideo.
3. Sistema según una cualquiera de las reivindicaciones 1 ó 2, caracterizado porque el sensor de capnografía transcutáneo del dispositivo (c) es preferentemente un oxicapnógrafo transcutáneo para el lóbulo de la oreja, que puede ser utilizado en pacientes de cualquier edad.
4. Sistema según una cualquiera de las reivindicaciones 1 a 3, caracterizado porque el programa informático (f5) de estimación de parámetros realiza las siguientes estimaciones:
5. Sistema según una cualquiera de las reivindicaciones 1 a 4, caracterizado porque el dispositivo (d) mide además la presión espiratoria media de CO2, PECO2, colocando el sensor/sonda de CO2 espiratorio en el interior de una bolsa estanca colocada en la salida espiratoria del ventilador mecánico, y calcula el espacio muerto fisiológico pulmonar, VD/VT, a partir de la relación entre:
6. Sistema según una cualquiera de las reivindicaciones 1 a 5, caracterizado porque las conexiones (e) en los dispositivos (a), (c) y (d) se realizan a través de sus puertos serie RS-232, y en el dispositivo (b) a través de su conexión de red Ethernet, dado que su ubicación suele ser remota.
7. Sistema según una cualquiera de las reivindicaciones 1 a 6, caracterizado porque el programa informático (f5) estima además los siguientes parámetros relacionados con la medida continua de la perfusión tisular esplácnica:
8. Sistema según una cualquiera de las reivindicaciones 1 a 7, caracterizado porque el dispositivo (f) de recepción, conversión, almacenamiento, integración, procesamiento, manejo y visualización de la información es un ordenador personal.
9. Uso del dispositivo descrito en una cualquiera de las reivindicaciones anteriores para medir, registrar y monitorizar la perfusión tisular esplácnica y el espacio muerto fisiológico pulmonar en tiempo real y de forma automatizada, ya sea de forma intermitente o en continuo dependiendo del parámetro a medir, caracterizado porque dicha medición, dicho registro y dicha monitorización comprenden al menos las siguientes etapas:
10. Uso según la reivindicación 9, caracterizado por la medición de la etapa 1) se realiza en uno de los órganos seleccionados entre estómago y colón recto-sigmoide.
11. Uso según la reivindicación 10, caracterizado porque cuando la medición de la etapa 1) se lleva a cabo en el estómago, se inhibe la secreción ácida de dicho órgano mediante administración de uno de los compuestos seleccionados entre anti-H2 o inhibidores de la bomba de protones, para incrementar la fiabilidad de la medida.
12. Uso según una cualquiera de las reivindicaciones 9 a 11, caracterizado porque en la etapa 3) se calibra "in vivo" el dispositivo (c) al inicio de la medición introduciendo un valor de la PaCO2 de una muestra de sangre.
13. Uso según una cualquiera de las reivindicaciones 9 a 12, caracterizado porque en la etapa 4) el PECO2 se mide mediante la colocación del sensor/sonda de CO2 espirado en una bolsa grande estanca conectada en la salida espiratoria del ventilador mecánico, donde se acumula el gas espirado y se determina la Presión de dicho gas en dicha bolsa.
Patentes similares o relacionadas:
Sistema y procedimiento para evaluar el riesgo asociado con un estado de glucosa, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un dispositivo informático configurado para realizar un procedimiento de análisis de un estado de glucosa, comprendiendo el procedimiento: identificar, […]
Procedimiento y aparato para proporcionar el procesamiento y control de datos en un sistema de comunicación médica, del 29 de Julio de 2020, de ABBOTT DIABETES CARE INC: U procedimiento, que comprende: ejecutar, en una unidad receptora , una rutina predeterminada asociada con una operación de un dispositivo de monitorización […]
 Dispositivo sensor para detección de señales bioeléctricas, del 29 de Julio de 2020, de CorTec GmbH: Dispositivo sensor para detectar senales bioelectricas y para implantar dentro o fuera de un cerebro, el dispositivo sensor que comprende […]
Dispositivo sensor para detección de señales bioeléctricas, del 29 de Julio de 2020, de CorTec GmbH: Dispositivo sensor para detectar senales bioelectricas y para implantar dentro o fuera de un cerebro, el dispositivo sensor que comprende […]
FUNDA ELECTRÓNICA PARA ADAPTACIÓN DE DISPOSITIVOS MÓVILES CON INSTRUMENTOS DE DIAGNÓSTICO MÉDICO MULTIDISCIPLINAR, del 27 de Julio de 2020, de RUESGA DELGADO,OSCAR: Funda electrónica para adaptación de dispositivos móviles con instrumentos de diagnóstico médico multidisciplinar que comprende una funda de uso electrónico […]
Cama eléctrica, del 8 de Julio de 2020, de Keeson Technology Corporation Limited: Una cama eléctrica, que comprende una estructura de cama, una pluralidad de láminas de cama, un dispositivo de despertador, un reloj y una caja de control […]
SÍSTEMA Y MÉTODO PARA EL TRATAMIENTO DE ADICCIONES DE UN INDIVIDUO QUE LO NECESITE, CON BAJAS TASAS DE RELAPSO, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención corresponde a un sistema, más particularmente a un sistema NFB, y método, que permite el tratamiento de adicciones en las que está […]
Aparato y método de algometría humana, del 1 de Julio de 2020, de The Children's Research Institute: Un método implementado por el procesador para medir objetivamente el dolor que comprende: aplicar estimulación eléctrica de una intensidad específica […]
MAMÓGRAFO ÓPTICO QUE UTILIZA INFRARROJO CERCANO EN GEOMETRÍA DE REFLECTANCIA DIFUSA, del 25 de Junio de 2020, de CONSEJO NACIONAL DE INVESTIGACIONES CIENTIFICAS Y TECNICAS (CONICET) (33.3%): Un dispositivo formador de imágenes mamográficas para análisis y detección de posibles inhomogeneidades en el tejido mamario de una paciente usando […]