MÉTODO PARA EL PROCESAMIENTO DEL TEJIDO ÓSEO ALOGÉNICO Y RECIPIENTE PARA LLEVARLO A CABO.
Método para el procesamiento del tejido óseo alogénico,y recipiente para llevarlo a cabo,
que comprende los siguientes cuatro procedimientos de aplicación sucesiva:
- Lavado individualizado de cada aloinjerto óseo en recipiente hermético y sumergido en suero fisiológico a 60°c durante 10 minutos y seguido 1 minuto de agitación manual enérgica.
- Centrifugación individualizada de cada aloinjerto, a 2.000 revoluciones por minuto durante 15 minutos para 1500 g. en recipiente especifico de PVC.
- Pasteurización individualizada de cada aloinjerto durante 90 minutos en recipiente estéril hermético con suero fisiológico precalentado a 60°C.
- Control microbiológico final, pesando el suero de la pasteurización a través de filtro de papel con tamaño de poro de 0,45 {mi}m, y cultivando dicho filtro en medio de cultivo para microorganismos aerobios, anaerobios y hongos.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201031896.
Solicitante: GARCIA RODRIGUEZ, Luis Antonio.
Nacionalidad solicitante: España.
Inventor/es: GARCIA RODRIGUEZ,Luis Antonio, FERNÁNDEZ MALLO,Olvido.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61F2/28 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61F FILTROS IMPLANTABLES EN LOS VASOS SANGUINEOS; PROTESIS; DISPOSITIVOS QUE MANTIENEN LA LUZ O QUE EVITAN EL COLAPSO DE ESTRUCTURAS TUBULARES, p. ej. STENTS; DISPOSITIVOS DE ORTOPEDIA, CURA O PARA LA CONTRACEPCION; FOMENTACION; TRATAMIENTO O PROTECCION DE OJOS Y OIDOS; VENDAJES, APOSITOS O COMPRESAS ABSORBENTES; BOTIQUINES DE PRIMEROS AUXILIOS (prótesis dentales A61C). › A61F 2/00 Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00). › Huesos (articulaciones A61F 2/30).
- A61L2/04 A61 […] › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 2/00 Procedimientos o aparatos para desinfectar o esterilizar materiales u objetos distintos a los productos alimenticios y a las lentes de contacto; Sus accesorios (pulverizadores de desinfectantes A61M; esterilización de envases o del contenido del envase asociado a su contenedor B65B 55/00; tratamiento del agua, agua residual o de alcantarilla C02F; desinfección del papel D21H 21/36; dispositivos de desinfección para retretes E03D; artículos que incluyen accesorios para la desinfección, ver las subclases apropiadas para estos artículos, p. ej. H04R 1/12). › Calor (A61L 2/08 tiene prioridad).
- A61L27/36 A61L […] › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › que contienen ingredientes de composición indeterminada o sus productos de reacción.
- B01L3/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01L APARATOS DE LABORATORIO PARA LA QUIMICA O LA FISICA, DE USO GENERAL (aparatos de uso médico o farmacéutico A61; aparatos para aplicaciones industriales o aparatos de laboratorio cuya estructura y funciones son comparables a las de aparatos industriales similares, ver las clases relativas a los aparatos industriales, en particular las subclases B01 y C12; aparatos de separación o de destilación B01D; dispositivos de mezcla o de agitación B01F; atomizadores B05B; tamices, cribas B07B; tapones, capuchones B65D; manipulación de líquidos en general B67; bombas de vacío F04; sifones F04F 10/00; grifos, válvulas F16K; tubos, empalmes para tubos F16L; aparatos especialmente adaptados al estudio y análisis de materiales G01, particularmente G01N; aparatos eléctricos u ópticos, ver las subclases apropiadas en las secciones G y H). › Recipientes o utensilios para laboratorios, p. ej. cristalería de laboratorio (botellas B65D; equipos para enzimología o microbiología C12M 1/00 ); Cuentagotas (recipientes para volumetría G01F).
PDF original: ES-2392725_A1.pdf
Fragmento de la descripción:
Método para el procesamiento del tejido óseo alogénico y recipiente para llevarlo a cabo.
OBJETO DE LA INVENCION
La invención, tal como expresa el enunciado de la presente memoria descriptiva, se refiere a un método para el procesamiento del tejido óseo alogénico y a un recipiente para llevarlo a cabo.
Más en particular, el objeto de la invención se centra en el desarrollo de una nueva metodología de procesamiento para aloinjertos óseos, que reúne las características de sencillez, eficacia, efectividad y eficiencia, permitiendo obtener aloinjertos de mayor calidad biológica que los obtenidos con otros métodos de procesamiento, suponiendo, por tanto, una mejorada alternativa a lo ya conocido en este campo. Además, la invención comprende un segundo aspecto relativo a un recipiente específico adaptado para llevar a cabo una de las etapas del procedimiento.
ANTECEDENTES DE LA INVENCION
Como es sabido, llamamos Injerto Osteotendinoso a cualquier material biológico compuesto por tejido óseo, tendinoso o combinación de ambos, extraído de su emplazamiento original para ser utilizado en un lugar distinto de este.
Los aloinjertos osteotendinosos son portadores de elementos celulares y humorales susceptibles de producir una reacción inmunitaria huésped contra injerto en el receptor.
El contenido celular del injerto (células del tejido óseo, células del estroma tisular, precursores hematopoyéticos, vasos y nervios) sufre fenómenos de necrosis isquémica desde el momento de su extracción (autoinjertos) o desde el momento del fallecimiento del donante (aloinjertos) ; la duración de la isquemia y su carácter de fría o caliente determina cambios irreversibles en el interior del injerto en una doble vertiente: por una parte se produce deterioro de la matriz orgánica e inactivación de factores humorales osteoinductores (BMPs, citoquinas de la familia de los TGF tipo , relacionados con el contenido colágeno de la matriz) , por otra parte los fenómenos de necrosis favorecen la contaminación de los injertos.
Ambos fenómenos deben ser evitados para garantizar la calidad de los injertos. Se pueden producir, además, reacciones de hidrólisis y oxidación como la peroxidación lipídica.
Todos estos fenómenos altamente nocivos para la calidad e incluso la supervivencia del injerto necesitan de la presencia de “agua libre” (15, 33) en el interior del tejido. De hecho, la inmovilización del agua libre es uno de los principales objetivos que debe cumplir la preservación de los aloinjertos osteotendinosos, la cual puede conseguirse a través de varias vías:
- Ultracongelación: Por debajo de –80º no existe agua libre en el estroma tisular (las moléculas de H2O están inmovilizadas en forma de cristales de hielo) , además del efecto de destrucción celular que produce la congelación rápida. La ultracongelación (20, 26, 28, 29, 34, 41) es, por tanto, un excelente medio de preservación de injertos osteotendinosos.
- Liofilización (17) : Aplicación de un procedimiento de congelación-deshidratación (sublimación del contenido en agua desde partículas de hielo sólido a vapor de agua) . La deshidratación desde la fase de hielo sólido previene también la desnaturalización proteica que puede producirse durante el proceso de congelación aislado.
- El tercer método para inmovilizar el agua libre es la inmersión en fluidos con muy elevada concentración de solutos. La salazón de determinados alimentos como método de conservación por periodos prolongados conseguía precisamente la inmovilización del agua libre, impidiendo o retardando los fenómenos de putrefacción. En el caso de los tejidos para uso en la clínica se emplea en ocasiones el glicerol a determinada concentración, en especial para la piel y para la obtención de matriz ósea desmineralizada (27, 33) .
La incorporación de los aloinjertos osteotendinosos se consigue a través de mecanismos de osteoconducción y osteoinducción. Los aloinjertos no son osteoformadores directos de tejido óseo. Por tanto, todo aquello que mejore aquellos dos mecanismos será beneficioso para el resultado final.
El tejido óseo alogénico está compuesto por la matriz ósea, las células propias del tejido óseo (osteoblastos/osteocitos y osteoclastos) , tejido hematopoyético, médula ósea grasa, vasos y nervios, todos ellos incluidos en la red tridimensional de sales cálcicas que constituye el soporte físico del tejido óseo.
Atendiendo a las propiedades biológicas óptimas de un aloinjerto osteotendinoso, es vital la
ES 2 392 725 Al
preservación de la matriz ósea, tanto su fracción orgánica como inorgánica. El resto de componentes del tejido carece de propiedades beneficiosas y podría, o debería, ser eliminado.
Desde el punto de vista de los fenómenos de osteoinducción, lo más importante es la preservación de la matriz ósea, compuesta por fibras colágenas y otras proteínas (proteínas de adhesión celular, osteocalcina, BMPs, etc.) .
Gracias al conjunto de las dos fases de la matriz ósea, orgánica e inorgánica, el tejido óseo posee sus propiedades mecánicas características, combinando dos propiedades aparentemente contradictorias como son rigidez y elasticidad.
Las fibras colágenas flexibilidad y resistencia a la flexión, torsión y tensión. La matriz mineralizada le confiere resistencia a la compresión y la dureza necesaria para servir de soporte al conjunto del organismo.
Desde el punto de vista de los fenómenos de osteoconducción, lo importante es mantener intacta la matriz ósea mineralizada, esto es, la estructura física del tejido óseo.
Existe evidencia de que la eliminación de ciertos componentes de la matriz orgánica de los aloinjertos mejora sus propiedades biológicas:
- La eliminación del contenido en lípidos, material abundante especialmente en áreas metáfisodiafisarias, mejora la incorporación de los aloinjertos. Estudios en animal de experimentación comparando el comportamiento biológico de aloinjertos con y sin eliminación de los lípidos, demostraron que los sometidos a eliminación del contenido en lípidos (4, 17, 26, 39, 40, 44) mediante cloroformo-metanol mostraron:
- Mejor incorporación.
- Histomorfometría: Mayor formación y reabsorción ósea.
- Gammagrafía a las 3 semanas del implante: captación del isótopo por parte del injerto (mayor tasa de remodelación ósea) .
- Conservación de las propiedades mecánicas.
- La presencia de grasa en el interior de los aloinjertos puede dificultar determinadas aplicaciones clínicas: la impactación de fragmentos de tejido esponjoso para relleno de cavidades, durante la cirugía de recambio protésico de cadera, se facilita si los fragmentos han sido lavados para eliminar el contenido graso. En caso contrario, al ser la grasa un líquido incompresible, los esfuerzos mecánicos para la impactación serán menos eficaces (7) y persistirá cierta tendencia al deslizamiento por el efecto lubricante de la propia grasa.
- La eliminación del contenido en proteínas libres disminuye el riesgo de transmisión de
enfermedades vehiculadas por priones (5, 8, 10, 11, 13, 18, 19, 25, 31, 38, 42, 43)
.
- La reducción del contenido celular disminuye la capacidad inmunogénica de los aloinjertos y reduce la posibilidad de transmisión de patógenos intracelulares: el tejido óseo no procesado puede ser vehículo de transmisión de patógenos, incluyendo HIV, HVC y HTLV. Debemos tener en cuenta, además, que los tests de que disponemos son capaces de detectar los patógenos conocidos a día de hoy, pero en cualquier momento podrían aparecer otros nuevos, intra o extracelulares, no detectables hasta el conocimiento de la enfermedad que transmitan y se desarrollen los tests de detección fiables, algo parecido a lo que ocurrió con el VIH durante los primeros años de la década de los 80 (9) .
Por otra parte, la aplicación de bajas dosis de calor (hasta 60º C y hasta 10 horas) destruye bacterias y virus patógenos sin alterar las propiedades mecánicas ni la efectividad clínica (3, 6, 12, 16, 21, 24, 30, 32, 35-37) .
La revisión... [Seguir leyendo]
Reivindicaciones:
1. MÉTODO PARA EL PROCESAMIENTO DEL TEJIDO ÓSEO ALOGÉNICO, caracterizado porque comprende cuatro procedimientos o fases de aplicación sucesiva consistentes en:
- Lavado de cada aloinjerto de manera individualizada, en recipiente hermético y sumergido en suero fisiológico a 60º centígrados de temperatura, en condiciones de esterilidad, con una duración de 10 minutos, y seguido de agitación manual enérgica durante 1 minuto en el mismo recipiente hermético de lavado.
- Centrifugación de cada aloinjerto óseo de manera individualizada, manteniendo las condiciones de esterilidad, a 2.000 revoluciones por minuto (1.500 g) en centrifugadora de laboratorio durante 15 minutos.
- Pasteurización de cada aloinjerto óseo de manera individualizada, con la finalidad de destruir mediante calor hongos y bacterias patógenas, para lo cual se introduce en un recipiente estéril de cierre hermético, con código de identificación individual para cada aloinjerto, añadiendo suero fisiológico precalentado a 60º centígrados hasta cubrir por completo el injerto óseo, agitándose durante 90 minutos.
- Control microbiológico final, para lo cual, bajo campana de flujo laminar con condiciones de esterilidad, se hace pasar el suero en el que se realizó la pasteurización a través de un filtro de papel con tamaño de poro de 0, 45 μm, cultivando directamente el filtro en medio de cultivo para microorganismos aerobios, anaerobios y hongos.
2. MÉTODO PARA EL PROCESAMIENTO DEL TEJIDO ÓSEO ALOGÉNICO, según la reivindicación 1, caracterizado porque en la fase de pasteurización, los recipientes se introducen en grupos de cuatro en una termoagitadora de laboratorio con control de temperatura y velocidad de agitación, programándose el procedimiento a 60º centígrados y a una velocidad de agitación orbital de 40 ciclos por minuto.
3. RECIPIENTE para llevar a cabo un método para el procesamiento del tejido óseo alogénico como el descrito en la reivindicación 1 ó 2, concretamente para llevar a cabo la etapa de centrifugación comprendida en dicho método, caracterizado porque consiste en un recipiente diseñado y construido específicamente para este procedimiento en PVC resistente a autoclave, con rejilla en su parte inferior para permitir la salida de los materiales a eliminar y mantenerlos separados del aloinjerto durante la centrifugación.
4. RECIPIENTE, según la reivindicación 3, caracterizado porque dicho recipiente tiene las siguientes dimensiones: MEDIDAS EXTERIORES. Altura: 120 milímetros. Anchura: 99 milímetros. Rosca de cierre: 6 espiras con paso de rosca de 5 milímetros. MEDIDAS INTERIORES. Profundidad: 97 milímetros (con rejilla colocada: 82 milímetros) . Anchura: 76 milímetros. MEDIDAS DE LA REJILLA. Altura: 15 milímetros. Anchura: 74, 5 milímetros. Diámetro de los orificios: 6 milímetros.
Patentes similares o relacionadas:
Dispositivos modulares para puntos de atención y usos de los mismos, del 29 de Julio de 2020, de Labrador Diagnostics LLC: Un sistema para la detección automatizada de un analito a partir de una muestra de fluido corporal, que comprende: un dispositivo de fluidos que comprende: […]
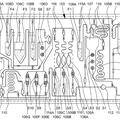 Dispositivo de análisis y método para examinar una muestra, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Dispositivo de análisis para probar una muestra (P) biológica particular por medio de un cartucho que puede ser recibido,
comprendiendo el dispositivo […]
Dispositivo de análisis y método para examinar una muestra, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Dispositivo de análisis para probar una muestra (P) biológica particular por medio de un cartucho que puede ser recibido,
comprendiendo el dispositivo […]
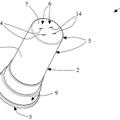 Un recipiente para la transferencia selectiva de muestras de material biológico, del 29 de Julio de 2020, de COPAN ITALIA S.P.A.: Un recipiente para el transporte selectivo de muestras de material biológico o material de origen biológico, que comprende un cuerpo que tiene al menos un compartimento […]
Un recipiente para la transferencia selectiva de muestras de material biológico, del 29 de Julio de 2020, de COPAN ITALIA S.P.A.: Un recipiente para el transporte selectivo de muestras de material biológico o material de origen biológico, que comprende un cuerpo que tiene al menos un compartimento […]
DISPOSITIVO PARA LA SELECCIÓN DE ESPERMATOZOIDES, del 23 de Julio de 2020, de INSTITUTO NACIONAL DE INVESTIGACION Y TECNOLOGIA AGRARIA Y ALIMENTARIA (INIA): Dispositivo para la selección de espermatozoides que comprende una unidad de selección que comprende a su vez un compartimento de carga (1b) […]
Bolsas para el transporte de muestras y procedimiento de formación de dichas bolsas, del 22 de Julio de 2020, de Coveris Flexibles UK Limited: Bolsa para el transporte de muestras que comprende un bolsillo para alojar un recipiente que contiene una muestra y un cierre […]
Uso de un sistema de banco de células de crioconservación cerrado de alta capacidad y procedimiento para descongelar y dispensar células almacenadas, del 22 de Julio de 2020, de Boehringer Ingelheim Animal Health USA Inc: Uso de un sistema de banco de células de crioconservación de fase cerrada y alta capacidad para almacenar grandes volúmenes de células, en el que el uso comprende las siguientes […]
Dispositivo microfluídico para generar una secuencia de sustancias en un canal microfluídico, del 22 de Julio de 2020, de EUROPEAN MOLECULAR BIOLOGY LABORATORY: Un aparato microfluídico para proporcionar una o más sustancias líquidas a una red de canales microfluídicos , comprendiendo el aparato microfluídico una red de canales […]
Sistema microfluídico, del 22 de Julio de 2020, de Menarini Silicon Biosystems S.p.A: Un sistema microfluídico para el aislamiento de partículas de al menos un tipo dado de una muestra; comprendiendo el sistema microfluídico una entrada , a […]