Dispositivo para la amplificación de la reacción en cadena termo-dependiente de secuencias de ácidos nucleicos diana.
Dispositivo para efectuar reacciones enzimáticas y/o de biología molecular que requieren al menos dostemperaturas de incubación diferentes,
que comprende al menos un cartucho (1) en forma circular que comprendevarias cámaras de reacción (13), en las que se depositan previamente los cebadores, un depósito (11) y los canales(12), caracterizado porque:
- este cartucho (1) que posee una geometría de revolución, en el cual el depósito (11) está situadosensiblemente en el centro, las cámaras de reacción (13) que están repartidas en círculo alrededor de dichodepósito, y los canales (12) que unen dicho depósito (11) con dichas cámaras (13), los canales están previstosesencialmente de forma radial;
- al menos una placa calefactora (2) que presenta al menos dos zonas distintas que se pueden calentar almenos a dos temperaturas diferentes, en particular la placa calefactora que presenta tres zonas distintas que sepueden calentar a tres temperaturas diferentes;
- los medios (3) de desplazamiento relativo entre dicho cartucho y dicha placa, que permiten una variacióncíclica de la temperatura de las cámaras de reacción.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10177401.
Solicitante: Pall Genedisc Technologies.
Nacionalidad solicitante: Francia.
Dirección: 1, rue du Courtil Parc d''Affaires CICEA - Bâtiment 1 5170 Bruz FRANCIA.
Inventor/es: FESTOC,GABRIEL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B01L3/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01L APARATOS DE LABORATORIO PARA LA QUIMICA O LA FISICA, DE USO GENERAL (aparatos de uso médico o farmacéutico A61; aparatos para aplicaciones industriales o aparatos de laboratorio cuya estructura y funciones son comparables a las de aparatos industriales similares, ver las clases relativas a los aparatos industriales, en particular las subclases B01 y C12; aparatos de separación o de destilación B01D; dispositivos de mezcla o de agitación B01F; atomizadores B05B; tamices, cribas B07B; tapones, capuchones B65D; manipulación de líquidos en general B67; bombas de vacío F04; sifones F04F 10/00; grifos, válvulas F16K; tubos, empalmes para tubos F16L; aparatos especialmente adaptados al estudio y análisis de materiales G01, particularmente G01N; aparatos eléctricos u ópticos, ver las subclases apropiadas en las secciones G y H). › Recipientes o utensilios para laboratorios, p. ej. cristalería de laboratorio (botellas B65D; equipos para enzimología o microbiología C12M 1/00 ); Cuentagotas (recipientes para volumetría G01F).
- B01L7/00 B01L […] › Aparatos de calentamiento o de enfriamiento (evaporadores B01D 1/00; secado de gases o vapores, p. ej. desecadores, B01D 53/26; autoclaves B01J 3/04; hornos de secado F26B; altos hornos, hornos F27 ); Dispositivos de aislamiento térmico.
PDF original: ES-2389763_T3.pdf
Fragmento de la descripción:
Dispositivo para la amplificación de la reacción en cadena termo-dependiente de secuencias de ácidos nucleicos diana.
La presente invención se refiere al campo de la genética.
Más precisamente, la presente invención se refiere a un dispositivo para la amplificación de secuencias nucleicas diana y a los modos de utilización de este dispositivo.
La presente invención tiene como objetivo principalmente permitir la detección y, llegado el caso, la cuantificación en tiempo real, de secuencias de ácido nucleico diana en una o varias muestras.
La detección de secuencias nucleicas diana es una técnica cada vez más utilizada en numerosos campos, y el abanico de aplicaciones de esta técnica está llamado a extenderse a medida que sea más fiable, más económica y más rápida. Así, en salud humana, la detección de ciertas secuencias de ácido nucleico permite en ciertos casos un diagnóstico fiable y rápido de infecciones víricas o bacterianas. Igualmente, la detección de ciertas particularidades genéticas puede permitir identificar susceptibilidades a ciertas enfermedades, o establecer un diagnóstico precoz de enfermedades genéticas o neoplásicas. La detección de secuencias nucleicas diana se utiliza también en la industria agroalimentaria, principalmente para asegurar la trazabilidad de productos, para detectar la presencia de organismos genéticamente modificados e identificarlos, o para efectuar un control sanitario de los alimentos.
Los procedimientos de detección basados en ácidos nucleicos implican casi sistemáticamente una reacción de hibridación molecular entre una secuencia nucleica diana y uno o varias secuencias nucleicas complementarias de dicha secuencia diana. Estos procedimientos presentan numerosas variantes como las técnicas conocidas por el experto en la técnica bajo las expresiones "técnicas de transferencia" (blot, dot blot, Southern blot, Polimorfismo de longitud del fragmento de restricción, etc.) , o también como los sistemas miniaturizados sobre los que se fijan previamente las secuencias complementarias de las secuencias diana ("biochips") . Dentro del marco de estas técnicas, las secuencias nucleicas complementarias se llaman generalmente sondas. Otra variante, que puede constituir en sí misma la base de un procedimiento de diagnóstico o no ser más que una etapa suplementaria en una de las técnicas mencionadas anteriormente (con el fin principalmente de aumentar la concentración de la secuencia diana y, por lo tanto, la sensibilidad del diagnóstico) , consiste en amplificar la secuencia de ácido nucleico diana. Se han descrito varias técnicas que permiten la amplificación específica de una secuencia de ácido nucleico, siendo la más utilizada la Reacción en Cadena de la Polimerasa (RCP) , o “Polymerase Chain Reaction” (PCR) . Dentro del marco de esta última técnica, se utilizan secuencias nucleicas complementarias de las secuencias diana, llamadas cebadores, para amplificar dichas secuencias diana.
Las reacciones de PCR implican una repetición de ciclos, cuyo número varía generalmente de 20 a 50, y que están compuestos cada uno de tres fases sucesivas, a saber: desnaturalización, hibridación, elongación. Respectivamente, la primera fase corresponde a la transformación de los ácidos nucleicos bicatenarios en ácidos nucleicos monocatenarios, la segunda fase a la hibridación molecular entre la secuencia diana y los cebadores complementarios de dicha secuencia, y la tercera fase a la elongación de los cebadores complementarios, hibridados en la secuencia diana, por una ADN polimerasa. Estas fases se llevan a temperaturas específicas: generalmente 95ºC para la desnaturalización, 72ºC para la elongación, y entre 30ºC y 65ºC para la hibridación, según la temperatura de hibridación (Tm) de los cebadores utilizados. También es posible efectuar las etapas de hibridación y la elongación a la misma temperatura (generalmente 60ºC) .
Una reacción de PCR consiste, por lo tanto, en un encadenamiento de ciclos térmicos repetitivos a lo largo del cual el número de moléculas de ADN diana que sirve de matriz se duplica teóricamente en cada ciclo. En realidad, el rendimiento de la PCR es inferior a 100%, aunque la cantidad de producto Xn obtenido después de n ciclos es:
Xn= Xn-1 (1 + rn) , en donde
Xn-1 es la cantidad de producto obtenido en el ciclo anterior, y rn el rendimiento de la PCR en el ciclo n (0 < rn º 1) .
Considerando el rendimiento constante, es decir idéntico para cada ciclo, la cantidad de producto Xn obtenido después de n ciclos, a partir de una cantidad inicial X0 es entonces:
Xn= X0 (1 + r) n (A)
En realidad, el rendimiento r disminuye a lo largo de la reacción de PCR, a causa de varios factores, tal como una cantidad limitante de al menos uno de los reactivos necesarios para la amplificación, la inactivación de la polimerasa por esos pases repetidos a 95ºC, o su inhibición por los pirofosfatos producidos por la reacción.
Debido a esta disminución del rendimiento, la cinética de una reacción de PCR presenta primero una fase exponencial (mientras que r es constante) , que evoluciona luego hacia una fase de meseta cuando r disminuye.
Durante la fase exponencial, la ecuación (A) anterior es válida, y puede escribirse también: log (Xn) = log (X0) + n log (1 + r)
Así, en la fase exponencial de la PCR, la curva que muestra la cantidad de producto, en una escala logarítmica, en función del número de ciclos, es una línea de pendiente (1 + r) y que corta el eje de ordenadas en un valor igual al logaritmo de la concentración inicial.
La medida en tiempo real de la cantidad de producto obtenido, puede permitir por lo tanto conocer la concentración inicial de la matriz, lo que es particularmente útil en un gran número de aplicaciones, por ejemplo, para medir la carga vírica de un enfermo, o también para conocer la variabilidad de un transcriptoma.
Generalmente, las PCR implican volúmenes de reacción que van desde 2 a 50 1l y se llevan a cabo en tubos, microtubos, capilares o sistemas conocidos por el experto en la técnica, bajo el término "microplacas" (en realidad, conjuntos de microtubos unidos) . Cada lote de tubos o de recipientes equivalentes se debe calentar por lo tanto a tres temperaturas que se corresponden con las diferentes fases de la PCR, y esto tantas veces como el número de ciclos deseados.
La utilización de tubos o de sistemas similares obligan al usuario a efectuar múltiples manipulaciones para preparar tantos tubos y soluciones (conocidas por el experto en la técnica bajo la expresión "mix PCR") como secuencias diana se deseen amplificar, incluso a partir de una muestra única de ácidos nucleicos, con la excepción de los procedimientos de amplificación "multiplex", que permiten la amplificación de varias secuencias diana simultáneamente en el mismo recipiente, utilizando cebadores denominados poco específicos que pueden hibridarse con varias secuencias diana, como por ejemplo, la técnica RAPD - polimorfismo del ADN amplificado aleatoriamente, por sus siglas en inglés, o utilizando cebadores específicos pero en un número superior, permitiendo cada pareja de cebadores utilizada, la amplificación de una secuencia diana. Estas amplificaciones multiplex corresponden a casos particulares y no son la norma. Además, no garantizan la ausencia de interacciones de una reacción de amplificación con otra, y por razones principalmente de posibles hibridaciones entre los cebadores, solo puede ser muy limitado el número de secuencias diana amplificadas por recipiente.
Estas diferentes manipulaciones implican numerosos inconvenientes.
En primer lugar, exigen mucho tiempo. En segundo lugar, no están exentas de riesgo desde el punto de vista de eventuales contaminaciones de un tubo a otro o desde el medio exterior (polvo, bacteria, aerosol o cualquier otro contaminante susceptible de contener moléculas de ácidos nucleicos o moléculas susceptibles de influir sobre la eficacia de la reacción de amplificación) . Además, no aseguran una homogeneidad de volumen y de concentración en los reactivos de un tubo a otro. Finalmente, imponen la utilización de volúmenes manipulables manualmente, generalmente superiores a 1 1l, lo que tiene una incidencia sobre los costes ligados a la realización de las PCR, siendo los reactivos utilizados costosos.
La utilización de dispositivos diseñados para automatizar al... [Seguir leyendo]
Reivindicaciones:
1. Dispositivo para efectuar reacciones enzimáticas y/o de biología molecular que requieren al menos dos temperaturas de incubación diferentes, que comprende al menos un cartucho (1) en forma circular que comprende varias cámaras de reacción (13) , en las que se depositan previamente los cebadores, un depósito (11) y los canales (12) , caracterizado porque:
- este cartucho (1) que posee una geometría de revolución, en el cual el depósito (11) está situado sensiblemente en el centro, las cámaras de reacción (13) que están repartidas en círculo alrededor de dicho depósito, y los canales (12) que unen dicho depósito (11) con dichas cámaras (13) , los canales están previstos esencialmente de forma radial;
- al menos una placa calefactora (2) que presenta al menos dos zonas distintas que se pueden calentar al menos a dos temperaturas diferentes, en particular la placa calefactora que presenta tres zonas distintas que se pueden calentar a tres temperaturas diferentes;
- los medios (3) de desplazamiento relativo entre dicho cartucho y dicha placa, que permiten una variación cíclica de la temperatura de las cámaras de reacción.
2. Dispositivo de acuerdo con la reivindicación 1, en el que dichas cámaras de reacción (13) están previstas en la periferia de dicho cartucho.
3. Dispositivo de acuerdo con la reivindicación 1 o 2, en el que la reacción enzimática es una amplificación en cadena termo-dependiente de secuencias de ácidos nucleicos, y en el que las zonas de la placa calefactora (2) se pueden calentar al menos a dos temperaturas diferentes, que se corresponden con las fases de los ciclos de amplificación de dichos ácidos nucleicos.
4. Dispositivo de acuerdo con la reivindicación 3, caracterizado porque:
- los cebadores específicos de las secuencias diana que se van a amplificar se distribuyen previamente en las cámaras de reacción (13) ,
- el depósito (11) está destinado a recibir un fluido compuesto principalmente por una muestra de ácidos nucleicos que se va a analizar y los reactivos necesarios para una reacción de amplificación en cadena con la polimerasa, con la excepción de los cebadores,
- la placa calefactora (2) presenta tres zonas distintas que se pueden calentar a tres temperaturas distintas, que se corresponden con las tres fases de los ciclos de amplificación en cadena con la polimerasa.
5. Dispositivo de acuerdo con la reivindicación 3 o 4, para la amplificación en cadena termo-dependiente de secuencias de ácidos nucleicos medida en tiempo real, caracterizado porque comprende unos medios ópticos (5) de excitación/medición de la fluorescencia, dispuestos de manera que excitan y miden en cada ciclo la fluorescencia del contenido de las cámaras de reacción.
6. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 5, en el que las distintas zonas de calentamiento de la placa (2) están repartidas en al menos dos o tres porciones de disco.
7. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 5, en el que las distintas zonas de calentamiento de la placa (2) se reparten en las porciones de la corona.
8. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 7, en el que dichos medios de desplazamiento (3) autorizan la rotación de dicho cartucho (1) y/o de dicha placa calefactora (2) .
9. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 8, en donde el cartucho (1) está en contacto directo con la placa calefactora (2) .
10. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 9, en donde la placa (2) está provista de un revestimiento que favorece el desplazamiento relativo entre dicho cartucho (1) y dicha placa (2) .
11. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 10, en donde dicha placa calefactora
(2) comprende dos o tres termobloques distintos (21, 22, opcionalmente, 23) conectados a unos medios de programación de su temperatura.
12. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 11, que comprende unos medios ópticos (5) de excitación/medición de la fluorescencia dispuestos encima o a un lado del cartucho.
13. Dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 12, que comprende además unos medios (4) que permiten conducir el fluido presente en el depósito (11) a las cámaras de reacción (13) .
14. Dispositivo de acuerdo con la reivindicación 13, en el que dichos medios de conducción (4) incluyen un
dispositivo de pistón (41) , y el fluido se conduce a las cámaras de reacción por un aumento de la presión.
15. Dispositivo de acuerdo con la reivindicación 13, en donde dichos medios de conducción (4) incluyen una bomba (41) , y el fluido es conducido a las cámaras de reacción por un restablecimiento de la presión después de establecer una presión inferior.
16. Dispositivo de acuerdo con la reivindicación 5, en el que las cámaras de reacción (13) del cartucho (1) están cerradas.
17. Procedimiento para la amplificación de ácido nucleico gracias a un dispositivo de acuerdo con una cualquiera de las reivindicaciones 1 a 16, que comprende las siguientes etapas:
- llenar al menos parcialmente el depósito (11) con un fluido que contiene una muestra de ácidos nucleicos
que se va a analizar, así como todo lo necesario para una reacción de amplificación con la excepción de los cebadores y, en su caso, un agente intercalante fluorescente de los ácidos nucleicos;
- distribuir dicho fluido en las cámaras de reacción (13) del cartucho (1) , en las que se han depositado previamente los cebadores y, en su caso, una o varias sondas marcadas;
- poner en marcha los medios (3) de desplazamiento relativo entre el cartucho y la placa calefactora para
conducir sucesivamente y tantas veces como se quiera el contenido de cada cámara de reacción a dos, tres o más temperaturas definidas por las dos, tres o más zonas de dicha placa calefactora (2) .
18. Procedimiento para la amplificación de acuerdo con la reivindicación 17, en el que la etapa de distribución del fluido en las cámaras de reacción (13) se efectúa aplicando una presión inferior en el interior del cartucho, restableciendo a continuación la presión.
Patentes similares o relacionadas:
Dispositivos modulares para puntos de atención y usos de los mismos, del 29 de Julio de 2020, de Labrador Diagnostics LLC: Un sistema para la detección automatizada de un analito a partir de una muestra de fluido corporal, que comprende: un dispositivo de fluidos que comprende: […]
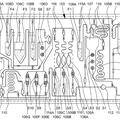 Dispositivo de análisis y método para examinar una muestra, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Dispositivo de análisis para probar una muestra (P) biológica particular por medio de un cartucho que puede ser recibido,
comprendiendo el dispositivo […]
Dispositivo de análisis y método para examinar una muestra, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Dispositivo de análisis para probar una muestra (P) biológica particular por medio de un cartucho que puede ser recibido,
comprendiendo el dispositivo […]
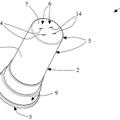 Un recipiente para la transferencia selectiva de muestras de material biológico, del 29 de Julio de 2020, de COPAN ITALIA S.P.A.: Un recipiente para el transporte selectivo de muestras de material biológico o material de origen biológico, que comprende un cuerpo que tiene al menos un compartimento […]
Un recipiente para la transferencia selectiva de muestras de material biológico, del 29 de Julio de 2020, de COPAN ITALIA S.P.A.: Un recipiente para el transporte selectivo de muestras de material biológico o material de origen biológico, que comprende un cuerpo que tiene al menos un compartimento […]
DISPOSITIVO PARA LA SELECCIÓN DE ESPERMATOZOIDES, del 23 de Julio de 2020, de INSTITUTO NACIONAL DE INVESTIGACION Y TECNOLOGIA AGRARIA Y ALIMENTARIA (INIA): Dispositivo para la selección de espermatozoides que comprende una unidad de selección que comprende a su vez un compartimento de carga (1b) […]
Sistema microfluídico, del 22 de Julio de 2020, de Menarini Silicon Biosystems S.p.A: Un sistema microfluídico para el aislamiento de partículas de al menos un tipo dado de una muestra; comprendiendo el sistema microfluídico una entrada , a […]
Un dispositivo y método para calentar o enfriar una muestra, del 22 de Julio de 2020, de Cell Therapy Catapult Limited: Un dispositivo para calentar o enfriar una o más muestras, comprendiendo el dispositivo una pluralidad de miembros que pueden funcionar en uso para calentar […]
Bolsas para el transporte de muestras y procedimiento de formación de dichas bolsas, del 22 de Julio de 2020, de Coveris Flexibles UK Limited: Bolsa para el transporte de muestras que comprende un bolsillo para alojar un recipiente que contiene una muestra y un cierre […]
Uso de un sistema de banco de células de crioconservación cerrado de alta capacidad y procedimiento para descongelar y dispensar células almacenadas, del 22 de Julio de 2020, de Boehringer Ingelheim Animal Health USA Inc: Uso de un sistema de banco de células de crioconservación de fase cerrada y alta capacidad para almacenar grandes volúmenes de células, en el que el uso comprende las siguientes […]