ESPIRALES METÁLICAS ENTRELAZADAS CON POLÍMEROS O FIBRAS BIOLÓGICOS O BIODEGRADABLES O SINTÉTICOS PARA LA EMBOLIZACIÓN DE UNA CAVIDAD CORPORAL.
Dispositivo de oclusión de vasos para ocluir flujo sanguíneo en un paciente,
comprendiendo el dispositivo: a) una espiral, que comprende un lumen y un primer y un segundo extremo, y dimensionada para la inserción en un punto de uso en una red vascular del paciente; b) un elemento resistente al estiramiento que presenta un primer extremo unido fijamente al primer extremo de la espiral y un segundo extremo unido fijamente al segundo extremo de la espiral; y c) una pluralidad de fibras, en el que el dispositivo está caracterizado por el hecho de que cada una de las fibras se envuelve alrededor del elemento resistente al estiramiento por lo menos dos veces
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/018087.
Solicitante: MICRO THERAPEUTICS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 9775 Toledo Way Irvine, CA 92618.
Inventor/es: PATTERSON, WILLIAM, R., SLEE, EARL, H., HENKES,HANS, MONSTADT,HERMANN, WILDER,Tom, MCCARTHY,Thomas, STRAUSS,Brian.
Fecha de Publicación: .
Fecha Solicitud PCT: 23 de Mayo de 2005.
Clasificación Internacional de Patentes:
- A61B17/12P
- A61L31/02B
- A61L31/10 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 31/00 Materiales para otros artículos quirúrgicos. › Materiales macromoleculares.
- A61L31/12D6
- A61L31/16 A61L 31/00 […] › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
Clasificación PCT:
- A61B17/12 A61 […] › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › A61B 17/00 Instrumentos, dispositivos o procedimientos quirúrgicos, p. ej. torniquetes (A61B 18/00 tiene prioridad; dispositivos anticonceptivos, pesarios, dispositivos para su introducción A61F 6/00; cirugía ocular A61F 9/007; cirugía otorrina A61F 11/00). › para ligar o comprimir partes tubulares del cuerpo, p. ej. los vasos sanguíneos, el cordón umbilical.
- A61L31/16 A61L 31/00 […] › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania.
PDF original: ES-2357243_T3.pdf
Fragmento de la descripción:
Campo de la invención
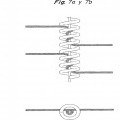
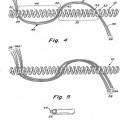
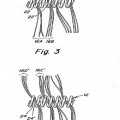
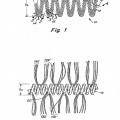
Esta invención se refiere a dispositivos de oclusión de vasos para formar una oclusión (embolia) en un lugar vascular deseado, particularmente en el sitio de un aneurisma. Los dispositivos son espirales de alambre helicoidal preferiblemente con materiales fibrosos entrelazados que proporcionaban una mayor área superficial para facilitar 5 altas velocidades de bioacciones deseadas tales como liberación de material bioactivo o interacciones embólicas entre la superficie del dispositivo y el flujo sanguíneo del paciente. Las espirales pueden ir recubiertas de por lo menos una única capa que incluya un material bioactivo.
Antecedentes
La embolia de una cavidad del cuerpo (por ejemplo la oclusión de un aneurisma del vaso sanguíneo cerebral 10 mediante espirales desmontables, embolia líquida, embolia de partículas, embolia de balón) es un tratamiento que puede tener una elevada incidencia de recurrencia. Debido a una curación insuficiente en la interfaz aneurisma/arteria madre, las fuerzas mecánicas y biológicas, que no se comprenden completamente, crean una nueva expansión del aneurisma. Esto es, el aneurisma se reforma o se repite después del tratamiento endovascular embólico. 15
En un tratamiento se empaquetan espirales de Pt/Ir en aneurismas de modo que ocupan 20% a 30% del volumen del aneurisma y reducen el flujo de entrada de sangre en el aneurisma. La sangre aneurismática, de un 70% a un 80% por volumen, coagula por estancamiento. Preferiblemente, la sangre coagulada se organiza y procede a través de una serie de etapas similares a las que se producen en cualquier herida en el cuerpo: (1) hemostasis, (2) inflamación, (3) formación de tejido, y (4) remodelación. Un aneurisma así tratado está excluido de la circulación 20 arterial. Por otra parte, por motivos que se comprenden parcialmente, la sangre coagulada puede no organizarse, la masa de la espiral se compacta y/o el flujo de sangre nueva –junto con el tejido arterial enfermo- permite la expansión del aneurisma. De este modo, el aneurisma aparece y permanece susceptible a la ruptura y a hemorragia cerebral.
Con el desarrollo de la ingeniería de tejidos, se crearon dispositivos con la intención de dirigir o mejorar la curación 25 de la interfaz aneurisma/arteria en lugar de basarse en la reacción individual de cada paciente a la embolia de una cavidad del aneurisma. Los dispositivos embólicos, tales como espirales electrolíticamente separadas de Pt/Ir, se han diseñado con revestimientos que se hinchan en solución acuosa o que provocan una ligera respuesta inflamatoria.
Una forma de dispositivo contiene un hidrogel de poliacrilamida unido a la espiral separable de Pt/Ir. Mientras la 30 espiral reside en sangre, el hidrogel se hincha y ocupa más espacio que las espirales metálicas desnudas, dando lugar a densidades de empaquetamiento más elevadas ( 40% a 50%).
Otras espirales utilizan un polímero biodegradable PGLA (ácido poliglicólico poliláctico -- el mismo material utilizado en suturas absorbibles) tal como un revestimiento bioactivo de la espiral para provocar una ligera respuesta inflamatoria en el aneurisma que activa la organización aneurismática por las etapas de curación de la herida 35 citadas anteriormente.
Ambos enfoques presentan el mismo problema: están limitados por el pequeño tamaño de estas espirales y el hecho de que las espirales tengan que suministrarse a través de un microcatéter con el menor DI de 0,04 cm (0,015"). Las espirales pueden tener un mínimo de 0,09 cm de área superficial (DE 2,54 cm, 0,01 2,54 cm 1", en un tramo de 1 cm). Colocar un revestimiento, un hidrogel o un revestimiento bioactivo, y asegurar que la espiral tratada 40 se mueva a través de un catéter con un DI de 0,04 cm (0,015") pone un límite finito a la cantidad de hidrogel o de revestimiento bioactivo aplicado a la espiral. En general, la cantidad de material está limitada por la superficie de la espiral y el catéter de aplicación. Existen datos limitados a la ineficacia de las espirales revestidas. Sin embargo, la respuesta de los médicos indica que los resultados no son mejores que las espirales metálicas desnudas.
Las espirales helicoidales son una forma de dispositivo que se ha empleado ampliamente. Hans Henkes, y otros, 45 NEUROSURGERY 54, Nº 2, 268 (2004) describen los resultados sobre 1800 procedimientos que implican espirales helicoidales y concluyen que dichos dispositivos son seguros y eficaces para oclusión en pacientes con aneurismas intracraneales.
Hasta ahora se ha propuesto una serie de variaciones en las espirales helicoidales. Por ejemplo, en la patente americana el número 5.226.911 de Chee y Narient se describe enrollar de 5 a 100 fibras de polímero biocompatible 50 a través de las espirales helicoidales. Dacrón, ácido poliglicólico, ácido poliláctico, fluoropolímeros, nailon y seda se encuentran entre los polímeros sugeridos para estas fibras. La patente americana número 5.382.259 de Phelps y Van describe recubrimientos tubulares fibrosos trenzados o tejidos con y sin borla para espirales helicoidales. La patente americana número 5.549.624 de Mirigian y Van describe un dispositivo de espiral helicoidal con bucles fibrosos añadidos donde se indica que aumentan la trombogenicidad del dispositivo. La patente americana número 55 5.658.308 de Snyder describe un dispositivo metálico helicoidal que tiene de uno a varios cientos de filamentos axiales fibrosos que atraviesan su centro y opcionalmente filamentos unidos a los devanados de la espiral. Se indica que estos filamentos son bioactivos o no bioactivos y mejoran la capacidad de la espiral para ocluir el sitio en el cual va colocada. La patente americana número 5, 935.145 de Villar y Aganon describe dos elementos fibrosos
de espirales helicoidales unidos, cada uno de un material diferente. Uno de los materiales es preferiblemente biodegradable. El otro es preferiblemente no biodegradable. La patente americana número 6.299.627 de Eder y otros describe dispositivos con espirales o trenzados y dos revestimientos que incluyen un revestimiento interior y otro revestimiento seleccionados para afectar a la solubilidad de la capa interior. Además, el documento US 6193728 describe un dispositivo de oclusión de vasos que presenta todas las características del preámbulo de la 5 reivindicación 1.
Todo este trabajo sugiere que aunque los encajes de la espiral helicoidal son dispositivos de oclusión de vasos interesantes existen oportunidades para mejorar su rendimiento con el fin de conseguir un rendimiento óptimo en términos de facilidad de suministro y colocación en el sitio de tratamiento y en términos de nivel y velocidad de oclusión del vaso obtenidos. 10
DESCRIPCIÓN DE LA INVENCIÓN
Exposición de la invención
Hemos descubierto ahora mejoras en los dispositivos de oclusión de vasos que comprenden una espiral, por ejemplo, una espiral metálica entrelazada con fibras biológicas, biodegradables o de polímero sintético.
Existe la necesidad de un dispositivo embólico que pueda aumentar la superficie efectiva de modo que puedan 15 estar presentes niveles más altos de agentes biológicos, biodegradables, o sintéticos para embolizar una cavidad corporal y dirigir o provocar una respuesta de curación.
Se buscaba disponer una mayor área superficial en un dispositivo embólico de espiral añadiendo fibras. Aumentando el área superficial de contacto con la sangre inicial entre sangre y tejido aneurismático pueden utilizarse agentes bioactivos (biológicos, biodegradables, o sintéticos) en concentraciones más elevadas o en 20 cantidades mayores que como se ha utilizado anteriormente. La misma concentración o cantidad puede distribuirse sobre una mayor superficial de contacto.
Más concretamente, hemos descubierto que proporcionando un área superficial adicional grande pero controlada a un dispositivo de espiral helicoidal en forma de fibras entrelazadas en la espiral proporciona un dispositivo mejorado. La cantidad de área superficial adicional proporcionada por las fibras entrelazadas debe ser por lo menos 25 0,1 veces el área superficial proporcionada por la propia espiral metálica, hasta tanto como 10 o más veces el área superficial proporcionada por la propia espiral metálica.
De este modo, esta invención proporciona un dispositivo de oclusión de vasos según se define en la reivindicación independiente 1.
Los elementos fibrosos pueden realizarse de un material bioactivo o un material no... [Seguir leyendo]
Reivindicaciones:
1. Dispositivo de oclusión de vasos para ocluir flujo sanguíneo en un paciente, comprendiendo el dispositivo:
a) una espiral, que comprende un lumen y un primer y un segundo extremo, y dimensionada para la inserción en un punto de uso en una red vascular del paciente;
b) un elemento resistente al estiramiento que presenta un primer extremo unido fijamente al primer extremo de la 5 espiral y un segundo extremo unido fijamente al segundo extremo de la espiral; y
c) una pluralidad de fibras, en el que el dispositivo está caracterizado por el hecho de que cada una de las fibras se envuelve alrededor del elemento resistente al estiramiento por lo menos dos veces.
2. Dispositivo según la reivindicación 1, caracterizado por el hecho de que el elemento resistente al estiramiento atraviesa axialmente el lumen de la espiral. 10
3. Dispositivo según la reivindicación 1, caracterizado por el hecho de que el elemento resistente al estiramiento comprende un alambre metálico.
4. Dispositivo según la reivindicación 3, caracterizado por el hecho de que el alambre metálico comprende un metal seleccionado de platino, paladio, rodio, renio, iridio, oro, plata, tungsteno y tantalio y una aleación de dos o más de estos metales o un metal súper elástico. 15
5. Dispositivo según la reivindicación 1, caracterizado por el hecho de que el elemento resistente al estiramiento comprende un polímero.
6. Dispositivo según la reivindicación 5, caracterizado por el hecho de que el polímero es no biodegradable o biodegradable.
7. Dispositivo según la reivindicación 1, caracterizado por el hecho de que el elemento resistente al estiramiento 20 comprende, además, un revestimiento bioactivo.
8. Dispositivo según la reivindicación 7, caracterizado por el hecho de que el revestimiento bioactivo se selecciona de un factor de crecimiento, un gen, un oligonucleótido, un péptido, un biopolímero marino, un monosacárido, un disacárido, un polisacárido, un colágeno o combinaciones de los anteriormente mencionados.
9. Dispositivo según la reivindicación 7, caracterizado por el hecho de que el revestimiento bioactivo comprende un 25 polímero.
10. Dispositivo según la reivindicación 1, caracterizado por el hecho de que la espiral comprende un alambre metálico.
11. Dispositivo según la reivindicación 10, caracterizado por el hecho de que el alambre metálico comprende un metal seleccionado de platino, paladio, rodio, renio, iridio, oro, plata, tungsteno, tantalio, una aleación de dos o más 30 de estos metales, o un metal súper elástico.
12. Dispositivo según la reivindicación 1, caracterizado por el hecho de que la espiral comprende una hélice principal que ella misma está enrollada en una forma secundaria.
13. Dispositivo según la reivindicación 12, caracterizado por el hecho de que la forma secundaria es una hélice.
14. Dispositivo según la reivindicación 1, caracterizado por el hecho de que las fibras comprenden un material 35 bioactivo o no bioactivo.
15. Dispositivo según la reivindicación 1, caracterizado por el hecho de que las fibras comprenden un copolímero de ácido glicólico o ácido láctico.
16. Dispositivo según la reivindicación 1, caracterizado por el hecho de que las fibras comprenden, además, un revestimiento bioactivo. 40
17. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el revestimiento bioactivo es un revestimiento hidrófilo lubricante o un revestimiento hidrófobo.
18. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el revestimiento bioactivo comprende un copolímero.
19. Dispositivo según la reivindicación 18, caracterizado por el hecho de que el copolímero comprende ácido láctico 45 y ácido glicólico.
20. Dispositivo según la reivindicación 1, caracterizado por el hecho de que las fibras comprenden un polímero no biodegradable.
21. Dispositivo según la reivindicación 20, caracterizado por el hecho de que el polímero no biodegradable se selecciona de un polietileno, un poliacrílico, un polipropileno, un cloruro de polivinilo, una poliamida, un poliuretano, 50
una polivinilpirrolidona, un alcohol polivinílico, un polivinilacetato, un acetato de celulosa, un poliestireno, un politetrafluoroetileno, un poliéster, seda, nailon, tereftalato de polietileno o algodón.
22. Dispositivo según la reivindicación 1, caracterizado por el hecho de que las fibras comprenden un polímero biodegradable.
23. Dispositivo según la reivindicación 22, caracterizado por el hecho de que el polímero biodegradable se 5 selecciona de ácido poliglicólico, policaprolactona, polihidroxibutirato valerato, poliortoéster, ácido poliláctico, poli (p-dioxanona), poli (valetolactona), poli (ácido tartrónico), poli (ácido malónico), poli (fumarato de propileno), un policarbonato a base de tirosina, y un copolímero de polietileneóxido y tereftalato de polibutileno.
24. Dispositivo según la reivindicación 19, caracterizado por el hecho de que la relación entre ácido glicólico y láctico se selecciona de 99:1; 1:99, 95:5; 5:95, 50:50; 90:10 y 10:90. 10
25. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el material de revestimiento se selecciona de un factor de crecimiento, un gen, un oligonucleótido, un péptido, un biopolímero marino, un monosacárido, un disacárido, un polisacárido, un colágeno o combinaciones de los anteriormente mencionados.
26. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el revestimiento bioactivo se aplica a la espiral y al elemento resistente al estiramiento. 15
27. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el revestimiento bioactivo se aplica a la fibra como una única capa.
28. Dispositivo según la reivindicación 26, caracterizado por el hecho de que el revestimiento bioactivo se aplica a la espiral y al elemento resistente al estiramiento en una única capa.
29. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el revestimiento bioactivo se dispersa 20 por toda la fibra.
30. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el revestimiento bioactivo favorece la adhesión celular y es trombogénico.
31. Dispositivo según la reivindicación 16, caracterizado por el hecho de que el material del revestimiento bioactivo se selecciona de colágeno, fibrinógeno, vitronectina, factor de crecimiento endotelial vascular, un péptido que 25 comprende la secuencia arginina - glicina - ácido aspártico (RGD).
32. Dispositivo según la reivindicación 1, caracterizado por el hecho de que cada una de las fibras comprende un primer y un segundo extremo y cada uno del primer y el segundo extremo de las fibras se extiende libremente desde la espiral.
33. Procedimiento para realizar un dispositivo de oclusión de vasos, que comprende las etapas de: 30
a) obtener un núcleo de alambre enrollado helicoidalmente que comprende un lumen, un primer y un segundo extremo y una separación de agarre de fibras entre devanados adyacentes cuando no se encuentra bajo tensión;
b) extender el núcleo de alambre en un estado extendido;
c) insertar un elemento resistente al estiramiento en el lumen del núcleo de alambre enrollado helicoidalmente y unir de manera fija un primer extremo del elemento resistente al estiramiento a por lo menos un extremo del alambre 35 enrollado helicoidalmente;
d) unir fijamente un segundo extremo del elemento resistente al estiramiento a un segundo extremo del alambre enrollado helicoidalmente;
e) envolver una pluralidad de fibras alrededor del elemento resistente al estiramiento por lo menos dos veces; y
f) relajar la espiral provocando de este modo que el devanado adyacente de la espiral agarre las fibras. 40
34. Procedimiento según la reivindicación 33, caracterizado por el hecho de que la envoltura es a través de múltiples devanados de la espiral.
35. Procedimiento según la reivindicación 33, caracterizado por el hecho de que cada una de las fibras comprende un primer y un segundo extremo, comprendiendo el procedimiento, además, disponer el primer y el segundo extremo de cada una de las fibras para extenderse libremente desde la espiral. 45
Patentes similares o relacionadas:
Endoprótesis híbrida helicoidal, del 22 de Julio de 2020, de MEDINOL LTD.: Componente de endoprótesis principal para formar una endoprótesis, que comprende: una sola tira que tiene una pluralidad de arrollamientos […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composición de fármaco y revestimiento asociado, del 1 de Julio de 2020, de W.L. GORE & ASSOCIATES, INC.: Un producto sanitario para administrar un agente terapéutico a un tejido, y el producto tiene una capa de revestimiento aplicada en una superficie del producto, y la capa […]
Método de preparación de un artículo elastomérico antimicrobiano, del 20 de Mayo de 2020, de ALLEGIANCE CORPORATION: Un método de preparación de un artículo elastomérico antimicrobiano, que comprende: recubrir un artículo elastomérico con una composición de recubrimiento antimicrobiano […]
Formulación de Mesna y su uso, del 29 de Abril de 2020, de AuXin Surgery SA: Un dispositivo para administrar una formulación de Mesna a tejidos y/u órganos, que comprende una primera cámara que comprende el Mesna en forma sólida, una segunda cámara […]
Nuevos dispositivo médico y composición para ingeniería tisular basados en A-PRP, máquinas y procesos de fabricación, del 18 de Marzo de 2020, de Regen Lab SA: Una composición que comprende al menos un ácido hialurónico de bajo peso molecular y al menos un ácido hialurónico de alto peso molecular caracterizada por que: […]
Método de fabricación de dispositivos médicos antitrombogénicos, del 12 de Febrero de 2020, de Covidien LP (100.0%): Un metodo para proporcionar un dispositivo medico, en donde el dispositivo medico comprende: un cuerpo tubular expandible que comprende una pluralidad de […]
Emulsiones de copolímero de politetrafluoroetileno, del 12 de Febrero de 2020, de W.L. GORE & ASSOCIATES, INC.: Un método de preparación de una emulsión de agua en disolvente que comprende un copolímero de tetrafluoroetileno disuelto en un disolvente orgánico miscible […]