PROCEDIMIENTO DE TRATAMIENTO DE TRASTORNOS DE OJO SECO Y UVEITIS.
Uso de un portador farmacéuticamente aceptable y una cantidad farmacéuticamente efectiva de un compuesto de fórmula 1:
Tipo: Resumen de patente/invención. Número de Solicitud: W05016646US.
Solicitante: ALCON, INC.
Nacionalidad solicitante: Suiza.
Dirección: BOSCH 69, P.O. BOX 62,6331 HUNENBERG.
Inventor/es: GAMACHE, DANIEL, A., HELLBERG, MARK, R., KLIMKO, PETER, G..
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/047 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen dos o más grupos hidroxilo, p. ej. sorbitol.
- A61K31/22 A61K 31/00 […] › de ácidos acíclicos, p. ej. pravastatina.
Clasificación PCT:
- A61K31/047 A61K 31/00 […] › que tienen dos o más grupos hidroxilo, p. ej. sorbitol.
- A61K31/22 A61K 31/00 […] › de ácidos acíclicos, p. ej. pravastatina.
- A61P27/02 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 27/00 Medicamentos para tratar los trastornos de los sentidos. › Agentes oftálmicos.
Clasificación antigua:
- A61K31/047 A61K 31/00 […] › que tienen dos o más grupos hidroxilo, p. ej. sorbitol.
- A61K31/22 A61K 31/00 […] › de ácidos acíclicos, p. ej. pravastatina.
- A61P27/02 A61P 27/00 […] › Agentes oftálmicos.
Fragmento de la descripción:
Procedimiento de tratamiento de trastornos de ojo seco y uveítis.
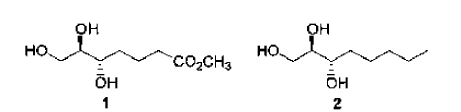
La presente invención está dirigida a la preparación de un medicamento para el tratamiento de los trastornos de ojo seco. Particularmente, la presente invención está dirigida hacia el uso de ácido 5,6,7-trihidroxiheptanoico y sus análogos según la fórmula (1), para la preparación de un medicamento para el tratamiento del ojo seco y la uveítis en mamíferos.
Antecedentes de la invención
El ojo seco, también conocido genéricamente como keratoconjunctivitis sicca, es un trastorno oftalmológico común que afecta a millones de americanos cada año. La condición está particularmente extendida entre las mujeres post-menopáusicas debido a los cambios hormonales que siguen al cese de la fertilidad. El ojo seco puede afligir a un individuo con una gravedad variable. En los casos leves, un paciente puede experimentar ardor, una sensación de sequedad e irritación persistente, tal como los causados frecuentemente por pequeños cuerpos que se alojan entre el párpado del ojo y la superficie del ojo. En los casos graves, la visión puede ser considerablemente perjudicada. Otras enfermedades, tales como la enfermedad de Sjögren, y penfigoide cicatricial manifiestan complicaciones de ojo seco.
Aunque parece que el ojo seco puede resultar de una serie de causas patogénicas no relacionadas, todas las presentaciones de la complicación comparten un efecto común, que es la rotura de la película lagrimal preocular, lo que resulta en la deshidratación de la superficie exterior expuesta y muchos de los síntomas indicados anteriormente (Lemp, Report of the National Eye Institute/Industry Workshop on Clinical Trials in Dry Eyes, The CLAO Journal, volumen 21, número 4, páginas 221-231 (1995)).
Los médicos han adoptado varios enfoques respecto al tratamiento del ojo seco. Un enfoque común ha sido suplementar y estabilizar la película lagrimal ocular usando las denominadas lágrimas artificiales instiladas a lo largo del día. Otros enfoques incluyen el uso de inserciones oculares que proporcionan un sustituyente de lágrima o estimulación de la producción de lágrima endógena.
Los ejemplos del enfoque de sustitución de lágrima incluyen el uso de soluciones salinas isotónicas tamponadas, soluciones acuosas que contienen polímeros solubles en agua que hacen la solución más viscosa y de, esta manera, que se derramen menos fácilmente por el ojo. La reconstitución de la lágrima se intenta también proporcionando uno o más componentes de la película lacrimal, tal como fosfolípidos y aceites. Las composiciones fosfolípidas han demostrado ser útiles en el tratamiento del ojo seco; véase, por ejemplo, McCulley and Shine, Tear film structure and dry eye, Contactologia, volumen 20 (4), páginas 145-49 (1998); y Shine and McCulley, Keratoconjunctivitis sicca associated with meibomian secretion polar lipid abnormality, Archives of Ophthalmology, volumen 116 (7), páginas 849-52 (1998). Ejemplos de composiciones fosfolípidas para el tratamiento del ojo seco se divulgan en las patentes US Nos. 4.131.651 (Shah et al.), 4.370.325 (Packman), 4.409.205 (Shively), 4.744.980 y 4.883.658 (Holly), 4.914.088 (Glonek), 5.075.104 (Gressel et al.), 5.278.151 (Korb et al.), 5.294.607 (Glonek et al.), 5.371.108 (Korb et al.) y 5.578.586 (Glonek et al.). La patente U.S. No. 5.174.988 (Mautone et al.) divulga sistemas de suministro de fármacos fosfolípidos que implican fosfolípidos, propelentes y una sustancia activa.
Otro enfoque implica la provisión de sustancias lubricantes en vez de lágrimas artificiales. Por ejemplo, la patente U.S. No. 4.818.537 (Guo) divulga el uso de una composición lubricante basada en liposomas y la patente U.S. No. 5.800.807 (Hu et al.) divulga composiciones que contienen glicerina y propilenglicol para tratar el ojo seco.
Aunque estos enfoques han encontrado cierto éxito, sin embargo persisten problemas en el tratamiento del ojo seco. El uso de sustituyentes de lágrima, aunque temporalmente efectivo, requiere generalmente de una aplicación repetida a lo largo de las horas de vigilia de un paciente. No es poco común para un paciente tener que aplicar una solución de lágrima artificial de diez a veintes veces a lo largo del día. Dicha tarea, además de ser molesta y requerir tiempo, es potencialmente muy cara. Se ha informado de que los síntomas transitorios de ojo seco asociados con cirugía refractiva duran, en algunos casos, de seis semanas a seis meses o más después de la cirugía.
Aparte de los esfuerzos dirigidos principalmente al alivio de los síntomas asociados con el ojo seco, se han perseguido también procedimientos y composiciones dirigidas al tratamiento de la condición de ojo seco. Por ejemplo, la patente U.S. No. 5.041.434 (Lubkin) divulga el uso de exteroides sexuales, tales como estrógenos conjugados, para tratar las condiciones de ojo seco en mujeres post-menopáusicas; la patente U.S. No. 5.290.572 (MacKeen) divulga el uso de composiciones iónicas de calcio finamente dividido para estimular la producción de película lacrimal preocular; y la patente U.S. No. 4.966.773 (Gressel et al.) divulga el uso de partículas microfinas de uno o más retinoides para la normalización del tejido ocular.
Algunos informes de la literatura reciente sugieren que los pacientes que padecen síndrome de ojo seco exhiben, de manera desproporcionada, las características distintivas de inflamación excesiva en tejidos oculares relevantes, tales como las glándulas meibomianas y lacrimales. Se ha divulgado el uso de varios compuestos para tratar a los pacientes de ojo seco, tales como esteroides [por ejemplo, la patente U.S. No 5.958.912; Marsh, et al., Topical nonpreserved methylprednisolone therapy for keratoconjunctivitis sicca in Sjögren syndrome, Ophthalmology, 106 (4): 811-816 (1999); Pflugfelder, et al. Patente U.S. No. 6.153.607], inhibidores de liberación de citoquina (Yanni, J.M.; et al. WO 0003705 A1), ciclosporina A [Tauber, J. Adv. Exp. Med. Biol. 1998, 438 (Lacrimal Gland, Tear Film, and Dry Eye Syndromes 2), 969], y 15-HETE (Yanni et al., Patente US No. 5.696.166).
La uveítis es una condición inflamatoria intraocular que se limitada normalmente a las estructuras oculares anteriores y puede ser gestionadas con corticoesteroides tópicos. El proceso inflamatorio puede extenderse detrás de las lentes para afectar la pars plana, la cavidad vítrea, la coroides y la retina. Estas manifestaciones intermedias y posteriores son relativamente raras pero contribuyen, de manera desproporcionada, a morbosidad visual y presentan serias dificultades terapéuticas. Los corticoesteroides tópicos constituyen la primera línea de tratamiento para la mayoría de las uveítis que suponen una amenaza para la visión. Su uso prolongado está limitado por los efectos adversos debilitantes y universales. Los agentes de segunda línea que permiten una reducción del uso de esteroides, tales como ciclosporina y azatioprina, ofrecen enfoques alternativos. Desafortunadamente, su uso está limitado frecuentemente por una estrecha ventana terapéutica y efectos secundarios adversos considerables.
Lee et al. han divulgado que los compuestos 1 y 2 inhiben la quimotaxis inducida por LTB4 de neutrófilos tan potentes como lipoxina A4 [Lee et al., Biochemical and Biophysical Research Communications 1991, 180 (3), 1416-21]. Se ha informado de que la lipoxina A4 y ciertos análogos de la misma son agentes antiinflamatorios (véase, por ejemplo, Serhan et al., patente US número 5.441.951). Se han reivindicado ciertos análogos de lipoxina para tratar el ojo seco (Gamache et al., Patente US No. 6.645.978 B1). Sin embargo, conforme a nuestro conocimiento, no se ha descrito ningún compuesto de la presente invención para tratar el ojo seco o la uveítis.
Resumen de la invención
La presente invención está dirigida a la elaboración de un medicamento para el tratamiento del ojo seco y la uveítis. Según los usos de la presente invención, un ácido 5,6,7-trihidroxiheptanoico o un análogo según la fórmula (1) es usado en la elaboración de un medicamento a ser administrado a un paciente. Preferentemente, el ácido 5,6,7-trihidroxiheptanoico o análogo según la fórmula (1) se administrará en una composición oftálmica dosificada tópicamente a un ojo de un paciente.
Descripción detallada de la invención
Si no se indica...
Reivindicaciones:
1. Uso de un portador farmacéuticamente aceptable y una cantidad farmacéuticamente efectiva de un compuesto de fórmula 1:
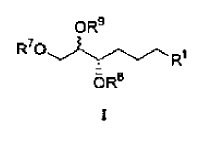
en la que
2. Uso según la reivindicación 1, en el que para el compuesto de fórmula 1:
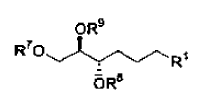
3. Uso según la reivindicación 2, en el que el compuesto de fórmula 1 tiene la configuración:
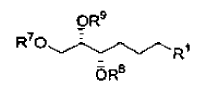
4. Uso según la reivindicación 1, en el que el compuesto de fórmula 1 tiene la configuración:
5. Uso según la reivindicación 3, en el que el medicamento es para tratar la uveítis.
6. Uso según la reivindicación 3, en el que el medicamento es para tratar el ojo seco.
7. Uso según la reivindicación 5, en el que el compuesto es seleccionado de entre el grupo que comprende:
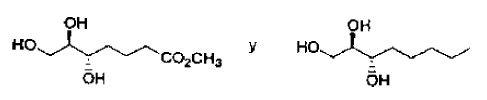
8. Uso según la reivindicación 6, en el que el compuesto es seleccionado de entre el grupo que comprende:
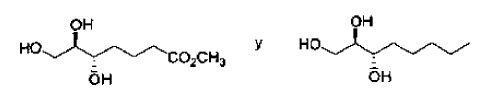
9. Uso según la reivindicación 5, en el que la cantidad farmacéuticamente aceptable es de 0,1 a 1% (p/v).
10. Uso según la reivindicación 6, en el que la cantidad farmacéuticamente aceptable es de 0,00003 a 0,001% (p/v).
11. Uso según la reivindicación 9, en el que el portador farmacéuticamente aceptable comprende uno o más ingredientes seleccionados de entre el grupo que comprende tensoactivos, agentes de tonicidad, tampones, conservantes, co-solventes y agentes para aumentar la viscosidad.
12. Uso según la reivindicación 10, en el que el portador farmacéuticamente aceptable comprende uno o más ingredientes seleccionados de entre el grupo que comprende tensoactivos, agentes de tonicidad, tampones, conservantes, co-solventes y agentes para aumentar la viscosidad.
Patentes similares o relacionadas:
Formulaciones farmacéuticas de estatinas y ácidos grasos omega-3 para encapsulación, del 27 de Mayo de 2020, de Catalent Ontario Limited: Una cápsula de gelatina blanda multifase para administración oral, comprendiendo la cápsula de gelatina blanda: una forma de dosificación […]
Proteínas de unión a antígeno para proproteína convertasa subtilisina kexina tipo 9 (PCSK9), del 6 de Mayo de 2020, de AMGEN INC.: Una proteína de unión a antígeno, donde dicha proteína de unión a antígeno (i) comprende (a) un dominio variable de cadena ligera que comprende una secuencia […]
Análogos deuterados de ácido 4hidroxibutírico, del 8 de Abril de 2020, de CONCERT PHARMACEUTICALS, INC: Una composición farmacéutica que comprende un compuesto de Fórmula IV **(Ver fórmula)** en la que: A es hidrógeno, deuterio, -CH2-C(O)OR2 o -CH(R1)-C(O)OR2; […]
Composición farmacéutica para administración oral que comprende una concentración elevada de taxano, del 18 de Marzo de 2020, de Dae Hwa Pharma. Co., Ltd: Una composición farmacéutica para administración oral, que comprende (a) de un 4 a un 40 % en peso de un taxano, (b) de un 10 a un 30 % en peso de un triglicérido de cadena […]
Composiciones tópicas que comprenden fipronilo y permetrina y procedimientos de uso, del 22 de Enero de 2020, de Boehringer Ingelheim Animal Health USA Inc: Composición tópica para el tratamiento y prevención de una infestación ectoparasitaria que comprende: de 2% (p/p) a 15% (p/p) de fipronil; […]
Trastornos neurodegenerativos y métodos de tratamiento y diagnóstico de los mismos, del 8 de Enero de 2020, de THE UNIVERSITY OF QUEENSLAND: Triheptanoína para su uso en el tratamiento, prevención y/o retraso del inicio de una enfermedad de la neurona motora (MND) en un animal, en el que […]
Composición que contiene el compuesto de monoacetil diacilglicerol como principio activo para prevenir o tratar la dermatitis atópica, del 1 de Enero de 2020, de Enzychem Lifesciences Corporation: Una composición para uso en la prevención o el tratamiento de la dermatitis atópica, en donde la composición es para administración oral y en donde la composición comprende […]
Composición que contiene un compuesto de monoacetildiacilglicerol como principio activo para la prevención o tratamiento de enfermedades pulmonares obstructivas crónicas, del 1 de Enero de 2020, de Enzychem Lifesciences Corporation: Composición farmacéutica que comprende un compuesto de monoacetildiacilglicerol de Fórmula 1 como principio activo para utilizar en la prevención o el tratamiento […]