SISTEMAS YH METODOS PARA CUIDADO DE ORGANOS EX-VIVO.
Un módulo desechable de uso individual (634) para un sistema de preservación de corazón,
comprendiendo el módulo desechable de uso individual un chasis (635) dimensionado y conformado para interasegurar el módulo de uso individual (634) con un módulo de uso múltiple (650) para la interoperación electromecánica en un sistema de preservación de corazón, un dispositivo de cámara de órganos (104) montado al chasis para contener un corazón durante la perfusión y que incluye una interfaz para conectar a una vena pulmonar del corazón caracterizado por una interfaz de bomba (300) para recibir una fuerza de bombeo desde una bomba (334) para trasladar la fuerza de bombeo a un fluido de perfusión para bombear el fluido de perfusión (108) al dispositivo de cámara de órgano y porque dicho dispositivo de cámara de órgano incluye una interfaz (162) para conectar a una aorta (158) del corazón
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/036211.
Solicitante: TRANSMEDICS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 600 WEST CUMMINGS PARK, SUITE 3050 WOBURN, MA 01801 ESTADOS UNIDOS DE AMERICA.
Inventor/es: TAYLOR, RONALD, NEWELL, SCOTT, ELBETANONY,AHMED, OCHS,BURT, LEZBERG,PAUL, CARPENTER,DAVID, BRINGHAM,RICHARD, SOUSA,DENNIS, FISHMAN,ROBERT, HASSANEIN,WALEED, GOFF,LAWRENCE, KYI,STANLEY, CECERE,GIOVANNI, ALGAMIL,HOSS, KHAYAL,TAMER, ROURKE,JOHN.
Fecha de Publicación: .
Fecha Solicitud PCT: 7 de Octubre de 2005.
Fecha Concesión Europea: 9 de Junio de 2010.
Clasificación Internacional de Patentes:
- A01N1/02 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › A01N 1/00 Conservación de cuerpos humanos o animales, o partes de ellos. › Conservación de partes vivas.
- A01N1/02M2P
Clasificación PCT:
- A01N1/02 A01N 1/00 […] › Conservación de partes vivas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Campo de la invención La invención se refiere en general a sistemas, métodos y dispositivos para el cuidado de órganos ex-vivo. Más particularmente, en diversas realizaciones, la invención se relaciona con el cuidado de un órgano ex-vivo en condiciones fisiológicas o cercanas a las fisiológicas. Antecedentes de la invención Las técnicas de preservación de órganos actuales involucran típicamente el almacenamiento hipotérmico del órgano en una solución de perfusión química sobre hielo. En el caso de un corazón este es detenido típicamente y luego enfriado con la solución de almacenamiento/cardioplégica en un estado hipotérmico, no funcional. Estas técnicas utilizan una variedad de soluciones cardioplégicas, ninguna de las cuales protege suficientemente el corazón de daño en el miocardio resultante de la isquemia. Tales lesiones son particularmente indeseables cuando un órgano, tal como un corazón, pretende ser transplantado de un donante a un receptor. Además, del daño del miocardio que resulta de la isquemia, la reperfusión de un corazón puede exacerbar la lesión del miocardio y puede causar lesiones vasculares coronarias endoteliales y el músculo liso, que pueden llevar a una disfunción vasomotora coronaria. Usando modalidades convencionales, tales lesiones se incrementan como una función de la longitud de tiempo que un órgano es mantenido ex-vivo. Por ejemplo, en el caso de un corazón, típicamente puede mantenerse ex-vivo solamente por unas pocas horas antes de que sea inutilizable para un transplante. Este período de tiempo relativamente breve limita el número de receptores que pueden ser alcanzados desde un sitio dado del donante, restringiendo por lo tanto el número de receptores para un corazón recolectado. Aún dentro de las pocas horas de límite de tiempo, el corazón sin embargo puede ser dañado significativamente. Un asunto significativo es que no puede haber una indicación evidente del daño. Debido a esto, pueden transplantarse menos órganos en estado óptimo, dando como resultado una disfunción del órgano postransplante u otras lesiones. Así, sería deseable desarrollar técnicas que puedan extender el tiempo durante el cual un órgano puede ser preservado en un estado ex-vivo saludable. Tales técnicas reducirían el riesgo de fallos en un transplante y aumentarían las reservas de donantes y receptores potenciales. La preservación efectiva de un órgano ex-vivo también proveería numerosos otros beneficios. Por ejemplo, una preservación prolongada ex-vivo permitiría un monitoreo y prueba funcional más cuidadoso del órgano recolectado. Esto a su vez permitiría una detección más temprana y reparación potencial de defectos en el órgano recolectado, reduciendo adicionalmente la probabilidad de fallos en el transplante. La capacidad para llevar a cabo reparaciones sencillas en el órgano también permitiría que muchos órganos con defectos menores sean salvados, mientras que las técnicas de transplante actuales requieren que sean descartados. Además, puede alcanzarse una coincidencia más efectiva entre el órgano y un receptor particular, reduciendo adicionalmente la probabilidad de un rechazo eventual del órgano. Las técnicas actuales de transplante se basan fundamentalmente en la coincidencia en los tipos sanguíneos del donante y el receptor, lo cual por si mismo es un indicador relativamente no confiable de si el órgano va a ser o no rechazado por el receptor. Una prueba más preferida de compatibilidad de órganos es una prueba de comparación del Antígeno de Leucocito Humano (HLA), pero las modalidades de preservación de órganos isquémicos en frío actuales impiden el uso de esta prueba, la cual puede frecuentemente requerir 12 horas o más para terminarse.
El cuidado prolongado y confiable de órganos ex-vivo también proveería beneficios fuera del contexto del transplante de órganos. Por ejemplo, un cuerpo de un paciente, como un todo, puede tolerar típicamente niveles mucho más bajos de quimio, bio y radioterapia que muchos órganos en particular. Un sistema de cuidado de órganos ex-vivo puede permitir que un órgano sea retirado del cuerpo y tratado aisladamente, reduciendo el riesgo de daño a otras partes del cuerpo. La US 6,673,594 divulga un aparato de acuerdo con la porción precaracterizante de la reivindicación
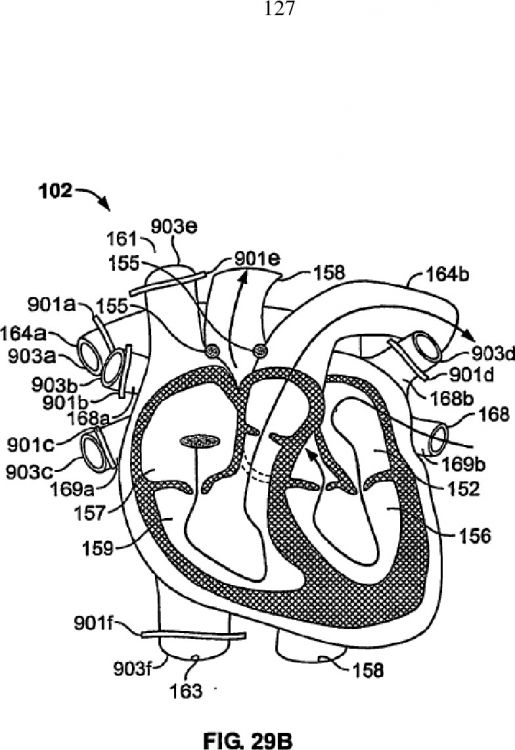
1. Resumen de la invención La presente invención proporciona un módulo desechable de uso individual para un sistema de preservación de corazón de acuerdo con la reivindicación 1. La invención apunta a las deficiencias de la técnica anterior, mediante, en varias realizaciones, la provisión de sistemas como métodos y dispositivos mejorados relativos con el cuidado de órganos ex-vivo portátiles Breve descripción de los dibujos Las siguientes figuras representan realizaciones ilustrativas de la invención en las cuales numerales de referencia se refieren a elementos similares. Estas realizaciones representadas pueden no estar dibujadas a escala y deben entenderse como ilustrativas de la invención y no como limitantes, siendo a cambio el alcance de la invención definido por las reivindicaciones anexas. La Figura 1 es un diagrama esquemático de un sistema de cuidado de órganos portátil de acuerdo con una realización ilustrativa de la invención. La Figura 2 es un diagrama que representa un corazón recolectado. La Figura 3 es un diagrama conceptual que representa el corazón recolectado de la Figura 2 interconectado con el sistema de cuidado de órganos de la Figura 1 en una configuración de modo de flujo normal de acuerdo con una realización ilustrativa de la invención. La Figura 4 es un diagrama conceptual que representa al corazón recolectado de la Figura 2 interconectado con el sistema de cuidado de órganos de la Figura 1 en una configuración de modo de flujo retrógrado de acuerdo con una realización ilustrativa de la invención. Las Figuras 5A-5F muestran diversas vistas de un ensamblaje de cámara para órganos del tipo empleado en el sistema de cuidado de órganos de la Figura 1 de acuerdo con una realización ilustrativa de la invención. Las Figuras 6A-6F muestran pistas diversas de un dispositivo calentador por perfusión del tipo empleado en el sistema de cuidado de órganos de la Figura 1 de acuerdo con una realización ilustrativa de la invención. La Figura 7 muestra una vista más detallada de un elemento calentador resistivo a título de ejemplo del tipo empleado en la disposición de calentamiento de las Figuras 6A-6F. Las Figuras 8A-8C muestran diversas vistas de un dispositivo de interfaz de bomba de fluidos por perfusión de acuerdo con una realización ilustrativa de la invención. La Figura 9 muestra una vista en perspectiva de un lado del impulsor de bomba de un dispositivo de bomba de fluidos de perfusión del tipo representado en la Figura 1, junto con un soporte para montar con el dispositivo de interfaz de bomba de perfusión. La Figura 10 muestra una vista lateral del dispositivo de interfaz de bomba para fluidos por perfusión de las Figuras 8A-8C acoplado con el lado impulsor de la bomba del dispositivo de bomba de fluidos de perfusión de la Figura 9. La Figura 11 representa un diagrama de bloques de un esquema de control ilustrativo para controlar la operación del sistema de cuidado de órganos de la Figura 1.
La Figura 12 es un diagrama de bloques de un subsistema de adquisición de datos a título de ejemplo del tipo que puede ser empleado con un sistema de cuidado de órganos ilustrativo de La Figura 1. La Figura 13 es un diagrama de bloques de un subsistema del control de calentamiento a título de ejemplo del tipo que puede ser empleado para mantener la temperatura del fluido de perfusión en el sistema de cuidado de órganos ilustrativo de la Figura 1. La Figura 14 es un diagrama de bloques de un subsistema de manejo de potencia a título de ejemplo del tipo que puede ser empleado en el sistema de cuidado de órganos ilustrativo de la Figura 1. La Figura 15 es un diagrama de bloques de un subsistema de control de bombeo a título de ejemplo del tipo que puede ser empleado para controlar la operación de un dispositivo de bomba para fluidos de perfusión en el sistema de cuidado de órganos ilustrativo de La Figura 1. La Figura 16 es una gráfica que representa una onda r con la cual el subsistema de control de bombeo de la Figura 15 se sincroniza de acuerdo con una realización ilustrativa de la invención. Las Figuras 17A-17J representan pantallas de despliegue a título de ejemplo del tipo que pueden ser empleadas con una interfaz de operador de acuerdo con una realización ilustrativa de la invención. Las Figuras 18A y 18B muestran una implementación a título de ejemplo del sistema de la Figura 1 de acuerdo con una realización ilustrativa de la invención. Las Figuras 19A-19C muestran...
Reivindicaciones:
1. Un módulo desechable de uso individual (634) para un sistema de preservación de corazón, comprendiendo el módulo desechable de uso individual un chasis (635) dimensionado y conformado para interasegurar el módulo de uso individual (634) con un módulo de uso múltiple
(650) para la interoperación electromecánica en un sistema de preservación de corazón, un dispositivo de cámara de órganos (104) montado al chasis para contener un corazón durante la perfusión y que incluye una interfaz para conectar a una vena pulmonar del corazón caracterizado por una interfaz de bomba (300) para recibir una fuerza de bombeo desde una bomba (334) para trasladar la fuerza de bombeo a un fluido de perfusión para bombear el fluido de perfusión (108) al dispositivo de cámara de órgano y porque dicho dispositivo de cámara de órgano incluye una interfaz (162) para conectar a una aorta (158) del corazón.
2. El módulo de uso individual de la reivindicación 1 que comprende una tercera interfaz (166) para conectar a una arteria pulmonar (164) del corazón.
3. El módulo de uso individual de la reivindicación 2, donde el dispositivo de cámara incluye aberturas (228) a través de las cuales pasan las interfaces de la arteria pulmonar y la aorta.
4. El módulo de uso individual de la reivindicación 1 que comprende un reservorio (160) para contener el fluido de perfusión montado sobre el chasis y en comunicación fluida con el dispositivo de cámara de órganos.
5. El módulo de uso individual de la reivindicación 1 que comprende una válvula de selección de flujo (112) para seleccionar el bombeo entre el fluido de perfusión a la interfaz de la aorta y el bombeo del fluido de perfusión a la interfaz de vena pulmonar.
6. El módulo de uso individual de la reivindicación 1 que comprende un calentador de fluidos (110) para mantener al menos el fluido de perfusión que se provee al dispositivo de cámara de órganos a una temperatura entre aproximadamente 32ºC y aproximadamente 37ºC
7. El módulo de uso individual de la reivindicación 6, donde el calentador de fluido incluye al menos una placa calentada (250, 252) en contacto directo con el fluido de perfusión.
8. El módulo de uso individual de la reivindicación 7 que incluye al menos un sensor de temperatura (120, 122) para detectar una temperatura de la placa calentada.
9. El módulo de uso individual de la reivindicación 6, donde el calentador de fluido incluye un par de placas calentadas (250, 252) entre las cuales fluye el fluido de perfusión que va a ser calentado.
10. El módulo de uso individual de la reivindicación 6 que comprende un sensor de temperatura
(124) para detectar la temperatura del fluido de perfusión.
11. El módulo se uso individual de la reivindicación 10, donde el sensor de temperatura detecta la temperatura del fluido de perfusión bien a medida que sale o entra del calentador de fluidos.
12. El módulo de uso individual de la reivindicación 6, donde el calentador de fluidos incluye un elemento calentador en (286) en contacto con una placa, siendo la placa para contacto directo con el fluido de perfusión.
13. El módulo de uso individual de la reivindicación 12 que comprende un sensor de temperatura (120, 122) para detectar la temperatura del elemento calentador.
14. El módulo de uso individual de la reivindicación 1, que comprende una interfaz óptica (678) para comunicar con una interfaz óptica correspondiente sobre el módulo de uso múltiple cuando se interasegura con el módulo de uso múltiple.
15. El módulo de uso individual de la reivindicación 1 que comprende un oxigenador (114) en comunicación fluida con el reservorio para proveer oxígeno al fluido de perfusión.
16. El módulo de uso individual de la reivindicación 1 que comprende un sensor de oxígeno (140) para determinar un nivel de oxígeno y preferiblemente un nivel de saturación de oxígeno en el fluido de perfusión.
17. El módulo de uso individual de la reivindicación 16, donde el sensor de oxígeno mide un hematocrito del fluido de perfusión.
18. El módulo de uso individual de la reivindicación 16, donde el sensor de oxígeno está posicionado para medir el nivel de oxígeno del fluido de perfusión que entra al corazón.
19. El módulo de uso individual de la reivindicación 16, donde el sensor de oxígeno esta posicionado en un camino de flujo de perfusión hacia fuera del corazón.
20. El módulo de uso individual de la reivindicación 16, donde el sensor de oxígeno incluye una cubeta en línea (812) a través de la cual pasa el fluido de perfusión, una fuente óptica (816) para dirigir la luz hacia el fluido de perfusión que pasa a través de la cubeta, y un sensor óptico (816) para medir una calidad óptica del fluido de perfusión que pasa a través de la cubeta.
21. El módulo de uso individual de la reivindicación 16, donde el sensor de oxígeno incluye una cubeta en línea sin uniones a través de la cual pasa el fluido de perfusión.
22. El módulo de uso individual de la reivindicación 1 que comprende un sensor de rata de flujo (134, 136, 138) para detectar una rata de flujo del fluido de perfusión hacia o desde el dispositivo de cámara de órganos.
23. El módulo de uso individual de la reivindicación 6 que comprende una cámara de equilibrio (186) localizada entre el calentador de fluidos y el dispositivo de cámara de órganos.
24. El módulo de uso individual de la reivindicación 23, donde la cámara de equilibrio está localizada entre el calentador de fluidos y una interfaz del dispositivo de cámara de órganos para conectar bien sea a una vena pulmonar o a una aorta de un corazón.
25. El módulo de uso individual de la reivindicación 6 que comprende una cámara de equilibrio (188) localizada entre la interfaz de bomba y el calentador de fluidos.
26. El módulo de uso individual de la reivindicación 1 que comprende un puerto de muestreo (754, 755 758) para tomar muestras de fluidos desde el dispositivo de cámara de órganos.
27. El módulo de uso individual de la reivindicación 1 que comprende una pluralidad de puertos para tomar muestras de fluidos desde el dispositivo de cámara de órganos, interasegurado de tal manera que el fluido de muestra de uno primero de la pluralidad de puertos evita la toma de muestras simultáneamente de fluidos de un segundo puerto de la pluralidad.
28. El módulo de uso individual de la reivindicación 1 que comprende uno o más procesadores (150) para recolectar información de uno o más sensores en un módulo de uso individual.
29. El módulo de uso individual de la reivindicación 28 que comprende una interfaz óptica para proveer la información de uno o más sensores al módulo de uso múltiple.
30. El módulo de uso individual de la reivindicación 1, donde la interfaz de bomba se monta sobre el chasis del módulo de uso individual e incluye características (332 328) para interasegurar con características coincidentes en la bomba en respuesta al interaseguramiento entre los módulos de uso individual y uso múltiple para formar una interconexión hermética a los fluidos entre la interfaz de bomba y la bomba.
31. El módulo de uso individual de la reivindicación 1 que comprende extender axialmente protuberancias sobre la interfaz de bomba, estando las protuberancias dimensionadas y conformadas hasta aproximadamente para descansar sobre una o más superficies del módulo de
61 uso múltiple durante el interaseguramiento entre el módulo de uso múltiple y el módulo de uso individual para ejercer una fuerza de compresión entre la interfaz de bomba y la bomba de tal forma que la interfaz de bomba esté alineada para recibir una cabeza impulsora de bomba.
32. El módulo de uso individual de la reivindicación 1, donde la interfaz de bomba incluye una membrana flexible (316, 318) para aislar el fluido de perfusión de la bomba.
33. El módulo de uso individual de la reivindicación 1, donde el dispositivo de cámara de órganos incluye una primera cubierta con pestañas (198) para cubrir el dispositivo de cámara de órganos, incluyendo la primera cubierta con pestañas un marco externo (198a) y una membrana plegable flexible (198b) dispuesta sobre el marco exterior.
34. El módulo de uso individual de la reivindicación 33, donde la membrana plegable flexible está dimensionada y conformada para extenderse dentro del dispositivo de cámara de órganos.
35. El módulo de uso individual de la reivindicación 1, donde el dispositivo de cámara de órganos incluye una segunda cubierta con pestañas (196) para cubrir la primera cubierta con pestañas.
36. El módulo de uso individual de la reivindicación 35, donde la segunda cubierta con pestañas es sustancialmente rígida.
37. El módulo de uso individual de la reivindicación 1, donde el dispositivo de cámara de órganos incluye una interfaz de vena pulmonar para la interconexión de fluidos con una vena pulmonar del corazón.
38. El módulo de uso individual de la reivindicación 1, donde el dispositivo de cámara de órganos incluye un dispositivo de almohadillas (222) para soportar el corazón, incluyendo el dispositivo de almohadillas uno o más de al menos un electrodo (142, 144) para proporcionar estimulación eléctrica al corazón; o al menos un sensor para monitorear las señales eléctricas del corazón.
39. El módulo de uso individual de la reivindicación 38, donde el al menos un electrodo sensor está dimensionado, conformado y posicionado sobre el dispositivo de almohadilla para proveer interconexión sin suturas con el corazón.
40. El módulo de uso individual de la reivindicación 38, donde las señales incluyen una onda r para el corazón.
41. El módulo de uso individual de la reivindicación 1, donde el dispositivo de cámara de órganos incluye una membrana resellable (230) para resellar automáticamente después de ser perforada.
42. El módulo de uso individual de la reivindicación 1, donde el dispositivo de cámara de órganos incluye un tubo de desviación (810) para transferir el fluido de perfusión a través de una parte interna del dispositivo de cámara de órganos entre la interfaz de la aorta y la tercera interfaz, y entre la interfaz de vena pulmonar y la tercera interfaz.
43. El módulo de uso individual de la reivindicación 5 que comprende una línea por goteo (769) para proveer un flujo lento de un fluido de perfusión hacia la interfaz de aorta cuando la interfaz de vena pulmonar es seleccionada en la válvula selectora de flujo.
44. El módulo de uso individual de la reivindicación 1 que comprende un puerto de infusión (766) para inyectar soluciones químicas en el fluido de perfusión.
45. El módulo de uso individual de la reivindicación 1 que comprende adicionalmente, un reservorio (160) montado en el chasis en comunicación fluida con el dispositivo de cámara de órganos dimensionado y conformado para contener el fluido de perfusión para el corazón, y un calentador (110) para mantener al menos el fluido de perfusión provisto al dispositivo de cámara de órganos a una temperatura entre aproximadamente 32ºC y aproximadamente 37ºC.
46. El módulo de uso individual de la reivindicación 1 que comprende adicionalmente, un reservorio 160 montado al chasis en comunicación fluida con el dispositivo de cámara de órganos dimensionado y conformado para contener fluido de perfusión para el corazón, y un procesador 150 para monitorear y controlar, al menos en parte la operación del módulo inteligente de uso individual.
47. Un sistema de cuidado de órganos que comprende: un módulo de uso múltiple portátil que incluye un chasis portátil; y un módulo desechable de uso individual interoperable de acuerdo con cualquier reivindicación precedente.
48. El sistema de la reivindicación 47 cuando es dependiente de la reivindicación 6, donde el calentador es un calentador de estado sólido.
49. El sistema de la reivindicación 47 cuando es dependiente de la reivindicación 6, donde el calentador es localizado en uno de los módulos de uso individual desechable del módulo de uso múltiple portátil.
50. El sistema de la reivindicación 47 que comprende un oxigenador (114) en comunicación fluida con un suministro de gas que contiene oxígeno para proveer el gas que contiene oxígeno al fluido de perfusión.
51. El sistema de la reivindicación 50 donde el suministro de gas es un suministro de gas incorporado (172).
52. El sistema de la reivindicación 47 que comprende al menos un procesador (150) para recolectar información de uno o más sensores sobre el módulo desechable, y para proveer la información a una interfaz de usuario.
53. El sistema de la reivindicación 47 que comprende al menos un procesador, localizado sobre el módulo de uso múltiple para controlar, al menos en parte, la operación del módulo de uso individual desechable.
54. El sistema de la reivindicación 47 que incluye al menos un procesador para recolectar información de uno o más sensores, para identificar las anormalidades de operación y para comunicar las anormalidades de operación al módulo de uso múltiple portátil.
55. El sistema de la reivindicación 47 que comprende una bomba pulsátil (106) y un controlador para controlar una característica de bombeo de la bomba pulsátil con base al menos en parte en una característica fisiológica monitoreada de un corazón contenido en el dispositivo de cámara de órganos.
56. El sistema de la reivindicación 55 donde las características fisiológicas incluyen una rata a la cual el corazón está latiendo, incluyendo las características de bombeo o un volumen de detención en el cual la bomba pulsátil bombea, y el controlador ajusta el volumen de detención de la bomba pulsátil en respuesta a la rata a la cual está latiendo el corazón.
57. El sistema de la reivindicación 55, donde la característica de bombeo incluye un tiempo en el cual la bomba bombea el fluido de perfusión hacia el corazón, incluyendo la característica fisiológica una representación de una porción del corazón que está en un estado diastólico, y el controlador bombea el fluido de perfusión al corazón durante el estado diastólico de la porción del corazón.
58. El sistema de la reivindicación 57, donde el estado diastólico es un estado diastólico de un ventrículo del corazón y donde el ventrículo es un ventrículo izquierdo.
59. El sistema de la reivindicación 57, donde el estado diastólico es un estado diastólico de un atrio del corazón y donde el atrio es un atrio derecho.
60. El sistema de la reivindicación 55, donde la característica de bombeo incluye una conformación de forma de onda representativa de una rata y un volumen de detención en el cual la bomba bombea el fluido de perfusión al corazón, y el controlador altera la conformación de la forma de onda en respuesta a la característica fisiológica del corazón.
61. El sistema de la reivindicación 55, donde la característica de bombeo incluye un volumen de flujo de fluido por unidad de tiempo en el cual la bomba bombea el fluido de perfusión y el controlador altera el volumen de flujo en respuesta a la característica fisiológica del corazón.
62. El sistema de la reivindicación 55 donde la característica fisiológica incluye una onda r del corazón y el controlador sincroniza el bombeo del fluido de perfusión con la onda r.
63. El sistema de la reivindicación 55 donde la característica fisiológica incluye una onda r del corazón y donde la bomba es sincronizada para bombear el fluido de perfusión con la bomba r, y es ajustada por un retraso de bombeo seleccionable.
64. El sistema de la reivindicación 55, donde la característica fisiológica es indicativa de la presión y preferiblemente incluye una rata de flujo de fluido hacia afuera del corazón.
65. El sistema de la reivindicación 47 que incluye un sistema de baterías tolerante a los fallos que incluye una pluralidad de baterías (352a-352c) interaseguradas de tal manera que toda la pluralidad de baterías no puede ser retirada del sistema al menos mientras el sistema está en operación.
66. El sistema de la reivindicación 47 que incluye una interfaz de usuario inalámbrica para proveer información y para recibir comandos desde un operador.
67. Un método para preservar un corazón ex-vivo que comprende, colocar un corazón en el dispositivote cámara de órganos de un sistema de cuidado de órganos portátil de acuerdo con la reivindicación 47, bombear un fluido de perfusión al corazón, estando el fluido de perfusión a una temperatura de entre aproximadamente 25ºC y aproximadamente 37ºC, y a un volumen de entre aproximadamente 200 mL/minuto y aproximadamente 5 L/minuto, monitorear una o más características fisiológicas del corazón mientras está latiendo en la cámara protectora, y ajustar una característica de bombeo con base al menos en parte en las características fisiológicas para preservar el corazón ex-vivo.
68. El método de la reivindicación 67, donde las características fisiológicas incluyen una onda r del corazón y el método incluye sincronizar el bombeo del fluido de perfusión con la bomba.
69. Un método para preservar un corazón ex-vivo que comprende, colocar un corazón sobre uno o más electrodos en el dispositivo de cámara de órganos de un sistema de cuido portátil de órganos de acuerdo con la reivindicación 47, bombear un fluido de perfusión al corazón, estando el fluido de perfusión a una temperatura de entre aproximadamente 25ºC y aproximadamente 37ºC y a un volumen de entre aproximadamente 200 mL/minuto y aproximadamente 5 L/minuto, y monitorear las señales eléctricas de los electrodos mientras se bombea el fluido de perfusión hacia el corazón para preservar el corazón ex-vivo.
70. Un método para transportar un corazón ex-vivo que comprende, colocar un corazón para transplante en el dispositivo de cámara de órganos de un sistema de cuidado de órganos portátil de acuerdo con la reivindicación 47, bombear un fluido de perfusión hacia el corazón a través de una aorta del corazón, proveer un flujo del fluido de perfusión fuera del corazón a través de un ventrículo derecho del corazón, y
64 transportar el corazón en el sistema de de cuidado de órganos portátil desde un sitio del donante hasta un sitio del receptor a la vez que se bombea el fluido de perfusión en el corazón a través de la aorta y proveer el flujo del fluido de perfusión fuera del corazón a través del ventrículo derecho.
71. Un método para preservar un corazón ex-vivo que comprende, colocar un corazón en el dispositivo de cámara de órganos de un sistema de cuidado de órganos portátil de acuerdo con la reivindicación 47, proveer un fluido de perfusión al corazón mientras el corazón está en la cámara protectora, y hacer fluir el fluido de perfusión hacia el corazón a través de un canal formado entre dos placas calientes para calentar el fluido de perfusión a una temperatura de entre aproximadamente 32ºC y aproximadamente 37ºC para preservar el corazón ex-vivo.
72. Un método para evaluar un corazón para transplante que comprende, colocar un corazón en el dispositivo de cámara de órganos de un sistema de cuidado de órganos portátil de acuerdo con la reivindicación 47, bombear un fluido de perfusión en el corazón a través de una aorta del corazón, proveer un flujo del fluido de perfusión fuera del corazón a través de un ventrículo derecho del corazón, transportar el corazón a través del sistema de cuidado de órganos portátil desde un sitio de un donante hasta un sitio de un receptor mientras que se bombea el fluido de perfusión hacia el corazón a través de la aorta y se provee el flujo del fluido de perfusión hacia afuera del corazón a través del ventrículo derecho, antes de transplantar el corazón entre un recipiente, operar un control de flujo externo para la cámara protectora para alterar un flujo del fluido de perfusión de tal forma que el fluido de perfusión se bombee hacia el corazón a través del atrio izquierdo del corazón y fluya hacia afuera del corazón a través de ventrículo derecho y el ventrículo izquierdo del corazón, y llevar a cabo una evaluación del corazón.
73. Un método para proveer terapia a un corazón que comprende, colocar un corazón en el dispositivo de cámara de órganos de un sistema de cuidado de órganos portátil de acuerdo con la reivindicación 47, bombear un fluido de perfusión en el corazón a través de una aorta en el corazón, proveer un flujo del fluido de perfusión fuera del corazón a través de un ventrículo derecho del corazón, operar un control de flujo externo a la cámara protectora para alterar un flujo del fluido de perfusión de tal forma que el fluido de perfusión se bombea hacia el corazón a través de un atrio izquierdo del corazón y fluya fuera del corazón a través del ventrículo derecho y el ventrículo izquierdo del corazón, y administrar uno o más tratamientos inmunosupresores, quimioterapia, terapia genética y terapia de irradiación al corazón.
74. Un método para mantener un corazón ex-vivo que comprende, colocar el corazón en un sistema de cuidado de órganos de acuerdo con la reivindicación 47, bombear un fluido de perfusión al corazón en menos de 30 minutos después de la explantación, estando el fluido de perfusión a una temperatura de entre aproximadamente 32ºC y aproximadamente 37ºC.
75. Un método para mantener un corazón ex-vivo que comprende colocar el corazón en un sistema de cuidado de órganos de acuerdo con la reivindicación 47 sin detener el corazón, y
65 bombear un fluido de perfusión al corazón en menos de 30 minutos después de la explantación, estando el fluido de perfusión a una temperatura de entre aproximadamente 32ºC y aproximadamente 37ºC.
76. Un método para evaluar un corazón para transplante que comprende,
5 colocar un corazón en el dispositivo de cámara de órganos de un sistema de cuidado de órganos portátil de acuerdo con la reivindicación 47, bombear un fluido de perfusión hacia adentro del corazón a través de un ventrículo del corazón durante un periodo de al menos 12 horas, estando el fluido de perfusión a una temperatura de entre aproximadamente 32ºC y aproximadamente 37ºC, y llevar a cabo una prueba de HLA sobre el corazón mientras el fluido de perfusión se está bombeando.
Patentes similares o relacionadas:
Un dispositivo y método para calentar o enfriar una muestra, del 22 de Julio de 2020, de Cell Therapy Catapult Limited: Un dispositivo para calentar o enfriar una o más muestras, comprendiendo el dispositivo una pluralidad de miembros que pueden funcionar en uso para calentar […]
Uso de un sistema de banco de células de crioconservación cerrado de alta capacidad y procedimiento para descongelar y dispensar células almacenadas, del 22 de Julio de 2020, de Boehringer Ingelheim Animal Health USA Inc: Uso de un sistema de banco de células de crioconservación de fase cerrada y alta capacidad para almacenar grandes volúmenes de células, en el que el uso comprende las siguientes […]
Sistema y aparato para la auditoría de muestras biológicas en almacenamiento en frío, del 15 de Julio de 2020, de Kustodian Ltd: Un sistema para la auditoría remota en vivo de muestras biológicas mientras están contenidas en una vasija llena de fluido refrigerante , comprendiendo el sistema: […]
APARATO PARA CONTENER Y TRANSPORTAR UN ÓRGANO EX-VIVO CONECTADO A UNA MÁQUINA DE PERFUSIÓN, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: Aparato para contener y transportar un órgano ex-vivo conectado a una máquina de perfusión por medio de al menos dos conductos de perfusión (A), que permite poner o sacar […]
Procedimiento de conservación de células, tejidos u órganos en hipotermia, del 24 de Junio de 2020, de Etablissement Français du Sang: Procedimiento in vitro o ex vivo de conservación de las células animales, preferiblemente de células humanas, en hipotermia intensa, que comprende una etapa que consiste en […]
Sistemas de conservación y procesamiento de espermatozoides, del 17 de Junio de 2020, de XY, LLC: Un procedimiento para producir una muestra de esperma de mamífero no humano adecuada para la fertilización in vitro, que incluye la etapa de: […]
Sorbente polimérico para la eliminación de impurezas de sangre completa y productos sanguíneos, del 17 de Junio de 2020, de Cytosorbents Corporation: Un método para tratar la sangre y los productos sanguíneos almacenados que maximiza la vida útil y/o minimiza una complicación relacionada con la transfusión […]
Kit para acondicionamiento y purificación ex-vivo de un órgano explantado, del 17 de Junio de 2020, de Aferetica S.r.l: Un kit para acondicionamiento y purificación ex vivo de un órgano explantado, comprendiendo: - medios de conexión a y de dicho órgano ; […]