PROCEDIMIENTO PARA LA PREPARACION DE HIDROCLORURO DE CINACALCET.
Procedimiento para preparar base de cinacalcet, que comprende:
proporcionar el compuesto V de estructura: ** ver fórmula** convertir el resto hidroxilo del compuesto V en un buen grupo saliente para obtener el compuesto VI de estructura: ** ver fórmula** y combinar el compuesto VI con (R)-1-naftiletilamina (NEA) en presencia de una base a una temperatura de aproximadamente 50ºC a aproximadamente 120ºC para obtener base de cinacalcet
Tipo: Resumen de patente/invención. Número de Solicitud: W06019131US.
Solicitante: TEVA PHARMACEUTICAL INDUSTRIES LTD..
Nacionalidad solicitante: Israel.
Dirección: 5 BASEL STREET, P.O. BOX 3190,49131 PETAH TIQVA.
Inventor/es: WIZEL, SHLOMIT, EISENSTADT, AMIHAI, LIFSHITZ-LIRON,REVITAL, AVHAR-MAYDAN,SHARON, RAIZI,YURIY, RAMATY,REVITAL.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- C07C209/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 209/00 Preparación de compuestos que contienen grupos amino unidos a una estructura carbonada. › con formación de grupos amino unidos a átomos de carbono acíclicos o a átomos de carbono de ciclos distintos de los ciclos aromáticos de seis miembros.
- C07C209/22 C07C 209/00 […] › por sustitución de otros grupos funcionales.
Clasificación PCT:
- C07C209/08 C07C 209/00 […] › con formación de grupos amino unidos a átomos de carbono acíclicos o a átomos de carbono de ciclos distintos de los ciclos aromáticos de seis miembros.
- C07C209/22 C07C 209/00 […] › por sustitución de otros grupos funcionales.
- C07C211/30 C07C […] › C07C 211/00 Compuestos que contienen grupos amino unidos a una estructura carbonada. › formando parte el ciclo aromático de seis miembros de un sistema cíclico condensado formado por dos ciclos.
Fragmento de la descripción:
Procedimiento para la preparación de hidrocloruro de cinacalcet.
Campo de la invención
La presente invención se refiere a un procedimiento para preparar cinacalcet, (R)-a-metil-N-[3-[3-(trifluorometil)fenil] propil]-1-naftalenmetanamina.
Antecedentes de la invención
La (R)-a-metil-N-[3-[3-(trifluorometil)fenil]propil]-1-naftalenmetanamina (a la que se hace referencia en la presente memoria como "cinacalcet" o "CNC") tiene un número CAS de 226256-56-0, una fórmula de C22H22F3N y la siguiente estructura:
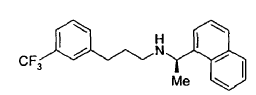
Esta molécula es la forma de base libre del hidrocloruro de cinacalcet (a la que se hace referencia en la presente memoria como "CNC-HCl"), con un número CAS de 364782-34-3 y la siguiente estructura:
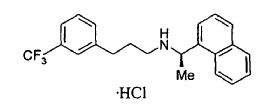
El CNC-HCl se comercializa como SENSIPARTM, y es el primer fármaco en una clase de compuestos conocidos como calcimiméticos que deben ser aprobados por la FDA.
Los calcimiméticos son una clase de moléculas pequeñas oralmente activas que hacen disminuir la secreción de PTH activando los receptores de calcio. Normalmente, la secreción de PTH se regula mediante el receptor sensor de calcio. Los agentes calcimiméticos aumentan la sensibilidad de dicho receptor al calcio, que inhibe la liberación de hormona paratiroidea y disminuye los niveles de la misma en pocas horas. Los calcimiméticos son utilizados para tratar hiperparatiroidismo, una afección caracterizada por la sobresecreción de PTH que se produce cuando los receptores de calcio de las glándulas paratiroideas no responden adecuadamente al calcio presente en la sangre. Los niveles elevados de hormona paratiroidea (PTH), un indicador de hiperparatiroidismo secundario, están asociados con un metabolismo alterado de calcio y fósforo, dolor de huesos, fracturas y un mayor riesgo de muerte cardiovascular. Como calcimimético, el CNC-HCl está aprobado para el tratamiento de hiperparatiroidismo secundario en pacientes con enfermedades renales crónicas sometidos a diálisis. El tratamiento con CNC-HCl disminuye los niveles en suero de PTH, así como el producto de ion calcio/fósforo, una medida de la cantidad de calcio y fósforo presente en la sangre.
La patente US nº 6.011.068 da a conocer la actividad de receptores de iones inorgánicos, particularmente moléculas activas como receptoras de calcio, tales como las que presentan la estructura general de cinacalcet.
La patente US nº 6.211.244 da a conocer compuestos activos como receptores de calcio relacionados con cinacalcet y métodos para preparar dichos compuestos. De acuerdo con dicha patente, el cinacalcet se puede preparar haciendo reaccionar 1-acetil naftaleno con 3-[3-(trifluorometil)fenil]propilamina en presencia de isopropóxido de titanio para obtener una imina correspondiente al cinacalcet, seguido de tratamiento con cianoborohidruro de sodio metanólico y la resolución de la base de cinacalcet racémica mediante cromatografía líquida quiral, de acuerdo con el esquema 1:
Esquema 1
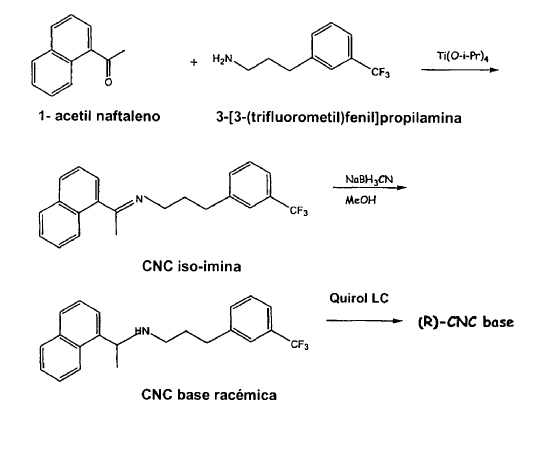
Similarmente, utilizando el procedimiento dado a conocer en la patente US nº 6.211.244, así como en DRUGS OF THE FUTURE (2002) 27 (9): 831, se puede obtener el enantiómero de cinacalcet deseado haciendo reaccionar (R)-1-(1-naftil)etilamina con 3-[3-(trifluorometil)fenil]propionaldehído en presencia de isopropóxido de titanio para producir la imina que se corresponde con cinacalcet, seguido de tratamiento con cianoborohidruro de sodio etanólico, de acuerdo con el esquema siguiente:
Esquema 2

La patente US nº 6.211.244 da a conocer otro procedimiento para la síntesis de cinacalcet. Dicho procedimiento incluye el tratamiento de 3-trifluorometilcinamilnitrilo, que se puede preparar tal como se da a conocer en la patente US nº 4.966.988, con hidruro de aluminio de diisobutilo, seguido de tratamiento del complejo intermedio de aluminio-imina con (R)-1-(1-naftil)etilamina, y reducción del producto intermedio de imina con cianoborohidruro de sodio etanólico, de acuerdo con el siguiente esquema 3:
Esquema 3
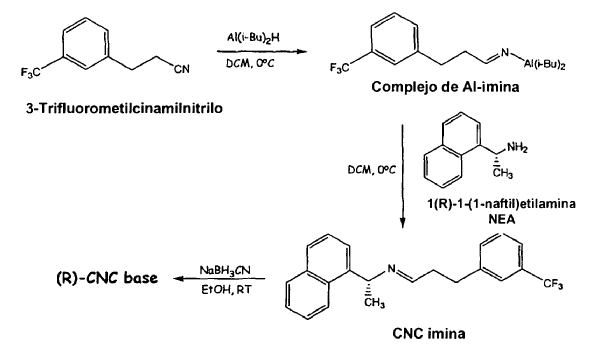
Sin embargo, estos tres procedimientos requieren la utilización de reactivos, tales como isopropóxido de titanio, que es altamente higroscópico y costoso, así como tóxico, y cianoborohidruro de sodio etanólico o metanólico, que son altamente tóxicos e inflamables, además de perjudiciales para el medio ambiente, dificultando la aplicabilidad de dichos procedimientos a escala industrial. Además, no se detalla la descripción de dichos procedimientos.
Además, la única ruta sintética conocida para el precursor del procedimiento descrito en el esquema 2, concretamente el 3-[3-(trifluorometil)fenil]propionaldehído (FMPP), se da a conocer en la nota al pie 12 de Tetrahedron Letters (2004) 45: 8355 y se describe en el esquema 4:
Esquema 4
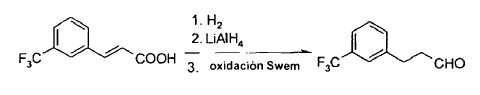
en el que se lleva a cabo la reducción del doble enlace del correspondiente derivado de ácido cinámico, seguida de reducción del resto de ácido carboxílico al correspondiente alcohol, que a continuación se oxida al aldehído mediante oxidación Swem. La reacción de oxidación Swem incluye la utilización de reactivos, tales como cloruro de oxalilo y DMSO, que son perjudiciales para el medio ambiente, y además no proporciona un rendimiento elevado, lo que hace que el procedimiento sea difícil aplicar a escala industrial.
De este modo, resulta deseable un procedimiento alternativo para la preparación de base de cinacalcet y sal de cinacalcet que sea más directo, con un rendimiento más elevado, inocuo para el medio ambiente y aplicable a una producción a escala industrial. La presente invención da a conocer una alternativa de este tipo.
Sumario de la invención
En una primera forma de realización, la presente invención da a conocer un procedimiento para preparar base de cinacalcet a partir del compuesto V, tal como se ilustra en el esquema 5, que comprende:
Esquema 5
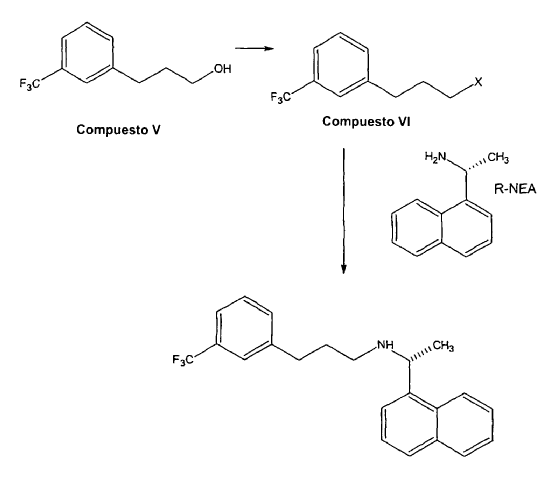
El procedimiento para la conversión del resto hidroxilo del compuesto V en un buen grupo saliente comprende combinar una solución de compuesto V en un disolvente orgánico aprótico seleccionado de entre el grupo que consiste en un hidrocarburo alifático clorado, acetonitrilo, un éter C2-6 y un hidrocarburo aromático C6-8 con un reactivo que presenta un buen grupo saliente para obtener una mezcla de reacción; y mantener la mezcla de reacción a una temperatura de entre aproximadamente 0ºC y aproximadamente 50ºC, dependiendo del reactivo, para obtener el compuesto VI. Opcionalmente, el compuesto IV se puede recuperar.
El procedimiento de convertir el compuesto VI en base de cinacalcet comprende combinar una solución del compuesto VI en un disolvente orgánico seleccionado entre el grupo que consiste en un hidrocarburo aromático C6-8, un alcohol C1-4, un éster C3-6, una cetona C3-6 y acetonitrilo, o en una mezcla de agua y un hidrocarburo aromático C6-8, con (R)-1-naftiletilamina (al que se hace referencia en la presente memoria como R-NEA) en presencia de una base, para obtener una mezcla de reacción y mantener dicha mezcla de reacción a una...
Reivindicaciones:
1. Procedimiento para preparar base de cinacalcet, que comprende:
proporcionar el compuesto V de estructura:
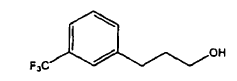
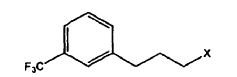
2. Procedimiento según la reivindicación 1, en el que la conversión del resto hidroxilo del compuesto V en un buen grupo saliente comprende:
3. Procedimiento según la reivindicación 2, en el que el disolvente orgánico aprótico se selecciona de entre el grupo que consiste en diclorometano, tetrahidrofurano, y tolueno, siendo preferentemente el disolvente orgánico aprótico tolueno.
4. Procedimiento según la reivindicación 2 ó 3, en el que el reactivo se selecciona de entre el grupo que consiste en haluro de tionilo, haluro de sulfonilo alifático y haluro de sulfonilo aromático, seleccionándose preferentemente el reactivo de entre el grupo que consiste en bromuro de tionilo, cloruro de tionilo, cloruro de metansulfonilo (MsCl), cloruro de bencensulfonilo, cloruro de 4-nitrobencensulfonilo (NsCl), y cloruro de p-toluensulfonilo (TsCl), siendo más preferentemente el reactivo cloruro de metansulfonilo.
5. Procedimiento según cualquiera de las reivindicaciones 2 a 4, en el que el reactivo es añadido gradualmente a la solución que contiene el compuesto V.
6. Procedimiento según cualquiera de las reivindicaciones 2 a 4, en el que el reactivo es añadido gradualmente a una temperatura de aproximadamente 0ºC a aproximadamente 10ºC.
7. Procedimiento según cualquiera de las reivindicaciones 2 a 6, en el que la mezcla de reacción contiene una base orgánica o inorgánica, seleccionándose preferentemente la base orgánica o inorgánica de entre el grupo que consiste en una amina o un carbonato alcalino, seleccionándose más preferentemente la amina o el carbonato alcalino de entre el grupo que consiste en trietilamina, diisopropiletilamina, amina terciaria, K2CO3, NaHCO3, Na2CO3, y KHCO3, siendo dicha base todavía más preferentemente la trietilamina.
8. Procedimiento según cualquiera de las reivindicaciones 2 a 7, en el que la mezcla de reacción se mantiene durante aproximadamente 0,5 a aproximadamente 24 horas, manteniéndose preferentemente la mezcla de reacción durante aproximadamente 0,5 horas a aproximadamente 5 horas.
9. Procedimiento según cualquiera de las reivindicaciones 1 a 8, en el que el compuesto VI está presente como una solución en un disolvente orgánico seleccionado de entre el grupo que consiste en un hidrocarburo aromático C6-8, un alcohol C1-4, un éster C3-6, una cetona C3-6, y acetonitrilo o una mezcla de agua y un hidrocarburo aromático C6-8.
10. Procedimiento según la reivindicación 9, en el que el disolvente orgánico se selecciona de entre el grupo que consiste en tolueno, etanol, alcohol isopropílico, EtOAc, metilisobutilcetona (MIBK), acetona, y acetonitrilo.
11. Procedimiento según la reivindicación 9, en el que el compuesto VI está presente como una solución en acetonitrilo o una mezcla de agua y tolueno.
12. Procedimiento según cualquiera de las reivindicaciones 1 a 11, en el que la (R)-1-naftiletilamina está presente en una cantidad de aproximadamente 1 a aproximadamente 1,5 equivalentes molares en relación con el compuesto VI.
13. Procedimiento según cualquiera de las reivindicaciones 1 a 12, en el que la base se selecciona de entre el grupo que consiste en carbonatos alcalinos y aminas.
14. Procedimiento según la reivindicación 13, en el que la base es una amina terciaria.
15. Procedimiento según la reivindicación 13, en el que la base se selecciona de entre el grupo que consiste en K2CO3, Na2CO3, NaHCO3, KHCO3, tributilamina (TBA), y diisopropiletilamina, siendo preferentemente la base K2CO3.
16. Procedimiento según cualquiera de las reivindicaciones 1 a 15, en el que la base es añadida a la solución del compuesto VI y (R)-1-naftiletilamina.
17. Procedimiento según cualquiera de las reivindicaciones 1 a 16, en el que el compuesto VI y la (R)-1-naftiletilamina se combinan a una temperatura de aproximadamente 70ºC a aproximadamente 100ºC.
18. Procedimiento según cualquiera de las reivindicaciones 1 a 17, en el que la combinación se lleva a cabo durante aproximadamente 5 a aproximadamente 90 horas, llevándose a cabo preferentemente la combinación durante aproximadamente 21 a 40 horas.
19. Procedimiento según cualquiera de las reivindicaciones 1 a 18, en el que se añade un catalizador de transferencia de fase durante la combinación del compuesto VI y la (R)-1-naftiletilamina, siendo preferentemente el catalizador de transferencia de fase el bromuro de tetrabutilamonio (TBAB).
20. Procedimiento según la reivindicación 9, que comprende además recuperar el residuo de base de cinacalcet por filtración y evaporación del disolvente.
21. Procedimiento según la reivindicación 9, en el que la base de cinacalcet que presenta menos de 0,2 por ciento en superficie de (R)-1-naftiletilamina se prepara en un procedimiento que comprende:
22. Procedimiento según la reivindicación 21, en el que la base de cinacalcet presenta menos de 0,1 por ciento en superficie de (R)-1-naftiletilamina.
23. Procedimiento según la reivindicación 21 ó 22, en el que, antes de la etapa (b), se lleva a cabo un calentamiento a una aproximadamente 50ºC hasta aproximadamente 80ºC.
24. Procedimiento según cualquiera de las reivindicaciones 21 a 23, en el que la solución de base de cinacalcet comprende un disolvente seleccionado de entre el grupo que consiste en tolueno, acetato de etilo, DCM, y mezclas de los mismos.
25. Procedimiento según cualquiera de las reivindicaciones 21 a 24, en el que el disolvente está presente en una cantidad suficiente para obtener una solución.
26. Procedimiento según cualquiera de las reivindicaciones 21 a 25, en el que la acidificación de la solución es por adición de ácido clorhídrico.
27. Procedimiento según cualquiera de las reivindicaciones 21 a 26, en el que la neutralización es por lavado con una solución saturada de NaHCO3, y a continuación lavado con agua.
28. Procedimiento según la reivindicación 27, en el que la recuperación de la base libre de cinacalcet es por evaporación del disolvente en exceso.
29. Procedimiento según cualquiera de las reivindicaciones 1 a 28, en el que el compuesto V se prepara a partir del compuesto II de la estructura siguiente, en la que R es un alquilo C1 a C6 alifático, ramificado o cíclico, puenteado o no puenteado:
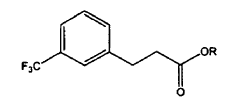
mediante la reducción del resto carbonilo del compuesto II.
30. Procedimiento según la reivindicación 29, en el que el compuesto II se prepara a partir del compuesto X de la estructura siguiente, en la que R es un alquilo C1 a C6 alifático, ramificado o cíclico, puenteado o no puenteado:
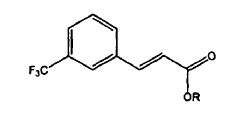
mediante la reducción del enlace doble.
31. Procedimiento según cualquiera de las reivindicaciones 1 a 30, en el que el compuesto V se prepara a partir del compuesto IV, (2E)-3-[3-(trifluorometil)fenil]prop-2-en-1-ol,
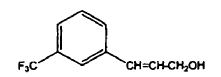
mediante la reducción del enlace doble del compuesto IV.
32. Procedimiento según la reivindicación 31, en el que el compuesto IV se prepara a partir del compuesto X por reducción de un carbonilo.
33. Procedimiento según cualquiera de las reivindicaciones 1 a 32, en el que el compuesto V se prepara como una mezcla del compuesto V y IV a partir de una mezcla de los compuestos II y III, en el que el compuesto III es 2-propenal, 3-[3-trifluorometil)fenil], con la estructura siguiente:
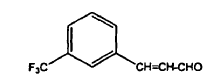
mediante la reducción del carbonilo.
34. Procedimiento según cualquiera de las reivindicaciones 1 a 33, en el que el compuesto V se prepara a partir de una mezcla del compuesto II y el compuesto IX de la estructura siguiente:
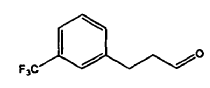
mediante la reducción del carbonilo.
35. Procedimiento según la reivindicación 34, en el que la mezcla de compuestos II y IX se prepara a partir de una mezcla de los compuestos II y III por reducción del enlace doble.
Patentes similares o relacionadas:
Procedimiento para la preparación de N,N-dialquilbencilaminas halogenadas en núcleo, del 30 de Agosto de 2017, de LANXESS DEUTSCHLAND GMBH: Procedimiento para la preparación de compuestos de fórmula (I)**Fórmula** en la que n representa 0, 1, 2 o 3, preferentemente representa 1 o 2, de manera especialmente […]
Procedimiento para la preparación de 2,2-difluoroetilamina partiendo de un compuesto de bencilamina, del 10 de Mayo de 2017, de Bayer Intellectual Property GmbH: Un procedimiento para la preparación de 2,2-difluoroetilamina de fórmula (I) CHF2CH2NH2 (I) que comprende las etapas (i) y (ii): etapa (i): reacción de 2,2-difluoro-1-haloetano […]
Procedimiento para la preparación de 2,2-difluoroetilamina a partir de 2,2-difluoro-1-cloroetano, del 16 de Noviembre de 2016, de Bayer Intellectual Property GmbH: Un procedimiento para la preparación de 2,2-difluoroetilamina que comprende las siguientes etapas: etapa (i): reacción de 2,2-difluoro-1-cloroetano de […]
Procedimiento para la preparación de bencilaminas disustituidas halogenadas, particularmente dialquilbencilaminas halogenadas, del 19 de Octubre de 2016, de BAYER CROPSCIENCE AKTIENGESELLSCHAFT: Procedimiento para la preparación de compuestos de Fórmula (I)**Fórmula** donde R1 representa hidrógeno, alquilo de 1 a 8 átomos de carbono, alquenilo […]
Procedimiento para la preparación de 2,2-difluoroetilamina, del 17 de Agosto de 2016, de Bayer Intellectual Property GmbH: Procedimiento para la preparación de 2,2-difluoroetilamina, que comprende la reacción de 2,2-difluoro-1-haloetano de fórmula general (I): CHF2-CH2Hal (I), […]
 Método de fabricación de etilenaminas, del 13 de Enero de 2016, de UNION CARBIDE CHEMICALS & PLASTICS TECHNOLOGY LLC: Un método para la fabricación de etilenaminas, comprendiendo el método las etapas de:
(a) fabricar una composición de etilenaminas que comprende una mezcla de etilenaminas […]
Método de fabricación de etilenaminas, del 13 de Enero de 2016, de UNION CARBIDE CHEMICALS & PLASTICS TECHNOLOGY LLC: Un método para la fabricación de etilenaminas, comprendiendo el método las etapas de:
(a) fabricar una composición de etilenaminas que comprende una mezcla de etilenaminas […]
Procedimiento de preparación de derivados de 2,2-difluoroetilamina partiendo de n (2,2 difluoroetil)prop-2-en-1 amina, del 31 de Diciembre de 2014, de Bayer Intellectual Property GmbH: Un procedimiento de preparación de derivados de 2,2-difluoroetilamina de la fórmula (IV)**Fórmula** que comprende las etapas (i) y (ii) siguientes: etapa (i): reacción […]
Procedimiento para la preparación de 2,2-difluoroetilamina partiendo de prop-2-en-1-amina, del 2 de Julio de 2014, de Bayer Intellectual Property GmbH: Un procedimiento para la preparación de 2,2-difluoroetilamina de fórmula (I) CHF2CH2NH2 (I) que comprende las etapas (i) y (ii): etapa (i): reacción […]