Derivados de piridazin-3(2H)-ona inhibidores selectivos de la isoforma B de la monoaminooxidasa.
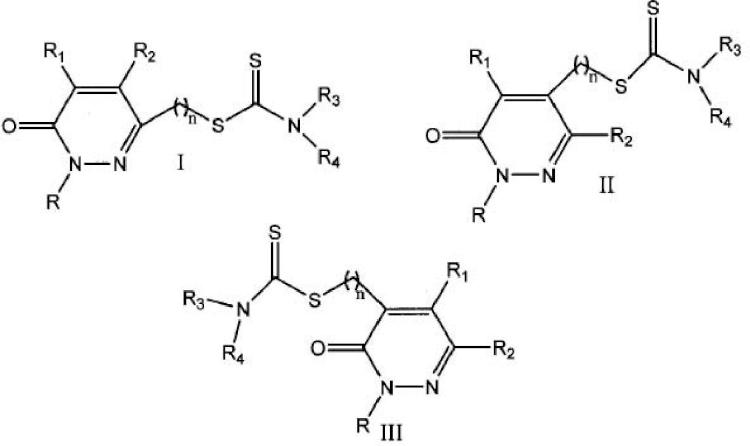
Esta invención se refiere a derivados de piridazin-3(2H)-ona de estructura general I,
II y III, que son inhibidores selectivos de la MAO-B, y a su uso para preparar medicamentos destinados a tratar trastornos derivados de la hiperactividad de la MAO-B, en particular trastornos degenerativos del sistema nervioso central (SNC), como la enfermedad de Parkinson (EP), la enfermedad de Alzheimer (EA) y otras demencias. Se trata de derivados de piridazin-3(2H)-ona que presentan fragmentos de ditiocarbamato enlazados a la posición 4, 5 ó 6 a través de una cadena alquílica de longitud variable (n = 1, 2, 3). Esta invención también se dirige a la preparación de dichos compuestos.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201400162.
Solicitante: UNIVERSIDADE DE VIGO.
Nacionalidad solicitante: España.
Inventor/es: VIÑA CASTELAO,DOLORES, TERÁN MOLDES,María Del Carmen, BESADA PEREIRA,Pedro, COSTAS CAAMAÑO,Tamara, VILA MOLARES,Noemí, COSTAS LAGO,María Del Carmen.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/501 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › no condensadas y conteniendo otros heterociclos.
- A61P25/14 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › para el tratamiento de movimientos anormales, p.ej. corea, disquinesia.
- A61P25/16 A61P 25/00 […] › Medicamentos contra el Parkinson.
- A61P25/28 A61P 25/00 […] › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
- C07D237/14 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 237/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,2 o diazina-1,2 hidrogenada. › Atomos de oxígeno.
Fragmento de la descripción:
isoenzimas desempeñan un papel importante en la regulación de la concentración de aminas biógenas en el cerebro; éste hecho junto con la selectividad de sustrato determina la importancia clínica de los inhibidores de MAO (lMAO) . Así, la MAO-A tiene mayor afinidad por la serotonina (5-hidroxitriptamina, 5-HT) , adrenalina (A) y
noradrenalina (NA) y es inhibida selectivamente por la clorgilina y moclobemida, mientras que la MAO-B degrada preferentemente la J3-feniletilamina y la bencilamina.y es inhibida selectivamente por la selegilina y rasagilina. También existen algunos IMAO que carecen de selectividad, como la iproniacida. En la figura 1 se detalla la estructura de los compuestos IMAO citados anteriormente.
el
el I ~
N #'
h o
~ ~~'
I . .
# Clorglhna
el
0,
~N~
Selegilina I ~
o ~NH-NH
U
lProniacida) ---
Figura 1
H
N~Nl
o Moclobemida ~O
CX{~
Rasagilina HN-/
Estudios funcionales sobre ambas isoenzimas han puesto de manifiesto que las MAO desempeñan un papel importante en la regulación de la concentración de aminas 15 biógenas en el cerebro, que están involucradas en distintos procesos patológicos que afectan al SNC, lo que determina la importancia clínica de los IMAO (Curr. Med, Chem. 11, 2033-2043, 2004) . La inhibición de la MAO-A en el SNC potencia los niveles de noradrenalina y serotonina, dos neurotransmisores implicados en trastornos depresivos, mientras que la inhibición de la MAO-B incrementa los niveles de dopamina, que en la EP se encuentran mermados, lo que explica que los IMAO-A se utilicen como antidepresivos y ansiolíticos y los IMAO-B para el tratamiento de la EP. La EA es una enfermedad neurodegenerativa progresiva que supone el tipo mas habitual de demencia senil. Aunque su etiología es múltiple y compleja está asociada a la acumulación de placas f3-amiloides (f3A) en el cerebro, que puede promover la pérdida de neuronas colinérgicas en la corteza cerebral y en el hipocampo, 10 que explica la deficiencia cognitiva y la pérdida de memoria que se manifiesta a corto plazo en los pacientes con la EA (Velázquez Farmacología Básica y Clínica 17 ed. Panamericana: Madrid 2005, 329-335) . Por consiguiente, el tratamiento farmacológico tradicional de la EA implica la administración de inhibidores de la acetilcolinesterasa (Rang y Dale Farmacología 6U ed. Elsevier: Barcelona 2008, 515-516 ) , enzima que degrada la acetilcolina. Sin embargo, se han realizado estudios que evidencian un incremento de actividad de la MAO-B en el cerebro de pacientes que sufren deteminados trastornos neurodegenerativos como por ejemplo la EP o la EA (Biochem. Pharmacol. 38, 555561, 1989) Y han surgido nuevas expectativas terapéuticas. El aumento de actividad de la MAO-B cerebral origina un incremento de las especies reactivas de oxígeno (ROS) que contribuyen al estrés oxidativo y a la muerte neuronal. Aunque se requieren mas estudios para clarificar los efectos beneficiosos de los IMAO-B en los procesos neurodegenerativos, como la EA, dichos efectos se relacionan con la reducción de ROS, que son neurotóxicas, y con el incremento de monoaminas en el cerebro de estos pacientes (Neurotoxicology 25, 271-277, 2004; Journal of Neuroscience Research 79,
172-179, 2005) En la actualidad la principal aplicación terapéutica de los IMAO-B es en el tratamiento de la EP (Translational Neurodegeneration 1:10, 2012; Translational Neurodegeneration 2:19, 2013) , un trastorno neurológico que afecta a la actividad motora y que se debe a una disminución de los niveles de dopamina en el estriado, provocada por la muerte progresiva de neuronas nigroestriadas. Aunque el tratamiento clásico de la EP ha sido la administración de L-dopa (precusor de la dopamina) asociada a un inhibidor de la enzima dopa descarboxilasa periférica, alternativas terapéuticas más recientes implican la administración de inhibidores de la catecol-orto-metiltrasferasa (COMT) , como la entecapona, y también de IMAO-B selectivos, como la selegilina y la rasagilina (Translational Neurodegeneration 1: 1O, 2012) . Existen numerosos artículos y patentes que describen compuestos que actúan como inhibidores selectivos de la MAO-B y sus aplicaciones en trastornos neurodegenerativos, como por ejemplo derivados de cumarina (ES 2343347; J Med. Chem. 54, 7127-7131, 2011) (compuesto 1, figura 2) , y-cromonas (Bioorg. Med. Chem. Lett. 20, 2709-2712, 2010; Bioorg. Med. Chem. Lett. 21, 707-709, 2011) (compuesto 2, figura 2) , pirazolinas y otros derivados de diazaheterocic1ºs (J Med. Chem. 48, 71137122, 2005; Bioorg. Med Chem. Lett 20, 6479-6482, 2010; J. Med. Chem. 49, 37433747, 2006; J. Med Chem. 50, 5364-5371, 2007) (compuestos 3 y 4, figura 2) , tiazolilhidrazinas (J Med. Chem. 53, 6516-6520, 2010; Arch. Pharm. Chem. Lije Sci. 346, 17-22, 2013) (compuesto 5, figura 2) , ditiolanotionas (W02006/089861) (compuesto 6, figura 2) , y aminas o amidas derivadas de sistemas heterocíclicos (EP 1524267; WO 2004/007429; EP1524265, J. Med. Chem. 50, 922-931, 2007) (compuestos 7 y 8, figura 2) .
o Br
o :;:::::;-
, O
I
N..........N el
o H2N--\
S
s-s s
Q---- ('
F N o Figura 2 En la figura 2 se detalla la estructura de diversos compuestos con actividad IMAO-B. La piridazina es una diazina poco frecuente en productos naturales. Sin embargo, este heteronúcleo forma parte de un reducido grupo de estructuras reconocidas como privilegiadas, debido a su capacidad de generar compuestos activos frente a numerosas dianas, (Med. Chem. Comun. 2, 935-941, 2011) . Los derivados de piridazina poseen un amplio espectro de actividad fannacológica (cardiotónica, antihipertensiva, antiagregante plaquetaria, hipolipemiante, analgésica y antiinflamatoria, antinociceptiva, antidepresiva, ansiolítica, antagonista del GABA, hipoglucemiante, antiinfecciosa o antineoplásica entre otras) y muchos de ellos son análogos con estructura de 3 (2H) -piridazinona (Progress in Medicinal Chemistr y , EIsevier Science Publishers Biomedical Division: Amsterdam 1990, 1-49; Progress in Medicinal Chemistr y , EIsevier Science Publishers Biomedical Division: Amsterdam 1992, 141183; Med. Chem. Res 22, 2539-2552, 2013) . El anillo de piridazina está presente en compuestos que actúan como inhibidores selectivos de la MAO-B, se trata de sistemas policíclicos condensados (J. Med. Chem. 49, 3743-3747, 2006; J. Med Chem. 50, 5364-5371, 2007; J. Med. Chem. 49, 62646272, 2007) (compuesto 4, figura 2) . Además, existen artículos y patentes referidos a derivados de piridazina sencillos que actúan sobre otras dianas terapéuticas eficaces en trastornos neurodegenerativos, como por ejemplo agonistas del receptor GABAA (WO 15 2012/068161; WO 2010/127968) (compuesto 9, figura 3) , agonistas del receptor cannabinoide CB2 (WO 2011/097553) (compuesto 10, figura 3) , activadores de la proteína transportadora del glutamato (WO 2013/019938) (compuesto 11, figura 3) , moduladores la y-secretasa (Med. Chem. Lett. 1, 184-187, 2010; Bioorg. Med Chem. Lett. 21, 4016-4019, 2011) (compuesto 12, figura 3) , o inhibidores de la oligomerización de la proteína tau (Biochemistr y , 48, 7732-7745, 2009) (compuesto 13, figura 3) , algunos de los cuales son derivados de 3- (2H) -piridazinona (compuestos 10,
Y 13) .
Sin embargo, no se conocen derivados de 3 (2H) -piridazinona que actúen como IMAOB selectivos.
~
~JX"
o N____
10 /
o
OCH3
O
"'00'Q NH2
:;::::;;-
N
I S
N~ :::::::-.... 13
~O O
Figura 3 Los compuestos de la presente invención carecen de relación estructural con los descritos hasta el momento y se comportaron como inhibidores selectivos frente a la MAO-B. Se trata de nuevos derivados de 3 (2H) -piridazinona sustituidos en las posiciones 4, 5 o 6 con fragmentos de ditiocarbamato, enlazados a dichas posiciones a través de una cadena alquílica de longitud variable, que inhiben selectivamente la actividad de la MAO-B cuando se evalúa in vitro su bioactividad.
Descripción de la invención La presente invención se refiere a nuevos compuestos derivados de piridazinona sustituidos en C4, C5 o C6 con fragmentos de ditiocarbamato y de estructura general 1,
11 Y III, respectivamente, que son inhibidores selectivos in vitro de la MAO-B, y a su posible uso para preparar medicamentos destinados a tratar trastornos derivados de la hiperactividad de la MAO-B, en particular trastornos degenerativos del sistema nervioso central (SNC) , como la enfermedad de Pakinson (EP) , la enfermedad de Alzheimer (EA) y otras demencias.
Se trata de derivados de piridazin-3 (2H) -ona que presentan...
Reivindicaciones:
1. Moléculas de fórmula (1) (H) Y (IH) :
o o N-N
N-N
/ H
R /
R
IÍ
N-N
/
R HI
En donde: n es un número entero seleccionado de 1, 2, 3, 4, 5, 6, 7, 8; R es un grupo seleccionado de: un átomo de hidrógeno, un grupo alquilo CI-C6, un
grupo carboxialquilo CI-C6, un grupo haloalquilo CI-C6, un grupo arilo C6-C12, un grupo aralquilo C6-CI2, un grupo heteroarilo C4-C12; R1 es un grupo seleccionado de: un átomo de hidrógeno, un grupo alquilo CI-C6, un átomo de halógeno, R2 es un grupo seleccionado de: un átomo de hidrógeno, un grupo alquilo CI-C6, un átomo de halógeno, R3, R4 idénticos o diferentes se seleccionan de: un átomo de hidrógeno, un grupo alquilo CI-C6, grupo heterocicloalquilo saturado CI-C6, un grupo arilo C6-C12, un grupo aralquilo C6-C12, un grupo heteroarilo C4-C12, O bien R3 y R4 forman un ciclo seleccionado de: un cicloalquilo Cs-Cs, un heterocicloalquilo Cs-Cs, un heterocic1ºalquilo Cs-Cs N-alquilo ·sustituido, un heterocic1ºalquilo Cs-Cs N-arilo sustituido, un heterocicloalquilo Cs-Cs Ncicloalquilo sustituido, un heterocicloalquilo Cs-Cs N-aralquilo sustituido, un heterocic1ºalquilo Cs-Cs N -acilo sustituido; y sus sales farmacéuticamente aceptables.
2. Una molécula según la reivindicación 1, donde n es un número entero seleccionado de 1, 2, 3.
3. Una molécula según la reivindicación 1 o la reivindicación 2, donde R es un 5 grupo seleccionado de: metilo, fenilo o bencilo.
4. Una molécula según cualquiera de las reivindicaciones 1 a 3, donde R1 es un átomo de hidrógeno.
5. Una molécula según cualquiera de las reivindicaciones 1 a 4, donde R2 es un átomo de hidrógeno o un grupo metilo.
6. Una molécula según cualquiera de las reivindicaciones 1 a 5, donde R3 y R4 forman un grupo seleccionado de la siguiente lista:
. /
~-N
\
7. Una molécula según la reivindicación 1, la cual se incluye en la siguiente lista:
CH3 s (
yN~ CH3
o S
syO o /N-N# Idu Id2 o S
CH3
syO
o Id3 S o syO
Iat.5
CH 3
syO S
S
Id4 o /N-N# 1825 CH3
syO
S
syO
S
Id5
) -.
8. --NO
S s
L
o o N-N IIC2 N-N IIc3
Ph Ph
<
) -NQ <.
8. --NI\
S
""----1
O
O
N-N N-N
< IIC4 < IIcs Ph
8) ---/\ Ph O S
O
N N-{
) lNCJ
S Ph
""----1
II1c3
O O S
N-N
IIcu
) lNI\
<Ph ""----1
IlIcs S
) l/\
Ph
N N-\
""----1
O
IlIcu
8. Un medicamento que comprende una molécula de fórmula (1) , (II) o (III) según cualquiera de las reivindicaciones 1 a 7 o una sal de ésta en un soporte farmacéuticamente aceptable, con uno o más excipientes farmacéuticos aceptables.
9. Un medicamento que comprende una molécula de fórmula (I) , (II) o (III) según la. reivindicación 8 que incluya uno o más agentes terapéuticos adicionales.
10. Uso de una molécula de fórmula (I) , (II) o (III) según cualquiera de las reivindicaciones 1 a 7, para la preparación de un medicamento para prevenir y/o
tratar trastornos derivados de la hiperactividad de la MAO-B, en particular trastornos degenerativos del sistema nervioso central.
11. Uso según la reivindicación 10, para el prevención y/o tratamiento de trastornos degenerativos preferentemente Parkinson, Alzheimer, demencia senil o ataxia.
12. Un método para la síntesis de una molécula de fórmula (I) , (II) o (III) según cualquiera de las reivindicaciones 1 a 7 caracterizado por que comprende al menos una etapa como se describe en el esquema 1, en donde la 6 (5) (4) -bromoalquil3 (2H) -piridazinona de fórmula (IV) , (IX) o (XIII) , una amina secundaria de fórmula V y disulfuro de carbono (CS2) reaccionan en presencia de base en un disolvente a temperatura ambiente.
/3 _
Condiciones básicas HN . •
" disolvente R4
V
Esquema 1
13. Un método según la reivindicación 12, en donde el disolvente es dim~tilformamida (DMF) y la base K3P04.
Patentes similares o relacionadas:
Sales de butirato para uso en enfermedades inflamatorias, del 17 de Junio de 2020, de Birrbeheer B.V: Una preparación que comprende una sal de butirato para uso en el tratamiento de un sujeto que padece una enfermedad que está asociada con inflamación sistémica, […]
Rhoq como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Rhoq como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Rhoq como diana farmacológica para el cribado, ensayo, y/o […]
ARHGEF6 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Arhgef6 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Arhgef6 como diana farmacológica para el cribado, ensayo, y/o […]
Nuevos derivados de piperazina y piperidina, síntesis y uso de los mismos en la inhibición de la oligomerización de VDAC, la apoptosis y la disfunción mitocondrial, del 3 de Junio de 2020, de The National Institute for Biotechnology in the Negev Ltd: Compuesto de Fórmula general (Id): **(Ver fórmula)** en la que L2 es un grupo de enlace seleccionado del grupo que consiste en un alquilamidileno […]
Agonista de receptores de 5-HT4 para gastroparesia, del 3 de Junio de 2020, de RAQUALIA PHARMA INC: Una composición farmacéutica para su uso en el tratamiento de la gastroparesia que comprende una cantidad terapéuticamente eficaz de ácido 4-{[4-({[4-(2,2,2-trifluoroetoxi)-1,2-bencisoxazol-3-il]oxi}metil)piperidin-1-il]metil}tetrahidro-2H-piran-4-carboxílico […]
Derivados de indolin-2-ona, del 27 de Mayo de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto de fórmula **(Ver fórmula)** en la que A es fenilo o un grupo heteroarilo de cinco o seis miembros, que contiene […]
Compuesto de péptido farmacológicamente activo, procedimiento de preparación y uso del mismo, del 29 de Abril de 2020, de Messina, Angela Anna: Un péptido sintético que consiste en la secuencia de aminoácidos IAAQLLAYYFT (ID de SEC nº 1).
Derivados de 4-(p-quinonil)-2-hidroxibutanamida para el tratamiento de enfermedades mitocondriales, del 15 de Abril de 2020, de PTC THERAPEUTICS, INC. (100.0%): Un compuesto seleccionado entre el grupo que consiste en: • 2-5 hidroxi-2-metil-4-(2,4,5-trimetil-3,6-dioxociclohexa-1,4-dienil)butanamida y • su forma de […]