Microelectrodos nanoestructurados y dispositivos de biodetección que los incorporan.
Microelectrodo nanoestructurado adaptado para generar una carga en respuesta a un estímulo biomolecular,
en el que dicha nanostructura está nanotexturizada y es puntiaguda o fractal, y en el que el microelectrodo nanoestructurado puede presentar una sonda biomolecular en la superficie del mismo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA2009/001212.
Solicitante: THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO.
Nacionalidad solicitante: Canadá.
Dirección: 27 King's College Circle Toronto, ON M5S 1A1 CANADA.
Inventor/es: KELLEY,Shana, TAFT,Bradford, SOLEYMANI,LEYLA, FANG,ZHICHAO, SARGENT,EDWARD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12Q1/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones.
- C12Q1/68 C12Q […] › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- C40B60/00 C […] › C40 TECNOLOGIA COMBINATORIA. › C40B QUIMICA COMBINATORIA; BIBLIOTECAS, p. ej. QUIMIOTECAS (bibliotecas combinatorias in silico de ácidos nucleicos, proteínas o péptidos G16B 35/00; química combinatoria in silico G16C 20/60). › Aparatos especialmente adaptados para su empleo en química combinatoria o con bibliotecas.
- G01N27/30 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 27/00 Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R). › Electrodos, p. ej. electrodos para el análisis; Semicélulas (G01N 27/414 tiene prioridad).
- G01N27/327 G01N 27/00 […] › Electrodos bioquímicos.
- G01N27/403 G01N 27/00 […] › Conjuntos de células y de electrodos.
- G01N27/416 G01N 27/00 […] › Sistemas (G01N 27/27 tiene prioridad).
- G01N33/53 G01N […] › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
PDF original: ES-2517919_T3.pdf


Fragmento de la descripción:
detallada de la invención
La presente divulgación describe microelectrodos nanoestructurados (NME), que pueden usarse en un dispositivo de biodetección, tal como un chip de biodetección.
NME
La figura 1A muestra un diagrama esquemático de un dispositivo a modo de ejemplo que incorpora NME. En el ejemplo mostrado, el dispositivo es un chip que tiene una matriz de ocho cables. En este ejemplo, el NME está formado por cables de oro que se estrechan hasta una anchura de 5 micrómetros. El cable se proporciona sobre un sustrato de Si y SÍO2, aunque pueden usarse otros materiales de sustrato adecuados. Sobre el cable, se deposita una capa aislante, tal como S¡2, para aislar eléctricamente y pasivar el cable. Se crea una abertura, en este caso un orificio de 5 nm, en la capa aislante para exponer una parte del cable.
La figura 1B es una vista lateral de la parte del chip en la que se ubica la abertura, mostrando las capas del dispositivo. Las técnicas de fotolitografía conocidas más comúnmente pueden ser adecuadas para crear una abertura, tal como aberturas de 1 nm a 1 pm de diámetro. Esto puede lograrse normalmente en instalaciones de fabricación existentes con alta robustez y reproduciblidad. Dado que sólo esta superficie expuesta es activa electroquímicamente, puede usarse electrodeposición (Menke et al. Nature Mater. 26, 5, 914-919) para hacer crecer un NME dentro de este espacio.
La figura 1C es un esquema en sección transversal de un ejemplo de deposición de NME, usando Pd para el NME. Este procedimiento se describirá en mayor detalle a continuación.
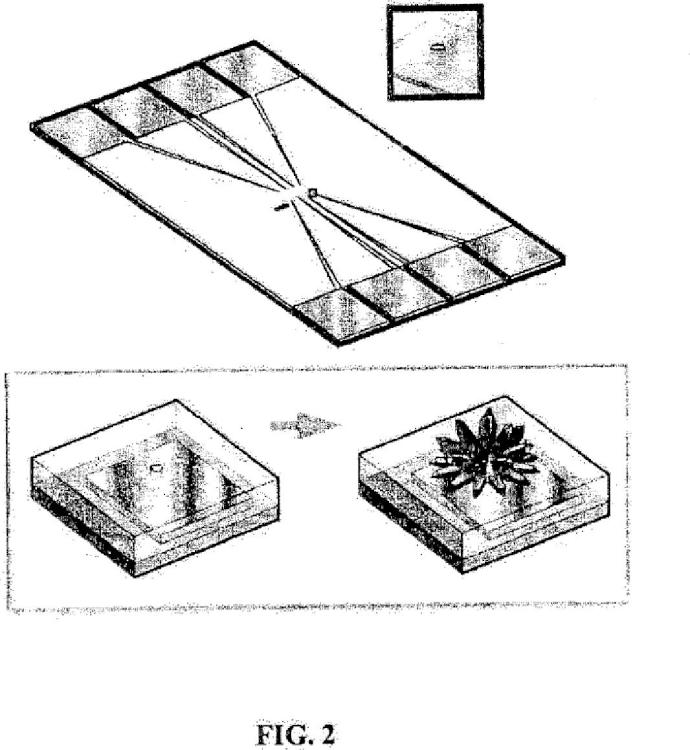
Se hace referencia ahora a la figura 2, que también ilustra la formación de un NME sobre un chip. Como en la figura 1 A, se proporcionan electrodos pequeños in situ sobre un chip, definiéndose la posición y el contacto eléctrico de los NME fotolitográficamente. Como en la figura 1, este chip es un chip pasivo multiplexado 8 veces. Sobre un sustrato de silicio, se crea un patrón de una capa de oro de ~35 nm de grosor, usando técnicas de fotolitografía convencionales, para conectar ocho cables de Au de 5 pm de ancho a zonas de metal grandes para la conexión a instrumentación fuera del chip. Se deposita una capa de SÍO2 aislante sin perforar y se crea un patrón para crear aberturas de ~5 nm (por ejemplo, mediante grabado con ácido) en el extremo de cada uno de los cables de Au, para exponer una sección del cable. Entonces se galvaniza un NME de metal en esta abertura usando electrodeposición.
El NME puede comprender diferentes materiales conductores. Algunos ejemplos de NME se han formado tal como sigue, aunque son posibles variaciones y se describirán en mayor detalle a continuación: Se depositaron NME de Pd fractales ramificados en una disolución acuosa que contenía 5 mM de H2PdCl4 y ,5 M de HCIO4 usando amperimetría de potencial de CC a -25 mV durante 15 s. Se depositaron NME de Pd semiesféricos con rugosidad a escala nanométrica en una disolución acuosa que contenía 5 mM de H2PdCU y ,5 M de HCI usando amperimetría de potencial de CC a -1 mV durante 3 s. Se fabricaron NME de Pd semiesféricos lisos en la misma disolución a mV durante 3 s. Se fabricaron NME de Au en un baño de oro que contenía una disolución ,1 M de HAuCL y H2SO4 ,5 M a -1mV durante 4 segundos. Se fabricaron NME de Pt en un baño de platino que contenía una disolución 5 mM de H2PtCI6 y H2SO4 ,5 M a -1 mV durante 5 s. Pueden controlarse el tamaño y la morfología de NME variando la concentración de sal de metal, el tipo y la concentración del electrolito de soporte y el potencial y la duración de la electrodeposición.
La figura 3 es un esquema de un NME con sondas con espaciadores en la monocapa de sonda y entre el electrodo y la sonda. Puede ponerse en comunicación una disolución química que contiene un catión metálico con la superficie del NME y un electrodo de referencia. El electrodo de referencia puede ser un NME o un electrodo convencional sobre el mismo cable. Puede proporcionarse una polarización eléctrica entre el NME y el electrodo de referencia. Entonces puede eliminarse la disolución química y lavarse los electrodos. Entonces puede ponerse en comunicación una disolución que contiene la molécula de sonda con la superficie del NME. Puede modificarse o funcionalizarse la molécula de sonda de manera que se une a la superficie del NME. Por ejemplo, puede funcionalizarse la molécula de sonda con un grupo tiol, amina o carboxilato.
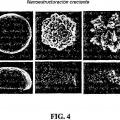
En la figura 4 se muestran NME con nanoestructuración creciente. Inesperadamente, la variación de las condiciones
de electrodeposición permitieron el crecimiento de microelectrodos semiesféricos extremadamente lisos (izquierda); estructuras fractales a escala nanométrica altamente ramificadas (derecha); o semiesferas con rugosidad a escala nanométrica (centro). La estructura a la izquierda se produjo con HCI como electrolito de soporte con un potencial aplicado de mV. Las estructuras del centro también se produjeron con HCI como electrolito de soporte pero con un potencial aplicado de -1 mV. La estructura a la derecha se realizó con HCIO4 como electrolito de soporte y un potencial aplicado de -25 mV. La barra de escala en la figura corresponde a 5 p.m a menos que se indique lo contrario.
La figura 5 ilustra etapas implicadas en la detección de secuencias específicas (Lapierre et al., Anal. Chem. 75:6327, Ratilainen et al., Biochemistry 39:7781, Tomlins et al., Science 31:644). En este ejemplo, en primer lugar se modifican NME de Pd con secuencias de sonda derivatizadas con tiol y entonces se hibridan las secuencias diana. Entonces se transduce la presencia de la diana usando un sistema de indicador electrocatalitico. La electrocatálisis proporciona amplificación electrónica, o aumento, facilitando una lectura de sensibilidad alta: pueden resultar cientos de electrones de cada acontecimiento de complejación biomolecular. El enfoque usado en el presente documento se basa en el aceptor de electrones primario Ru(NH3)6 3+, que se atrae electrostáticamente hacia las superficies del electrodo a niveles que se correlacionan con la cantidad de ácido nucleico unido. La inclusión de Fe(CN)63' durante la lectura electroquímica sirve para regenerar el sustrato de Ru (III), ya que la especie Fe (III) es incluso más fácil de reducir, pero se repele electrostáticamente desde el electrodo y por tanto sólo experimenta reducción química mediante Ru (II). Este método también es libre de marcador y no requiere que se procese la muestra de ninguna manera.
El dispositivo de biodetección puede proporcionarse en forma de un chip, tal como un chip de circuito integrado (IC). En general, un IC que incorpora el NME puede tener un sustrato con un cable eléctricamente conductor que está recubierto por una capa aislante. La capa aislante tiene una abertura que expone una parte del cable, y el NME se proporciona en la parte expuesta del cable. El NME es sensible a un estímulo biomolecular. En particular, el NME puede funcionalizarse con moléculas de sonda que experimentan una reacción de hibridación con una biomolécula diana (por ejemplo, una secuencia de ácido nucleico), dando como resultado una carga generada en el NME. El IC también tiene un almacenamiento de carga (por ejemplo, un condensador o una batería) en comunicación eléctrica con el cable para almacenar esta carga generada. En un uso típico, el NME puede estar expuesto a una muestra durante una duración de tiempo o un periodo de integración conocidos, y la carga almacenada a lo largo de ese tiempo sería entonces indicativa de la presencia y/o cantidad de la biomolécula diana.
La carga almacenada puede comunicarse con un dispositivo de cálculo para su análisis, o puede presentarse (por ejemplo, a través de un componente de presentación digital) para la lectura directa de la carga almacenada tras el periodo de integración.
Un IC de este tipo puede fabricarse usando equipo de fabricación de IC común, permitiendo que se fabrique este dispositivo fácilmente y que sea menos costoso que otras formas de microelectrodos de biodetección. Los materiales usados pueden ser aquéllos que ya se usan comúnmente en la fabricación de IC. Por ejemplo, el sustrato puede estar hecho de silicio, cuarzo, vidrio, cerámica, sílice, zafiro, arsenuro de galio u otros materiales usados actualmente para IC. Los sustratos o soportes pueden incorporar material conductor para que sirva como electrodo. También pueden usarse soportes conductores con una superficie de oro. Los soportes comprenden habitualmente una superficie lisa (plana), o al menos una estructura en la que las sondas o p que van a estudiarse están aproximadamente en el mismo plano. El soporte puede ser un electrodo o puede estar unido a un electrodo.
El cable puede estar... [Seguir leyendo]
Reivindicaciones:
1. Microelectrodo nanoestructurado adaptado para generar una carga en respuesta a un estímulo biomolecular, en el que dicha nanostructura está nanotexturizada y es puntiaguda o fractal, y en el que el microelectrodo nanoestructurado puede presentar una sonda biomolecular en la superficie del mismo. 5
2. Microelectrodo según la reivindicación 1, estando dicho microelectrodo compuesto por un material seleccionado del grupo que consiste en: un metal noble, una aleación de un metal noble, un polímero conductor, un óxido de metal, un siliciuro de metal, un nitruro de metal, carbono o una combinación de cualquiera de los mismos.
3. Microelectrodo según la reivindicación 1, en el que la carga se genera por medio de un sistema de indicador electrocatalítico.
4. Microelectrodo según la reivindicación 3, en el que dicho sistema de indicador electrocatalítico comprende hexamina de rutenio, ferricianuro de potasio o una combinación de hexamina de rutenio y ferricianuro. 15
5. Microelectrodo según la reivindicación 1, en el que el estímulo biomolecular es hibridación de ácido nucleico o unión de proteína a proteína.
6. Microelectrodo según la reivindicación 1, que comprende además una sonda seleccionada del grupo que consiste 20 en: moléculas de sonda tiolada, ácidos nucleicos, ácidos nucleicos peptídicos, ácidos nucleicos bloqueados o oligómeros de fosforodiamidato-morfolino terminados con tioles, ácidos nucleicos, ácidos nucleicos peptídicos, ácidos nucleicos bloqueados, aminas, carboxilatos, proteínas o péptidos funcionalizados con moléculas de anclaje adecuadas y anticuerpos funcionalizados con moléculas de anclaje adecuadas.
7. Dispositivo de biodetección que comprende:
un sustrato,
al menos un cable eléctricamente conductor sobre el sustrato, 30
una capa aislante que recubre el cable, teniendo la capa aislante una abertura que define un espacio en el que se expone una parte del cable,
el microelectrodo nanoestructurado según la reivindicación 1 depositado dentro de la abertura; 35
en el que el microelectrodo está adaptado por medio de un sistema de indicador electrocatalítico para generar una carga en respuesta a un estímulo biomolecular; en el que el microelectrodo nanoestructurado puede presentar una sonda biomolecular en la superficie del mismo; y en el que dicho microelectrodo está en contacto eléctrico con la parte expuesta del cable. 40
8. Dispositivo de biodetección según la reivindicación 7, en el que el cable comprende un material seleccionado del grupo que consiste en: Au, Al, W, TiN y polisilicio.
9. Dispositivo de biodetección según la reivindicación 7, en el que el sustrato comprende un material seleccionado 45 del grupo que consiste en: silicio, sílice, cuarzo, vidrio, zafiro, arsenuro de galio, germanio, carburo de silicio, compuestos de indio, sulfuro de selenio, material cerámico, plástico, policarbonato y otros polímeros o combinaciones de los mismos.
10. Dispositivo de biodetección según la reivindicación 7, en el que la capa aislante está compuesta por un material 50 seleccionado de dióxido de silicio, nitruro de silicio, óxido de silicio dopado con nitrógeno y parileno o combinaciones de los mismos.
11. Dispositivo de biodetección según la reivindicación 7, en el que se proporciona una pluralidad de microelectrodos en una matriz, y cada microelectrodo puede tratarse individualmente. 55
12. Dispositivo de biodetección según la reivindicación 7, en el que la sonda se selecciona del grupo que comprende: ácidos nucleicos, ácidos nucleicos peptídicos, ácidos nucleicos bloqueados, proteínas o péptidos funcionalizados con moléculas de anclaje adecuadas; y en el que el estímulo biomolecular es hibridación de ácido nucleico o unión de proteína a proteína. 60
13. Dispositivo de biodetección según la reivindicación 7, en el que el dispositivo de biodetección está contenido dentro de un cartucho de biodetección y en el que el cartucho de biodetección también incluye una cámara de muestra para recibir una muestra biológica.
14. Dispositivo de biodetección según la reivindicación 13, en el que la cámara de biodetección comprende un tampón que comprende sodio, fosfato, cloruro, magnesio o combinaciones de los mismos.
15. Dispositivo de biodetección según la reivindicación 13 ó 14, en el que el cartucho de biodetección comprende además una cámara de purificación para purificar o aislar la muestra.
16. Método para llevar a cabo un procedimiento de biodetección usando un microelectrodo nanoestructurado, comprendiendo dicho método:
proporcionar el dispositivo de la reivindicación 7;
polarizar el microelectrodo con respecto a un electrodo de referencia; medir un flujo de carga de referencia o de corriente de referencia entre el microelectrodo y el electrodo de referencia; exponer el microelectrodo a un estímulo biomolecular;
medir por medio del sistema de indicador electrocatalítico un flujo de carga o de corriente generado en el 15 microelectrodo en respuesta al estímulo biomolecular; y
determinar la cantidad de estímulo biomolecular presente comparando el flujo de carga medido o de corriente medido frente al flujo de carga de referencia o de corriente de referencia.
Patentes similares o relacionadas:
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]
Sistema y dispositivos de ensayo de actividad enzimática, del 1 de Julio de 2020, de Københavns Universitet (KU): Un dispositivo de actividad enzimática adecuado para la determinación de la actividad de degradación enzimática de los biopolímeros en una muestra líquida, […]
Sistema y método para medir una concentración de analito corregida usando un sensor electroquímico, del 20 de Mayo de 2020, de CILAG GMBH INTERNATIONAL: Un método para determinar una concentración de un analito en una muestra, el método comprendiendo: introducir una muestra que incluye un analito en una […]
Sistemas, dispositivos y métodos para mejorar la precisión de biosensores usando el tiempo de llenado, del 18 de Marzo de 2020, de LIFESCAN, INC.: Un método para medir una concentración de analito corregida en una muestra de sangre, el método comprendiendo: detectar una presencia de la muestra de […]
Sistemas, dispositivos y métodos para mejorar la precisión de biosensores usando el tiempo de llenado, del 18 de Marzo de 2020, de LIFESCAN, INC.: Un sistema electroquímico, que comprende: una celda electroquímica que tiene un electrodo inferior y un electrodo superior ; […]
Medida de analito ajustada en temperatura para sistemas de biosensor, del 19 de Febrero de 2020, de Ascensia Diabetes Care Holdings AG: Un método para determinar una concentración de analito en una muestra de un fluido biológico, que comprende las siguientes etapas: determinar […]
Métodos analíticos y de diagnóstico que utilizan apirasa de Shigella flexneri, del 19 de Febrero de 2020, de ApiRays Bioscience AB: Método para reducir la cantidad de nucleósido difosfatos y/o nucleósido trifosfatos contaminantes, que comprende las etapas de a. proporcionar […]
Procedimiento de detección y de identificación directa de un microorganismo en una muestra biológica diluida en un caldo de enriquecimiento, del 19 de Febrero de 2020, de BIOMERIEUX: Procedimiento de detección de al menos un microorganismo presente en una muestra colocada en un contenedor cerrado, comprendiendo dicho método esencialmente las etapas siguientes: […]