Métodos para la detección e identificación de beta lactamasas de espectro extendido.
Un método para la detección y/o identificación de la presencia de microbios con una ß-lactamasa de espectro extendido de CTX-M en un espécimen,
que comprende:
obtener una muestra del espécimen para ser analizada para la presencia de una ß-Lactamasa de espectro extendido de CTX-M;
poner en contacto la muestra con un conjunto de cebadores de amplificación en condiciones suficientes para proporcionar productos de amplificación de ácidos nucleicos basados en la polimerasa, en donde el conjunto de cebadores de amplificación comprende al menos un par de cebadores que comprende un primer y segundo cebador, dichos cebadores primero y segundo que comprenden al menos 12 nucleótidos consecutivos seleccionados del grupo que consiste en:
sec. con núms. de ident.; 1 y 2 ;
sec. con núms. de ident.; 3 y 4;
sec. con núms. de ident.; 6 y 7;
sec. con núms. de ident.; 8 y 9;
sec. con núms. de ident.; 27 y 28; y
sec. con núms. de ident.; 29 y 30; o las complementarias de estas,
en donde dicho conjunto de cebadores comprende uno o más cebadores con una base universal, en donde dicho conjunto de cebadores de amplificación se hibridan conjuntamente, y producen productos de amplificación diana en la presencia de isoformas de CTX-M 1-82;
proporcionar reactivos y condiciones para la extensión de los cebadores para generar los productos de amplificación diana; y
determinar la presencia y/o cantidad de los productos de amplificación diana, en donde la presencia del producto de amplificación diana indica la presencia de dicha ß-lactamasa de espectro extendido de CTX-M.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/024832.
Solicitante: Becton Dickinson Infusion Therapy Systems Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1 BECTON DRIVE FRANKLIN LAKES, NJ 07417-1880 ESTADOS UNIDOS DE AMERICA.
Inventor/es: ROGER-DALBERT, CELINE, LIPPE,CATHERINE, DUTEAUD,ISABELLE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C12P19/34 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Polinucleótidos, p. ej. ácidos nucleicos, oligorribonucleótidos.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
PDF original: ES-2545793_T3.pdf





Fragmento de la descripción:
Métodos para la detección e identificación de beta lactamasas de espectro extendido Referencia a la lista de secuencias
La presente solicitud se presenta junto con una lista de secuencias en formato electrónico. La lista de secuencia se proporciona como un archivo denominadoGENOM.097VPC.txt, creado el 18 de febrero de 2010 que es de 15.2 KB en tamaño. La información en formato electrónico de la lista de secuencias se incorpora en la presente como referencia en su totalidad.
Antecedentes de la invención Campo de la invención
Las modalidades descritas en la presente descripción se relacionan con el diagnóstico molecular, y, particularmente, el diagnóstico que se usa para detectar e identificar microbios que portan beta lactamasas de espectro extendido (ESBLs), y particularmente genes CTX-M.
Descripción de la técnica relacionada
Las [3-lactamasas confieren resistencia contra fármacos de p-lactámicos. Estas enzimas destruyen el anillo p-lactámico de los antibióticos p-lactámicos, tales como penicilina, cefalosporinas, cefamicinas, y carbapenemos (etiapenemo). Estos antibióicos tienen un elemento común en su estructura molecular: un anillo de cuatro átomos conocido como un beta-lactámico. La enzima lactamasa rompe ese anillo libre, lo que desactiva las propiedades antibacteriales de la molécula.
Las p-lactamasas de espectro extendido (ESBLs) son cada vez más responsables de infecciones nosocomiales que se elevan por todo el mundo, y de forma alarmante, por emergencia comunitaria también (Rossolini y otros 2008, CMI). Las ESBLs son beta-lactamasas que hidrolizan cefalosporina de espectro extendido con una cadena lateral de oxiimino. Estas cefalosporinas incluyen cefotaxima, ceftriaxona, y ceftazidima, así como el aztreonam oxiimino monobactam. Así las ESBLs confieren resistencia a estos antibióticos y a beta lactámicos oxiimino relacionados. Las ESBLs más conocidas se derivan de los genes TEM-1, TEM-2, o SHV-1, e incluyen mutaciones que alteran la configuración de aminoácidos alrededor del sitio activo de estas [3- lactamasas. Esto extiende el espectro de antibióticos p-lactámicos susceptibles a la hidrólisis por estas enzimas.
Las variantes clásicas TEM y SHV, tal como genes TEM y SHV, en realidad se están extendiendo rápidamente por todo los Estados Unidos de América, después de haber afectado a la mayor parte de Europa, mientras que un nuevo tipo de ESBL, CTX-M, es predominante en América del Sur, el Mediterráneo y los países de Europa del Este (Govinden y otros 2007, AJB). La última, que debe su nombre a su alta actividad frente a cefotaxima, se observó en los finales de 1980 en Japón, Europa y Argentina, más específicamente en Alemania en 1989 (Naas y otros 2008, CMI). Se considera que es el grupo más exitoso de todos (Rasmussen & Hoiby 2004, CJM). Su aspecto podría ser una consecuencia del uso incrementado de ceftriaxona y/o cefotaxima para tratar infecciones bacterianas, y su origen es conocido por ser de genes cromosómicos residentes en los miembros del género K/uyvera. Hasta hoy día, más de 85 derivados de CTX-M, que se clasifican en 5 grupos filogenéticos (CTX-M-1, 2, 8, 9 y 25), se han documentado de acuerdo con el sitio web de la Clínica Lahey, accesible en la dirección web lahey.org/Studieso.
Los genes de resistencia CTX-M se encuentran en fnferobacfer/aceae y se pueden transmitir fácilmente a través de plásmidos entre especies. Las especies de Enterobacterias que incluyen K/eós/e/Za pneumon/ae, Esc/rer/c/r/a co//, y similares que poseen los genes CTX-M se consideran que sean la principal causa de infección del tracto urinario. Otras Enteroóacter/aceae, tal comofnferoóacferc/oacae, Proteos m/raM/s, Sa/mone/Zaenfer/ca, Enferobacferaerogenes, así como también K/eós/e//a oxyfoca, pueden además albergar genes CTX-M. La detección de cepas resistentes a CTX-M es especialmente crucial, ya que requiere el aislamiento de otros pacientes en hospitales, y dejaría sólo los carbapenémicos como el principal tratamiento para las infecciones.
Hasta hace poco, la única manera de saber la resistencia de una cepa fue realizar una prueba manual de susceptibilidad antimicrobiana. Las pruebas de susceptibilidad sufren de muchos inconvenientes, que incluyen la cantidad de tiempo para obtener un resultado, es dec/r, entre 48 a 96 horas. En primer lugar, el operador necesita para aislar la cepa bacteriana de las muestras, lo que podría tomar hasta 48 horas; después proceder con la identificación bioquímica, que son otras 18 a 24 horas, y luego con la prueba manual de susceptibilidad antimicrobiana, que además podría tardar hasta 24 horas. Adicionalmente a la demora en la obtención de resultados, los métodos de pruebas manuales también sufren de otros problemas, como la falta de reproducibilidad debido a un almacenamiento
inadecuado de los discos de antibióticos, la difusión indebida de algunos discos de antibióticos, y la falta en la estandarización del proceso.
La especificidad y exactitud de la detección de ESBLs es crucial, ya que los resultados falsos negativos pueden llevar a los médicos a diseñar un régimen inadecuado de antibióticos, por ejemplo, el tratamiento de un individuo con una Infección de ESBL con cefalosporinas de tercera generación o con aztreonam. Esto plantea riesgos innecesarios para el Individuo tratado, y además aumenta las probabilidades de contaminación cruzada dentro de un ambiente clínico, por e/emp/o, un hospital. Como algunas cepas que producen ESBL no se mostrarán en la resistencia /n v/fro a todas las cefalosporinas de tercera o cuarta generación mediante el uso de los puntos de parada sugeridos, el Instituto Estándar Clínico y de Laboratorio, (CLSI), recomienda informar las Enferoóacfer/aceae que producen ESBL como resistentes a penicilinas, cefalosporinas y aztreonam, ya que podrían terminar siendo clínicamente resistentes (CLSI, M100-S18). La capacidad de los organismos que albergan genes de resistencia CTX-M para hidrolizar las cefalosporinas más nuevas y aztreonam hace su detección aún más difícil. Las directrices de CLSI plantean la amenaza de diagnosticar mal la presencia de cepas que producen CTX-M, en dependencia de los fármacos usados tanto en la selección inicial como en pruebas de confirmación.
Las modalidades descritas en la presente descripción proporcionan ventajas sobre otros métodos usados para detectar e identificar bacterias que tienen ESBLs, por e/emp/o, genes de resistencia CTX-M, que incluyen la mejora de la especificidad, la disponibilidad de los resultados en un período de tiempo más corto, y elimina la necesidad de realizar etapas adicionales, tales como electroforesis en gel de agarosa, para detectar ESBLs. (Lartigue y otros 2004, FEMS ML; Pitout y otros 2004, JCM; Pitout y otros2007, CMI). Además, las modalidades descritas en la presente descripción ofrecen ventajas sobre otros métodos informados para la detección de ESBLs, que incluyen CTX-M, en que los métodos y composiciones descritos en la presente descripción están diseñados específicamente para la detección e identificación de ¡soformas recientemente descubiertas del gen CTX-M, que no eran conocidas por la época del desarrollo de los ensayos descritos, por ejemplo, en la publicación de solicitud de patente de Estados Unidos núm. US20070248954. Los métodos descritos en US20070248954 usan cebadores que no son totalmente complementarios a las secuencias de las ¡soformas de CTX-M recientemente descubiertas, lo que podría comprometer la especificidad, o incluso dar lugar a resultados falsos negativos.
Resumen de la Invención
De acuerdo con un aspecto de la presente Invención se proporciona un método como se define por las reivindicaciones para detectar y/o Identificar la presencia de microbios con una p-lactamasa de espectro extendido CTX-M en una muestra.
De acuerdo con un aspecto de la presente Invención se proporciona un estuche como se define por las reivindicaciones para la detección y/o Identificación de la presencia de microbios con una p-lactamasa de espectro extendido CTX-M en una muestra.
La presente Invención se relaciona además con el uso de cebadores y sondas de acuerdo con las modalidades descritas en la presente descripción, en donde los cebadores o sondas tienen las secuencias de acuerdo con cualquiera de las secuencias como se definen en las sec. con núms. de ¡dent.; 1-24.
Breve descripción de las figuras
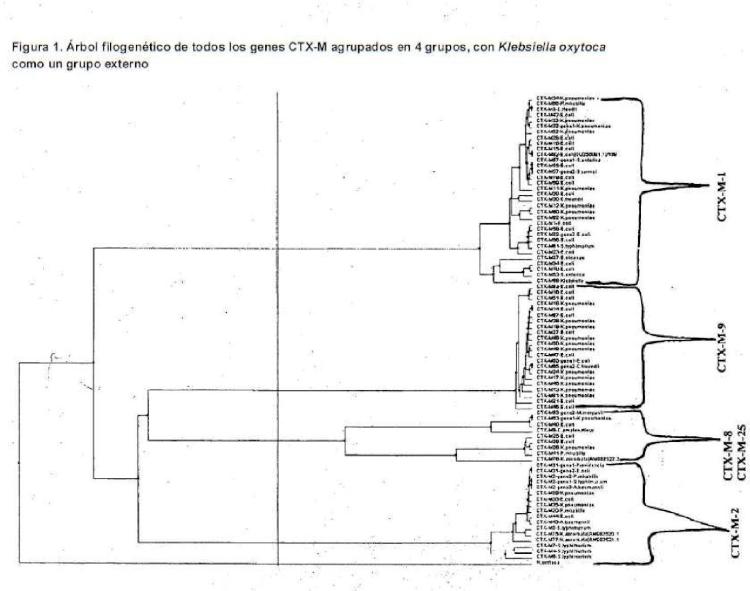
La figura 1 es un árbol filogenètico de todos los genes CTX-M agrupados en 4 grupos, con K/e¡bs/e//a oxyfoca como un grupo externo.
La figura 2 es un alineamiento de secuencias, que muestra la ubicación de los cebadores descritos en la presente descripción para detectar el grupo CTX-M-1 (ctxm1-616F/sec. con núm. de... [Seguir leyendo]
Reivindicaciones:
1. Un método para la detección y/o identificación de la presencia de microbios con una [5-lactamasa de espectro extendido de CTX-M en un espécimen, que comprende:
obtener una muestra del espécimen para ser analizada para la presencia de una p-Lactamasa de espectro extendido de CTX-M;
poner en contacto la muestra con un conjunto de cebadores de amplificación en condiciones suficientes para
proporcionar productos de amplificación de ácidos nucleicos basados en la polimerasa, en donde el conjunto
de cebadores de amplificación comprende al menos un par de cebadores que comprende un primer y segundo
cebador, dichos cebadores primero y segundo que comprenden al menos 12 nucleótidos consecutivos
seleccionados del grupo que consiste en:
sec. con núms. de ¡dent.; 1 y 2 ;
sec. con núms. de ¡dent.; 3 y 4;
sec. con núms. de ¡dent.; 6 y 7;
sec. con núms. de ¡dent.; 8 y 9;
sec. con núms. de ¡dent.; 27 y 28; y
sec. con núms. de ¡dent.; 29 y 30; o las complementarlas de estas,
en donde dicho conjunto de cebadores comprende uno o más cebadores con una base universal, en donde dicho conjunto de cebadores de amplificación se hlbrldan conjuntamente, y producen productos de amplificación diana en la presencia de ¡soformas de CTX-M 1-82;
proporcionar reactivos y condiciones para la extensión de los cebadores para generar los productos de amplificación diana; y
determinar la presencia y/o cantidad de los productos de amplificación diana, en donde la presencia del producto de amplificación diana Indica la presencia de dicha [3-lactamasa de espectro extendido de CTX-M.
2. El método de la reivindicación 1, que además comprende poner en contacto dicha muestra con al menos una sonda que híbrida con al menos un producto de amplificación diana.
3. El método de la reivindicación 1, caracterizado además porque dicho conjunto de cebadores de amplificación comprende una pluralidad de pares de cebadores de amplificación, en donde dicha pluralidad de pares de cebadores de amplificación se hibridan conjuntamente con, y producen productos de amplificación diana en la presencia de ácidos nucleicos de CTX-M a partir de cada una de las cepas bacterianas enumeradas en la Tabla 1.
4. El método de la reivindicación 2, caracterizado además porque dicha sonda se selecciona del grupo que consiste en una sonda de baliza molecular, una sonda fluorescente TAQMAN^, y una sonda fiuorescente scorplon.
5. El método de la reivindicación 1, que además comprende poner en contacto dicha muestra con una o más sondas, en donde dicha una o más sondas híbrida conjuntamente con los productos de amplificación diana de los grupos de CTX-M CTX-M-1, CTX-M-2, CTX-M-8, CTX-M-9, y CTX-M-25, bajo condiciones suficientes para proporcionar productos de amplificación de ácidos nucleicos basados en la polimerasa.
6. El método de la reivindicación 1, caracterizado además porque dicho conjunto de cebadores de amplificación comprende al menos dos cebadores, en donde cada cebador se selecciona del grupo que consiste en:
CYGCTTCCTGGGTTGTGG (sec. con núm. de ¡dent.:1);
TTGRGGCTGGGTGAAGTAAG (sec. con núm. de ident.:2);
GGTMTGCCGAAATSWTGG (sec. con núm. de ¡dent.:3);
CGCAGCCAGAAHATCCCGAC (sec. con núm. de ident.:4);
TGTRTGCSCAGGCGAACG (sec. con núm. de ¡dent.:6);
GTAGAGCGTCTGTGYGTTAFCG (sec. con núm. de ident.:7);
TTTATGCGCAGACGAGTG (sec. con núm. de ¡dent.:8);
AAAGCACCTGCGTATTATCT (sec. con núm. de ident.:9); o la complementaria de estas.
7. El método de la reivindicación 6, que además comprende poner en contacto dicha muestra con al menos una sonda, en donde dicha al menos una sonda comprende al menos 12 nucleótidos consecutivos seleccionados del grupo que consiste en la sec. con núm. de ¡dent.: 5, sec. con núm. de ¡dent.:10, sec. con núm. de ident.:31, sec. con núm. de ident.:32, y sec. con núm. de ¡dent.:33.
8. El método de la reivindicación 1, caracterizado además porque dicho conjunto de cebadores de amplificación comprende al menos dos cebadores, en donde cada cebador comprende al menos 12 nucleótidos consecutivos seleccionados del grupo que consiste en :
CYGCTTCCTGGGTTGTGG (sec. con núm. de ident.:1);
TTGRGGCTGGGTGAAGTAAG (sec. con núm. de ident.:2);
GGTMTGCCGAAATSWTGG (sec. con núm. de ident.:3);
CGCAGCCAGAAHATCCCGAC (sec. con núm. de ident.:4);
CAGCACCAGTAARGTGATG (sec. con núm. de ident. :27);
TTGTAGTTAAYCARGTCYGARG (sec. con núm. de ident.:28);
CGGTGATGAACGCTTTCC (sec. con núm. de ident.:29);
ATCGGCAGGCTTGATCTC (sec. con núm. de ident.:30); o la complementaria de estas.
9. El método de la reivindicación 8, que además comprende poner en contacto dicha muestra con al menos una sonda, en donde dicha al menos una sonda comprende al menos 12 nucleótidos consecutivos seleccionados del grupo que consiste en la sec. con núm. de ident.:5, sec. con núm. de ident.:10, sec. con núm. de ident.:31, sec. con núm. de ident.:32, y sec. con núm. de ident.: 33.
10. Un estuche para la detección y/o identificación de la presencia de microbios con [5-lactamasas de espectro extendido de CTX-M en un espécimen, que comprende:
un conjunto de cebadores de amplificación en donde el conjunto de cebadores de amplificación comprende una pluralidad de pares de cebadores, y en donde dicho conjunto de cebadores de amplificación comprende uno o más cebadores con una base universal, en donde dicha pluralidad de pares de cebadores de amplificación se hibridan conjuntamente a, y produce productos de amplificación diana en la presencia de, ¡soformas 1-82 de CTX-M bajo condiciones suficientes para proporcionar productos de amplificación de ácidos nucleicos basados en la polimerasa, en donde el conjunto de cebadores de amplificación comprende al menos un par de cebadores que comprende un primer y segundo cebador, dichos primero y segundo cebadores que comprenden al menos 12 nucleótidos consecutivos seleccionados del grupo que consiste en: sec. con núms. de ident.; 1 y 2 sec. con núms. de ident.; 3 y 4; sec. con núms. de ident.; 6 y 7; sec. con núms. de ident.; 8 y 9; sec. con núms. de ident.; 27 y 28; y
sec. con núms. de ident.; 29 y 30; o las complementarias de estas.
11. El estuche de la reivindicación 10, que además comprende al menos una sonda que se híbrida con al menos una secuencia diana.
12. El estuche de la reivindicación 11, caracterizado además porque dicha sonda se selecciona del grupo que consiste en un sonda de baliza molecular, una sonda fluorescente TAQMAN^, y una sonda fluorescente scorpion.
13. El estuche de la reivindicación 10, que además comprende al menos una sonda que se puede hibridar con los productos de amplificación diana de al menos dos productos de amplificación diana del grupo CTX-M bajo dichas condiciones suficientes para proporcionar productos de amplificación de ácidos nucleicos basados en la polimerasa.
14. El estuche de la reivindicación 10, que además comprende una o más sondas, en donde dichas una o más sondas se pueden hibridar conjuntamente a los productos de amplificación diana de los grupos CTX-M CTX-M- 1, CTX-M-2, CTX-M-8, CTX-M-9, y CTX-M-25, bajo condiciones estándar de PCR.
15. El estuche de la reivindicación 10, caracterizado además porque dicho conjunto de cebadores de amplificación comprende al menos dos cebadores, seleccionados del grupo que consiste en:
CYGCTTCCTGGGTTGTGG (sec. con núm. de ident.:1);
TTGRGGCTGGGTGAAGTAAG (sec. con núm. de ident.:2);
GGTMTGCCGAAATSWTGG (sec. con núm. de ¡dent.:3);
CGCAGCCAGAAHATCCCGAC (sec. con núm. de ¡dent.:4);
TGTRTGCSCAGGCGAACG (sec. con núm. de ident.:6);
GTAGAGCGTCTGTGYGTTATCG (sec. con núm. de ¡dent.:7);
TTTATGCGCAGACGAGTG (sec. con núm. de ident.:8);
AAAGCACCTGCGTATTATCT (sec. con núm. de ident.:9); o la complementaria de estas.
16. El estuche de la reivindicación 15, que además comprende al menos una sonda, en donde dicha al menos una sonda comprende al menos 12 nucleótidos consecutivos seleccionados del grupo que consiste en la sec. con núm. de ¡dent.:5, sec. con núm. de ident.:10, sec. con núm. de ident.:31, sec. con núm. de ident.:32, y sec. con núm. de ¡dent.:33.
17. El estuche de la reivindicación 10, caracterizado además porque dicho conjunto de cebadores de amplificación comprende al menos dos cebadores, en donde cada cebador se selecciona del grupo que consiste en:
CYGCTTCCTGGGTTGTGG (sec. con núm. de ¡dent.:1);
TTGRGGCTGGGTGAAGTAAG (sec. con núm. de ¡dent.:2);
GGTMTGCCGAAATSWTGG (sec. con núm. de ¡dent.:3);
CGCAGCCAGAAHATCCCGAC (sec. con núm. de ¡dent.:4);
CAGCACCAGTAARGTGATG (sec. con núm. de ¡dent.:27);
TTGTAGTTAAYCARGTCYGARG (sec. con núm. de ¡dent.:28);
CGGTGATGAACGCTTTCC (sec. con núm. de ¡dent.:29);
ATCGGCAGGCTTGATCTC (sec. con núm. de ¡dent.:30); o la complementaria de estas.
18. El estuche de la reivindicación 17, que además comprende al menos una sonda, en donde dicha al menos una sonda comprende al menos 12 nucleótidos consecutivos seleccionados del grupo que consiste en la sec. con núm. de ¡dent.:5, sec. con núm. de ¡dent.:10, sec. con núm. de ¡dent.:31, sec. con núm. de ¡dent.:32, y sec. con núm. de ¡dent.:33.
19. El estuche de la reivindicación 10, que además comprende un par de cebadores de amplificación que se híbrida con ácidos nucleicos que flanquean una secuencia diana dentro o que Incluyen parte de un gen carbapenamasa.
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
MÉTODOS PARA EL DIAGNÓSTICO DE ENFERMOS ATÓPICOS SENSIBLES A COMPONENTES ALERGÉNICOS DEL POLEN DE OLEA EUROPAEA (OLIVO), del 23 de Julio de 2020, de SERVICIO ANDALUZ DE SALUD: Biomarcadores y método para el diagnostico, estratificación, seguimiento y pronostico de la evolución de la enfermedad alérgica a polen del olivo, kit […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Secuenciación dirigida y filtrado de UID, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento para generar una biblioteca de polinucleótidos que comprende: (a) generar una primera secuencia del complemento (CS) de un polinucleótido diana a partir […]
Métodos para la recopilación, estabilización y conservación de muestras, del 8 de Julio de 2020, de Drawbridge Health, Inc: Un método para estabilizar uno o más componentes biológicos de una muestra biológica de un sujeto, comprendiendo el método obtener un […]
Evento de maíz DP-004114-3 y métodos para la detección del mismo, del 1 de Julio de 2020, de PIONEER HI-BRED INTERNATIONAL, INC.: Un amplicón que consiste en la secuencia de ácido nucleico de la SEQ ID NO: 32 o el complemento de longitud completa del mismo.
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Aislamiento de ácidos nucleicos, del 24 de Junio de 2020, de REVOLUGEN LIMITED: Un método de aislamiento de ácidos nucleicos que comprenden ADN de material biológico, comprendiendo el método las etapas que consisten en: (i) efectuar un lisado […]