Concentración y enriquecimiento de células microbianas y ácidos nucleicos microbianos a partir de fluidos corporales.
Un método para aislar microorganismos de una muestra sanguínea que tiene o se sospecha que tiene microorganismos y células hospedantes,
comprendiendo dicho método:
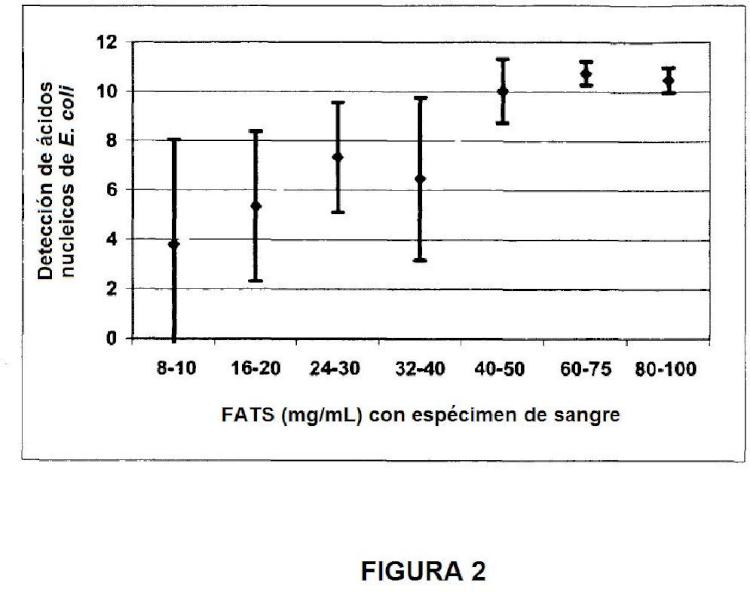
a. poner en contacto la muestra de sangre con una formulación de saponinas, donde la saponina es una disolución de saponina tratada en autoclave y filtrada (FATS) o una disolución de saponina tratada en autoclave, filtrada y calentada (HFATS) presente en una concentración final de 40 mg/mL a 100 mg/mL; y
b. obtener microorganismos aislados;
donde los microorganismos aislados comprenden ácidos nucleicos.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA2008/001414.
Solicitante: UNIVERSITE LAVAL.
Nacionalidad solicitante: Canadá.
Dirección: Vice-rectorat à la recherche et à la création, Pavillon des Sciences de l'Education, 2320, Rue des Bibliothèques, Local 1434 Quebec, QC G1V 0A6 CANADA.
Inventor/es: HULETSKY,ANN, PEYTAVI,RÉGIS, BELLEY-MONTFORT,LUCILE, MARTINEAU,ISABELLE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C11D1/66 QUIMICA; METALURGIA. › C11 ACEITES, GRASAS, MATERIAS GRASAS O CERAS ANIMALES O VEGETALES; SUS ACIDOS GRASOS; DETERGENTES; VELAS. › C11D COMPOSICIONES DETERGENTES; UTILIZACION DE UNA SOLA SUSTANCIA COMO DETERGENTE; JABON O SU FABRICACION; JABONES DE RESINA; RECUPERACION DE LA GLICERINA. › C11D 1/00 Composiciones de detergentes a base esencialmente de compuestos tensioactivos; Utilización de estos compuestos como detergentes. › Compuestos no iónicos.
- C12N1/00 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo.
- C12N1/06 C12N […] › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › Lisis de microorganismos.
- C12N1/14 C12N 1/00 […] › Microorganismos fúngicos (cultivo de setas A01G 18/00; como novedades vegetales A01H 15/00 ); Sus medios de cultivo.
- C12N1/16 C12N 1/00 […] › Levaduras; Sus medios de cultivo.
- C12N1/20 C12N 1/00 […] › Bacterias; Sus medios de cultivo.
- C12N15/10 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12P19/34 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Polinucleótidos, p. ej. ácidos nucleicos, oligorribonucleótidos.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
PDF original: ES-2531455_T3.pdf
Fragmento de la descripción:
Concentración y enriquecimiento de células microbianas y ácidos nucleicos microbianos a partir de fluidos corporales
Campo de la invención
Esta invención se refiere a la concentración y enriquecimiento de células microbianas y ácidos nucleicos microbianos a partir de muestras sanguíneas. La invención también se refiere a la detección de células microbianas en muestras sanguíneas.
Antecedentes de la invención
El desarrollo de ensayos diagnósticos moleculares rápidos para detectar infecciones humanas es la prioridad con mayor puntuación dentro de la Organización Mundial de la Salud para la mejora de la salud de la población mundial (Daar et al., 22, Nat. Genet., 32: 229-232). Las infecciones sanguíneas graves son una causa importante de mortalidad en pacientes hospitalizados en todo el mundo y suponen uno de los retos más importantes en cuidados intensivos. Por ejemplo, estimaciones recientes de la incidencia de sepsis son de 24 casos por 1. en los Estados Unidos. La carga humana y económica de la sepsis es considerable (Grossi et al., 26, Surg. Infect. (Larchmt), 7: S87-S91). A pesar de los avances en enfermedades infecciosas y el tratamiento de cuidados intensivos y de los numerosos intentos por desarrollar nuevos tratamientos, la tasa de mortalidad de la sepsis sigue siendo inaceptablemente alta, oscilando entre el 2% y el 5%. El reconocimiento de los signos de infección sanguínea severa y/o de sepsis severa y la realización de una diagnosis temprana y precisa de la misma son claves para mejorar los cuidados y aumentar la tasa de supervivencia. De hecho, un diagnóstico rápido podría aumentar la supervivencia de un paciente reduciendo el intervalo de tiempo entre la toma de muestra sanguínea y la aplicación de la terapia antimicrobiana.
Existe una necesidad de ensayos diagnósticos eficaces y precisos para determinar infecciones de fluidos corporales que i) recuperen células microbianas suficientes para su detección, ii) recuperen células microbianas de forma rápida, iii) recuperen una gran diversidad de especies microbianas, y iv) identifiquen patógenos de forma rápida y precisa. La presente invención busca satisfacer ésta y otras necesidades.
Durante varias décadas se han usado diferentes estrategias para tratar de satisfacer dichas necesidades. El estándar actual es un sistema de cultivo sanguíneo basado en un caldo de cultivo que favorece el crecimiento de los microorganismos presentes en una muestra de sangre, permitiéndoles multiplicarse hasta un nivel detectable (Cockerill et al., 1996, J. Clin. Microbiol., 34: 2-24; Murray et al., 1991, J. Clin. Microbiol., 29: 91-95). Sin embargo, dicha técnica implica el subcultivo posterior en medio sólido para el aislamiento e identificación de especies microbianas. Por consiguiente, se requieren varios días para obtener un diagnóstico preciso.
Las saponinas son glucósidos tensioactivos naturales que tienen propiedades superficiales. Son producidos principalmente por plantas pero también por animales marinos inferiores y algunas bacterias. Consisten en un resto azúcar ligado a una aglicona hidrofóbica (saponegina). La gran complejidad de la estructura de la saponina se debe a la variabilidad de la estructura de la aglicona, a la naturaleza de las cadenas laterales y a la posición de la unión de dichas funciones en la aglicona (Francis et al., 22, British J of Nutrition, 88: 587-65). Se sabe que las saponinas interaccionan con membranas de células eucarióticas. Las saponinas se usan habitualmente en concentraciones de ,4%-,2% para permeabilizar membranas plasmáticas. Dicha permeación puede conducir incluso a la destrucción de la membrana generando la muerte celular. Este proceso depende de la concentración aplicada y de la estructura molecular específica de la saponina usada (Melzig, et al. 21, Planta Med., 67: 43-48). Se ha demostrado que el sitio de unión a la membrana es un colesterol (Milgate et al.. 1995, Nutrition Research, 15, no. 8; 1223-1249). Una vez unidas al colesterol, las saponinas inducen cambios en la estructura de la membrana y en la permeabilidad asociadas a la alteración de la homeostasis iónica entre el compartimento intracelular y el extracelular. En levaduras, en la membrana en lugar de colesterol hay moléculas de ergosterol. Algunos estudios han demostrado que las saponinas esteroideas (saponinas neutras) preservan tanto la actividad hemolítica como la fúngica, mientras que las saponinas triterpenoides (saponinas ácidas) solo muestran actividad hemolítica sin actividad antifúngica detectable. Se ha sugerido que las saponinas triterpenoides pueden presentar una afinidad más débil por el ergosterol que el colesterol (Takechi et al. 23, Phytother. Res., 17: 83-85). Leconte et al. (Leconte et al. 1997, Phytochem., 44: 575- 579) demostraron que los cicloiridales, una clase de triterpenoides procedentes de varias especies de Iris, fueron capaces de estabilizar membranas de levadura tras un tratamiento de ruptura mediante saponinas esteroideas. Se han detectado saponinas triterpenoides en muchas legumbres tales como semillas de soja, judías, guisantes y alfalfa, así como en alliums, té, espinaca, remolacha azucarera, quinoa, regaliz, girasol, castaña de indias y ginseng. Un grupo ampliamente estudiado de saponinas triterpenoides es el producido a partir de Quillaja saponaria, un árbol nativo de la región de los Andes (Francis et al., 22, British J of Nutrition, 88: 587-65). Las saponinas representan el 2-25% del material extraíble de dicha fuente (Barr, et al., 1998, Ad Drug Deliv Rev, 32: 247-271). Las preparaciones de saponina disponibles comercialmente pueden inhibir el crecimiento bacteriano. Los contaminantes antibacterianos de bajo peso molecular pueden ser eliminados de las saponinas disponibles comercialmente
mediante purificación de los extractos por filtración (Dorn, G., Detoxification of saponins, Patente de EE.UU. ne 3.883.425, 1975).
Dorn et al. (Patente de EE.UU. 4.164.449) desarrollaron un método para lisar componentes sanguíneos con un mínimo de ,1 mg/mL y un máximo de 2 mg/mL de saponina purificada. Este método concentra células microbianas mediante centrifugación y las células recuperadas son inoculadas sobre una placa de agar. Un producto basado en este método se vende comercialmente como lsostat®/lsolator (anteriormente conocido como Isolator 1) y contiene 1,83 mg/mL de saponina purificada una vez mezclada con la muestra de sangre (Carter-Wallace, Inc., Cranbury, N.J. 8512-181). Este método permite la detección de bacteremia y fungemia de bajo nivel provocadas por Enterobacteriacae, Staphylococcus epidermidis y levaduras en entre 1 y 2 días (McLaughlin et al. 1983, J. Clin. Microbiol., 18: 127-131; Kiehn et al., 1983, J. Clin. Microbiol., 18: 3-34). El aumento de sensibilidad y el menor tiempo de detección pueden deberse a la concentración de células microbianas del volumen inicial de muestra sanguínea. Otra explicación para la mejor detección obtenida con el Isolator 1 puede estar relacionada con la liberación de microorganismos intracelulares después de la lisis de algunos leucocitos por tratamiento con saponina. (Taylor, 1994, Eur. J. Clin. Microbiol. Infect. Dis., 13: 249-252 ; Murray et al., 1991, J. Clin. Microbiol., 29: 91-95). Algunos fabricantes de sistemas de cultivo sanguíneo han suplementado sus medios de cultivo sanguíneo con saponina (Murray et al., 1991, J. Clin. Microbiol., 29: 91-95; sistema Becton Dickinson BACTEC; sistema bifásico Hoffman La Roche Septi-Chek).
Varios grupos compararon medios de cultivo sanguíneo suplementados con saponina (variando entre ,3 mg/mL y 2 mg/mL de saponina cuando se combina con una muestra sanguínea) o producto Isolator 1 (1,83 mg/mL de saponina cuando se combina con una muestra sanguínea) con los medios de cultivo sanguíneo estándar para detectar microorganismos en pacientes septicémicos. Estas referencias sugieren que la detección de microorganismos en un espécimen de sangre no puede basarse solo en un método que use saponina. De hecho, demostraron que el Isolator 1 no fue eficaz en la detección de la especie Pseudomonas en bacteremia de bajo nivel (Kiehn et al., 1983, J. Clin. Microbiol., 18: 3-34; Henry et al., 1983, J. Clin. Microbiol., 17: 864-869; Murray et al., 1991, J. Clin. Microbiol., 29: 91-95). Otro grupo obtuvo limitaciones similares para la detección de especies anaeróbicas (McLaughlin et al., 1983, J. Clin. Microbiol., 18:127-131).
Spears et al. (Publicación EPO n2.745.849) presentaron el uso de una saponina o Tritón en disolución salina para lisis sanguínea completa. Su método está dirigido a procesar especímenes sanguíneos con el objetivo de eliminar inhibidores de posteriores análisis de ácidos nucleicos. En este método, la muestra sanguínea es lisada mediante la adición... [Seguir leyendo]
Reivindicaciones:
1. Un método para aislar microorganismos de una muestra sanguínea que tiene o se sospecha que tiene microorganismos y células hospedantes, comprendiendo dicho método:
a. poner en contacto la muestra de sangre con una formulación de saponinas, donde la saponina es una disolución de saponina tratada en autoclave y filtrada (FATS) o una disolución de saponina tratada en autoclave, filtrada y calentada (HFATS) presente en una concentración final de 4 mg/mL a 1 mg/mL; y
b. obtener microorganismos aislados;
donde los microorganismos aislados comprenden ácidos nucleicos.
2. El método de la reivindicación 1, en el que los microorganismos aislados son viables y/o activos metabólicamente.
3. El método de la reivindicación 1 ó de la reivindicación 2, en el que la concentración final de saponina va de 75 mg/mL a 1 mg/mL.
4. El método de una cualquiera de las reivindicaciones 1 a 3, en el que dicha formulación de saponina ha sido filtrada para eliminar el material particulado fino superior a ,2 pm.
5. El método de una cualquiera de las reivindicaciones 1 a 4, en el que dicha formulación de saponina comprende una saponina seleccionada del grupo que consiste en saponina esteroidea, saponina triterpenoide y combinaciones de las mismas.
6. El método de una cualquiera de las reivindicaciones 1 a 5, en el que la formulación de saponina es una formulación de saponina triterpenoide.
7. El método de una cualquiera de las reivindicaciones 1 a 6, en el que dicha formulación de saponina es una disolución de saponina tratada en autoclave, filtrada y calentada (HFATS).
8. El método de una cualquiera de las reivindicaciones 1 a 7, en el que la muestra de sangre es sangre humana.
9. El método de una cualquiera de las reivindicaciones 1 a 8, en el que la obtención de microorganismos aislados comprende al menos una etapa de centrifugación y/o al menos una etapa de filtración.
1. El método de una cualquiera de las reivindicaciones 1 a 9, en el que dicho método proporciona el aislamiento de los microorganismos presentes en una concentración tan baja como de ,2 a 22 CFU por mL de muestra de sangre.
11. El método de una cualquiera de las reivindicaciones 1 a 1, que además comprende lisar los microorganismos aislados y aislar los ácidos nucleicos procedentes de los mismos.
12. El método de una cualquiera de las reivindicaciones 1 a 11, en el que los microorganismos aislados están sustancialmente libres de inhibidores de la amplificación.
13. El método de una cualquiera de las reivindicaciones 1 a 12, en el que los microorganismos son seleccionados del grupo que consiste en bacterias, levaduras, hongos y combinaciones de los mismos.
14. El método de la reivindicación 13, en el que los microorganismos son microorganismos que pueden causar una infección del torrente sanguíneo.
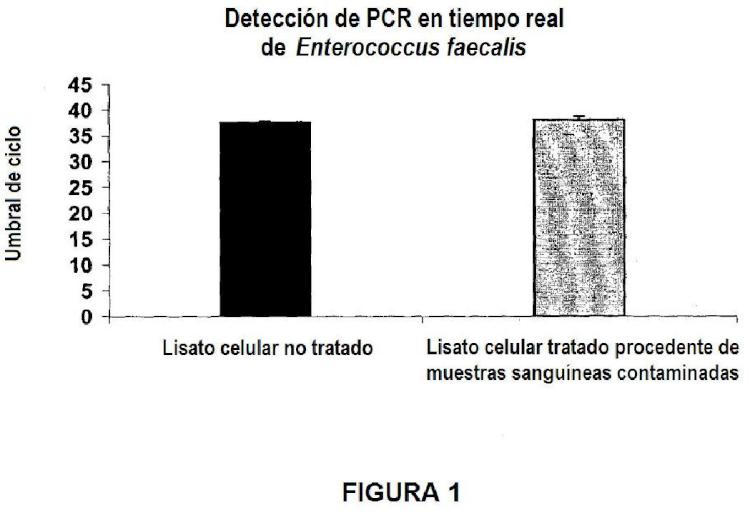
15. El método de una cualquiera de las reivindicaciones 1 a 12, en el que los microorganismos se seleccionan del grupo que consiste en Enterococcus faecalis, Enterococcus faecium , Escherichia coli, Haemophilus influenzae, Klebsiella oxytoca, Klebsiella pneumoniae, Proteus mirabilis, Pseudomonas aeruginosa, Serratia marcescens, Staphylococcus aureus, Staphylococcus epidermidis, Staphylococcus haemolyticus, Staphylococcus hominis, Staphylococcus warneri, Stenotrophomonas maltophilia, Streptococcus agalactiae, Streptococcus anginosus, Streptococcus dysgalactiae, Streptococcus mutans, Streptococcus pneumoniae, Streptococcus pyogenes, Streptococcus sanguinis, Candida albicans, Candida glabrata, Candida krusei, Candida parapsilosis, Candida tropicalis y Aspergillus fumigatus.
16. El método de una cualquiera de las reivindicaciones 1 a 15, que además comprende amplificar dichos ácidos nucleicos.
17. Un método para detectar microorganismos de una muestra sanguínea que tiene o se sospecha que tiene microorganismos y células hospedantes, comprendiendo dicho método:
a. poner en contacto una muestra de sangre con una formulación de saponina hasta una concentración final de saponina en el intervalo de 75 mg/mL a 1 mg/mL, donde dicha formulación de saponina es una disolución de saponina tratada en autoclave, filtrada y calentada (HFATS);
b. aislar microorganismos que tengan ácidos nucleicos usando al menos una etapa de centrifugación y/o al menos una etapa de filtración; y
c. determinar la presencia de microorganismos aislados que tengan ácidos nucleicos.
18. El método de la reivindicación 17, en el que la determinación de la presencia de microorganismos aislados comprende amplificar ácidos nucleicos procedentes de dicho(s) microorganismo^).
19. El método de la reivindicación 17 ó de la reivindicación 18, en el que dicha muestra de sangre es sangre humana.
2. Un método para diagnosticar una infección del torrente sanguíneo en un sujeto, que comprende detectar microorganismos según el método de una cualquiera de las reivindicaciones 17 a 19, en el que la presencia de microorganismos es indicativa de una infección asociada a dichos microorganismos.
21. Un método para obtener ácidos nucleicos de microorganismos presentes en una muestra de sangre, comprendiendo dicho método:
a. poner en contacto la muestra de sangre con una formulación de saponinas, donde la saponina es una disolución de saponina tratada en autoclave y filtrada (FATS) o una disolución de saponina tratada en autoclave, filtrada y calentada (HFATS) presente en una concentración final de 4 mg/mL a 1 mg/mL;
b. obtener microorganismos aislados que comprenden ácidos nucleicos; y
c. lisar los microorganismos aislados para obtener a partir de ellos ácidos nucleicos.
22. El método de la reivindicación 21, en el que la obtención de microorganismos aislados comprende al menos una etapa de centrifugación y/o al menos una etapa de filtración.
23. El método de la reivindicación 21 ó 22, que además comprende amplificar los ácidos nucleicos procedentes de dichos microorganismos con el propósito de identificación y/o diagnóstico.
Patentes similares o relacionadas:
Método para preparar una disolución acuosa que contiene medio de cultivo y agente quelante, del 22 de Julio de 2020, de Kyowa Kirin Co., Ltd: Método para preparar una disolución acuosa que presenta una filtrabilidad de membrana mejorada que comprende un medio de cultivo, en el que el medio de […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Formulación alimenticia a base de algas, productos de panadería, bollería y pastelería que la comprenden, método de obtención de la misma y su uso, del 10 de Junio de 2020, de JUAN Y JUAN INDUSTRIAL, S.L. UNIPERSONAL: Una formulación alimenticia caracterizada por que comprende microalgas frescas en forma de pasta de la especie Chlorella vulgaris, en una proporción comprendida entre el […]
Preparación de aceite microbiano que contiene ácidos grasos poliinsaturados, del 10 de Junio de 2020, de DSM IP ASSETS B.V.: Un aceite microbiano que comprende al menos el 50% de ácido araquidónico (ARA) basado en el aceite y que tiene un contenido en triglicéridos de al menos el 90%.
Microorganismo modificado para la producción optimizada de 2,4-dihidroxibutirato con eflujo de 2,4- dihidroxibutirato aumentado, del 27 de Mayo de 2020, de METABOLIC EXPLORER: Microorganismo Escherichia coli modificado genéticamente para producir 2,4-dihidroxibutirato por fermentación, en el que dicho microorganismo se […]
Cepas termoestables, productos y métodos de las mismas, del 29 de Abril de 2020, de Triphase Pharmaceuticals Pvt. Ltd: Un producto alimenticio que comprende un microorganismo termoestable de Lactobacillus, en donde el microorganismo termoestable se selecciona […]
Composición para inducir la proliferación o acumulación de células T reguladoras, del 29 de Abril de 2020, de The University of Tokyo: Composición para su uso en un método de tratamiento o prevención de una enfermedad infecciosa mediante la inducción de proliferación o acumulación […]
Métodos de cultivo semicontinuo repetido, del 5 de Febrero de 2020, de Mara Renewables Corporation: Un método de cultivo semicontinuo repetido de un microorganismo Thraustochytrid productor de aceite que comprende las etapas de: (a) proporcionar un recipiente que comprende […]