COMPOSICIÓN FARMACÉUTICA SÓLIDA DE RESINA DE INTERCAMBIO CATIÓNICO.
La presente invención se refiere a una composición farmacéutica sólida de resina de intercambio catiónico que permite la preparación de una suspensión estable de la resina en un vehículo acuoso,
y presenta una buena facilidad de resuspensión de la misma en el caso de la formación de un sedimento. Dicha composición comprende hidroxipropilmetilcelulosa y almidón pregelatinizado como excipientes funcionales. También se refiere a una forma sólida para la administración oral que la comprende, a la utilización de la misma para la preparación de formas sólidas orales, y a dicha composición para su uso en el tratamiento de la hiperpotasemia.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201231270.
Solicitante: LABORATORIOS RUBIO, S.A..
Nacionalidad solicitante: España.
Inventor/es: FABREGAS VIDAL,JOSE LUIS, GÓMEZ TOMÁS,Joaquín, RUIZ XIVILLÉ,Núria.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C08L25/06 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08L COMPOSICIONES DE COMPUESTOS MACROMOLECULARES (composiciones basadas en monómeros polimerizables C08F, C08G; pinturas, tintas, barnices, colorantes, pulimentos, adhesivos D01F; filamentos o fibras artificiales D06). › C08L 25/00 Composiciones de homopolímeros o copolímeros de compuestos que tienen uno o más radicales alifáticos insaturados, que tienen cada uno solamente un enlace doble carbono-carbono, y estando al menos uno terminado por un ciclo carbocíclico aromático; Composiciones de derivados de tales polímeros. › Poliestireno.
Fragmento de la descripción:
Composición farmacéutica sólida de resina de intercambio catiónico Campo de la técnica La presente invención está enmarcada en el ámbito del desarrollo de composiciones para el tratamiento de la hiperpotasemia que comprenden una resina de intercambio catiónico.
Estado de la técnica anterior
El potasio tiene múltiples funciones en el cuerpo: regula la actividad de los músculos de tejido liso, los músculos del corazón y los músculos esqueléticos, interviene en reacciones enzimáticas implicadas en la digestión y otros procesos metabólicos del cuerpo, y juega un papel en la homeostasis, el mecanismo utilizado por el cuerpo para mantener un equilibrio entre los muchos procesos eléctricos y químicos del cuerpo.
Casi todo el potasio en el cuerpo se encuentra en forma intracelular, mientras que sólo aproximadamente un 2% se encuentra en los líquidos extracelulares. Los análisis de sangre revelan los niveles de potasio extracelular y no son indicativos de la cantidad de potasio intracelular. El movimiento del potasio dentro o fuera de las células puede cambiar el nivel plasmático de potasio, si bien no hay cambio en la cantidad total de potasio en el cuerpo.
La hiperpotasemia o hipercalemia es un trastorno hidroelectrolítico que se define cuando el nivel elevado de potasio plasmático se encuentra por encima de aproximadamente 5, 5 mmol/l.
Las causas de la hiperpotasemia pueden ser debidas a un aumento del aporte de potasio, una redistribución del mismo, o una disminución de su excreción renal. Los síntomas asociados con la hiperpotasemia son generalmente inespecíficos e incluyen malestar general, palpitaciones y debilidad muscular. Niveles muy elevados de potasio constituyen una urgencia médica, ya que existe riesgo de arritmias cardíacas.
Los tratamientos de la hiperpotasemia incluyen, por ejemplo, las terapias con gluconato de calcio, glucosainsulina, bicarbonato sódico, diálisis, o resinas de intercambio catiónico.
La terapia con una resina de intercambio catiónico es la más recomendada para el control diario de potasio en una situación de hiperpotasemia fruto de una insuficiencia renal crónica. Dicha terapia implica la eliminación de potasio del cuerpo mediante el reemplazo en el tracto digestivo de los iones potasio por iones calcio o sodio procedentes de una resina de intercambio catiónico, generalmente una resina de poliestireno sulfonato.
En Europa, la dosis recomendada es de 15 g de poliestireno sulfonato cálcico hasta tres o cuatro veces al día. En los EE.UU., el producto comercializado es el poliestireno sulfonato sódico administrado según la misma posología. Sin embargo, en Japón y Corea, la dosis aceptada es de 5 g de resina hasta tres veces al día.
Habitualmente, la resina de poliestireno sulfonato se administra oralmente en forma de suspensión en agua. Debe tenerse en cuenta que la resina es un polvo prácticamente insoluble en agua, que tiene tendencia a sedimentar rápidamente. Además, dado que por razón de su dosis para que el tratamiento sea efectivo la resina debe tomarse en una gran cantidad, durante la ingestión de la misma el paciente tiene una sensación desagradable prolongada en la cavidad bucal. Esto se traduce en un bajo grado de cumplimiento de las indicaciones de la prescripción en lo que se refiere a la toma del medicamento según la pauta posológica recomendada.
Por tanto, la problemática de la terapia de la hiperpotasemia con resinas de intercambio catiónico reside principalmente en la dificultad de preparar una suspensión de la misma suficientemente estable, la dificultad de resuspender la resina en el caso de formación de un sedimento, y la mala palatabilidad debido a la repetida ingestión oral de una gran dosis de resina a lo largo del día (cada 8 horas) .
En el estado de la técnica se han descrito diferentes aproximaciones para abordar uno o más de los problemas mencionados.
En la solicitud de patente europea EP-A-0564154 se describen formulaciones en forma de suspensiones acuosas estables, que contienen una resina de intercambio iónico (que lleva incorporada una sustancia farmacéutica activa ligada en forma de resinato de la misma) , un agente espesante para aumentar la viscosidad, y un aminoácido que actúa como estabilizador de la dispersión.
En la solicitud de patente norteamericana US-A-2007/0248564 se describen suspensiones acuosas estables de poliestireno sulfonato sódico, listas para usar y destinadas al tratamiento de la hiperpotasemia, que comprenden silicato de aluminio y magnesio como agente suspensor y que están exentas de sorbitol.
La solicitud de patente internacional WO-A-2010/132662 se refiere a composiciones pulverulentas que comprenden al menos un 40% de un principio activo captador de potasio y que resultan apropiadas para el tratamiento de hiperpotasemia. En particular, se describen composiciones que contienen un principio activo captador de potasio, un agente suspensor, un agente deslizante, sorbitol y agua.
En la solicitud de patente europea EP-A-1004310 se describen composiciones acuosas gelificadas que comprenden una resina de intercambio iónico y uno o más agentes gelificantes.
También se describen composiciones gelificadas en la solicitud de patente europea EP-A-1031345. Dichas composiciones comprenden al menos un agente gelificante, agua y una resina de poliestireno sulfonato, que presenta un tamaño medio de partícula comprendido entre 5 y 100 μm. Las composiciones se deben mantener en condiciones refrigeradas para obtener la consistencia de gel, lo que dificulta el proceso de producción. En este documento también se describe la mejora del cumplimiento que se ha observado en algunos hospitales japoneses en los que se administra la resina en forma de preparación de gelatina. Sin embargo, también se indica que dichos preparados presentan una mala palatabilidad.
La solicitud de patente europea EP-A-0976408 se dirige a formulaciones para el tratamiento de la hiperpotasemia que contienen resinas de intercambio catiónico como ingrediente activo, carboximetilcelulosa sódica como agente gelificante e hidroxipropilcelulosa como agente aglutinante. Dichas formulaciones están en forma de polvo o gránulos que deben tomarse previa suspensión de las mismas en agua. En este documento se subrayan los problemas de mala palatabilidad de este tipo de fármacos, y se pretende preparar una nueva formulación que sea fácilmente dispersable en agua, que además dicha dispersión no forme agregados después de prepararla y que pueda resuspenderse con facilidad en caso de formarse un precipitado. La valoración de la palatabilidad de dichas composiciones se efectúa suspendiendo 3, 7 g, que corresponden a 3, 3 g de resina de intercambio catiónico, en 33 ml de agua, que corresponden a la posología empleada habitualmente en Japón. Estas composiciones presentan el inconveniente de una elevada viscosidad cuando se emplean en condiciones europeas (15 g de resina en 100 ml de agua) y que contienen iones sodio, lo que no resulta aconsejable en general, y tampoco para los enfermos de insuficiencia renal.
En el mercado norteamericano se encuentra también el producto SPS® Suspension que es una suspensión de la resina de poliestireno sulfonato sódico en sorbitol, un líquido de alta densidad que se utiliza para estabilizar la suspensión. Sin embargo, en Chaudhur y , et al., Am. J. Kidney Dis., 1997, 30 (1) , 120-122, se ha descrito que el uso concomitante de dicha resina y sorbitol puede producir necrosis intestinales.
Ninguna de las soluciones propuestas resuelve satisfactoriamente la problemática de la administración oral de resinas de intercambio iónico para el tratamiento de la hiperpotasemia.
Subsiste pues la necesidad de disponer de una composición para la administración oral de resinas de intercambio iónico que, una vez constituida, permita la formación de una suspensión estable de la misma, una resuspensión fácil en el caso de la formación de un sedimento, una palatabilidad mejorada y ausencia de iones sodio, a fin de conseguir cumplimiento por parte del paciente de la pauta posológica que se le prescribe.
Resumen de la invención El objeto de la presente invención es una composición farmacéutica sólida que comprende una resina de intercambio catiónico como principio activo.
Forma parte también del objeto de la invención dicha composición para su uso en el tratamiento de la hiperpotasemia.
Forma parte también del objeto de la invención la utilización de dicha composición para preparar formas sólidas de una resina de intercambio catiónico para su administración por vía oral.
También forma parte del objeto de la invención una forma sólida para administración por...
Reivindicaciones:
1. Composición farmacéutica sólida, caracterizada porque comprende una resina de intercambio catiónico, hidroxipropilmetilcelulosa y almidón pregelatinizado.
2. Composición según la reivindicación 1, caracterizada porque comprende además un agente saborizante y, opcionalmente, un sistema edulcorante.
3. Composición según la reivindicación 1 ó 2, caracterizada porque la resina se selecciona de entre el grupo formado por el poliestireno sulfonato cálcico y el poliestireno sulfonato sódico.
4. Composición según la reivindicación 3, caracterizada porque la resina es poliestireno sulfonato cálcico.
5. Composición según la reivindicación 3, caracterizada porque la resina es poliestireno sulfonato sódico.
6. Composición según cualquiera de las reivindicaciones 1 a 5, caracterizada porque el contenido de resina de intercambio catiónico está comprendido entre el 95, 0 % y el 99, 8 % en peso con respecto al peso total de la composición.
7. Composición según cualquiera de las reivindicaciones 1 a 6, caracterizada porque el contenido de hidroxipropilmetilcelulosa se encuentra comprendido entre el 0, 1% y el 2, 5% en peso con respecto al peso total de la composición.
8. Composición según cualquiera de las reivindicaciones 1 a 7, caracterizada porque el contenido de almidón pregelatinizado se encuentra comprendido entre el 0, 1% y el 2, 5% en peso con respecto al peso total de la composición.
9. Composición según la reivindicación 1, caracterizada porque comprende entre el 95, 0 % y el 97, 5% en peso de resina de intercambio catiónico, entre el 1, 25% y el 2, 5% en peso de HPMC, y entre el 1, 25% y el 2, 5% en peso de almidón pregelatinizado.
10. Composición según la reivindicación 2, caracterizada porque comprende entre el 0, 1% y el 1% en peso de un agente saborizante y entre el 0, 05% y el 0, 5% en peso de un sistema edulcorante.
11. Composición según cualquiera de las reivindicaciones 1 a 10 para su uso en el tratamiento de la hiperpotasemia.
12. Uso de la composición según cualquiera de las reivindicaciones 1 a 11 para la preparación de un medicamento para el tratamiento de la hiperpotasemia.
13. Uso según la reivindicación 12, en el que el medicamento se administra por vía oral.
14. Uso de la composición según cualquiera de las reivindicaciones 1 a 11 para preparar formas farmacéuticas sólidas de una resina de intercambio catiónico.
15. Forma sólida para administración por vía oral, caracterizada porque comprende una cantidad terapéuticamente efectiva de la composición según cualquiera de las reivindicaciones 1 a 11.
16. Forma sólida según la reivindicación 15, caracterizada porque se presentan en forma de dosis unitaria o en un envase a granel para su dosificación unitaria en el momento de la administración al paciente.
17. Forma sólida según la reivindicación 16, caracterizada porque la dosis unitaria se encuentra contenida en un envase en forma de sobre monodosis.
18. Forma sólida según la reivindicación 17, caracterizada porque comprende una cantidad de resina de intercambio catiónico comprendida entre 5 g y 20 g, una cantidad de HPMC comprendida entre 0, 08 g y 0, 33 g, y una cantidad de almidón pregelatinizado comprendida entre 0, 08 g y 0, 33 g.
19. Forma sólida según la reivindicación 18, caracterizada porque comprende 15 g de resina de intercambio catiónico, 0, 25 g de HPMC y 0, 25 g de almidón pregelatinizado.
20. Forma sólida según la reivindicación 19, caracterizada porque comprende además 0, 1 g de agente saborizante, y una combinación de 0, 02g de sucralosa y 0, 01g de neohesperidina DC como sistema edulcorante.
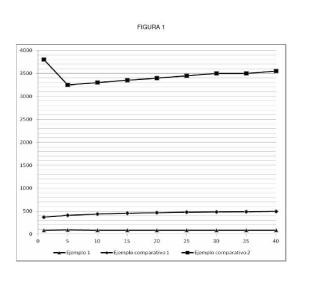
FIGURA 1 FIGURA 2 FIGURA 3 FIGURA 4
Patentes similares o relacionadas:
NANOPARTÍCULAS MULTIFUNCIONALES PARA TERAGNOSIS, del 30 de Julio de 2020, de UNIVERSIDAD DE GRANADA: Nanopartículas multifuncionales para teragnosis. La presente invención se refiere al campo de la medicina, en particular a nanopartículas (NP) […]
Aditivo para prevenir la separación de fases de aditivo de perfil bajo en composiciones de poliéster termoendurecido insaturado, del 8 de Abril de 2020, de LUBRIZOL ADVANCED MATERIALS, INC.: Una composición de moldeo de resina insaturada que comprende (a) un aditivo para evitar la separación de fases; (b) un polímero polimerizado […]
Método para reducir los efectos negativos de las impurezas adhesivas en los sistemas de materiales que contienen papel reciclable, del 1 de Abril de 2020, de Archroma IP GmbH: Método para reducir los efectos negativos de las impurezas adhesivas en el procesamiento de papel reciclable caracterizado porque comprende la adición de una […]
Recipiente con recubrimiento, del 18 de Diciembre de 2019, de Graphic Packaging International, LLC: Una pieza en bruto para formar un recipiente para almacenar un artículo, comprendiendo la pieza en bruto: una porción de pared y una porción de […]
Aditivos químicos para hacer biodegradables los materiales poliméricos, del 11 de Diciembre de 2019, de Bio-tec Environmental, LLC: Un aditivo biodegradable que aumenta la biodegradación del material polimérico cuando se añade a este, de manera que comprende: furanona como compuesto quimioatrayente; […]
Un método para preparar una composición que incluye posos de café, del 23 de Octubre de 2019, de Home Acrylic Inc: Un método para preparar un compuesto que incluye posos de café, el cualcomprende: deshidratar de un 20% a un 50% en peso de posos de café de modo que un contenido […]
NANOPARTÍCULAS MULTIFUNCIONALES PARA TERAGNOSIS, del 17 de Octubre de 2019, de UNIVERSIDAD DE GRANADA: NANOPARTÍCULAS MULTIFUNCIONALES PARA TERAGNOSIS La presente invención se refiere al campo de la medicina, en particular a nanopartículas (NP) funcionalizadas […]
Procesos para el reciclaje de desechos de poliestireno, del 4 de Septiembre de 2019, de Polystyvert Inc: Un proceso para el reciclaje de desechos de poliestireno, que comprende: la disolución de dichos desechos de poliestireno en p-cimeno […]