BIOMARCADOR DE CÉLULAS CARTILAGINOSAS HUMANAS.
Biomarcador de células cartilaginosas humanas.
La presente invención se refiere al uso de un biomarcador en la selección de células destinadas al trasplante,
en concreto, un biomarcador de células precursoras del cartílago que comprende al menos un producto de expresión del gen susd-2 y sus derivados.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201030791.
Solicitante: SERVICIO ANDALUZ DE SALUD.
Nacionalidad solicitante: España.
Inventor/es: ALAMINOS MINGORANCE,MIGUEL, CAMPOS MUÑOZ,Antonio, HERNANDEZ CORTES,Pedro, MORALES VILLAESCUSA,Alvaro.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K35/32 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Huesos; Osteocitos; Osteoblastos; Tendones; Tenocitos; Dientes; Odontoblastos; Cartílago; Condrocitos; Membrana sinovial.
- C12N5/077 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células mesenquimales, p. ej. Células óseas, células cartilaginosas, Células del estroma de la médula ósea, células adiposas o células musculares.
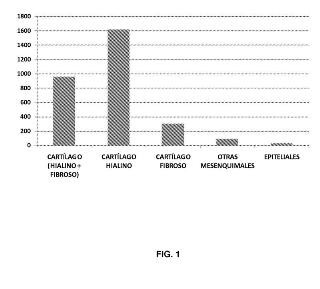
Fragmento de la descripción:
Biomarcador de células cartilaginosas humanas.
Campo de la técnica
La presente invención se encuadra en el campo de la biomedicina y, más específicamente, de la ingeniería tisular y medicina regenerativa. En concreto, la presente invención se refiere al uso de un biomarcador en la selección de células destinadas al trasplante.
Estado de la técnica anterior
El cartílago es un tejido conectivo especializado, el cual posee una matriz flexible firme que resiste a las tensiones mecánicas. Participa en el sostén del cuerpo, por estar íntimamente asociado al sistema esquelético. El cartílago posee células llamadas condrocitos, que ocupan cavidades pequeñas llamadas lagunas dentro de la matriz extracelular que secretan. La matriz extracelular del cartílago no está vascularizada ni inervada, y no posee vasos linfáticos; sin embargo, las células reciben su nutrición a partir de los vasos sanguíneos de los tejidos conectivos circundantes y del líquido sinovial por difusión a través de la matriz. La matriz extracelular está compuesta por glucosaminoglucanos y proteoglucanos, íntimamente asociados con fibras de colágeno y elásticas embebidas en la matriz (Deiters y Prehm, Arthritis Res Ther. 2008; 10(1):R8).
Según las fibras que se encuentren en la matriz extracelular, existen tres tipos de cartílago (Finn y Geneser, 3ª ed., 2000):
• Cartílago Hialino: La matriz extracelular es flexible y semitranslúcida, de color gris azuloso, rica en colágeno tipo II. Es el más frecuente del cuerpo. Se encuentra en nariz, laringe, extremos ventrales de las costillas (en los sitios en los que éstas conectan con el esternón), y en los anillos traqueales y bronquiales. Este cartílago forma el modelo cartilaginoso de muchos de los huesos durante el desarrollo embrionario, y constituye las placas epifisiarias de los huesos en crecimiento.
• Cartílago Elástico: El cartílago elástico se encuentra en orejas, conductos auditivos externo e interno, epiglotis y laringe (cartílago cuneiforme). En casi todos los aspectos, el cartílago elástico es idéntico al cartílago hialino, y frecuentemente se relaciona con él. La capa fibrosa externa de pericondrio (tejido conectivo denso irregular, encargado del crecimiento y la regeneración del cartílago) es rica en fibras elásticas. La matriz del cartílago elástico posee abundantes fibras elásticas ramificadas que varían entre finas y gruesas, interpuestas con haces de fibras colágenos de tipo II, aportando mayor flexibilidad que la matriz del cartílago hialino. Los condrocitos del cartílago elástico son más abundantes y de mayor tamaño que los del cartílago hialino.
• Fibrocartílago: Se encuentra en discos intervertebrales, sínfisis del pubis y discos articulares, e insertado en el hueso. Se encuentra asociado con cartílago hialino y con tejido conectivo denso. A diferencia de los otros dos tipos de cartílago, el fibrocartílago no posee pericondrio, tiene una cantidad escasa de matriz extracelular rica en condroitín sulfato y dermatán sulfato y presenta haces de colágeno tipo II. Los condrocitos suelen encontrase alineados en filas paralelas alternativas con los haces gruesos de colágeno.
Numerosas patologías pueden afectar al cartílago humano, siendo muy frecuentes las enfermedades de origen autoinmune, infeccioso, traumático o degenerativo, destacando por su elevada frecuencia la artrosis, la artritis y las úlceras de la superficie articular. Todas estas enfermedades presentan una altísima incidencia y suponen un gran gasto sanitario en nuestro medio.
Los tratamientos convencionales para la reparación del cartílago articular incluyen microfracturas, mosaicoplastias, y el uso de autoinjertos y trasplantes heterólogos. El trasplante autólogo de condrocitos ha surgido como una alternativa al tratamiento clínico convencional de los defectos cartilaginosos, siendo posible en muchos casos reducir el dolor y mejorar la función articular del paciente mediante el implante autólogo de condrocitos. Hasta el momento, la investigación en este campo se basa en el cultivo de condrocitos para su aplicación clínica como células en suspensión (ACI, autologous chondrocyte implant) o, más recientemente, para su cultivo sobre membranas biocompatibles, aplicándose al paciente como una membrana sobre la cual se cultiva una monocapa de células cartilaginosas (MACI, membrane autologous chondrocyte implant). Sin embargo no existe un tejido artificial óptimo para el crecimiento de dichos condrocitos.
Desde 1987, múltiples investigadores han desarrollado protocolos de cultivo e implante clínico de condrocitos cultivados en laboratorio en más de 12.000 pacientes (Marlovits et al., Eur J Radiol. 2006, 57(1):24-31), siendo los resultados muy variables de un estudio a otro. Mientras algunos ensayos sugieren que el uso de estas técnicas puede resolver los problemas articulares de forma muy efectiva, la mayoría de los estudios, incluyendo metaanálisis y trabajos de revisión, demuestran que la utilidad del implante autólogo de condrocitos es muy limitada. Probablemente, esto se deba a la baja densidad del tejido cartilaginoso formado o la insuficiente cantidad y calidad de las células implantadas en el paciente. En general, el cartílago generado tras el implante autólogo de condrocitos es rico en colágeno tipo I, con características bioquímicas y biomecánicas deficientes y muy distintas de las existentes en el cartílago nativo, rico en colágeno tipo II (Tuli et al., Arthritis Res Ther. 2003, 5(5):235-238). Este hecho podría deberse, con elevada probabilidad, a que las células utilizadas para la terapia celular del cartílago podrían presentar bajos índices de viabilidad celular o bien por el uso de células diferentes a condrocitos bien diferenciados y funcionales.
Numerosos investigadores han demostrado que las células adultas humanas tienden a desdiferenciarse y a perder funcionalidad cuando se mantienen en cultivo durante tiempos prolongados (Rodríguez-Morata et al., Ann Vasc Surg. 2008, 22(3):440-448; Alaminos et al., J Cell Physiol. 2007, 211(3):692-698). Del mismo modo, es muy frecuente encontrar células mesenquimales o conectivas contaminantes de los cultivos de condrocitos, especialmente los fibroblastos procedentes del pericondrio. Por ese motivo, es importante desarrollar métodos que permitan controlar los niveles de diferenciación de las células cultivadas para asegurar el uso de células bien diferenciadas en la terapia celular del cartílago y evitar el uso de células contaminantes. A pesar de ello, hasta la fecha no se han descrito marcadores suficientemente específicos de los condrocitos humanos, utilizándose hasta el momento criterios puramente morfológicos junto con la expresión de colágeno II o agrecán, compuestos existentes en la matriz extracelular del cartílago hialino maduro.
El gen sushi domain containing protein-2 (susd-2; número de acceso genbank AK026431), está conservado en mamíferos (chimpancé, perro, vaca, ratón, rata) aves (pollo) peces (pez cebra) e invertebrados (mosca de la fruta, mosquito y C. elegans). En humanos, el gen susd-2 está localizado en el cromosoma 22q11-q12. La expresión de SUSD2 no ha sido determinada hasta la fecha en células del cartílago humano o animal. La predicción de los niveles de expresión se puede llevar a cabo utilizando programas informáticos como e-Northern (Northern-Blot virtual), el cual indica que los niveles de ARNm podrían ser elevados en riñón y pulmón, pero no en cartílago (Gene-Cards, http://www.genecards.org/cgi-bin/carddisp.pl?gene=SUSD2&search=SUSD2).
Para asegurar el éxito de la terapia celular con condrocitos autólogos, sería necesario contar con un marcador específico del condrocito humano que se exprese en la superficie o en el citoplasma de las células mantenidas en cultivo. Además, el campo de la técnica carece de una plataforma biocompatible que provea las condiciones óptimas para la regeneración del tejido cartilaginoso.
Explicación de la invención
La presente invención provee un nuevo biomarcador de condrocitos en cultivo que permite la identificación específica de las células de linaje cartilaginoso frente a otras células de estirpe mesenquimal o conectiva presentes en el cultivo. El uso del biomarcador de la presente invención junto con una plataforma de crecimiento específica para condrocitos optimiza la regeneración del tejido cartilaginoso.
Los inventores de la presente solicitud han descubierto que, sorprendentemente,...
Reivindicaciones:
1. Biomarcador de células precursoras del cartílago caracterizado porque comprende al menos un producto de expresión del gen susd-2.
2. Biomarcador según la reivindicación 1 caracterizado porque comprende la SEQ ID No 1.
3. Biomarcador según la reivindicación 1 caracterizado porque comprende la SEQ ID No 2.
4. Uso de un biomarcador según cualquiera de las reivindicaciones 1 a 3, en la selección de células in vitro destinadas al transplante.
5. Uso según la reivindicación 4 en la selección de células in vitro para la preparación de un implante celular.
6. Uso según la reivindicación 4 en la selección de células in vitro para la preparación de un tejido artificial.
Patentes similares o relacionadas:
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en osteoblastos, del 22 de Enero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en osteoblastos, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava […]
Métodos y composiciones para la condrogénesis in vitro e in vivo, del 18 de Diciembre de 2019, de Lineage Cell Therapeutics, Inc: Una composición que comprende una línea celular progenitora embrionaria clonal para su uso en un método in vivo de generación de cartílago, comprendiendo la composición: […]
Composición para el tratamiento de lesiones tisulares, del 11 de Septiembre de 2019, de Organes Tissus Régénération Réparation Remplacement: Composición farmacéutica o dermatológica para su aplicación como medicamento para el tratamiento de lesiones tisulares elegidas entre lesiones del sistema locomotor, lesiones […]
 Armazones de colágeno estabilizados y esterilizados con aditivos activos unidos, del 31 de Julio de 2019, de Synovis Orthopedic and Woundcare, Inc: Un proceso para fabricar un bioimplante esterilizado químicamente que comprende un tejido biológico y heparina, en el que la heparina se conjuga covalentemente […]
Armazones de colágeno estabilizados y esterilizados con aditivos activos unidos, del 31 de Julio de 2019, de Synovis Orthopedic and Woundcare, Inc: Un proceso para fabricar un bioimplante esterilizado químicamente que comprende un tejido biológico y heparina, en el que la heparina se conjuga covalentemente […]
Aparato para el procesamiento de dientes en material óseo, del 12 de Junio de 2019, de TT Tooth Transformer S.r.l: Aparato para procesar dientes en material óseo que comprende un dispositivo reactor , adecuado para tratar dichos dientes por inmersión en líquidos, dicho dispositivo […]
Aparato y método de producción de un implante óseo dental, del 22 de Mayo de 2019, de Kometabio Inc: Un método de producción de un auto implante óseo, que comprende: proporcionar uno o más dientes ; convertir dicho uno o más dientes, en […]
Células STRO-1brillantes para su uso en el tratamiento de enfermedades de tejidos conectivos, del 14 de Marzo de 2019, de Mesoblast, Inc: Células precursoras mesenquimales (MPC) que son células multipotenciales STRO-1brillantes para usar en el tratamiento o la prevención de una enfermedad derivada de la […]
Firma molecular de manchas cutáneas pigmentarias, asociada con la organización de la matriz extracelular, del 6 de Febrero de 2019, de L'OREAL: Método de caracterización de una mancha pigmentaria cutánea aparente o sospechosa en un ser humano, que comprende comparar los niveles de expresión, en […]