Anticuerpos neutralizantes del factor estimulante de colonias de granulocitos y macrófagos humano.
Un anticuerpo monoclonal humano o fragmento del mismo que comprende
(a) una región variable de la cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO:
19 y que además comprende una región variable de la cadena pesada seleccionada de:
(i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 21;
(ii) una secuencia de aminoácidos como se muestra en SEQ ID NO: 22;
(iii) una secuencia de aminoácidos como se muestra en SEQ ID NO: 52; y
(iv) una secuencia de aminoácidos como se muestra en SEQ ID NO: 53;
o
(b) una región variable de la cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 54 y que además comprende una región variable de la cadena pesada seleccionada de:
(i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 23;
(ii) una secuencia de aminoácidos como se muestra en SEQ ID NO: 26; y
(iii) una secuencia de aminoácidos como se muestra en SEQ ID NO: 28;
o
(c) una región variable de la cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 55 y que además comprende una región variable de la cadena pesada seleccionada de:
(i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 21; y
(ii) una secuencia de aminoácidos como se muestra en SEQ ID NO: 22;
o
(d) una cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 34 y que además comprende una cadena pesada seleccionada de:
(i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 35;
(ii) una secuencia de aminoácidos como se muestra en SEQ ID NO: 37;
(iii) una secuencia de aminoácidos como se muestra en SEQ ID NO: 40;
(iv) una secuencia de aminoácidos como se muestra en SEQ ID NO: 42; y
(v) una secuencia de aminoácidos como se muestra en SEQ ID NO: 48.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/003528.
Solicitante: Amgen Research (Munich) GmbH .
Nacionalidad solicitante: Alemania.
Dirección: STAFFELSEESTRASSE 2 81477 MUNCHEN ALEMANIA.
Inventor/es: WOLF, ANDREAS, RAUM, TOBIAS, HEPP, VIESER,EVA, PETSCH,SILKE, ZEMAN,STEVEN, BRUCKMAIER,SANDRA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra citoquinas, linfoquinas o interferones.
PDF original: ES-2545769_T3.pdf
Fragmento de la descripción:
Anticuerpos neutralizantes del factor estimulante de colonias de granulocltos y macrófagos humano
La presente Invención se refiere a anticuerpos y fragmentos de los mismos que neutralizan la actividad del factor estimulante de colonias de granulocltos macrófagos (GM-CSF) humano como se define en las reivindicaciones. La Invención se refiere además a composiciones farmacéuticas que comprenden tales anticuerpos y fragmentos de los mismos así como a tales anticuerpos y fragmentos de los mismos para su uso en un método de tratamiento de enfermedades Inflamatorias o de una enfermedad tumoral u otra afección con apoptosls celular retrasada, supervivencia o proliferación celular aumentada.
Originalmente descrito como un estímulo potente del crecimiento y la diferenciación de células precursoras de granulocltos y macrófagos /n v/fro, el factor estimulante de colonias de granulocltos-macrófagos (GM-CSF) es una glucoproteína de aproximadamente 23 kDa con una estructura de haz de cuatro hélices alfa que se une a un receptor heterodlmérlco compuesto de subunldades que pertenecen a la familia de receptores de cltoqulnas de tipo 1. Estimula la maduración de entre otros macrófagos, neutrófllos, granulocltos, eoslnófllos y células dendrítlcas presentadoras de antígenos, para aumentar su capacidad funcional en combatir Infecciones. Los experimentos de eliminación genética, es decir, experimentos de silenciar o eliminar el gen de Interés - aquí GM-CSF - en ratones Indicaron que GM-CSF es esencial para mantener la actividad funcional de algunas poblaciones de macrófagos tal como los Implicados en depurar el surfactante en el pulmón y en responder a ciertos tipos de Infección o respuestas ¡nmunltarlas.
Mientras que GM-CSF tienen potentes actividades estimuladoras /n v/fro sobre células progenltoras para neutrófllos, eoslnófllos, macrófagos, y en un menor grado células erltroldes y megacarlocítlcas, los resultados obtenidos /n v/vo con ratones con eliminación del gen sugieren que el principal papel fisiológico de GM-CSF es mantener o estimular la actividad funcional de macrófagos y granulocltos maduros y estimular la presentación de antígenos al sistema ¡nmunltarlo. Flace lo último mediante sus efectos directos sobre la producción de células dendrítlcas y macrófagos, pero también aumentando la expresión del complejo mayor de hlstocompatlbllldad de clase II y receptores Fe en macrófagos y células dendrítlcas.
GM-CSF estimula las actividades funcionales de neutrófllos, eoslnófllos y monocltos-macrófagos. Estas Incluyen aumento de la actividad qulmlotáctlca, expresión aumentada de moléculas de adhesión celular y adhesión aumentada a superficies, y actividad fagocítlca aumentada así como Inhibición y retraso de apoptosls de estas células. Los neutrófllos representan la primera línea de defensa contra agresiones. La muerte programada de neutrófllos se retrasa por estímulos prolnflamatorlos Incluyendo GM-CSF para asegurar una resolución apropiada de la Inflamación en tiempo y lugar. GM-CSF también estimula la capacidad de estas células de mediar la cltotoxlcldad celular dependiente de anticuerpos y destruir microorganismos ¡ntracelularmente y tiene un efecto de sensibilización' sobre estas células para aumentar su respuesta a estímulos posteriores para el estallido oxldatlvo (producción de anión superóxldo), desgranulación y liberación de agentes antlmlcroblanos, y qulmlotaxla. Además, GM-CSF estimula la liberación de cltoqulnas y mediadores secundarlos de estas células Incluyendo IL-1, G-CSF, M- CSF y leucotrlenos de neutrófllos, así como IL-1, TNF, IL-6, G-CSF, M-CSF, y prostaglandlnas de macrófagos.
Está claro de lo anterior que GM-CSF desempeña un papel en activar y mantener las poblaciones celulares necesarias para rechazar la Infección. Sin embargo, en algunos casos la activación de estas poblaciones celulares puede ser Indeseable. Por ejemplo, la activación de las líneas celulares anteriores cuando no hay patógeno presente produce en muchos casos afecciones Inflamatorias agudas y/o crónicas que, en casos extremos, pueden ser potenclalmente mortales. De forma similar, la sobreexpresión de GM-CSF puede producir activación Inmunltarla excesiva, lo que produce Inflamación. En tales casos, puede ser deseable neutralizar la actividad de GM-CSF de modo que los síntomas de estas afecciones Inflamatorias se eliminen o al menos se mitiguen.
En el estado de la técnica existen ejemplos de tal actividad neutralizante. El documento WO 03/068924 describe anticuerpos monoclonales que se unen a y neutralizan GM-SCF humano. Kanakura et al. (1991), Blood, Voi. 77, No. 5, pp. 1033-1043, los documentos EP 344957 y EP 265384 describen anticuerpos monoclonales contra GM-CSF. Se describen anticuerpos adicionales contra GM-CSF en Oggero et al. (2004), Molecular Dlverslty, Voi. 8, No. 3, pp. 257-269.
Por ejemplo, se encontró que un anticuerpo neutralizante antl-GM-CSF contribuía a un aumento en la tasa de apoptosls de eoslnófilos en muestras de sangre periférica (Kankaanranta et al. (2000) Journal of Allergy and Clínica! Immunology 106, 77-83). Como la supervivencia aumentada de eoslnófllos se correlaciona con asma, se esperaría que un aumento en la apoptosls de eoslnófilos mitigara los síntomas asmáticos.
En enfermedades Inflamatorias crónicas tal como asma, artritis reumatolde, y esclerosis múltiple, los niveles de GM- CSF aumentan localmente y en algunos casos sistèmicamente y se han correlacionado con el proceso Inflamatorio en estas enfermedades.
Por tanto es un fin de la invención mejorar en los modos de neutralizar actividad de GM-CSF aumentada y/o ¡ndeseada previamente conocidos en el estado de la técnica.
Según esto, un aspecto de la invención se refiere a un anticuerpo monoclonal humano o fragmento del mismo que se une específicamente a y neutraliza GM-CSF de primates, dicho anticuerpo o fragmento se describe en el presente documento.
El término "se une específicamente" o expresiones relacionadas tal como "unión específica", "unirse específicamente", "unidor específico", etc., como se usan en el presente documento se refieren a la capacidad del anticuerpo monoclonal humano o fragmento del mismo de distinguir entre GM-CSF de primates y cualquier número de otros antígenos potenciales diferentes de GM-CSF de primates a tal nivel que, de un grupo de una pluralidad de diferentes antígenos como potenciales compañeros de unión, solo GM-CSF de primate se une, o se une significativamente. En el significado de la invención, GM-CSF de primate se une "significativamente" cuando, de entre un grupo de una pluralidad de antígenos diferentes igualmente accesibles como potenciales compañeros de unión, GM-CSF de primate se une al menos 10 veces, preferiblemente 50 veces, lo más preferiblemente 100 veces o mayor más frecuentemente (en un sentido cinético) que cualquier otro antígeno diferente de GM-CSF de primate. Tales medidas cinéticas se pueden realizar en un aparato Biacore.
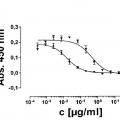
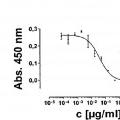
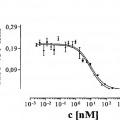
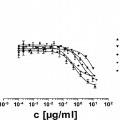
Como se usa en el presente documento, "neutralización", "neutralizar", "neutralizante" y variantes gramaticalmente relacionadas de los mismos se refieren a la atenuación parcial o completa del/de los efecto(s) biológico(s) de GM- CSF. Tal atenuación parcial o completa del/de los efecto(s) biológico(s) de GM-CSF resulta de modificación, interrupción y/o eliminación de la transducción de señales mediada por GM-CSF, manifestada, por ejemplo, en señalización intracelular, proliferación celular o liberación de sustancias solubles, aumento o disminución de activación génica intracelular, por ejemplo esa que produce la expresión de receptores de superficie para ligandos diferentes de GM-CSF. Como entiende un experto en la materia, existen múltiples modos de determinar si un agente, por ejemplo, un anticuerpo en cuestión o fragmento del mismo se va a clasificar como neutralizados Como un ejemplo, esto se puede lograr por un ensayo ¡n vitro estándar realizado generalmente como sigue: en un primer experimento de proliferación, una línea celular, cuyo grado de proliferación se sabe que depende de la actividad de GM-CSF, se incuba en una serle de muestras con concentraciones variables de GM-CSF, después de la incubación se mide el grado de proliferación de la línea celular. De esta medida, se determina la concentración de GM-CSF que permite una proliferación semlmáxlma de las células. Un segundo experimento de proliferación se realiza después empleando en cada una de una serie de muestras el mismo número de células usadas en el primer experimento de proliferación, la concentración anteriormente determinada de GM-CSF y, esta vez, concentraciones variables de un anticuerpo o fragmento del mismo que se sospecha que es un neutralizador de GM-CSF.... [Seguir leyendo]
Reivindicaciones:
Un anticuerpo monoclonal humano o fragmento del mismo que comprende
(a) una región variable de la cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 19 y que además comprende una región variable de la cadena pesada seleccionada de:
(I) una secuencia de aminoácidos como se muestra en SEQ ID NO: 21;
(¡I) una secuencia de aminoácidos como se muestra en SEQ ID NO: 22;
(¡II) una secuencia de aminoácidos como se muestra en SEQ ID NO: 52; y
(¡v) una secuencia de aminoácidos como se muestra en SEQ ID NO: 53;
o
(b) una reglón variable de la cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 54 y que además comprende una reglón variable de la cadena pesada seleccionada de:
(i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 23;
(¡i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 26; y
(¡II) una secuencia de aminoácidos como se muestra en SEQ ID NO: 28;
o
(c) una reglón variable de la cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 55 y que además comprende una reglón variable de la cadena pesada seleccionada de:
(I) una secuencia de aminoácidos como se muestra en SEQ ID NO: 21; y
(¡i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 22;
o
(d) una cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 34 y que además comprende una cadena pesada seleccionada de:
(i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 35;
(¡i) una secuencia de aminoácidos como se muestra en SEQ ID NO: 37;
(i¡¡) una secuencia de aminoácidos como se muestra en SEQ ID NO: 40;
(¡v) una secuencia de aminoácidos como se muestra en SEQ ID NO: 42; y
(v) una secuencia de aminoácidos como se muestra en SEQ ID NO: 48.
El anticuerpo monoclonal humano o fragmento del mismo según la reivindicación 1, que comprende una reglón variable de la cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 19 y que comprende además una reglón variable de la cadena pesada seleccionada de una secuencia de aminoácidos como se muestra en SEQ ID NO: 21 y 52.
El anticuerpo monoclonal humano o fragmento del mismo según la reivindicación 1, que comprende una cadena ligera que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 34 y que comprende una cadena pesada que comprende una secuencia de aminoácidos como se muestra en SEQ ID NO: 35.
El fragmento de anticuerpo monoclonal humano según cualquiera de las reivindicaciones 1 a 3, en donde dicho fragmento es un scFv, un Fv, un dlacuerpo, un diacuerpo en tándem, un Fab, un Fab' o un F(ab)2.
Una molécula de polinucleótido que tiene una secuencia de nucleótidos que codifica un anticuerpo monoclonal humano o fragmento del mismo como se muestra en cualquiera de las reivindicaciones 1-3.
Una composición farmacéutica que comprende un anticuerpo monoclonal humano o fragmento del mismo según cualquiera de las reivindicaciones 1-4 o la molécula de polinucleótido según la reivindicación 5.
Un anticuerpo monoclonal humano o fragmento del mismo según cualquiera de las reivindicaciones 1-4 o molécula de polinucleótldos según la reivindicación 5 que opcionalmente comprende uno o más agentes antiinflamatorlos adicionales, para su uso en un método de tratamiento de enfermedades Inflamatorias.
El anticuerpo monoclonal humano o fragmento del mismo o la molécula de polinucleótido para uso de la reivindicación 7, en donde dichas enfermedades Inflamatorias se eligen del grupo que consiste en artritis reumatolde (AR) (Incluyendo AR que es resistente a tratamiento con neutralizadores de TNF-alfa), asma,
esclerosis múltiple (EM), enfermedad pulmonar obstructiva crónica (EPOC), síndrome de dificultad respiratoria aguda (SDRA), flbrosls pulmonar Idiopàtica (FPI), enfermedad Intestinal Inflamatoria (Eli), uveítls, degeneración macular, colitis, psoriasis, degeneración wallerlana, síndrome antlfosfolípldo (SAF), síndrome coronarlo agudo, restenosls, ateroesclerosls, pollcondrltls recidivante (PR), hepatitis aguda o crónica, 5 Implantes ortopédicos fallidos, glomerulonefrltls, lupus o trastornos autolnmunltarlos.
9. Un anticuerpo monoclonal humano o fragmento del mismo según cualquiera de las reivindicaciones 1-4 o molécula de pollnucleótldo según la reivindicación 5, que opclonalmente comprende uno o más agentes anticancerosos adicionales, para su uso en un método de tratamiento de una enfermedad tumoral u otra
10 afección con apoptosls celular retrasada, supervivencia o proliferación celular aumentada.
10. El anticuerpo monoclonal humano o fragmento del mismo o la molécula de pollnucleótldo para uso de la reivindicación 9, en donde dicha enfermedad tumoral es un cáncer.
15 11. El anticuerpo monoclonal humano o fragmento del mismo o la molécula de pollnucleótldo para uso de la
reivindicación 10, en donde dicho cáncer es leucemia, mleloma múltiple, carcinoma gástrico o carcinoma de piel.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]
Anticuerpos del OPGL, del 15 de Julio de 2020, de AMGEN FREMONT INC.: Un anticuerpo, que comprende una cadena pesada y una cadena ligera, donde: a) la cadena pesada comprende: 1) una secuencia de aminoácidos recogida […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
Uso de reslizumab para tratar el asma eosinofílica moderada a grave, del 24 de Junio de 2020, de CEPHALON, INC.: Reslizumab para su uso en el tratamiento del asma eosinofílica, en donde: se proporcionan 3 mg/kg de reslizumab por vía intravenosa una […]
Anticuerpos anti-IL-23 humanos, composiciones, procedimientos y usos, del 17 de Junio de 2020, de Janssen Biotech, Inc: un anticuerpo para IL-23p19 aislado, en donde dicho anticuerpo se genera completamente humano a partir de expresión de fagos y se une a […]
Aislamiento y purificación de anticuerpos anti-IL-13 usando cromatografía de afinidad a Proteína A, del 27 de Mayo de 2020, de AbbVie Inc: Un método para producir una preparación de anticuerpo anti-IL-13 reducido en proteínas de célula hospedadora (reducido en HCP) a partir de una mezcla […]
Anticuerpos ANTI-IL-33 y usos de los mismos, del 29 de Abril de 2020, de REGENERON PHARMACEUTICALS, INC.: Un anticuerpo monoclonal humano o fragmento de unión al antígeno del mismo para usar en un método de tratamiento del asma crónica en un paciente que lo necesita, […]