PÉPTIDOS ÚTILES EN EL TRATAMIENTO Y/O CUIDADO DE LA PIEL Y/O MUCOSAS Y SU USO EN COMPOSICIONES COSMÉTICAS O FARMACÉUTICAS.
Péptidos de fórmula general (I):
****IMAGEN****
sus estereoisómeros,
mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, un procedimiento de preparación, composiciones cosméticas o farmacéuticas que los contienen y su uso para el tratamiento y/o cuidado de condiciones, desórdenes y/o enfermedades de la piel y/o mucosas.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201130441.
Solicitante: LIPOTEC, S.A..
Nacionalidad solicitante: España.
Inventor/es: GARCIA ANTON,JOSE MARIA, FERRER MONTIEL,ANTONIO VICENTE, ALMIÑANA DOMENECH,NURIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/08 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen de 5 a 11 aminoácidos.
- C07K7/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 5 a 11 aminoácidos.
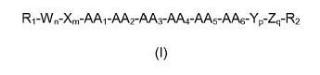
Fragmento de la descripción:
Péptidos útiles en el tratamiento y/o cuidado de la piel y/o mucosas y su uso en composiciones cosméticas o farmacéuticas
CAMPO DE LA INVENCIÓN
La presente invención se refiere a péptidos capaces de modular aquaporina-3 (AQP-3) y/o estimular la síntesis de colágeno en la piel y/o mucosas y a composiciones cosméticas o farmacéuticas que contienen dichos péptidos de utilidad en el tratamiento y/o cuidado de la piel y/o mucosas, preferentemente para el tratamiento y/o cuidado de aquellas condiciones, desórdenes y/o patologías de la piel y/o mucosas que mejoran o son prevenidas por la modulación de AQP-3 y/o la estimulación de la síntesis de colágeno.
ANTECEDENTES DE LA INVENCIÓN
La epidermis es la capa más externa de la piel. Sus células se diferencian para dar lugar a una barrera mecánica impermeable al agua, fundamental para permitir la vida terrestre. Por su localización, la epidermis sufre contactos con el exterior más frecuentes, más directos, y más dañinos que cualquier otro tejido en el cuerpo, por lo que su organización depende de los mecanismos de reparación y renovación disponibles.
La epidermis presenta una organización estratificada con tres capas o estratos principales (estrato basal, estrato granular y estrato córneo) , y se debe al estrecho equilibrio existente entre proliferación y diferenciación de queratinocitos. Cuando las células de la capa basal entran en diferenciación pierden su capacidad proliferativa y se mueven progresivamente hacia el estrato córneo. El estrato basal está compuesto por queratinocitos, y su actividad característica es la síntesis de queratina, una proteína que forma filamentos intermedios y que es la responsable de dar a la epidermis su dureza. Sobre esta capa se encuentran varias capas de células espinosas y encima de éstas se situa la capa de células granulares. El estrato de células granulares es fundamental para el mantenimiento de la impermeabilidad de la epidermis, que es su función más importante. El estrato de células granulares, además, marca el límite entre células metabólicamente activas y células muertas, muerte resultante de la pérdida progresiva de orgánulos y del llenado de sus citoplasmas con queratina según avanzan hacia el exterior, quedando las células reducidas a escamas planas completamente llenas de queratina densamente empaquetada. Estas células muertas se desprenden de la superficie de la piel aproximadamente una semana después de emerger de la capa basal. Esta particular organización del estrato córneo sirve para proteger la piel, y a su vez le permite mantener un cierto grado de flexibilidad reteniendo una cantidad de agua definida. La hidratación del estrato córneo es fundamental para determinar el aspecto, metabolismo, propiedades mecánicas, y la función de barrera de la piel.
El envejecimiento de la piel es un proceso complejo que comprende a su vez dos procesos diferenciados, envejecimiento intrínseco y envejecimiento extrínseco. El primero es debido a factores genéticos, y no sólo afecta a la piel sino a todos los órganos del cuerpo. El envejecimiento extrínseco es causado por factores ambientales, como la exposición a la contaminación, al humo de tabaco, a radiación ultravioleta, al viento, al clima frío… Ambos procesos se solapan en las zonas de la piel expuestas al exterior, y comparten procesos químicos. Por envejecimiento y envejecimiento de la piel se entiende la aparición de cambios visibles en la apariencia de la piel, así como aquellos apreciables al tacto, como por ejemplo y de manera no limitativa, el desarrollo de discontinuidades en la piel como arrugas, líneas finas, líneas de expresión, marcas de estiramiento, estrías, grietas, irregularidades o asperezas, aumento del tamaño de los poros, pérdida de la hidratación, pérdida de la elasticidad, pérdida de la firmeza, pérdida de la tersura, pérdida de la capacidad de recuperación de la deformación, pérdida de la resiliencia, descolgamiento de la piel como el descolgamiento de las mejillas, la aparición de bolsas bajo los ojos o la aparición de papada entre otros, cambios en el color de la piel como manchas, rojeces, ojeras o aparición de zonas hiperpigmentadas como manchas de la edad o pecas entre otros, diferenciación anómala, hiperqueratinización, elastosis, queratosis, pérdida de pelo, aspecto de piel de naranja, pérdida de la estructuración del colágeno y otros cambios histológicos del estrato córneo, de la dermis, de la epidermis, del sistema vascular (por ejemplo la aparición de venas de araña o telangiectasias) o de los tejidos cercanos a la piel.
Uno de los signos más claros del envejecimiento es la aparición de arrugas, debida tanto a la pérdida de colágeno como a la pérdida de elasticidad de la piel. A nivel ultraestructural, la red de colágeno de la piel se vuelve más densa con la edad, a pesar de la pérdida de contenido de colágeno total. Las fibras elásticas se degradan progresivamente y rompen en fragmentos, lo que conlleva la pérdida de elasticidad de la piel y la aparición de arrugas. El proceso empieza en fases relativamente tempranas de la vida, y se acelera a partir de los cuarenta años de edad. Se ha demostrado que las mujeres pierden un 2, 1% de su nivel de colágeno por año después de la menopausia y que el 30% del colágeno se pierde en los primeros cinco años después de la menopausia [Brincat M. et al., “A study of the decrease of skin collagen content, skin thickness, and bone mass in the postmenopausal woman”, (1987) , Obstet. Gynecol., 70, 840-845]. Así, se observa un aumento en la cantidad de arrugas y líneas finas, una pérdida de flexibilidad de la piel y las mujeres experimentan una sensación de "piel seca" o de piel tirante.
Este proceso se ve agravado por la acción de la familia de las metaloproteasas de matriz (MMP) , una familia de enzimas proteolíticas (endoproteasas) que pueden degradar de manera colectiva los componentes macromoleculares de la matriz extracelular (colágeno y elastina) y de la lámina basal. La degradación de las fibras ES 2 397 890 Al
de colágeno da lugar a una piel de apariencia descolgada y arrugada, especialmente en las zonas expuestas a luz solar, como tez, orejas, cuello, escote, cuero cabelludo, manos y brazos, lo que no es deseable.
Además, la exposición prolongada a la radiación ultravioleta, particularmente UVA y UVB, estimula la síntesis de MMP, que destruyen colágeno [Fisher G.J. et al., “Pathophysiology of premature skin aging induced by ultraviolet light”, (1997) , New Eng. J. Med., 337, 1419-1429; Fisher G.J., “Ultraviolet irradiation increases matrix metalloproteinase-8 protein in human skin in vivo”, (2001) , J. Invest. Dermatol., 117, 219-226], lo que es una de las causas principales del fotoenvejecimiento.
Diversas condiciones, desórdenes y enfermedades de la piel y/o mucosas tienen una de sus causas en niveles bajos de colágeno, bien sea por la disminución de su síntesis, bien sea por el aumento de su degradación. Entre ellas destacan la úlcera crónica, psoriasis [Flisiak I. et al., “Effect of psoriasis activity on metalloproteinase-1 and tissue inhibitor of metalloproteinase-1 in plasma and lesional scales”, (2006) , Acta Derm Venereol., 86, 17-21], condiciones orales como gingivitis y periodontitis, cáncer de piel [Kerkelä E. et al., ” Matrix metalloproteinases in tumor progression: focus on basal and squamous cell skin cancer”, (2003) , Exp Dermatol., 12, 109-125], metástasis [Sato H. et al., “Roles of membrane-type matrix metalloproteinase-1 in tumor invasion and metastasis”, (2005) , Cancer Sci., 96, 212-217], dermatitis [Katoh N. et al., “Increased levels of serum tissue inhibitor of metalloproteinase-1 but not metalloproteinase-3 in atopic dermatitis”, (2002) , Clin. Exp. Immunol., 127, 283-288], rosácea, telangiectasia, cuperosis, bolsas bajo los ojos, círculos oscuros en el área periorbital, venas varicosas / varices, alopecia [Jarrousse F. et al., “Identification of clustered cells in human hair follicle responsible for MMP-9 gelatinolytic activity: consequences for the regulation of hair growth”, (2001) , Int. J. Dermatol., 40, 385-392] celulitis, piel de naranja, desórdenes de cicatrización o reepitelización, y estrías entre otras. La dermatitis incluye las condiciones de la piel, desórdenes o enfermedades que provocan inflamación, como dermatitis por contacto, dermatitis atópica, piel sensible y eczema. Todas estas condiciones, desórdenes y enfermedades son, por tanto, susceptibles de ser tratadas con compuestos estimuladores de la síntesis de colágeno.
La pérdida de hidratación en pieles envejecidas y/o fotoenvejecidas es otra de las causas...
Reivindicaciones:
1. Un péptido de fórmula general (I)
R1-Wn-Xm-AA1-AA2-AA3-AA4-AA5-AA6-Yp-Zq-R2 (I)
sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, 5 caracterizado porque:
AA1 se selecciona del grupo formado por -Ser-, -Thr- y -Tyr-;
AA2 se selecciona del grupo formado por -Pro-y -Val-;
AA3 es -Ala-;
AA4 se selecciona del grupo formado por -Glu-, -Gly- y -Val-;
AA5 es -Gly-;
AA6 se selecciona del grupo formado por -Gln-, -Gly-, -His- y -Pro-;
W, X, Y, Z son aminoácidos y se seleccionan independientemente entre sí;
n, m, p y q se seleccionan independientemente entre sí y tienen un valor de 0 ó 1;
n+m+p+q es menor o igual a 2;
R1 se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido y R5-CO-, donde R5 se selecciona del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, arilo sustituido o no sustituido, aralquilo sustituido o no sustituido,
heterociclilo sustituido o no sustituido y heteroarilalquilo sustituido o no sustituido;
R2 se selecciona del grupo formado por -NR3R4, -OR3 y -SR3, donde R3 y R4 se seleccionan independientemente del grupo formado por H, grupo alifático no cíclico sustituido o no sustituido, aliciclilo sustituido o no sustituido, heterociclilo sustituido o no sustituido, heteroarilalquilo sustituido o no sustituido, arilo sustituido o no sustituido, y aralquilo sustituido o no sustituido; y
con la condición de que R1 y R2 no son a-aminoácidos.
2. Péptido según la reivindicación 1, caracterizado porque R1 se selecciona del grupo formado por H y R5-CO- donde R5 se selecciona del grupo formado por alquilo C1-C24 sustituido o no sustituido, alquenilo C2-C24 sustituido o no sustituido, alquinilo C2-C24 sustituido o no sustituido, cicloalquilo C3-C24 sustituido o no sustituido, cicloalquenilo C5-C24 sustituido o no sustituido, cicloalquinilo C8-C24 sustituido o no sustituido,
arilo C6-C30 sustituido o no sustituido, aralquilo C7-C24 sustituido o no sustituido, heterociclilo de 3-10 miembros de anillo sustituido o no sustituido y heteroarilalquilo sustituido o no sustituido de 2 a 24 átomos de carbono y de 1 a 3 átomos diferentes al carbono y una cadena alquílica de 1 a 6 átomos de carbono.
3. Péptido según la reivindicación 2, caracterizado porque R1 se selecciona del grupo formado por H, acetilo,
terc-butanoilo, hexanoilo, 2-metilhexanoilo, ciclohexancarboxilo, octanoilo, decanoilo, lauroilo, miristoilo, 35 palmitoilo, estearoilo, oleoilo y linoleoilo.
4. Péptido según cualquiera de las reivindicaciones anteriores, caracterizado porque R2 es -NR3R4 o -OR3, donde R3 y R4 se seleccionan independientemente del grupo formado por H, alquilo C1-C24 sustituido o no sustituido, alquenilo C2-C24 sustituido o no sustituido, alquinilo C2-C24 sustituido o no sustituido, cicloalquilo C3-C24 sustituido o no sustituido, cicloalquenilo C5-C24 sustituido o no sustituido, cicloalquinilo C8-C24
sustituido o no sustituido, arilo C6-C30 sustituido o no sustituido, aralquilo C7-C24 sustituido o no sustituido, heterociclilo de 3-10 miembros de anillo sustituido o no sustituido, y heteroarilalquilo sustituido o no sustituido de 2 a 24 átomos de carbono y de 1 a 3 átomos diferentes al carbono y una cadena alquílica de 1 a 6 átomos de carbono.
5. Péptido según la reivindicación 4, caracterizado porque R3 y R4 se seleccionan independientemente del 45 grupo formado por H, metilo, etilo, hexilo, dodecilo y hexadecilo.
6. Péptido según cualquiera de las reivindicaciones anteriores, caracterizado porque R1 se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo y palmitoilo, AA1 es -L-Tyr-, AA2 es -L-Pro-, AA3 es -L-Ala-, AA4 es -L-Glu-, AA5 es -L-Gly-, AA6 es -L-Gln-, y R2 es -NR3R4 o -OR3 donde R3 y R4 se seleccionan ES 2 397 890 Al
independientemente de H, metilo, etilo, hexilo, dodecilo y hexadecilo.
7. Péptido según cualquiera de las reivindicaciones 1 a 5, caracterizado porque R1 se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo y palmitoilo, AA1 es -L-Ser-, AA2 es -L-Val-, AA3 es -L-Ala-, AA4 es -L-Val-, AA5 es -L-Gly-, AA6 es -L-Gln-, y R2 es -NR3R4 o -OR3 donde R3 y R4 se seleccionan independientemente de H, metilo, etilo, hexilo, dodecilo y hexadecilo.
8. Péptido según cualquiera de las reivindicaciones 1 a 5, caracterizado porque R1 se selecciona del grupo formado por H, acetilo, lauroilo, miristoilo y palmitoilo, AA1 es -L-Ser-, AA2 es -L-Pro-, AA3 es -L-Ala-, AA4 es -L-Gly-, AA5 es -L-Gly-, AA6 es -L-Pro-, y R2 es -NR3R4 o -OR3 donde R3 y R4 se seleccionan independientemente de H, metilo, etilo, hexilo, dodecilo y hexadecilo.
9. Péptido según cualquiera de las reivindicaciones anteriores, caracterizado porque R1 se selecciona del grupo formado por H, acetilo y palmitoilo y R2 se selecciona del grupo formado por -OH y -NH2.
10. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en el tratamiento y/o cuidado de la piel y mucosas.
11. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en la modulación de AQP-3.
12. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en la estimulación de la síntesis de colágeno.
13. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en la hidratación de la piel y/o mucosas.
14. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en la mejora de la función barrera de la piel.
15. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en la reepitelización y/o cicatrización de la piel y/o mucosas.
16. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en el tratamiento, prevención y/o reparación de los signos de envejecimiento y/o fotoenvejecimiento de la piel.
17. Péptido según la reivindicación 16, donde el tratamiento, prevención y/o reparación de los signos de envejecimiento y/o fotoenvejecimiento de la piel reduce, previene y/o trata las arrugas faciales.
18. Péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 9, para su uso en el tratamiento y/o cuidado de las condiciones, desórdenes y/o enfermedades de la piel y/o mucosas seleccionadas del grupo formado por psoriasis, dermatitis, dermatitis atópica, dermatitis alérgica, eczema, espongiosis, edema, ictiosis hereditaria, xerosis senil, sequedad vaginal, hiperqueratosis palmar, hiperqueratosis plantar, arrugas, arrugas de expresión, estrías, pieles envejecidas, pieles fotoenvejecidas, cáncer de piel, desórdenes de cicatrización o reepitelización, úlcera crónica, acné, queloides, cicatrices hipertróficas, celulitis, piel de naranja, elastosis, elastosis actínica, queratosis, rosácea, telangiectasia, cuperosis, bolsas bajo los ojos, círculos oscuros en el área periorbital, venas varicosas o varices, alopecia, gingivitis, periodontitis procesos inflamatorios y penfigoide bulloso
19. Péptido según cualquiera de las reivindicaciones 10 a 18 en el que el uso se realiza mediante aplicación tópica, transdérmica, oral o parenteral de dicho péptido.
20. Péptido según la reivindicación 19 en el que la aplicación tópica o transdérmica se realiza mediante iontoforesis, sonoforesis, electroporación, presión mecánica, gradiente de presión osmótica, cura oclusiva, microinyecciones, mediante inyecciones sin agujas mediante presión, mediante parches microeléctricos, mascarillas faciales o cualquier combinación de ellas.
21. Procedimiento de preparación de un péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables según cualquiera de las reivindicaciones
a 10, caracterizado porque se realiza en fase sólida o en solución.
22. Procedimiento según la reivindicación 21, caracterizado porque los grupos protectores de los grupos amino libre se seleccionan del grupo formado por Boc, Fmoc, Trt, Troc, Teoc, Alloc, Mtt, Z, ClZ, Dnp, Dde, ivDde y Adpoc, los grupos protectores de los grupos carboxilo libre se seleccionan del grupo formado por ésteres de tBu, Bzl, Chx, All, Dmab, 2-fenilisopropilo, Fm y Trt, la cadena lateral de tirosina se protege con un grupo protector seleccionado del grupo formado por 2-BrZ, Bzl y tBu y la cadena lateral de metionina se emplea sin protección.
23. Composición cosmética o farmacéutica que comprende una cantidad cosmética o farmacéuticamente eficaz de al menos un péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, según cualquiera de las reivindicaciones 1 a 10, y al menos un excipiente o adyuvante cosmética o farmacéuticamente aceptable.
24. Composición según la reivindicación 23, caracterizada porque el péptido de fórmula general (I) se encuentra a una concentración comprendida entre el 0, 000001% y el 20% en peso, con respecto al peso total de la composición.
25. Composición según la reivindicación 24, caracterizada porque el péptido de fórmula general (I) se encuentra a una concentración comprendida entre el 0, 0001% y el 5% en peso, con respecto al peso total de la composición.
26. Composición según cualquiera de las reivindicaciones 23 a 25, caracterizada porque el péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado a un sistema de vehiculización o a un sistema de liberación sostenida cosmética o farmacéuticamente aceptable seleccionado del grupo formado por liposomas, liposomas mixtos, oleosomas, niosomas, etosomas, milicápsulas, microcápsulas, nanocápsulas, soportes lipídicos nanoestructurados, esponjas, ciclodextrinas, vesículas, micelas, micelas mixtas de tensioactivos, micelas mixtas fosfolípido-tensioactivo, miliesferas, microesferas, nanoesferas, lipoesferas, microemulsiones, nanoemulsiones, minipartículas, milipartículas, micropartículas, nanopartículas y nanopartículas sólidas lipídicas..
27. Composición según la reivindicación 26, caracterizada porque las nanocápsulas son nanocápsulas conteniendo microemulsiones..
28. Composición según cualquiera de las reivindicaciones 23 a 27, caracterizada porque el péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, se encuentra adsorbido sobre un polímero orgánico sólido o soporte mineral sólido cosmética o farmacéuticamente aceptable seleccionado del grupo formado por talco, bentonita, sílice, almidón y maltodextrina.
29. Composición según cualquiera de las reivindicaciones 23 a 37, caracterizada porque se presenta en una formulación seleccionada del grupo formado por cremas, emulsiones múltiples, composiciones anhidras, dispersiones acuosas, aceites, leches, bálsamos, espumas, lociones, geles, geles crema, soluciones hidroalcohólicas, soluciones hidroglicólicas, hidrogeles, linimentos, sueros, jabones, champús, acondicionadores, serums, ungüentos, mousses, pomadas, polvos, barras, lápices, vaporizadores, aerosoles, cápsulas, cápsulas de gelatina, cápsulas blandas, cápsulas duras, comprimidos, comprimidos recubiertos de azúcar, formas granuladas, gomas de mascar, soluciones, suspensiones, emulsiones, jarabes, elixires, films de polisacáridos, jaleas y gelatina.
30. Composición según cualquiera de las reivindicaciones 23 a 29, caracterizada porque se encuentra incorporada a un producto seleccionado del grupo formado por correctores de ojeras, fondos de maquillaje, lociones desmaquillantes, leches desmaquillantes, sombras de ojos, barras de labios, brillos labiales, protectores labiales y polvos.
31. Composición según cualquiera de las reivindicaciones 23 a 39, caracterizada porque el péptido de fórmula general (I) , sus estereoisómeros, mezclas de los mismos y/o sus sales cosmética o farmacéuticamente aceptables, se encuentra incorporado en un tejido, un tejido-no-tejido o un producto sanitario.
32. Composición según la reivindicación 31, caracterizada porque el tejido, tejido-no-tejido o producto sanitario se selecciona del grupo formado por vendas, gasas, camisetas, medias, calcetines, ropa interior, fajas, guantes, pañales, compresas, apósitos, cubrecamas, toallitas, parches adhesivos, parches no adhesivos, parches oclusivos, parches microeléctricos y mascarillas faciales.
33. Composición según cualquiera de las reivindicaciones 23 a 32, caracterizada porque comprende adicionalmente una cantidad cosmética o farmacéuticamente eficaz de al menos un adyuvante seleccionado del grupo formado por otros agentes moduladores de AQP-3, agentes moduladores de
ES 2 397 890 Al
aquaporinas, proteínas de la familia de las aquaporinas, otros agentes estimuladores de la síntesis de colágeno, agentes moduladores de la síntesis de PGC-1a, agentes moduladores de la actividad de PPARy, agentes que incrementan o reducen el contenido de triglicéridos de los adipocitos, agentes aceleradores o retrasadores de la diferenciación de los adipocitos, agentes lipolíticos o estimuladores de la lipólisis, agentes anticelulíticos, agentes adipogénicos, inhibidores de la agregación de los receptores de acetilcolina, agentes inhibidores de la contracción muscular, agentes anticolinérgicos, agentes inhibidores de elastasa, agentes inhibidores de las metaloproteasas de matriz, agentes estimuladores o inhibidores de la síntesis de melanina, agentes blanqueantes o despigmentantes, agentes propigmentantes, agentes autobronceantes, agentes antienvejecimiento, agentes inhibidores de la NO-sintasa, agentes inhibidores de l.
5. reductasa, agentes inhibidores de lisil- y/o prolil-hidroxilasa, agentes antioxidantes, agentes capturadores de radicales libres y/o anticontaminación atmosférica, agentes capturadores de especies reactivas carbonilo, agentes antiglicación, agentes antihistamínicos, agentes antivirales, agentes antiparasitarios, agentes emulsionantes, emolientes, disolventes orgánicos, propelentes líquidos, acondicionadores de la piel, humectantes, sustancias que retienen la humedad, alfahidroxiácidos, betahidroxiácidos, hidratantes, enzimas epidérmicas hidrolíticas, vitaminas, aminoácidos, proteínas, pigmentos o colorantes, tintes, biopolímeros, polímeros gelificantes, agentes espesantes, tensioactivos, agentes suavizantes, emulgentes, agentes aglutinantes, conservantes, agentes antiarrugas, agentes capaces de disminuir o tratar las bolsas bajo los ojos, agentes exfoliantes, agentes descamantes, agentes queratolíticos, agentes antimicrobianos, agentes antifúngicos, agentes fungistáticos, agentes bactericidas, agentes bacteriostáticos, agentes estimuladores de la síntesis de macromoléculas dérmicas o epidérmicas y/o capaces de inhibir o prevenir su degradación, agentes estimuladores de la síntesis de elastina, agentes estimuladores de la síntesis de decorina, agentes estimuladores de la síntesis de laminina, agentes estimuladores de la síntesis de defensinas, agentes estimuladores de la síntesis de chaperonas, agentes estimuladores de la síntesis de cAMP, proteínas de choque térmico, agentes estimuladores de la síntesis de HSP70, agentes estimuladores de la síntesis de proteínas de choque térmico, agentes estimuladores de la síntesis de ácido hialurónico, agentes estimuladores de la síntesis de fibronectina, agentes estimuladores de la síntesis de sirtuínas, agentes estimuladores de la síntesis de lípidos y componentes del estrato córneo, ceramidas, ácidos grasos, agentes inhibidores de la degradación de colágeno, agentes inhibidores de la degradación de elastina, agentes inhibidores de proteasas de serina, agentes estimuladores de la proliferación de fibroblastos, agentes estimuladores de la proliferación de queratinocitos, agentes estimuladores de la proliferación de adipocitos, agentes estimuladores de la proliferación de melanocitos, agentes estimuladores de la diferenciación de queratinocitos, agentes inhibidores de la acetilcolinesterasa, agentes dermorelajantes, agentes estimuladores de la síntesis de glicosaminoglicanos, agentes antihiperqueratosis, agentes comedolíticos, agentes antipsoriasis, agentes antidermatitis, agentes antieczema, agentes reparadores del DNA, agentes protectores del DNA, estabilizantes, agentes antiprurito, agentes para el tratamiento y/o cuidado de pieles sensibles, agentes reafirmantes, agentes redensificantes, agentes reestructurantes, agentes antiestrías, agentes astringentes, agentes reguladores de la producción de sebo, agentes antiperspirantes, agentes estimuladores de la cicatrización, agentes coadyuvantes de la cicatrización, agentes estimuladores de la reepitelización, agentes coadyuvantes de la reepitelización, factores de crecimiento de citoquinas, agentes calmantes, agentes antiinflamatorios, agentes anestésicos, agentes que actúen sobre la circulación capilar y/o la microcirculación, agentes estimuladores de la angiogénesis, agentes inhibidores de la permeabilidad vascular, agentes venotónicos, agentes que actúen sobre el metabolismo de las células, agentes destinados a mejorar la unión dermis-epidermis, agentes estimuladores del crecimiento del cabello, agentes inhibidores o retardadores del crecimiento del cabello, perfumes, agentes quelantes, extractos vegetales, aceites esenciales, extractos marinos, agentes provenientes de un procedimiento de biofermentación, sales minerales, extractos celulares, filtros solares y agentes fotoprotectores de naturaleza orgánica o mineral activos contra los rayos ultravioleta A y/o B, o mezclas de ellos.
34. Composición según la reivindicación 33, caracterizada porque el agente activo es de origen sintético o es un extracto vegetal o proviene de un procedimiento de biofermentación/ procedimiento biotecnológico.
35. Composición según cualquiera de las reivindicaciones 33 a 34 caracterizada porque el adyuvante se selecciona del grupo formado por agentes antiarrugas y/o agentes antienvejecimiento.
36. Composición según la reivindicación 35, caracterizada porque el agente antiarrugas y/o agente antienvejecimiento se selecciona del grupo formado por Acetil Hexapéptido-8, Acetil Heptapéptido-4, Acetil Octapéptido-3, Pentapéptido-18, Acetil Hexapéptido-30, la mezcla de Proteína de Trigo Hidrolizada, Proteína de Soja Hidrolizada, y Tripéptido-1, Diaminopropionoil Tripéptido-33, Tripéptido-10 Citrulina, la mezcla de Extracto de Fermento de Pseudoalteromonas, Proteína de Trigo Hidrolizada, Proteína de Soja Hidrolizada, Tripéptido-10 Citrulina y Tripéptido-1, Acetil Tetrapéptido-5, Acetil Tripéptido-30 Citrulina, Acetilarginiltriptofil Difenilglicina, Acetil Tetrapéptido-22, Dimetilmetoxi Cromanol, Dimetilmetoxi Cromanil Palmitato, Extracto de Fermento de Pseudoalteromonas, la mezcla de Lisina HCl, Lecitina y Tripéptido-9 Citrulina y la mezcla de Lisina HCl, Lecitina y Tripéptido-10 Citrulina.
37. Composición según cualquiera de las reivindicaciones 33 a 34, caracterizada porque el adyuvante se
selecciona del grupo formado por agentes humectantes, sustancias que retienen la humedad, hidratantes, emolientes.
38. Composición según la reivindicación 37, caracterizada porque el humectante, sustancia que retiene la humedad, hidratante, emoliente se selecciona del grupo formado por Extracto de Fermento de
Pseudoalteromonas, la mezcla de Glicerina, Extracto de Fermento de Pseudoalteromonas, Goma Xantana, Prolina, Alanina, Serina, Etilhexilglicerina y Caprilil Glicol, Acetil Dipéptido-3 Aminohexanoato, o Extracto de Fermento de Pseudoalteromonas
39. Composición según cualquiera de las reivindicaciones 33 a 34, caracterizada porque el adyuvante se selecciona del grupo formado por agentes estimuladores de la cicatrización, agentes coadyuvantes de la 10 cicatrización, agentes estimuladores de la reepitelización, agentes coadyuvantes de la reepitelización.
40. Composición según la reivindicación 39, caracterizada porque el agente estimulador de la cicatrización, agentes coadyuvante de la cicatrización, agente estimulador de la reepitelización, agentes coadyuvante de la reepitelización se selecciona del grupo formado por Extracto de Fermento de Pseudoalteromonas, Acetil Dipéptido-3 Aminohexanoato, Tripéptido-10 Citrulina, la mezcla de Extracto de Fermento de Pseudoalteromonas, Proteína de Trigo Hidrolizada, Proteína de Soja Hidrolizada, Tripéptido-10 Citrulina, y Tripéptido-1, la mezcla de Glicerina, Extracto de Fermento de Pseudoalteromonas, Goma Xantana, Prolina, Alanina, Serina, Etilhexilglicerina y Caprilil Glicol, Hexapéptido-10 o Acetil Tetrapéptido-22
OFICINA ESPANOLA DE PATENTES Y MARCAS ESPANA
INFORME SOBRE EL ESTADO DE LA TECNICA
51 Int. Cl. : C07K7/06 (2006A01) A61K38/08 (2006A01)
NAD solicitud: 201130441 22 Fecha de presentación de la solicitud: 25A03A2011 32 Fecha de prioridad:
DOCUMENTOS RELEVANTES
Categoría 56 Documentos citados Reivindicaciones afectadas
A WO 2004101609 A2 (SEDERMA) 25A11A2004, 1-40
reivindicacionesA
A WO 2009106715 A2 (SOCIETE D'EXTRACTION DES PRINCIPES ACTIFS SAAA (VINCIENCE) ) 1-40
03A09A2009, reivindicacionesA
Categoria de los documentos citados X: de particular relevancia Y: de particular relevancia combinado con otro/s de la misma categoria A: refleja el estado de la tecnica O: referido a divulgación no escrita P: publicado entre la fecha de prioridad y la de presentación de la solicitud E: documento anterior, pero publicado despues de la fecha de presentación de la solicitud
El presente informe ha sido realizado • para todas las reivindicaciones • para las reivindicaciones nD:
Fecha de realización del informe 26A02A2013 Examinador MA Novoa Sanjurjo Página 1/4
INFORME DEL ESTADO DE LA TECNICA
ND de solicitud: 201130441
Documentación minima buscada (sistema de clasificación seguido de los simbolos de clasificación) C07K, A61K Bases de datos electrónicas consultadas durante la busqueda (nombre de la base de datos y, si es posible, terminos de
busqueda utilizados) INVENES, EPODOC, REGISTRY, HCAPLUS, BIOSIS
Informe del Estado de la Tecnica Pagina 2/4
OPINIÓN ESCRITA
ND de solicitud: 201130441
Fecha de Realización de la Opinión Escrita: 26A02A2013
Declaración
Novedad (Art. 6.1 LP 11/1986) Reivindicaciones 1-40 Reivindicaciones SI NO
Actividad inventiva (Art. 8.1 LP11/1986) Reivindicaciones 1-40 Reivindicaciones SI NO
Se considera que la solicitud cumple con el requisito de aplicación industrialA Este requisito fue evaluado durante la fase de examen formal y tecnico de la solicitud (Articulo 31A2 Ley 11/1986) A
Base de la Opinión.
La presente opinión se ha realizado sobre la base de la solicitud de patente tal y como se publicaA
Consideraciones:
La invención consisteenun grupo de hexapeptidos defórmula general AA1AA2AA3AA4AA5AA6en la que AA1 es S, T o Y; AA2 es P o V; AA3 es A; AA4 es E, G o V; AA5 es G y AA6 es Q, G, H o PA Los peptidos de la invención presentan actividad moduladora de la proteina AQP-3, estimulan la producción de colageno y pueden utilizarse para hidratar la piel y las mucosasA Los peptidos de la invención tambien se utilizan en el tratamiento de los signos de envejecimiento de la pielA
Informe del Estado de la Tecnica Pagina 3/4
OPINIÓN ESCRITA
ND de solicitud: 201130441
1. Documentos considerados.
A continuación se relacionanlos documentos pertenecientes al estado de la tecnica tomados en consideración para la realización de esta opiniónA
Documento Número Publicación o Identificación Fecha Publicación
D01 WO 2004101609 A2 (SEDERMA) 25A11A2004
D02 WO 2009106715 A2 (SOCIETE D'EXTRACTION PRINCIPES ACTIFS SAAA (VINCIENCE) ) DES 03A09A2009
El doc umento D 01, describe pe ptidos derivados de el astina que i ncluyen l a se cuencia V GVAPG, que f avorecen l a producción de colageno y se utilizan para tratar las arrugas de la pielA El documento D02, describe peptidos derivados de AQP-3 que incluyen la secuencia NPARA Los peptidos se utilizan en preparaciones cosmeticas destinadas a hidratar la pielA
2. Declaración motivada según los artículos 29.6 y 29.7 del Reglamento de ejecución de la Ley 11/1986, de 20 de marzo, de Patentes sobre la novedad y la actividad inventiva; citas y explicaciones en apoyo de esta declaración Los documentos citados solo muestran el estado general de la tecnica y no se consideran de particular relevancia, ya que para una persona experta en la materia, no seria obvio aplicar las caracteristicas de los documentos citados y llegar a la invención tal ycomo se menciona en las reivindicaciones 1-40A Por lo tanto, el objeto de la presente solicitud cumple los requisitos de novedad y actividad inventiva de acuerdo con los Articulos 6 y 8 de la Ley de Patentes 11/1986A
Informe del Estado de la Tecnica Pagina 4/4
Patentes similares o relacionadas:
Péptido basado en colágeno tipo II alfa-1 útil para el tratamiento de una enfermedad de la superficie ocular, del 15 de Julio de 2020, de EYEBIO KOREA: Un péptido que consiste en una secuencia de aminoácidos representada por SEQ ID NO: 1.
Péptido que tiene actividad antiinflamatoria, y uso del mismo, del 8 de Julio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en una secuencia de aminoácidos de SEQ ID NO: 1, SEQ ID NO: 2 o SEQ ID NO: 3.
Péptido que tiene actividades antiinflamatoria, osteogénica y promotora del crecimiento del cabello, y uso del mismo, del 24 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que tiene actividad antiinflamatoria, que consiste en la secuencia de aminoácidos SEQ ID NO: 2.
Nueva inmunoterapia contra diversos tumores como el cáncer gastrointestinal y gástrico, del 24 de Junio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido seleccionado del grupo siguiente: a) péptido consistente en la secuencia conforme a la SEQ ID N.º 86, b) el péptido conforme a a), en la […]
Inmunoterapia WT1 para enfermedad angiogénica intraocular, del 17 de Junio de 2020, de INTERNATIONAL INSTITUTE OF CANCER IMMUNOLOGY, INC.: Una composición farmacéutica que comprende un péptido WT1 o péptido WT1 variante para su uso en el tratamiento y/o prevención de una enfermedad […]
Anticuerpos monoclonales humanizados y quiméricos para CD99, del 17 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un anticuerpo monoclonal humanizado aislado que se une específicamente a CD99 humano, y comprende: (a) una cadena ligera que comprende la secuencia de aminoácidos expuesta […]
Péptido con eficacia antiobesidad y antidiabética y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de SEQ ID NO: 1 o SEQ ID NO: 2.
Péptido que tiene actividades antiinflamatoria, osteogénica y de fomento del crecimiento del pelo, y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Péptido que tiene actividad antiinflamatoria, que consiste en secuencias de aminoácidos de SEQ ID NO: 3.