VACUNA CONTRA EL VIRUS DE PAPILOMA HUMANO.
Vacuna contra el virus de papiloma humano.
La infección por el virus del papiloma humano (VPH) es considerada la principal enfermedad de transmisión sexual y ha sido asociada causalmente al cáncer cervical.
Los inventores proporcionan una construcción de fórmula AVPH-[L-X]n, donde AVPH es un radical de un antígeno de un virus del papiloma humano; L es un conector de masa molecular entre 3400-20000 Da, X es un radical de la porción Fc de una inmunoglobulina o de un fragmento de la misma; y n es un entero entre 1 y 60. La construcción es útil como inmunógeno y para la fabricación de composiciones farmacéuticas para la prevención y/o tratamiento del cáncer cervical o de verrugas genitales en humanos
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200703070.
Solicitante: UNIVERSIDAD DE BARCELONA.
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: DOMINGO PEDROL,JOAN CARLES, RUEDA PALACIO,FELIX, DE MADARIAGA DE LAS HERAS,MARIA AFRICA.
Fecha de Solicitud: 14 de Noviembre de 2007.
Fecha de Publicación: .
Fecha de Concesión: 13 de Octubre de 2010.
Clasificación PCT:
- A61K39/12 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Antígenos virales.
- C07K14/025 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Papovaviridae, p. ej. virus de papiloma, virus del polioma, SV40, virus BK, virus JC.
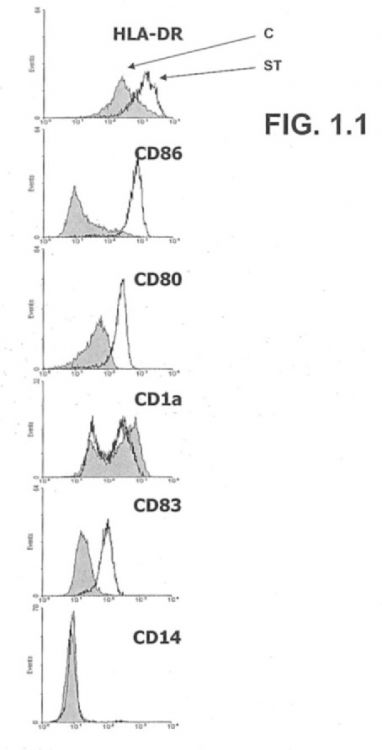
Fragmento de la descripción:
Vacuna contra del virus del papiloma humano.
Esta invención se refiere al campo de la medicina y específicamente a las vacunas contra el virus del papiloma humano (VPH). Los virus del papiloma son pequeños virus de ADN tumorales, los cuales son altamente específicos de especie.
Estado de la técnica anterior
La infección por el virus del papiloma humano (VPH) está considerada la principal enfermedad de transmisión sexual y se ha ligado casualmente al cáncer de cuello uterino. Es sobrepasada sólo por el cáncer de mama como la principal causa mundial de muerte por cáncer en mujeres. Se han identificado más de 100 tipos de VPH, 35 de los cuales infectan el tracto genital. De estos, los tipos de alto riesgo se hallan en >90% de los cánceres de cuello uterino invasivos, mientras que los tipos de bajo riesgo se asocian a lesiones cervicales benignas o verrugas genitales.
Conceptualmente, hay tres enfoques para el desarrollo de una vacuna VPH. El primer enfoque busca bloquear la neoplasia inducida por VPH previniendo el establecimiento de la infección en el epitelio, principalmente a través de la inducción de anticuerpos neutralizantes contra las proteínas de la cápside viral. Una vacuna profiláctica debería estimular la completa neutralización de los virus libres tras su exposición antes que la infección pueda producirse.
El desarrollo de vacunas preventivas contra VPH se ha complicado por la falta de modelos animales para los tipos VPH genitales mucosa-trópicos y por la dificultad de propagar el virus en cultivo. Estos problemas han sido parcialmente superados utilizando como modelos virus del papiloma animal cutáneos y de mucosa y por el desarrollo de partículas semejantes a virus ("virus-like particles", VLPs) y pseudoviriones. La expresión de L1, la proteína mayor de la cápside del virus, en sistemas de baculovirus, resulta en el auto-ensamblaje de las proteínas para formar partículas víricas vacías, indistinguibles de los viriones nativos. La utilidad de las VLPs de VPH en el desarrollo de vacunas ha promovido su generación para los tipos más comunes de VPH. La proteína menor de la cápside L2, la cual se co-ensambla con L1 para formar los viriones naturales, no es esencial para la formación de las VLPs. Además, cuando VLPs L1/L2 han sido usadas para la inmunización, la mayoría de los anticuerpos obtenidos reconocen epítopos de L1.
Una vacuna que ha demostrado ser un 100% efectiva previniendo el pre-cáncer cervical de alto grado y el cáncer cervical no invasivo asociado a los tipos 16 y 18 de VPH en ensayos clínicos fase III es Gardasil® de Merck. Esta es una vacuna tetravalente (esto es, cuatro antígenos) conteniendo VLPs de proteína LI recombinante de VPH de los tipos 6, 11, 16 y 18.
GlaxoSmithKline ha sometido a revisión una solicitud de marketing para otra vacuna, Cervarix®. Esta es una formulación bivalente (esto es, dos antígenos) de VLPs de L1 recombinantes de los tipos 18 y 16 de VPH.
Aunque la vacunación con vacunas preventivas VPH es capaz de generar sueros con altos títulos de anticuerpos neutralizantes, tal inmunización puede no ser capaz de generar efectos terapéuticos significativos en infecciones VPH establecidas o avanzadas que hayan escapado a la neutralización mediada por anticuerpos. Por lo tanto, el segundo enfoque para el desarrollo de vacunas se dirige a inducir una respuesta inmune celular (de ambos tipos, CD4+ y CD8+), las cuales pueden ser capaces tanto de prevenir, como de inducir la regresión de lesiones neoplásicas. Esta estrategia es conocida como inmunoterapia antígeno-específica, en la cual células efectoras, particularmente células T, son inducidas contra epítopos de antígenos VPH que se sabe son expresados por las células neoplásicas (antígenos específicos de tumor) tales como E6 y E7. Las oncoproteínas E6 o E7 son consistentemente expresadas en células de cáncer de cuello uterino establecido, mientras que L1 o L2 están ausentes. Ensayos en fases tempranas en humanos utilizando vacunas terapéuticas han mostrado que son seguras. Sin embargo, no se han obtenido evidencias de eficacia clínica. Un posible efecto terapéutico basado bien en un descenso de la carga viral, bien de persistencia viral y/o en una reducción del tamaño de las lesiones fue observado en ensayos clínicos en pacientes con lesiones cervicales pre-cancerosas, neoplasia anogenital intraepitelial o verrugas anogenitales. Sin embargo, en ausencia de ensayos clínicos randomizados con placebos controlados comparando el descenso en la progresión de las lesiones, solo es posible especular sobre la eficacia clínica de estas vacunas terapéuticas. Finalmente, el tercer enfoque trata de combinar profilaxis y terapia en una vacuna, en un intento de ofrecer total cobertura para personas que han sido recientemente expuestas a virus de alto riesgo y para personas que ya sufren infección y displasia actualmente. Están siendo desarrolladas vacunas quiméricas en las que VLPs quiméricas conteniendo la proteína E7 o motivos de E7 insertados en las proteínas L1 o L2 son capaces de inducir tanto una respuesta inmunológica de anticuerpos neutralizantes anti-Li como una respuesta de linfocitos T citotóxicos específicos de E7 que inhiben el crecimiento tumoral en modelos animales (cfr. K. Schafer et al., "Immune response to human papillomavirus 16 L1 E7 chimeric virus-like particles: induction of cytotoxic T cells and specific tumor protection", Int. J. Cancer 1999, vol. 81, pp. 881-8).
Partículas opsonizadas con anticuerpos incrementan su captación mediante la unión a receptores específicos presentes en células fagocíticas, produciendo como resultado un incremento en la activación de las células T. Los inmunocomplejos antígeno:anticuerpo se unen a los receptores Fc presentes en la superficie de las células presentadoras de antígeno (CPA), tales como, células dendríticas o macrófagos. Estos complejos son así internalizados y el antígeno procesado y presentado en el contexto de las moléculas que codifican los Complejos Mayores de Histocompatibilidad (CMH) para células T antígeno específicas. Los antígenos unidos a anticuerpos no se dispersan, ya que son reconocidos por receptores específicos en las CPA, lo que puede reducir el nivel de antígeno requerido para activar las células T. Sin embargo, aunque los inmunocomplejos han sido descritos como potentes inmunógenos (cfr. S. Amigorena, "Fc gamma receptors and cross-presentation in dendritic cells", J. Exp. Med. 2002, vol. 195 ppl-3), para conseguir este objetivo es necesario utilizar anticuerpos monoclonales, con posibles procesos de reacciones adversas, como ha sido observado en otros tratamientos con anticuerpos monoclonales (cfr. K. Tada et al., "Severe infusion reaction induced by trastuzumab: a case report", Breast Cancer 2003, vol. 10, pp. 167-9; R.J. Cersosimo, "Monoclonal antibodies in the treatment of cancer, Part 1", Am. J. Health Syst. Pharm. 2003, vol. 60, pp. 1531-48).
A pesar de las mencionadas vacunas, todavía existe la necesidad de nuevos tratamientos inmunológicos terapéuticos contra el VPH, causante del cáncer de cuello uterino o de otras enfermedades relacionadas con el VPH. La inmunoterapia puede tener un impacto inmediato en la incidencia del cáncer cervical, mientras que las vacunas profilácticas tardarán años a reducir la mortalidad debido a esta enfermedad.
Explicación de la invención
La presente invención se relaciona con las construcciones inmunogénicas y las vacunas contra el virus del papiloma humano (VPH). En un primer aspecto, la presente invención se refiere a una construcción con la fórmula AVPH-[L-X]n (fórmula I) donde AVPH es un radical de un antígeno de un virus papiloma humano (VPH); L es un conector de masa molecular entre 3400-20000 Da; X es un radical de la porción Fc de una inmunoglobulina o de un fragmento de la misma; y n es un entero entre 1 y 60.
Los inventores han hallado un incremento de 5-10 veces en la respuesta en los linfocitos T inducida por las células dendríticas (DC) cuando éstas son cebadas con la construcción de la invención, respecto a las VLPs de VPH solas. La construcción permite dirigir el HPVA a los receptores Fc de las CPAs in vivo o ex-vivo. Entre otros efectos, la captación del antígeno por los receptores Fc[gamma] produce inducción de maduración en células dendríticas, incrementa la eficiencia de la presentación de antígenos exógenos por los complejos mayores de histocompatibilidad de clase I e incremento de la activación de las células T hasta 10 veces por encima de la que produce el antígeno sólo. El uso de los fragmentos...
Reivindicaciones:
1. Construcción de fórmula (I):
donde
AVPH es un radical de un antígeno de un virus papiloma humano (VPH);
L es un conector de masa molecular entre 3400-20000 Da;
X es un radical de la porción Fc de una inmunoglobulina o de un fragmento de la misma; y
n es un entero entre 1 y 60.
2. Construcción según la reivindicación 1, donde el antígeno es una partícula similar a virus de VPH que comprende la proteína L1 de VPH.
3. Construcción según la reivindicación 2, donde el antígeno es una partícula similar a virus quimérica de VPH que comprende además al menos una proteína seleccionada del grupo que consiste en L2, E6 y E7 de VPH.
4. Construcción según cualquiera de las reivindicaciones 2-3, donde VPH es seleccionado de los VPH de los tipos 16 y 31.
5. Construcción según cualquiera de las reivindicaciones 1-4, donde L es polímero biradical seleccionado del grupo que consiste en polietilenglicol, polipropilenglicol, copolímeros de etilenglicol y propilenglicol, dextrano, ácido poliláctico, ácido poliláctico-glicólico y ácido hialurónico.
6. Construcción según la reivindicación 5, donde L es un biradical de polietilenglicol.
7. Construcción según cualquiera de las reivindicaciones 1-6, donde la inmunoglobulina es seleccionada del grupo que consiste en IgG, IgA, IgD, IgE, IgM, y combinaciones e híbridos de las mismas.
8. Construcción según la reivindicación 7, donde la inmunoglobulina es IgG humana.
9. Construcción según la reivindicación 8, donde X es un fragmento de la porción Fc de la IgG que comprende un fragmento totalmente glicosilado que comprende dos regiones CH3-CH2 con una región bisagra unida por puentes disulfuro.
10. Composición farmacéutica que comprende una cantidad terapéuticamente efectiva de al menos una de las construcciones tal como se definen en cualquiera de las reivindicaciones 1-9, junto con cantidades apropiadas de diluyentes o portadores farmacéuticamente aceptables.
11. Composición según la reivindicación 10, que además comprende cantidades efectivas de al menos un adyuvante para su administración como vacuna.
12. Composición según la reivindicación 11, donde el adyuvante es seleccionado del grupo que consiste en oligonucleótidos de poli (inosina:citosina), lipopolisacárido de enterobacteria, oligonucleótidos conteniendo CpG no metilado, factor estimulante de colonias granulocito-macrofágicas y sulfato potásico-alumínico.
13. Composición según la reivindicación 10, que comprende además un antígeno tumoral o un componente de un patógeno distinto de VPH.
14. Uso de una construcción como se define en cualquiera de las reivindicaciones 1-9 para la fabricación de un medicamento inmunogénico.
15. Uso de una construcción como se define en cualquiera de las reivindicaciones 1-9 para la fabricación de una composición farmacéutica para la prevención y/o tratamiento en humanos del cáncer cervical o de verrugas genitales.
16. Método de preparación de un cultivo de células terapéuticas que comprende las etapas de:
(i) extracción de las células efectoras del paciente;
(ii) adición de un agente que incremente la expresión de los receptores Fc en la superficie de las células efectoras; y
(iii) adición de la composición farmacéutica como se define en la reivindicación 10 sobre la células resultantes de la etapa (ii).
17. Método según la reivindicación 16, donde las células efectoras son células dendríticas.
18. Cultivo de células obtenible por el método de preparación definido en cualquiera de las reivindicaciones 16-17.
19. Método de preparación de una construcción como se define en cualquiera de las reivindicaciones 1-9, que comprende las etapas de:
(i) incubar cantidades apropiadas de AVPH y de un compuesto generador de L conteniendo grupos reactivos diferentes a ambos extremos;
(ii) incubar el producto resultante de la etapa (i) con cantidades apropiadas de un compuesto generador de X químicamente activado; y
(iii) separar la construcción AVPH-[L-X]n, de los compuestos que no hayan reaccionado.
Patentes similares o relacionadas:
Composición farmacéutica que comprende un complejo de carga portador polimérico y al menos un antígeno proteínico o peptídico, del 1 de Julio de 2020, de CureVac AG: Composición farmacéutica que incluye: (A) un complejo de carga portador polimérico, que comprende: a) un portador polimérico que comprende componentes catiónicos reticulados […]
Vacunas y diagnóstico de torque teno virus porcino, del 18 de Junio de 2020, de VIRGINIA TECH INTELLECTUAL PROPERTIES, INC.: Composición inmunogénica que comprende una proteína según SEQ ID NO. 16.
Estructuras artificiales de poliepítopos para uso en inmunoterapia, del 17 de Junio de 2020, de Invectys: Un vector de expresión de ADN o una mezcla de vectores de expresión de ADN que codifica al menos dos epítopos de CD4 de la transcriptasa inversa de la telomerasa […]
Métodos para proporcionar virosomas con adyuvante y virosomas con adyuvante obtenibles de esta manera, del 3 de Junio de 2020, de BESTEWIL HOLDING B.V: Un método para preparar los virosomas con adyuvante, que comprende las etapas de: (i) proporcionar una composición acuosa de los virosomas sin adyuvante que comprende […]
Ácido nucleico que comprende o codifica para un tallo-bucle de histona y una secuencia poli(A) o una señal de poliadenilación para aumentar la expresión de un antígeno patogénico codificado, del 3 de Junio de 2020, de CureVac AG: Secuencia de ácido nucleico que comprende o codifica en la dirección 5' → 3' para: i) • una región codificante, que codifica para al menos […]
Composiciones inmunogénicas de PCV2 multivalentes y métodos para producir dichas composiciones, del 27 de Mayo de 2020, de Boehringer Ingelheim Animal Health USA Inc: Una vacuna combinada multivalente para uso en un método para (i) la prevención de una infección por PCV2, o de reinfección por PCV2 o (ii) la reducción o eliminación […]
Vacuna que comprende un pestivirus atenuado, del 27 de Mayo de 2020, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Un pestivirus atenuado, con al menos una mutación en la secuencia codificadora de la glicopoteína E ms y al menos otra mutación en la secuencia […]
Proteínas de consenso del virus de la Fiebre Aftosa (VFA), secuencias codificantes y vacunas preparadas a partir de las mismas, del 6 de Mayo de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Molécula de ácidos nucleicos que comprende una secuencia de ácidos nucleicos seleccionada del grupo que consiste en SEC ID nº 1, SEC ID nº […]