Método de tratamiento de la enfermedad intestinal inflamatoria.
5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria que comprende administrar unadosis diaria inicial de (i) 2,
4 g of 5-ASA en forma de liberación controlada, administrada como: una dosis de 1,2 g dosveces al día; una dosis de 2,4 g una vez al día; o una dosis de 0,8 g tres veces al día, o (ii) 4,8 g de 5-ASA en formade liberación controlada, administrada como una dosis diaria una vez al día de 4,8 g, y, en donde cuando no se lograla remisión después de dicho tratamiento durante 4-8 semanas, se cambia la dosis inicial a una dosis diaria modificadade 4,8 g de 5-ASA en forma de liberación controlada administrada como 2,4 g dos veces al día (BID) hasta 8semanas
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/079739.
Solicitante: SHIRE DEVELOPMENT INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 725 CHESTER BROOK BLVD. WAYNE, PA PENNSYLVANIA 19087 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KARISTADT MEYEROFF,ROBYN GAIL, DIEBOLD,RONALD JOSEPH, PIERCE,DAVID MONTAGUE, MARTIN,PATRICK T.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/196 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › estando el grupo amino unido directamente a un ciclo, p. ej. ácido antranílico, ácido mefenámico, diclofenac, clorambucilo.
- A61P1/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del tracto alimentario o del aparato digestivo.
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
PDF original: ES-2398254_T3.pdf
Fragmento de la descripción:
Método de tratamiento de la enfermedad intestinal inflamatoria.
Esta solicitud reivindica la prioridad de la solicitud provisional de EE.UU. Nº 60/866401, presentada el 17 de noviembre de 2006.
Antecedentes La enfermedad intestinal inflamatoria (abreviadamente en lo sucesivo IBD por la expresión inglesa Inflammator y Bowel Disease) es una expresión usada en la técnica para abarcar genéricamente enfermedades intestinales, tales como colitis ulcerosa (abreviadamente UC por la expresión inglesa Ulcerative Colitis) , síndrome del intestino irritable, síndrome del colon irritable y enfermedad de Crohn (abreviadamente CD por la expresión Crohn’s Disease) . Para muchas de estas enfermedades, en particular la CD, la etiología de la enfermedad (bacteriana, viral, genética o autoinmunitaria) es desconocida. Las enfermedades intestinales inflamatorias, tales como la CD o la UC, han sido tratadas en el pasado con derivados del ácido salicílico (tales como el ácido 5-aminosalicílico, también conocido como 5-ASA, mesalamina o mesalazina; sales o ésteres de 5-ASA; y profármacos de 5-ASA, tal como sulfasalazina) . El 5-ASA se usa como tratamiento de primera elección para colitis ulcerosas de suaves a moderadas.
Se sabe que dosis de 5-ASA > 2 g/día no son más eficaces que dosis inferiores para mantener la remisión en pacientes con UC (Travis S, Nature Clinical Practice Gastroenterology & Hepatology (2005) 2, 564-565) . El 5-ASA administrado por vía oral actúa localmente desde el lado luminal del intestino inflamado después de la absorción por la mucosa del colon y del íleon, y es principalmente acetilado a su primer metabolito N-acetil-5-ASA (Ac-5-ASA) en la pared intestinal y en el hígado. Las directrices actuales para el tratamiento de la UC de suave a moderada activa sugieren que el tratamiento con 5-ASA por vía oral, ya sea como monoterapia o en combinación con una formulación tópica, debe ser prescrito durante aproximadamente 4 a 6 semanas para la inducción de la remisión (Carter MJ, et al., Gut 2004; 53: V1-16. y Kornbluth A, et al., Am. J. Gastroenterol. 2004; 99: 1371-85) .
Sin embargo, si los pacientes no logran la remisión en esta fase de inducción, no hay sugerencias de que la terapia continuada con 5-ASA en estas condiciones de como resultado la inducción de la remisión. Por tanto, el profesional clínico debe decidir la siguiente etapa apropiada en el modelo del tratamiento, que se conoce generalmente como la terapia "ascendente" o "escalada de terapia". La "etapa" de este modelo es generalmente terapia con corticosteroides, que es una terapia frecuentemente no tolerada por los pacientes debido a sus efectos secundarios.
Los pacientes que logran la remisión de la UC de suave a moderada activa, se mantienen generalmente en remisión usando una terapia continuada con 5-ASA (aminosalicilato) (Kornbluth A, et al., Am. J. Gastroenterol. 2004; 99: 1371-85) .
De D’Haens et al., es el trabajo "Once daily MMX mesalazine for the treatment of mild-to-moderate ulcerative colitis: a phase II, dose-ranging study", Alimentar y Pharmacology. Therapy, vol 24, 1 de enero de 2006, páginas 1087-1097. Este documento describe que mesalazina MMX (Multi Matrix System™) administrada como 2, 4 o 4, 8 g/día una vez al día es bien tolerada y eficaz para el tratamiento de colitis ulcerosa de suave a moderadamente activa.
Compendio de la invención.
De acuerdo con un primer aspecto de la presente invención se facilita 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria, que comprende administrar un dosis diaria inicial de (i) 2, 4 g de 5-ASA en forma de liberación controlada, administrada como: una dosificación de 1, 2 g dos veces al día; una dosificación de 2, 4 g una vez al día; o una dosis de 0, 8 g tres veces al día, o (ii) 4, 8 g de 5-ASA en forma de liberación controlada, administrada como una dosificación de 4, 8 g una vez al día, y, cuando no se logra la remisión después de dicho tratamiento durante 4-8 semanas, se cambia la dosis inicial a una dosis diaria modificada de 4, 8 g de 5-ASA en forma de liberación controlada administrada como 2, 4 g dos veces al día durante hasta 8 semanas.
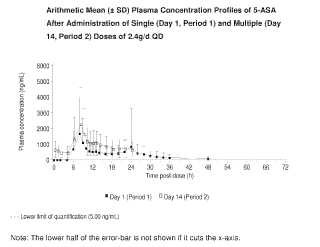
Las formulaciones útiles en el método de tratamiento de la presente invención exhiben un perfil de concentración en plasma in vivo con una sola dosis sustancialmente igual que el mostrado en la Figura 1, suministrando el 5-ASA en modo de liberación controlada.
Breve descripción de los dibujos La Figura 1 representa la media aritmética [± desviación típica (DT) ] de los perfiles de la concentración en plasma de 5-ASA después de administración de un sola dosis (día 1, período 1) y múltiples dosis (día 14, período 2) de 2, 4 g/día una vez al día de mesalamina MMX® en sujetos sanos normales. Los cuadrados en negro son los datos del día 1 (período 1) ; los cuadrados en blanco son los datos del día 14 (período 2) . La línea de trazo discontinuo representa el límite inferior de cuantificación (5, 00 ng/mL) . En el eje X se representa el tiempo después de la dosis en horas y en el eje Y la concentración en plasma en ng/mL.
La Figura 2 ilustra las concentraciones en plasma para formulaciones de liberación controlada de 5-ASA. Los círculos en blanco representan Asacol® (Norwich Eaton and Procter & Gamble) , 800 mg de 5- ASA; los cuadrados en blanco representan Asacol® (Norwich Eaton and Procter & Gamble) , 800 mg de 5-ASA; los rectángulos en blanco representan Colazol, balsalazida 2250 mg (Salix) (800 mg de 5-ASA) ; los triángulos en blanco representan Pentasa®, 1000 mg (Shire Pharmaceuticals) de 5-ASA; los triángulos invertidos en blanco representan 2000 mg de Salazopirina-EN, sulfasalazina (Watson Laboratories) (800 mg de 5-ASA) ; los círculos en negro representan 5-ASA MMX® (Lialda®, 2400 mg de 5-ASA) (Cosmo S.p.A. de Milán) ;y los cuadrados en negro representan MMX® (Lialda®, 4800 mg de 5-ASA) (Cosmo S.p.A. de Milán) . En el eje X se representa el tiempo después de la dosificación en horas y en el eje Y se representa la concentración en plasma de 5-ASA en ng/mL. Todos los niveles de concentración mostrados corresponden a tiempos posteriores a la administración de únicamente una sola dosis de medicación (es decir, después del día 1 de administración) .
Descripción detallada de la invención Definiciones Como se usan en la presente memoria, los siguientes términos tienen los significados dados a continuación:
Sujetos o pacientes se refiere a animales mamíferos que padecen la enfermedad intestinal inflamatoria, incluyendo los seres humanos pero sin limitarse a ellos.
Enfermedad intestinal inflamatoria se refiere a enfermedades intestinales incluyendo colitis ulcerosa (UC) (que a su vez incluye colitis ulcerosa de suave a moderada que tiene una puntuación de 4-10 en el índice de actividad de la enfermedad colitis ulcerosa (abreviadamente UC-DAI por la expresión inglesa UC-disease activity index) , con una puntuación sigmoidoscópica > 4 y una evaluación global del médico [Physician’s Global Assessment- (PGA) ] > 2) , síndrome de colon irritable y enfermedad de Crohn.
Las formas de liberación controlada de 5-ASA incluyen cualquier forma farmacéutica administrable por vía oral que exhiba un perfil de concentración en plasma in vivo para una sola dosis sustancialmente igual al mostrado en la Figura 1 y suministra el 5-ASA en un modo de liberación controlada. Se conocen en la técnica diversas formas de liberación controlada de 5-ASA, que incluyen Asacol® (Norwich Eaton and Procter & Gamble) , Colazol (Salix) , Balsalazida (Salix) , Pentasa® (Shire Pharmaceuticals) , salazopirina-EN, sulfasalazina (Watson Laboratories) y MMX® Lialda® (Cosmo S.p.A. de Milán)
Una forma de liberación controlada ilustrativa de mesalamina es mesalamina MMX (Multi Matrix System® (Lialda™, también conocida como Mezavant™ XL en el Reino Unido e Irlanda, y Mezavant™ en todas partes) , descrita en la patente de EE.UU. Nº 6.773.720 de Villa et al. Aunque no se requiere una dosis específica de mesalamina MMX®, una mesalamina MMX® ilustrativa es una composición farmacéutica para vía oral de liberación controlada con 1, 2 gramos de 5-ASA como ingrediente activo, que comprende un núcleo multi-matriz que consiste en una matriz lipófila y una matriz hidrófila en donde está dispersado el ingrediente activo. En la formulación ilustrativa, el ingrediente activo está presente en una cantidad mayor del 80%, generalmente 80-95%, en peso de la composición total.
La formulación de liberación controlada ilustrativa comprende: a) una matriz lipófila interna de ácido graso insaturado y/o hidrogenado, sus sales, ésteres o amidas,... [Seguir leyendo]
Reivindicaciones:
1. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria que comprende administrar una dosis diaria inicial de (i) 2, 4 g of 5-ASA en forma de liberación controlada, administrada como: una dosis de 1, 2 g dos veces al día; una dosis de 2, 4 g una vez al día; o una dosis de 0, 8 g tres veces al día, o (ii) 4, 8 g de 5-ASA en forma de liberación controlada, administrada como una dosis diaria una vez al día de 4, 8 g, y, en donde cuando no se logra la remisión después de dicho tratamiento durante 4-8 semanas, se cambia la dosis inicial a una dosis diaria modificada de 4, 8 g de 5-ASA en forma de liberación controlada administrada como 2, 4 g dos veces al día (BID) hasta 8 semanas.
2. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 1, en donde la enfermedad intestinal inflamatoria es colitis ulcerosa.
3. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 2, en donde la colitis ulcerosa es colitis ulcerosa de suave a moderada.
4. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 1, en donde la forma de liberación controlada de 5-ASA es mesalamina Multi Matrix System.
5. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 1, en donde la dosis diaria modificada se administra durante 8 semanas.
6. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 1, en donde la dosis diaria modificada se continúa hasta que se obtiene en el sujeto un índice de actividad de la enfermedad colitis ulcerosa (UC-DAI) de 1 o menos.
7. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 1, en donde la dosis diaria modificada se continúa hasta que se obtiene en el sujeto una puntuación de sigmoidoscopia de 1 o menos.
8. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 1, en donde la dosis diaria modificada se continúa hasta que se obtiene en el sujeto una evaluación global del médico (PGA) de 1 o menos.
9. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 1, en donde la dosis diaria modificada se continúa hasta que se obtiene en un sujeto una UC- DAI de 1 o menos, una puntuación de hemorragia rectal y de frecuencia de deposiciones de 0 y hay al menos una reducción de 1 punto en la puntuación de la sigmoidoscopia.
10. 5-ASA para uso en el tratamiento de la enfermedad intestinal inflamatoria de acuerdo con la reivindicación 9, en donde la dosis diaria modificada es 2, 4 g de 5-ASA administrada dos veces al día y se continúa hasta que se obtiene en el sujeto una puntuación combinada de evaluación global del médico y de sigmoidoscopia de 1 o menos y no se detecta en friabilidad de las mucosas.
Patentes similares o relacionadas:
 Hidrolizado de caseína para uso en el tratamiento de enfermedades inflamatorias, del 29 de Julio de 2020, de MJN U.S. Holdings, LLC: Una composición nutricional, que comprende un lípido o una fase grasa, una fuente de proteína y un hidrolizado de caseína para uso en el tratamiento […]
Hidrolizado de caseína para uso en el tratamiento de enfermedades inflamatorias, del 29 de Julio de 2020, de MJN U.S. Holdings, LLC: Una composición nutricional, que comprende un lípido o una fase grasa, una fuente de proteína y un hidrolizado de caseína para uso en el tratamiento […]
Aditivo para piensos, alimentos, agua potable o preparaciones farmacéuticas, del 20 de Julio de 2020, de ERBER AKTIENGESELLSCHAFT: Aditivo para piensos, alimentos, agua potable o preparaciones farmacéuticas, preparado a partir de al menos una especie de cornejo, en particular Cornus mas, Cornus officinalis, […]
Complemento alimenticio que comprende ácidos resínicos, del 15 de Julio de 2020, de HANKKIJA OY: Utilización no terapéutica de un complemento alimenticio que comprende una composición basada en ácido resínico que comprende más del 10 % (p/p) de ácidos […]
Cepa de Faecaslibacterium Prausnitzii CNCM I-4573 para el tratamiento y la prevención de una inflamación gastrointestinal, del 15 de Julio de 2020, de Institut national de recherche pour l'agriculture, l'alimentation et l'environnement: Cepa bacteriana de la especie Faecalibacterium prausnitzii depositada en la CNCM bajo el número de acceso CNCM I-4573, para su utilización en el tratamiento y/o la prevención […]
Antagonistas del receptor p2x7 derivados de N-[2-(4-fenoxipiperidin-1-il)-2-(1,3-tiazol-5-il)etil]benzamida y N-[2-(4-benciloxipiperidin-1-il)-2-(1,3-tiazol-5-il)etil]benzamida sustituidas, del 15 de Julio de 2020, de AXXAM S.P.A: Un compuesto de la siguiente fórmula (I) o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** incluyendo cualquier forma estereoquímicamente […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Compuestos utilizados como inhibidores de la quinasa reordenada durante la transfección (RET), del 1 de Julio de 2020, de GlaxoSmithKline Intellectual Property Development Limited: Un compuesto de acuerdo con la Fórmula (I), o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde: X es N o CR5; Y es un enlace; […]
Usos de composiciones de caseína, del 17 de Junio de 2020, de FONTERRA CO-OPERATIVE GROUP LIMITED: Uso de una composicion de caseina para aumentar la concentracion de leucina libre en suero sanguineo en un sujeto, en donde la composicion de caseina comprende o la caseina […]