Tratamiento de infecciones virales.
Un polipéptido de SEQ ID No. 2 o una de sus truncaciones, en donde uno o varios de los residuos de leucina (L) de SEQ ID No.
2 están reemplazados por triptófano (W), arginina (R) o lisina (K); en donde el polipéptido o una de sus truncaciones comprende 14-18 aminoácidos; y en donde el polipéptido tiene actividad antiviral
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2004/005360.
Solicitante: AI2 LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: MANCHESTER INCUBATOR BUILDING GRAFTON STREET MANCHESTER M13 9XX REINO UNIDO.
Inventor/es: DOBSON,CURTIS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/745 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Factores de coagulación sanguínea o de fibrinolisis.
PDF original: ES-2389078_T3.pdf
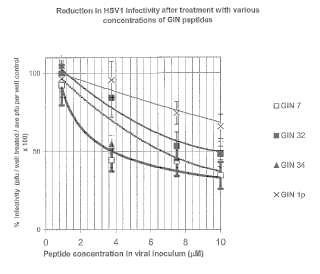
Fragmento de la descripción:
Tratamiento de infecciones virales
La presente invención se refiere a polipeptidos y a acidos nucleicos que los codifican con actividad antiviral. La invención tambien proporciona el uso de tales polipeptidos o acidos nucleicos como medicamentos.
Los agentes antivirales pueden dirigirse a uno de seis estadios del ciclo de replicación viral, siendo estos: 1. unión del virus con la celula; 2. penetración (o fusión de la membrana viral con la membrana celular) ; 3. ningun recubrimiento del virus; 4. replicación de los acidos nucleicos virales; 5. maduración de partfculas de virus de progenie; y 6. liberación del virus de progenie en fluidos extracelulares.
De estos seis estadios, la replicación (estadio 4 anterior) es el objeto, que es influenciado de la forma mas efectiva
por terapias antivirales convencionales. Sin embargo, la unión del virus con la celula es, sin duda, un objetivo mas atractivo, dado que el agente no necesita pasar a la celula huesped. Sin embargo, sigue siendo un area en la que se han desarrollado pocas terapias exitosas.
Por ello, un objeto de la presente invención consiste en proporcionar agentes terapeuticos que modulen la unión viral con las celulas.
Las lipoprotefnas (LPs) son complejos macromoleculares globulares presentes en suero y otros fluidos extracelulares, que consisten en lfpidos y protefnas y estan implicadas en el transporte de lfpidos alrededor del organismo. Fueron categorizadas de acuerdo con su densidad, siendo las clases principales la lipoprotefna de alta densidad (HDL) , lipoprotefna de baja densidad (LDL) y lipoprotefna de muy baja densidad (VLDL) . Sus protefnas se mencionan como apolipoprotefnas, y se ha descrito una cantidad de ellas, incluyendo apolipoprotefnas A, B, C, D, E,
F, G, H y J. Ademas, se han documentado varios subtipos de apolipoprotefnas A, B y C.
Se han descrito diversas interacciones que ligan las LPs con virus. Estas principalmente implican la unión de los virus con lipoprotefnas, lo cual da como resultado una menor inefectividad viral o, por el contrario, provee un metodo de transporte para que el virus ingrese en las celulas. Adicionalmente, diversos virus hacen uso de receptores celulares para LPs (por ejemplo, el receptor de LDL) como un medio de entrar en las celulas, a pesar de que estos 25 receptores tambien pueden ser liberados por celulas como agentes antivirales end6genos (por ejemplo, una forma soluble del receptor de VLDL es liberada en medio de cultivo por celulas HeLa e inhibe la infección por rinovirus humano) . Por otra parte, tambien se inform6 de la unión directa entre ciertas apolipoprotefnas y protefnas virales. Por ejemplo: a. la protefna nuclear de virus de hepatitis C se une con la apolipoprotefna All; b. el antfgeno de superficie del virus de hepatitis B se une con la apolipoprotefna H; y c. la protefna gp32 del virus de
inmunodeficiencia de simio (SlV) y la protefna gp41 del virus de inmunodeficiencia humana (HlV) se une con la apolipoprotefna A1.
El trabajo realizado en el laboratorio del inventor mostró que la presencia de virus herpes simplex latente de tipo 1 (HSV1) en el cerebro y la posición de un alelo particular de un gen específico -el alelo APOE-e4 del gen APOE- aumenta el riesgo de desarrollo de la enfermedad de Alzheimer (AD) . Tomados con el hallazgo adicional de que los 35 portadores de APOE-e4 sufran mas probablemente de herpes en la boca (que son lesiones halladas despues de la reactivación de HSV1 en el sistema nervioso periferico) , estos resultados sugirieron que es mas probable que los portadores de APOE-e4 padezcan de un dano por infecciones de HSV1 y sugieren que puede haber interacciones entre la apolipoprotefna E y ciertos virus (a pesar de que estas interacciones no necesariamente incluyen efectos antivirales) . Un posible modo de interacción entre HSV1 y apoE se refiere a los hallazgos independientes de que los
dos utilizan moleculas de proteoglucano de sulfato de heparano celular (HSPG) como su sitio inicial de unión con celulas, antes de la posterior unión con receptores secundarios que aumenta la posibilidad de que se produzca esa competencia en estos sitios de HSPG entre HSV1 y apoE con LPs, lo cual podría afectar la entrada viral.
Se mostró que la apolipoprotefna E tiene efectos sobre el sistema inmune (aparentemente, sin relación con su papel en el metabolismo de los lfpidos) incluyendo la supresión de la proliferación de linfocitos T. Se han examinado las 45 interacciones entre una cantidad de peptidos derivados de los residuos 130-169 de apoE con linfocitos (Clay et al., Biochemistr y , 34: 11142-11151 (1995) ) . Se pronostica que la región que consiste en residuos apoB 141-149 es particularmente importante. Se han descrito similares interacciones de tales peptidos en lfneas celulares neuronales.
El documento WO 94/04177 revela que la administración de partfculas que contienen peptidos helicoidales lipfdicos y anfipaticos permite la clearance de toxinas producida por microorganismos y puede incrementar la efectividad de
50 farmacos antibacterianos por medio de un efecto sobre las membranas bacterianas. Sin embargo, no se sugiere que este peptido derivado de apoA que contiene partfculas se pueda usar como medicamentos antivirales. Tampoco queda claro si la administración de los peptidos en partfculas que es un componente clave del desarrollo revelado (si las partfculas se forman antes de la administración o de forma end6gena) darfa como resultado la utilización efectiva de cualquier acción antiviral de cualquier componente de la partfcula.
55 Se mostró que un peptido helicoidal anfipatico derivado de apoA (descrito por Ananatharamiah en Meth. Enz., 128: 627-647 (1986) ) previene la fusión de membranas virales con membranas celulares y, por otra parte, previene la fusión de membranas de celulas infectadas (Srinivas et al. J. Cellular Biochem., 45: 224-237 (1991) ) . El peptido tambien era efectivo en la prevención de la fusión tanto para HSV1 como para HlV (Owens et al., J Clin. lnvest., 86: 1142-1150 (1990) ) . Sin embargo, el peptido no tuvo ningun efecto sobre la unión de HSV1 al menos con las celulas (Srinivas et al. supra) .
Azuma et al. informaron que los derivados peptfdicos de apoB tienen una fuerte acción antibacteriana, comparable con la de la gentamicina (Peptides, 21: 327-330 (2000) ) . ApoB 133-162 fue el mas efectivo, donde apoE 134-155 tenfa un efecto menor.
Owens et al. (1990, J. Clin lnvest Vol 86 (4) p1142-1150) revela que la apolipoprotefna A-1 y sus analogos peptfdicos helicoidales anfipaticos inhiben la formación del sincicio inducido por HlV. ltzhakl et al. (1998, Nature Medicine Vol 4 (12) p1344) trata interacciones entre Apo E y virus. Corder et al. (1998, Nature Medicine Vol 4 (10) p1182-1184) revela que los sujetos infectados con HlV con el alelo E4 para ApoE tienen demencia en exceso y neuropatfa periferica.
A la luz de la investigación descrita con anterioridad, el inventor realizó experimentos para evaluar si los peptidos derivados de ApoE (que son capaces de formar helices) tienen una actividad antiviral o no. Hall6 que una repetición en tandem de un fragmento peptfdico de ApoE, apoE141-149 (es decir, 2x LRKLRKRLL -SEQ lD No. 1) , tenfa de hecho una acción antiviral. Si bien el inventor no desea estar ligado a ninguna hip6tesis, cree que este fragmento evita la unión de partfculas virales a las celulas, dando como resultado una reducción de la infectividad de los virus medida por medio de una tecnica de ensayo de reducción de placas. El Ejemplo 1 ilustra cómo el peptido es efectivo contra virus tales como HSV1, HSV2 y HlV. Conforme a ello, este peptido puede ser efectivo cuando se aplica a virus directamente o cuando se aplica a virus en presencia de celulas y, por ello, el peptido se puede usar para inactivar partfculas sin virus hasta que alcancen sus celulas objeto.
A la luz de los datos generados para una repetición en tandem de apoE141-149 (es decir, 2x LRKLRKRLL-SEQ lD No. 1) , los inventores decidieron investigar otros fragmentos de apolipoprotefnas respecto de la actividad antiviral.
De acuerdo con un primer aspecto de la presente invención, se proporciona un polipeptido de SEQ lD No. 2 o una de sus truncaciones, en donde uno o varios de los residuos de leucina (L) de SEQ lD No. 2 estan reemplazados por tript6fano (W) , arginina (R) o lisina (K) ; en donde el polipeptido o una de sus truncaciones comprende 14-18 aminoacidos; y en donde el polipeptido tiene actividad antiviral.... [Seguir leyendo]
Reivindicaciones:
REIVINDICACIoNES
1. Un polipeptido de SEQ lD No. 2 o una de sus truncaciones, en donde uno o varios de los residuos de leucina
(L) de SEQ lD No. 2 estan reemplazados por tript6fano (W) , arginina (R) o lisina (K) ; en donde el polipeptido o una de sus truncaciones comprende 14-18 aminoacidos; y en donde el polipeptido tiene actividad antiviral.
2. El polipeptido de acuerdo con la reivindicación 1, en donde el aminoacido usado para reemplazar la leucina es tript6fano (W) .
3. El polipeptido de acuerdo con la reivindicación 1 o la reivindicación 2, en donde se realizan al menos dos sustituciones W, R o K.
4. El polipeptido de acuerdo con cualquiera de las reivindicaciones 1 a 3, en donde, ademas de al menos un residuo de leucina (L) , al menos otro aminoacido esta reemplazado por asparagina (N) , tirosina (Y) , cistefna (C) , metionina (M) , fenilalanina (F) , isoleucina (l) , glutamina (G) , histidina (H) o esta suprimido.
5. El polipeptido de acuerdo con cualquiera de las reivindicaciones 1 a 3 con la secuencia de aminoacidos: WRKWRKRWWWRKWRKRWW (SEQ lD No. 3) ; WRKWRKRWRKWRKR (SEQ lD No. 4) ; WRKWRKRWWLRKLRKRLL (SEQ lD No. 5) ; YRKYRKRYYYRKYRKRYY (SEQ lD No. 6) ; WRKWRKRWWRKWRKRWW (SEQ lD No. 52) ; WRKWRKRWRKWRKRW (SEQ lD No. 53) ; WRKWRKRWWFRKWRKRWW (SEQ lD No. 54) ; WRKWRKRWFFRKWRKRFF (SEQ lD No. 55) ; WRKCRKRCWWRKCRKRCW (SEQ lD No. 56) ; LRKLRKRLLWRKWRKRWW (SEQ lD No. 57) ; LRKLRKRLLLRKLRKRWW (SEQ lD No. 58) ; LRKLRKRLLWRKWRKRLL (SEQ lD No. 59) ; WRKWRKRLLLRKLRKRLL (SEQ lD No. 60) ; WRKLRKRLLLRKLRKRLL (SEQ lD No. 61) ; WRKWRKFFFRKWRKRWW (SEQ lD No. 62) ; WRKWRKRWWFRKFRKRFF (SEQ lD No. 63) ; RRKRRKRRRRRKRRKRRR (SEQ lD No. 64) ; o KRKKRKRKKKRKKRKRKK (SEQ lD No. 65) .
6. El polipeptido de acuerdo con cualquier reivindicación precedente, en donde se anade un aminoacido entre los aminoacidos 9 y 10 de la SEQ lD No 2.
7. El polipeptido de acuerdo con la reivindicación 6 que comprende WRKWRKRWWRWRKWRKRWWR (SEQ lD No. 66) .
8. Un polipeptido que comprende YRKYRKRYYYRKYRKRYY (SEQ lD No. 6) .
9. Un polipeptido que comprende LRKLRKRLLLRKLRK (SEQ lD No. 7) .
10. Un polipeptido que comprende LRKLRKRLRKLRKR (SEQ lD No. 8) .
11. Un polipeptido que comprende LRKLRKLRKLRKLRKLRK (SEQ lD No. 9) .
12. Un polipeptido de acuerdo con cualquier reivindicación precedente para usar como un medicamento.
13. El uso de un polipeptido de acuerdo con cualquiera de las reivindicaciones 1 a 11, en la fabricación de un medicamento para tratar infecciones virales.
14. Una secuencia de acidos nucleicos que codifica un polipeptido de acuerdo con cualquiera de las reivindicaciones 1 a 11.
15. Una secuencia de acidos nucleicos de acuerdo con la reivindicación 14 para usar como un medicamento.
Patentes similares o relacionadas:
Polipéptidos de unión a IL-17A, del 15 de Julio de 2020, de AFFIBODY AB: Polipéptido de unión a IL-17A, que comprende un motivo de unión BM a IL-17A, cuyo motivo consiste en una secuencia de aminoácidos seleccionada […]
Medios mejorados para la expresión de proteínas recombinantes dependientes de vitamina k, del 6 de Mayo de 2020, de CSL Behring Lengnau AG: Un procedimiento para mejorar la actividad de una proteína recombinante dependiente de vitamina K que comprende las siguientes etapas: a) proporcionar […]
Método para purificar y cuantificar la trombina y sus polipéptidos de degradación, del 25 de Marzo de 2020, de OMRIX BIOPHARMACEUTICALS LTD.: Un método cromatográfico de un solo paso para cuantificar α-trombina en una solución que comprende la α-trombina y al menos uno de un polipéptido de degradación […]
Direccionamiento de factores de coagulación al TLT-1 en plaquetas activadas, del 23 de Octubre de 2019, de NOVO NORDISK HEALTH CARE AG: Una proteína procoagulante que comprende (i) al menos un factor de coagulación, que es un polipéptido de FVII o un polipéptido de FIX, unido covalentemente […]
Sistemas de expresión específica de hígado optimizados para FVIII y FIX, del 23 de Octubre de 2019, de VRIJE UNIVERSITEIT BRUSSEL: Casete de expresión de ácido nucleico que comprende: - una repetición triple dispuesta en tándem de un elemento regulador de ácido nucleico específico de hígado, consistiendo […]
Composición y apósito para tratamiento de heridas, del 14 de Agosto de 2019, de Protege Biomedical, LLC: Una composición para la curación de heridas, que comprende: una mezcla sustancialmente homogénea que comprende una cantidad de mullita, en la que la cantidad de mullita es efectiva […]
 Activación de factor X, del 31 de Julio de 2019, de Baxalta Incorporated: Método para activar el factor de coagulación X (FX) que comprende;
a) poner en contacto una disolución acuosa que comprende FX con un material de […]
Activación de factor X, del 31 de Julio de 2019, de Baxalta Incorporated: Método para activar el factor de coagulación X (FX) que comprende;
a) poner en contacto una disolución acuosa que comprende FX con un material de […]
Métodos y composiciones para proteínas del factor IX modificadas, del 19 de Junio de 2019, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Una proteína del Factor IX (FIX) aislada que comprende la secuencia de aminoácidos como se expone en la SEQ ID NO: 3, en donde Xaa es leucina.