Proteinas termoestables y procedimientos de obtención y uso de las mismas.
Una proteína de unión de glucosa-galactosa termoestable (GGBP) que es una proteína GGBP de la SEC ID NO:
4que comprende las substituciones N39I, G82E, Q83K, N84D, Q175E, Q177H, L178M, N259E y N260S, y que tieneuna temperatura de fusión superior que la GGBP de la SEC ID NO:4.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/067154.
Solicitante: BECTON, DICKINSON AND COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1 BECTON DRIVE FRANKLIN LAKES, NJ 07417 ESTADOS UNIDOS DE AMERICA.
Inventor/es: AMISS,TERRY, GILL,ERIN, SHERMAN,DOUGLAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C30B29/58 QUIMICA; METALURGIA. › C30 CRECIMIENTO DE CRISTALES. › C30B CRECIMIENTO DE MONOCRISTALES (por sobrepresión, p. ej. para la formación de diamantes B01J 3/06 ); SOLIDIFICACION UNIDIRECCIONAL DE MATERIALES EUTECTICOS O SEPARACION UNIDIRECCIONAL DE MATERIALES EUTECTOIDES; AFINAMIENTO DE MATERIALES POR FUSION DE ZONA (afinamiento por fusión de zona de metales o aleaciones C22B ); PRODUCCION DE MATERIALES POLICRISTALINOS HOMOGENEOS DE ESTRUCTURA DETERMINADA (colada de metales, colada de otras sustancias por los mismos procedimientos o aparatos B22D; trabajo de materias plásticas B29; modificación de la estructura física de metales o aleaciones C21D, C22F ); MONOCRISTALES O MATERIALES POLICRISTALINOS HOMOGENEOS DE ESTRUCTURA DETERMINADA; TRATAMIENTO POSTERIOR DE MONOCRISTALES O DE MATERIALES POLICRISTALINOS HOMOGENEOS DE ESTRUCTURA DETERMINADA (para la fabricación de dispositivos semiconductores o de sus partes constitutivas H01L ); APARATOS PARA ESTOS EFECTOS. › C30B 29/00 Monocristales o materiales policristalinos homogéneos de estructura determinada caracterizados por los materiales o por su forma. › Compuestos macromoleculares.
PDF original: ES-2391908_T3.pdf
Fragmento de la descripción:
Proteínas termoestables y procedimientos de obtención y uso de las mismas
Antecedentes de la invención
Campo de la invención
La presente invención se refiere a proteínas de unión de glucosa-galactosa modificadas (GGBPs) , funcionales, que tienen una temperatura de fusión (Tm) mayor que una GGBP de referencia. La presente invención se refiere igualmente a ácidos nucleicos que codifican estas GGBPs termoestables, así como a procedimientos de uso de estas GGBPs termoestables.
Antecedentes de la invención
Un área de rápido avance en el desarrollo de biosensores es el uso de proteínas de unión periplásmicas (PBPs) , para determinar con exactitud concentraciones de analito, por ejemplo, glucosa, en muestras biológicas. En particular, las proteínas de unión de glucosa-galactosa (GGBPs) están siendo usadas como biosensores para medir cantidades de analito en escenarios fisiológicos farmacológicos e industriales. Las PBPs se consideran que son “no reactivos” y pueden usarse en una diversidad de escenarios incluyendo la medición de glucosa en la monitorización de la diabetes, medición de aminoácidos en otras enfermedades metabólicas, tal como deficiencia de histidasa, así como la medición de arabinosa durante la producción de etanol a partir de maíz. Sin embargo, las GGPBs de tipo salvaje, no pueden ser los candidatos los más ideales para la medición o determinación de concentraciones de analito por una diversidad de razones. Los biosensores que comprenden GGBPs tendrían que ser preferiblemente físicamente estables bajo las condiciones de uso para generar una señal cuantificable durante la unión de la glucosa. Cuando el fin deseado es monitorizar in vivo las concentraciones de glucosa en diabéticos, las proteínas tendrían que ser preferiblemente estables a las temperaturas fisiológicas. Adicionalmente, las GGBPs deberían tener preferiblemente estabilidad potenciada en la fabricación, transporte y almacenamiento del sensor, que pudiera potencialmente facilitar y posibilitar el fabricar a temperatura ambiente la proteína y los materiales sensores. Este procedimiento de fabricación podría incluir procedimientos de esterilización a alta temperatura para uso en un escenario clínico. Sin embargo, la exposición a altas temperaturas puede desnaturalizar la proteína, volviendo inservibles a las GGBPs para su fin deseado. De acuerdo con ello, existe una necesidad de GGBPs que sean capaces de resistir temperaturas superiores al mismo tiempo que se mantengan activas, de manera tal que puedan unirse el analito y usarse en biosensores en una diversidad de escenarios de temperatura superior.
Sumario de la invención
La presente invención se refiere a una proteína de unión de glucosa-galactosa modificada (GGBPs) , funcional, que es una proteína GGBP de la SEC ID NO:4, que comprende las substituciones N39I, G82E, Q83K, N84D, Q175E, Q177H, L178M, N259E y N260S, y que tiene una temperatura de fusión superior que la GGBP de la SEC ID N:4 que tiene una temperatura de fusión (Tm) mayor que una GGBP de referencia de la SEC ID NO:4.
La presente invención se refiere igualmente a ácidos nucleicos que codifican GGBPs termoestables.
La presente invención se refiere igualmente a GGBPs modificadas, funcionales, en las que la GGBP modificada, funcional, tiene una temperatura de fusión mayor que una GGBP de referencia y en la que la GGBP modificada comprende además al menos un marcador.
Breve descripción de las secuencias en el Listado de Secuencias
La SEC ID NO:1 es la secuencia de aminoácidos de GGBP (E. coli) de tipo salvaje (GenBank Acceso No. 2GBP) .
La SEC ID NO:2 es la secuencia de aminoácidos de GGBP (E. coli) de tipo salvaje (GenBank Acceso No. POAEE5) .
La SEC ID NO:3 es la secuencia de aminoácidos de 3M-GGBP, la cual tiene las substituciones de restos siguientes en comparación con la GGBP de tipo salvaje (SEC ID NO:1) : E149C, A213R, y L238S.
La SEC ID NO:4 es la secuencia de aminoácidos de W183C-GGBP, la cual tiene una substitución del resto W183C en comparación con la GGBP de tipo salvaje.
La SEC ID NO:5 es el aminoácido de un aminoácido etiqueta, útil para la purificación de péptidos, que puede agregarse a la N’-terminación de un polipéptido de interés.
La SEC ID NO:6 es el aminoácido de un aminoácido etiqueta, útil para la purificación de péptidos, que puede agregarse a la C’-terminación de un polipéptido de interés.
Breve descripción de los dibujos
La FIGURA 1 representa las curvas de estabilidad térmica de una proteína GGBP de referencia y de dos GGBPs termoestables modificadas.
La FIGURA 2 representa el espectro de emisión de la 3M-GGBP termoestable modificada en concentraciones crecientes de glucosa.
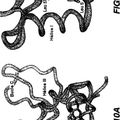
La FIGURA 3 representa aminoácidos representativos que pueden ser dirigidos para substitución.
Descripción detallada de la invención
La presente invención se refiere a una proteína de unión periplásmica modificada, funcional (GGBPs) , que es una proteína GGBP de la SEC ID NO:4, que comprende las substituciones N39I, G82E, Q83K, N84D, Q175E, Q177H, L178M, N259E y N260S, y que tiene una temperatura de fusión superior que la GGBP de la SEC ID N:4 que tiene una temperatura de fusión (Tm) mayor que una GGBP de referencia de la SEC ID NO:4.
La proteína de unión de glucosa-galactosa es un elemento de la clase bien conocida de proteínas de unión periplásmicas, en el que estas proteínas se caracterizan por su configuración tridimensional (estructura terciaria) , en lugar de por la secuencia de aminoácidos (estructura primaria) de la proteína. Cada elemento de la clase posee un motivo lóbulo-bisagra-lóbulo característico. Véase Dwyer, M.A. y Hellinga, H.W., Curr. Opin. Struc. Biol., vol. 14, págs. 495-504, (2004) . Normalmente, las PBPs se unirán a un analito específicamente en la región de hendidura entre los lóbulos de la PBP. Además, la unión de un analito en la región de hendidura dará lugar posteriormente a un cambio en la conformación de la PBP que permite que sea posible la detección del analito. En general, los cambios en la conformación de la PBP tras la unión al analito específico se caracterizan por las dos regiones lóbulo que se pliegan una con dirección a la otra alrededor y a través de la región bisagra. Véase Quiocho, F.A. y Ledvina, P.S., Mol. Microbiol., vol. 20, págs. 17-25, (1996) . Los ejemplos de PBPs incluyen proteína de unión de glucosa-galactosa (GGBP) , proteína de unión de maltosa (MBP) , proteína de unión de ribosa (RBP) , proteína de unión de arabinosa (ABP) , proteína de unión de dipéptido (DPBP) , proteína de unión de glutamato (GluBP) , proteína de unión de hierro (FeBP) , proteína de unión de histidina (HBP) , proteína de unión de fosfato (PhosBP) , proteína de unión de glutamina (QBP) , proteína de unión de leucina (LBP) , proteína de unión de leucina-isoleucina-valina (LIVBP) , proteína de unión de oligopéptido (OppA) , o derivados de las mismas, así como otras proteínas que pertenecen a las familias de proteínas conocidas como proteína de unión periplásmica tipo I (PBP-tipo I) y proteína de unión periplásmica tipo II (PBP-tipo II) .
Para los fines de la presente invención, una proteína de unión de glucosa-galactosa (GGBP) incluye cualquier proteína que posea estas características estructurales descritas en la presente invención y que pueda unirse específicamente a glucosa y/o galactosa.
En particular, la invención se refiere a la modificación de GGPBs. Una ”proteína modificada” se usa para indicar que una proteína puede crearse por substitución de uno o más aminoácidos en la estructura primaria (secuencia de aminoácidos) de una proteína o polipéptido de referencia. Los términos “proteína” y “polipéptido” se usan de manera intercambiable en la presente invención. La proteína de referencia no necesita ser una proteína de tipo salvaje, sino que puede ser cualquier proteína que esté dirigida para modificación para los fines de incrementar la estabilidad térmica. De acuerdo con ello, la proteína de referencia puede ser una proteína cuya secuencia haya sido previamente modificada con respecto a la proteína de tipo salvaje. Por supuesto, la proteína de referencia puede ser o no la proteína de tipo salvaje procedente de un organismo particular. Además, el término... [Seguir leyendo]
Reivindicaciones:
1. Una proteína de unión de glucosa-galactosa termoestable (GGBP) que es una proteína GGBP de la SEC ID NO:4 que comprende las substituciones N39I, G82E, Q83K, N84D, Q175E, Q177H, L178M, N259E y N260S, y que tiene una temperatura de fusión superior que la GGBP de la SEC ID NO:4.
2. Un biosensor para la medición de un analito, comprendiendo dicho biosensor la GGPB termoestable modificada de la reivindicación 1.
3. El biosensor de la reivindicación 2, en el que dicha GGBP termoestable comprende además al menos un marcador seleccionado entre el grupo que consiste en un marcador fluorescente, un radio-marcador, un marcador quimioluminiscente, un marcador fosforescente, un marcador colorimétrico y un marcador difusor de raman de superficie
potenciada.
4. El biosensor de la reivindicación 2 ó 3, en el que dicha GGBP termoestable está ocluida en una matriz polímera.
5. Un procedimiento de medición de la concentración de un analito en una muestra, comprendiendo dicho procedimiento la puesta en contacto del biosensor de las reivindicaciones 2 a 4 con dicha muestra.
6. Un dispositivo que comprende el biosensor de una cualquiera de las reivindicaciones 2 a 4, en el que dicha GGBP 15 termoestable está en proximidad óptica con un conducto óptico.
7. Un ácido nucleico aislado que codifica la GGBP termoestable modificada de la reivindicación 1.
8. Un vector que comprende el ácido nucleico de la reivindicación 7.
9. Una célula huésped que comprende el vector de la reivindicación 8.
10. Un procedimiento de obtención de la GGBP termoestable de la reivindicación 1, comprendiendo dicho procedi
miento el cultivo de la célula huésped de la reivindicación 9 en condiciones adecuadas para la expresión de proteína y el aislamiento de dicha proteína.
FIGURA 1
Temperatura (ºC)
FIGURA 2
Emisión (nm)
FIGURA 3
Patentes similares o relacionadas:
Cristal de compuesto de alquinilo de benceno 3,5-disustituido, del 24 de Junio de 2020, de TAIHO PHARMACEUTICAL CO., LTD.: Un cristal de (S)-1-(3-(4-amino-3-((3,5-dimetoxifenil)etinil)-1H-pirazolo[3,4-d]pirimidin-1-il)-1-pirrolidinilo)-2-propen- 1-ona, exhibiendo el cristal un espectro de difracción […]
Celulosa nanocristalina seca redispersable, del 18 de Febrero de 2015, de FPINNOVATIONS: Una H-NCC en forma sólida seca, dispersable en agua, que tiene un contenido de humedad inicial de al menos el 4 % en peso.
PROCEDIMIENTO PARA EL CHEQUEO DE CONDICIONES DE CRISTALIZACION DE MACROMOLECULAS BIOLOGICAS, del 1 de Agosto de 2007, de CONSEJO SUPERIOR INVESTIG. CIENTIFICAS: Procedimiento para el chequeo en condiciones de cristalización de macromoléculas biológicas.#El objeto de la presente invención es un procedimiento […]
CRISTALES DE GERMINACION PARA LA PREPARACION DE PEPTIDOS O PROTEINAS., del 1 de Mayo de 2007, de NOVO NORDISK A/S: Método de producción de microcristales de germinación para producir un péptido o proteína, donde el péptido o proteína es seleccionado del grupo compuesto de insulina […]
PROTEINAS FLUORESCENTES MODIFICADAS GENETICAMENTE DE LONGITUD DE ONDA LARGA., del 1 de Junio de 2006, de THE STATE OF OREGON ACTING BY AND THROUGH THE STATE BOARD OF HIGHER EDUCATION ON BEHALF OF THE UN: Molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína fluorescente funcional modificada genéticamente cuya […]
RECEPTOR HUMANO DE CISTENIL LEUCOTRIENO 2(CYSLT2)., del 1 de Marzo de 2006, de PFIZER LIMITED PFIZER INC.: Un polinucleótido aislado y/o purificado que consiste en uno o más de: (a) un polinucleótido que consiste en una secuencia de nucleótidos de la SEC […]
PROCEDIMIENTO DE CRISTALIZACION DE MACROMOLECULAS BIOLOGICAS MEDIANTE EL USO DE GELES DE ELECTROFORESIS., del 16 de Septiembre de 2004, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Procedimiento de cristalización de macromoléculas biológicas mediante el uso de geles de electroforesis. La presente invención se refiere a un procedimiento […]
 METODOS PARA IDENTIFICAR AGONISTAS INDIRECTOS DE IGF-1, del 22 de Diciembre de 2009, de GENENTECH, INC.: Un método para identificar agonistas indirectos del IGF-1 que comprende las etapas de:
(a) la determinación de la capacidad de N,N-bis-(3-D-gluconamidopropil)-desoxicolamina […]
METODOS PARA IDENTIFICAR AGONISTAS INDIRECTOS DE IGF-1, del 22 de Diciembre de 2009, de GENENTECH, INC.: Un método para identificar agonistas indirectos del IGF-1 que comprende las etapas de:
(a) la determinación de la capacidad de N,N-bis-(3-D-gluconamidopropil)-desoxicolamina […]