SOPORTE DE BIOSENSOR.
Soporte de biosensor, que consta de un cilindro (1) de material no-conductor de la electricidad,
que dispone un orificio (2) pasante coaxial con el eje del cilindro (1); una varilla de metal (3) dispuesta en dicho orificio (2) con su extremo superior (31) al ras de la base superior (11) del cilindro (1); una capa/recubrimiento de metal noble (4), de entre 1 a 1000 nanómetros, dispuesta sobre dicha base superior (11) y un protector (5) de un material no-conductor de la electricidad dispuesto sobre la capa/recubrimiento de metal noble (4) en la zona de conjunción de dicha capa (4) con la varilla de metal (3) y recubriendo una superficie de diámetro () mayor que el diámetro de la varilla (3).De aplicación para la detección específica de sustancias en medios acuosos
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200802126.
Solicitante: BIOLAN MICROBIOSENSORES, S.L.
Nacionalidad solicitante: España.
Provincia: VIZCAYA.
Inventor/es: ARQUERO CAVIA,DANIEL, ALBIZU LLUVIA,ASIER.
Fecha de Solicitud: 11 de Julio de 2008.
Fecha de Publicación: .
Fecha de Concesión: 17 de Diciembre de 2010.
Clasificación Internacional de Patentes:
- C12Q1/25 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen enzimas que no pueden ser clasificarsse en los grupos C12Q 1/26 - C12Q 1/70.
- G01N27/30 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 27/00 Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R). › Electrodos, p. ej. electrodos para el análisis; Semicélulas (G01N 27/414 tiene prioridad).
Clasificación PCT:
- C12Q1/25 C12Q 1/00 […] › en los que intervienen enzimas que no pueden ser clasificarsse en los grupos C12Q 1/26 - C12Q 1/70.
- G01N27/30 G01N 27/00 […] › Electrodos, p. ej. electrodos para el análisis; Semicélulas (G01N 27/414 tiene prioridad).
- G01N27/327 G01N 27/00 […] › Electrodos bioquímicos.
Fragmento de la descripción:
Soporte de biosensor.
La presente invención se basa en un dispositivo que sirve de base para la colocación de una sustancia enzimática u otra de cualquier índole con la finalidad de crear un biosensor para la detección específica de sustancias en medios acuosos.
En el estado de la técnica ya se conocen soportes similares, pero están basados en láminas macizas, preferiblemente circulares, de oro, carbón o platino. Dichas láminas están fabricadas de metal puro con un espesor de uno o varios milímetros. La parte exterior, donde se depositan las enzimas, está pulida y está al mismo nivel que el cilindro de plástico que lo aloja. En la parte interior de dicho cilindro de plástico, en la cara interna de la lámina de metal, se coloca normalmente una resistencia construida con carbón en polvo prensado. La impedancia típica de este carbón en polvo suele ser inferior a una decena de ohmnios. A continuación de este carbón prensado, se coloca una varilla de latón preferiblemente para que, una vez asome por el extremo opuesto a la lámina de oro, a través del cilindro de plástico que lo aloja, pueda recibirse la señal eléctrica procedente de la enzima depositada sobre la lámina.
La lámina, preferiblemente de oro, tiene un diámetro comprendido entre 3 y 6 mm.
Este tipo de soportes para la construcción de biosensores, tiene el inconveniente de que la señal eléctrica proveniente de la reacción química de la enzima es muy baja. Las pruebas hechas con enzimas, preferiblemente gluconasa, para la determinación del ácido glucónico, demostraron que para una lámina de 3 mm de diámetro y 0,1 mm de espesor, la respuesta a la enzima era de apenas 5 nanoamperios.
Aumentando el diámetro de la lámina de oro a 5 mm de diámetro, apenas se incrementó la señal otros 2 nanoamperios.
El biosensor así construido, una vez introducido en el circuito electrónico potenciostático, presenta problemas de medición por la muy baja señal de respuesta eléctrica de la enzima y además, un aumento de la temperatura del medio acuoso donde se realiza la medición falsea los datos al variar aproximadamente 2 nanoamperios por cada grado centígrado. Esto obliga a mantener rigurosamente el medio acuoso a una temperatura lo más constante posible.
La presente invención soluciona este problema de respuesta baja de señal de la enzima en presencia de la sustancia química para la que se ha diseñado. De igual forma, es válido para cualquier sustancia enzimática, pues la alta respuesta a la señal procede principalmente de la forma en que está construido el soporte objeto de esta patente.
Las sustancias enzimáticas necesitan un metal noble o carbón, donde colocarse para dar una respuesta a la sustancia para la que se diseñó. Este soporte, preferentemente de oro, no puede conectarse directamente mediante un cable o varilla conductora de electricidad al circuito electrónico potenciostático. Se debe colocar una impedancia que, en los sensores comerciales hasta el momento, está realizado mediante carbón prensado. Este carbón tiene que estar en contacto directo a la lámina, principalmente de oro, y no puede colocarse una resistencia electrónica convencional. Pero como la lámina de oro donde se deposita la encima es perfectamente conductora de la electricidad, por lo que la señal electrónica que produce la enzima es enmascarada frente a la alta señal parásita o de base generada por el circuito electrónico potenciostático.
El soporte de biosensor objeto del invento se caracteriza porque consta de:
- un cilindro de material no-conductor de la electricidad, que dispone un orificio pasante coaxial con el eje del cilindro
- una varilla de metal, dispuesta en dicho orificio con su extremo superior al ras de la base superior del cilindro
- una capa/recubrimiento de metal noble, de entre 1 a 1000 nanómetros, dispuesta sobre dicha base superior
- un protector de un material no-conductor de la electricidad, dispuesto sobre la capa/recubrimiento de metal noble en la zona de conjunción de dicha capa con la varilla de metal y recubriendo una superficie de diámetro mayor que el diámetro de la varilla.
La presente invención resuelve el problema de la baja señal que entrega la encima depositada sobre el soporte del biosensor a la presencia de la sustancia química para la que se diseñó. Además, reduce enormemente la señal parásita o de línea base generada por el circuito electrónico potenciostático. Debido a la topología aplicada para su manufacturado, el precio de fabricación es unas 300 veces menor que lo que hay en el mercado actualmente. La señal eléctrica que entrega la enzima es unas 30 veces superior a cualquier soporte actual para biosensores, pudiéndose aumentar de forma exponencial aumentando su diámetro.
El presente soporte para biosensores está orientado a un solo uso. Una vez agotada la función de la enzima, éste se desecha.
Para comprender mejor el objeto de la presente invención, se representa en los planos una forma preferente de realización práctica, susceptible de cambios accesorios que no desvirtúen su fundamento.
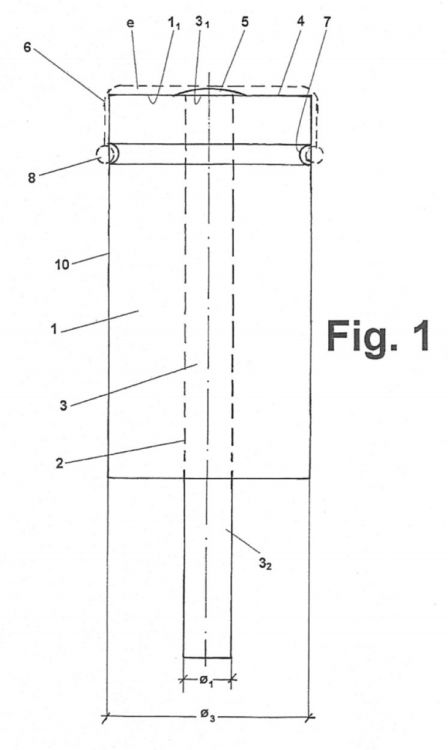
La figura 1 es una vista esquemática en alzado del biosensor objeto del invento.
La figura 2 es una vista en sección y muy ampliada de la zona de conjunción varilla (3)/capa de metal noble (4).
Se describe a continuación un ejemplo de realización práctica, no limitativa, del presente invento.
El soporte del biosensor comprende un cilindro (1) de plástico, preferiblemente policloruro de vinilo, con un orificio pasante (2) en su centro, haciendo de éste un tubo. El diámetro del cilindro (1) puede ser de cualquier diámetro (
Dicha varilla de metal (3) debe ser de un diámetro (
El extremo superior (31) de esta varilla de latón (3) se deja al ras del cilindro de plástico (1) y por el otro extremo (32) de deja asomar unos 5 mm o cualquier otra medida para su posterior amarre al circuito electrónico potencios- tático.
La zona del cilindro de plástico (1) donde la varilla de latón (3) se ha dejado al ras está refrendada/pulida. Para ello se empleará preferiblemente una máquina herramienta tal como un torno de revolución a baja velocidad para no fundir el cilindro de plástico con la fricción. La superficie así pulida debe quedar lo más lisa posible y sin quemar el plástico en el mecanizado debido a un exceso de velocidad de la máquina herramienta de torneado o pulido.
A su vez, en el cilindro de plástico (1) en su superficie lateral (10) y a una distancia preferiblemente de 2 mm desde el borde superior de la zona pulida, se practica una hendidura (7) en forma toroidal a modo de sujeción futura de una junta (8) de goma tórica para amarrar una membrana (6) permeable u osmótica como las utilizadas en diálisis.
Una vez torneado y preparado el soporte del biosensor, se le da una capa de oro de entre 1 y 1000 nanómetros, siendo preferiblemente de entre 30 y 100 nanómetros, en función del comportamiento de otras enzimas en cuanto a la respuesta de generación del flujo de electrones o corriente eléctrica frente a la presencia de la sustancia para la que ha sido diseñada. Este baño de oro se aplica mediante sputtering a través de un equipo comercial para tal fin.
Mediante este recubrimiento se hace conductora de electricidad toda la zona pulida del cilindro de plástico (1) más la varilla de latón (3).
Este oro, al ser una capa tan delgada, del orden de nanómetros, presenta una impedancia al paso de la corriente eléctrica que puede ser de unos 10 ohmnios desde la periferia hasta su centro.
La zona bañada de oro problemática es la del centro del cilindro de plástico (1), justo la zona donde está la varilla...
Reivindicaciones:
1. Soporte de biosensor, caracterizado porque consta de:
2. Soporte de biosensor, según reivindicación 1, caracterizado porque el cilindro (1) de material no-conductor dispone en su superficie lateral (10) de medios de sujeción de una membrana (6).
3. Soporte de biosensor, según reivindicación 1, caracterizado porque la capa/recubrimiento (4) es de oro con un espesor de entre 30 y 100 nanómetros.
4. Soporte de biosensor, según reivindicación 2, caracterizado porque la membrana 6 puede ser una membrana permeable o una membrana permeable líquida.
5. Soporte de biosensor, según reivindicación 1, caracterizado porque el protector (5) es una gota de una resina adherente a la capa/recubrimiento de metal noble (4).
Patentes similares o relacionadas:
Métodos para determinar el estado de carga y calibrar los electrodos de referencia en una batería de flujo redox, del 17 de Junio de 2020, de Lockheed Martin Energy, LLC: Un metodo para determinar el estado de carga de una semicelda dentro de una bateria de flujo redox que comprende un electrolito, comprendiendo dicho metodo: medir la tasa […]
PROCEDIMIENTO DE DETECCIÓN Y DETERMINACIÓN DE ION CLORURO EN MUESTRAS LÍQUIDAS, del 20 de Septiembre de 2019, de UNIVERSIDAD DE BURGOS: Procedimiento de determinación de ion cloruro que comprende el uso de un sensor constituido por tres electrodos, incluyendo cada electrodo […]
Método para determinar el bajo nivel de llenado en un biosensor electroquímico y sistema de detección de bajo nivel de llenado, del 28 de Agosto de 2019, de Ascensia Diabetes Care Holdings AG: Un método para detectar una condición de bajo nivel de llenado en un biosensor electroquímico, que comprende: aplicar una señal de excitación de prueba en forma […]
Procedimiento de determinación de un factor de escala para una salida de una célula electroquímica, del 26 de Junio de 2019, de F. HOFFMANN-LA ROCHE AG: Un procedimiento de determinación de un factor de escala (F) para poner en escala una salida de un sensor que comprende una primera célula electroquímica […]
Método de detección electroquímica, del 12 de Junio de 2019, de NANOCYL S.A: Método de detección de al menos un vapor de analito químico en un entorno gaseoso que comprende las etapas de: - proporcionar un sensor electroquímico basado […]
Sistema de análisis de biosensor electroquímico, del 22 de Abril de 2019, de F. HOFFMANN-LA ROCHE AG: Sistema de análisis de biosensor electroquímico para el análisis de un líquido de muestra, en particular de un líquido corporal, comprendiendo […]
Procedimiento de medición y monitorización in situ de la conductividad en sistemas acuosos de alta temperatura, del 4 de Marzo de 2019, de Baker Hughes, a GE company, LLC: Un procedimiento de monitorización de la conductividad en tiempo real en un sistema de generación de vapor sin interrupción del sistema de generación de vapor, […]
 Electrodo de referencia potenciométrico con membrana heterogénea, del 31 de Octubre de 2018, de SIEMENS HEALTHCARE DIAGNOSTICS INC.: Un electrodo de referencia potenciométrico para uso en un análisis electroquímico de una muestra acuosa, que comprende
un conductor eléctrico;
una capa […]
Electrodo de referencia potenciométrico con membrana heterogénea, del 31 de Octubre de 2018, de SIEMENS HEALTHCARE DIAGNOSTICS INC.: Un electrodo de referencia potenciométrico para uso en un análisis electroquímico de una muestra acuosa, que comprende
un conductor eléctrico;
una capa […]