ARCILLAS PILAREADAS CON CAPACIDAD DE ADSORCION DE HIDROGENO MEJORADA Y PROCEDIMIENTO DE OBTENCION DE LAS MISMAS.
Arcillas pilareadas con capacidad de adsorción de hidrógeno mejorada y procedimiento de obtención de las mismas.
Las arcillas de la invención son esmectitas pilareadas que se preparan poniendo en contacto una esmectita, preferiblemente montmorillonita sódica, con una disolución intercalante que contiene un polihidroxicatión de aluminio de manera que la relación entre la concentración de Al{sup,3+} contenido en la disolución intercalante y los gramos de arcilla está comprendida en el rango de 10 mmolar Al/g{sub,arcilla} a 150 mmolar Al/g{sub,arcilla}, separando la esmectita de la disolución acuosa y calentándola para formar Al{sub,2}O{sub,3}. Este procedimiento permite obtener arcillas pilareadas preparadas mediante intercalación de polihidroxicationes de aluminio y con adsorción de hidrógeno mejorada sin introducir en la estructura de la arcilla compuestos de carácter orgánico y/u otros metales adicionales al aluminio y los propios de la arcilla. Por ello, el uso de estas arcillaspilareadas para adsorber hidrógeno es también parte de la invención
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200702087.
Solicitante: UNIVERSIDAD PUBLICA DE NAVARRA.
Nacionalidad solicitante: España.
Provincia: NAVARRA.
Inventor/es: GIL BRAVO,ANTONIO, KORILI,SOPHIA.
Fecha de Solicitud: 26 de Julio de 2007.
Fecha de Publicación: .
Fecha de Concesión: 13 de Enero de 2010.
Clasificación Internacional de Patentes:
- B01J20/12 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 20/00 Composiciones absorbentes o adsorbentes sólidas o composiciones que facilitan la filtración; Absorbentes o adsorbentes para cromatografía; Procedimientos para su preparación, regeneración o reactivación. › Arcillas de origen natural o tierras decolorantes.
- B01J29/02C
- C01B3/50G
- C01B33/40 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01B ELEMENTOS NO METALICOS; SUS COMPUESTOS (procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01B 33/00 Silicio; Sus compuestos (C01B 21/00, C01B 23/00 tienen prioridad; persilicatos C01B 15/14; carburos C01B 32/956). › Arcillas.
Clasificación PCT:
- B01J20/12 B01J 20/00 […] › Arcillas de origen natural o tierras decolorantes.
- B01J29/04 B01J […] › B01J 29/00 Catalizadores que contienen tamices moleculares. › que tienen propiedades de intercambiadores de base, p. ej. zeolitas cristalinas, arcillas puenteadas.
- C01B3/56 C01B […] › C01B 3/00 Hidrógeno; Mezclas gaseosas que contienen hidrógeno; Separación del hidrógeno a partir de mezclas que lo contienen; Purificación del hidrógeno (producción de gas de agua o gas de síntesis a partir de materias carbonosas sólidas C10J). › por contacto con sólidos; Regeneración de los sólidos usados.
- C01B33/40 C01B 33/00 […] › Arcillas.
Fragmento de la descripción:
Arcillas pilareadas con capacidad de adsorción de hidrógeno mejorada y procedimiento de obtención de las mismas.
Campo técnico
La presente invención se refiere a materiales basados en arcillas pilareadas con capacidad mejorada de almacenamiento de hidrógeno mediante adsorción física, así como a su procedimiento de obtención y al uso de las mismas para el almacenamiento de hidrógeno mediante adsorción física.
Antecedentes de la invención
El hidrógeno se ha ido convirtiendo en una atractiva fuente de energía por diversas razones, entre las que se pueden citar su alta densidad de energía por unidad de peso o el hecho de que se puede producir fácilmente mediante la electrolisis del agua. Debido a su alta volatilidad, el almacenamiento de hidrógeno está siendo un problema para su aprovechamiento como fuente de energía. Y, sin embargo, el almacenamiento de hidrógeno es un proceso clave para el cambio, por ejemplo, de los motores convencionales de combustión interna a celdas de combustible de hidrógeno como fuente de energía en los automóviles.
El hidrógeno puede almacenarse presurizado, licuado, absorbido en metales (como hidruros) y fisisorbido (mantenido mediante interacciones físicas) en materiales adecuados [1]. El principal inconveniente del uso del hidrógeno presurizado es que se necesita un tanque de gran volumen para su almacenamiento. El hidrógeno licuado tiene que utilizarse a su temperatura de ebullición, que es de -253ºC. El tanque necesario para almacenarlo es también de grandes dimensiones y requiere aislamiento térmico, dado que el hidrógeno puede evaporarse. Los hidruros metálicos son capaces de absorber hidrógeno y lo desorben tras tratamiento a alta temperatura. Durante los ciclos de expansión/contracción se produce estrés en la lámina metálica y el material se desintegra, formando polvo que puede provocar bloqueos en la celda de combustible. Un gran número de investigadores [2-4] han tratado de resolver estos problemas y, por el momento, los hidruros de TiFe y MnTi parecen ser las mejores opciones de esta familia de materiales. Recientemente, se trabaja en aumentar la capacidad de absorción de H2 con hidruros basados en Mg. Estos materiales presentan una elevada capacidad de absorción, pero tienen como gran inconveniente que su velocidad de absorción es muy baja en las condiciones de temperatura de utilización. Un problema general de estos sistemas es, en función de la naturaleza de los metales, la desactivación por pequeñas cantidades de vapor de agua, oxígeno y CO2, así como de envenenamiento por otras impurezas presentes en la corriente.
El almacenamiento de hidrógeno basado en la fisisorción es un procedimiento con una eficacia energética más elevada que los anteriormente citados [5]. El bajo punto de ebullición del H2 (-253ºC) requiere temperaturas de alrededor de -200ºC para alcanzar la suficiente cantidad de H2 adsorbido. Recuperar el hidrógeno fisisorbido es un proceso rápido y que se puede realizar mediante pequeños cambios de presión y/o temperatura.
Las fuerzas de interacción entre el hidrógeno y el adsorbente tienen un carácter físico y la cantidad de hidrógeno adsorbido está relacionada con la superficie específica, con la estructura porosa, con el diámetro de poro promedio y con la naturaleza del material adsorbente.
Por todo ello, se están ensayando distintos materiales microporosos para utilizarlos en la adsorción de hidrógeno. Así, desde los años 60, todo tipo de materiales de carbón activado, preparados a partir de precursores minerales y orgánicos, han sido estudiados por su capacidad para adsorber hidrógeno. Estos materiales se obtienen por procesos termoquímicos y presentan diferentes tipos de estructuras para la adsorción de hidrógeno [5-8].
En una reciente revisión, Dillon y Heben [9] concluyen que hay muy pocos estudios sobre adsorbentes con características de carbón activado, capaces de mejorar la capacidad de almacenamiento de un tanque de alta presión a 27ºC. Se ha observado que los materiales carbonosos con microporos adsorben más hidrógeno que los materiales sin ningún tipo de porosidad.
Otro tipo de materiales que pueden emplearse en el almacenamiento de H2 mediante adsorción física son las nanofibras de carbón [10]. Las fibras se forman en determinadas condiciones durante el proceso de conversión de hidrocarburos, por ejemplo, sobre catalizadores soportados de Ni y Fe. Debido a que tienen la capacidad de poder llegar a desactivar completamente un catalizador, hasta los años 1990 muchos investigadores trataban de prevenir su crecimiento. Estas nanofibras de carbón consisten en grupos de láminas de grafito con diámetros entre 10 y 100 nm y longitud superior a varios cientos de µm. Se pueden formar a partir de conos de grafito o a partir de cilindros concéntricos. En concreto, la forma cónica tipo raspa de pescado es interesante desde el punto de vista de encontrar un adsorbente adecuado para el hidrógeno. En estos materiales se puede crear un elevado volumen de microporos si el espacio entre los conos es accesible al H2.
Diferentes resultados de almacenamiento de H2 en nanofibras de carbón y nanotubos han sido presentados y debatidos en la literatura. Las medidas de adsorción de H2 son difíciles de realizar y requieren unas condiciones perfectamente definidas como han demostrado varios investigadores [11-13].
Dillon y col. [9,14] han estudiado nanotubos sonificados con una disolución de HNO3, que adsorben un 10% en peso de H2 a temperatura ambiente. El tratamiento seguido permite la rotura y abertura de los tubos. Hirscher y col. [15] observaron también un aumento de la capacidad de adsorción de H2 en tubos sonificados en un depósito de paredes de titanio. Durante este proceso y con una disolución de HNO3 5 mol/l, se forman pequeñas partículas de titanio que se depositan en el interior de la estructura de los nanotubos. Tras lavado y secado, el titanio presenta muy buena capacidad de adsorción de H2 a temperatura ambiente y presión atmosférica.
Chen y col. [16] indican que la adsorción de H2 se favorece en nanotubos dopados con Li+ y K+. La presencia de estos iones en las nanofibras permite que se produzcan reacciones en estado sólido entre las fibras y los carbonatos y nitratos de Li+ y K+. El hidrógeno almacenado puede desorberse a más altas temperaturas, y el ciclo de adsorción-desorción se puede reproducir con una pequeña disminución de la capacidad de adsorción. Yang [17] observó que la capacidad de adsorción de hidrógeno puede medirse por la formación de LiOH y KOH, procedente también de la presencia de trazas de moléculas de H2O en el efluente gaseoso. Cuando el agua está presente en el efluente que contiene H2, reacciona con los compuestos de Li y K para formar LiOH y KOH, y se observa un aumento de la cantidad de hidrógeno adsorbida.
Las zeolitas también se han usado en el almacenamiento de hidrógeno [18-20], pues son materiales microporosos baratos. Además, en estos materiales se puede controlar el diámetro de cavidades y canales mediante el intercambio iónico con cationes de diferentes tamaños. Kazansky y col. [21] han estudiado faujasitas con una capacidad de almacenamiento de hidrógeno de 1,2% en peso. Langmi y col. [22] han encontrado que el comportamiento de las zeolitas con respecto a la adsorción de hidrógeno depende de su estructura y de la naturaleza de los cationes de cambio. La capacidad de adsorción más elevada medida, 2,19% en peso, corresponde a una zeolita CaX.
En los últimos treinta años, una de las familias de materiales con microporos que en mayor profundidad ha sido estudiada es la de las arcillas intercaladas, unos materiales que ofrecen las ventajas comerciales de ser baratos, estables y fáciles de preparar. Las arcillas están presentes en la corteza terrestre como componentes de rocas y están constituidas esencialmente por silicatos de aluminio/magnesio hidratados, de estructura cristalina laminar o fibrosa, que pueden contener otros elementos como hierro, calcio, sodio, potasio y otros. En estos materiales, los grupos tetraédricos SiO4 de su estructura están unidos entre sí para formar capas continuas tetraédricas, mientras que los grupos octaédricos AlO6 o MgO6 forman capas continuas octaédricas. Cuando se unen dos capas tetraédricas con una central octaédrica, se obtiene una lámina 2:1. A la familia...
Reivindicaciones:
1. Un procedimiento para la preparación de una esmectita pilareada que comprende las etapas de:
2. Procedimiento según la reivindicación 1, en el que la esmectita es montmorillonita sódica.
3. Procedimiento según la reivindicación 1 ó 2, en el que la disolución intercalante que contiene un polihidroxicatión de aluminio se obtiene mediante la reacción de AlCl3 con NaOH.
4. Procedimiento según la reivindicación 3, en el que la relación molar OH/Al oscila entre 1,0 y 2,5.
5. Procedimiento según la reivindicación 3, en el que el pH de la disolución intercalante está comprendido entre 3 y 5.
6. Procedimiento según la reivindicación 3, en el que la temperatura de envejecimiento de la disolución intercalante está comprendida entre 20ºC y la temperatura de reflujo, y el tiempo de envejecimiento de dicha disolución intercalante oscila entre 15 minutos y 48 horas.
7. Procedimiento según la reivindicación 3, en el que la temperatura de la etapa a) de contacto entre la esmectita y la disolución intercalante se lleva a cabo a una temperatura comprendida entre 20ºC y la temperatura de reflujo y el tiempo de contacto oscila entre 15 minutos y 48 horas.
8. Procedimiento según la reivindicación 7, en el que la etapa a) de contacto se lleva a cabo en un recipiente con agitación.
9. Procedimiento según la reivindicación 3, en el que la etapa b) de separación de la arcilla intercalada se lleva a cabo mediante filtración, centrifugación o decantación del sobrenadante tras dejar en reposo la mezcla de arcilla y disolución de intercalación.
10. Procedimiento según la reivindicación 9, en el que la etapa b) de separación de la arcilla intercalada se lleva a cabo mediante centrifugación a 4.500 r.p.m.
11. Procedimiento según la reivindicación 3, en el que la arcilla obtenida en la etapa b) se calcina a una temperatura comprendida entre 200ºC y 900ºC.
12. Procedimiento según la reivindicación 11, en el que la arcilla obtenida en la etapa b) sufre una etapa de secado previa a la calcinación a una temperatura entre 50ºC y 200ºC.
13. Procedimiento según la reivindicación 11, en el que la arcilla obtenida en la etapa b) sufre una etapa de secado previa a la calcinación mediante liofilización o atomización.
14. Procedimiento según una cualquiera de las reivindicaciones 11 a 13, en el que la arcilla obtenida en la etapa b) se calcina a una temperatura comprendida entre 200ºC y 500ºC, a presión atmosférica.
15. Procedimiento según la reivindicación 14, en el que la arcilla obtenida en la etapa b) se calcina durante un tiempo que oscila entre 0,15 y 100 horas.
16. Procedimiento según la reivindicación 15, en el que la arcilla obtenida en la etapa b) se calcina durante un tiempo que oscila entre 1 y 16 horas.
17. Procedimiento según una cualquiera de las reivindicaciones anteriores, en el que la relación entre la concentración de Al contenida en la disolución intercalante y los gramos de arcilla que se ponen en contacto con dicha disolución intercalante en la etapa a) es de 10, 30, 90 o 150 mmolar Al/garcilla.
18. Procedimiento según la reivindicación 17, en el que la esmectita es montmorillonita sódica, la disolución intercalante se prepara tratando una disolución de AlCl3 y NaOH durante 48 horas a 50ºC obteniendo una disolución de pH 3,0 y una relación molar de OH-/Al3+ = 2,0, la etapa a) de contacto entre la esmectita y la disolución intercalante se lleva a cabo a durante 24 horas a temperatura ambiente con agitación, la etapa b) de separación de la arcilla intercalada se lleva a cabo mediante centrifugación a 4.500 r.p.m., la arcilla obtenida en la etapa b) sufre una etapa de secado previa a la calcinación a 60ºC durante una noche y la arcilla secada obtenida se calcina a 200ºC durante 4 horas.
19. Procedimiento según la reivindicación 18, en el que la concentración de Al contenido en la disolución intercalante y los gramos de arcilla que se ponen en contacto con dicha disolución intercalante en la etapa a) es de 10 mmolar Al/garcilla.
20. Una arcilla pilareada obtenida según el procedimiento de una cualquiera de las reivindicaciones 1 a 19.
21. Arcilla pilareada según la reivindicación 20, que se ha obtenido a partir de montmorillonita sódica.
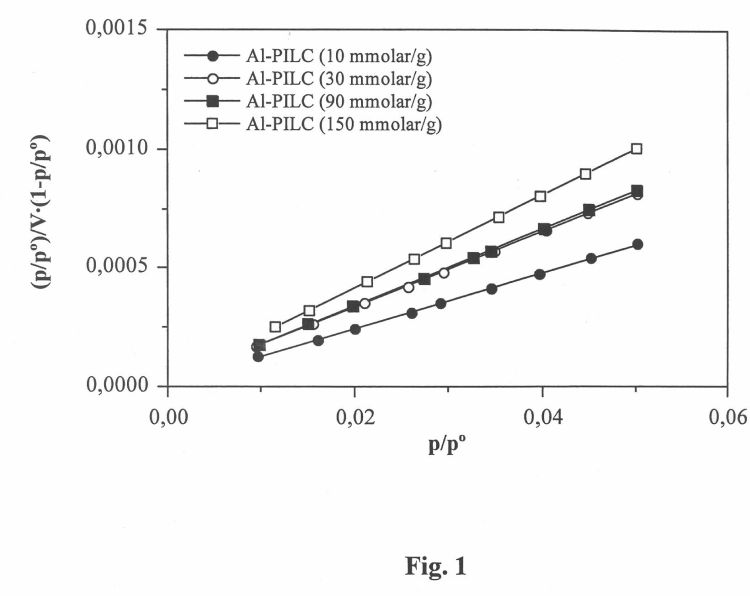
22. Arcilla pilareada según la reivindicación 21, en la que el volumen de los microporos varía entre 0,080 y 0,150 cm3/g y la superficie específica varía entre 230 y 400 m2/g.
23. Arcilla pilareada según la reivindicación 22, en la que el porcentaje en peso de alúmina (Al2O3) varía entre 33,00 y 35,00%.
24. Arcilla pilareada según la reivindicación 23, en la que el porcentaje en peso de alúmina (Al2O3) es de 33,06 ± 0,06%.
25. Uso de una arcilla pilareada según una cualquiera de las reivindicaciones 20 a 24 para la adsorción de hidrógeno.
26. Uso según la reivindicación 25, en el que la adsorción tiene lugar a -196ºC.
27. Uso según la reivindicación 26, en el que la arcilla pilareada es una arcilla de la reivindicación 24.
Patentes similares o relacionadas:
Arena para animales autoaglomerante extruida y método de fabricación de arena para animales autoaglomerante extruida, del 17 de Junio de 2020, de Pioneer Pet Products, LLC: Una arena para gatos autoaglomerante formada por gránulos de arena compuestos de pellas extruidas que contienen almidón y que tienen, cada una, una pluralidad de […]
Zeolitas granuladas con elevada capacidad de adsorción para la adsorción de moléculas orgánicas, del 19 de Febrero de 2020, de Süd-Chemie IP GmbH & Co. KG (100.0%): Granulado que comprende al menos una zeolita y al menos un mineral arcilloso con una capacidad de intercambio de cationes menor que 200 meq/100 g, […]
Perla adsorbente de material compuesto, proceso para su producción, proceso de separación de gas y lecho de adsorción de gas, del 24 de Julio de 2019, de GLATT SYSTEMTECHNIK GMBH: Perla adsorbente de material compuesto para la separación de al menos un componente gaseoso de una mezcla de gases, teniendo la perla adsorbente al menos un núcleo poroso y […]
Gránulo adsorbente de material compuesto, proceso para su producción y proceso de separación de gases, del 26 de Junio de 2019, de GLATT SYSTEMTECHNIK GMBH: Gránulo adsorbente de material compuesto para la separación de al menos un componente gaseoso de una mezcla gaseosa, en donde el adsorbente tiene al menos un núcleo que comprende […]
Dispositivo de extracción de humos, del 18 de Febrero de 2019, de BSH HAUSGERÁTE GMBH: Dispositivo de extracción de humos con una campana de extracción de humos, en el que el dispositivo de extracción de humos presenta un elemento de […]
Reducción de emisiones de mercurio de la combustión de carbón, del 1 de Febrero de 2019, de NOX II INTERNATIONAL, LTD: Un método para quemar carbón para reducir la cantidad de mercurio liberado a la atmósfera, que comprende aplicar una composición sorbente de mercurio […]
Método para protección de catalizador SCR y control de emisiones múltiples, del 23 de Enero de 2019, de THE BABCOCK & WILCOX COMPANY: Método para aumentar la vida activa de un catalizador SCR, caraterizado por que el método comprende las etapas de: proporcionar al menos un compuesto […]
Adsorbentes zeolíticos de bajo tenor de ligante y de elevada superficie externa, su procedimiento de preparación y sus usos, del 9 de Enero de 2019, de ARKEMA FRANCE: Adsorbente zeolítico que comprende por lo menos una zeolita FAU de porosidad jerarquizada, es decir, que tiene al mismo tiempo microporos y mesoporos […]