SINTESIS DE SILICE MESOPOROSA ORDENADA Y QUIRAL USANDO AMINOACIDOS.
Síntesis de silice mesoporosa ordenada y quiral usando aminoácidos.
Procedimiento para la obtención de un material con una estructura mesoporosa ordenada, con propiedades enantioselectivas, mediante la utilización de aminoácidos como agentes inductores de quiralidad. Además, el material mesoporoso obtenible por dicho procedimiento y a sus aplicaciones
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200930029.
Solicitante: UNIVERSIDAD DE ZARAGOZA..
Nacionalidad solicitante: España.
Provincia: ZARAGOZA.
Inventor/es: CORONAS CERESUELA,JOAQUIN, SEBASTIAN CABEZA,VICTOR, URIEL RUBIO,SANTIAGO, CASADO COTERILLO,CLARA, LACASTA ROLDAN,SUSANA, LOPEZ RAM DE VIU,MARIA PILAR.
Fecha de Solicitud: 1 de Abril de 2009.
Fecha de Publicación: .
Fecha de Concesión: 12 de Julio de 2011.
Clasificación Internacional de Patentes:
- B01J29/035 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 29/00 Catalizadores que contienen tamices moleculares. › Polimorfos de sílice cristalinos, p. ej. silicalitas.
- C01B37/02 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01B ELEMENTOS NO METALICOS; SUS COMPUESTOS (procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01B 37/00 Compuestos que tienen propiedades de tamices moleculares pero que no tienen propiedades de cambiadores de base. › Polimorfos de sílice cristalinos, p. ej. silicalitas.
Clasificación PCT:
- B01J29/035 B01J 29/00 […] › Polimorfos de sílice cristalinos, p. ej. silicalitas.
- C01B37/02 C01B 37/00 […] › Polimorfos de sílice cristalinos, p. ej. silicalitas.
PDF original: ES-2345868_A1.pdf
Fragmento de la descripción:
Síntesis de sílice mesoporosa ordenada y quiral usando aminoácidos.
La presente invención se refiere al procedimiento para la obtención de un material con una estructura mesoporosa ordenada, con propiedades enantioselectivas, mediante la utilización de aminoácidos como agentes inductores de quiralidad. Además, la invención se refiere al material mesoporoso obtenible por dicho procedimiento y a sus aplicaciones.
Estado de la técnica anterior
Como consecuencia de su tamaño de poro uniforme en el rango de pocos nanómetros y de su elevada área superficial1, los materiales de sílice mesoestructurada (sílice mesoporosa ordenada) constituyen un complemento a la utilización de las zeolitas convencionales en diversos campos de aplicación como la adsorción y la catálisis.
La mayoría de los materiales mesoporosos (por ejemplo, MCM-41 y MCM-48) se sintetizan a pH elevados mediante la utilización de moléculas surfactantes catiónicas con la función de agentes directores de la estructura2-4. Las moléculas surfactantes aniónicas y no-iónicas también son de gran interés para su utilización como agentes directores de la estructura. Aunque en este último caso su interacción con las moléculas precursoras de silicio se realiza o bien mediante la utilización de pH bajos (cuando, rebasado el punto isoeléctrico de la sílice las correspondientes especies existentes en disolución tienen carga positiva)5, o bien mediante la utilización de una fuente de silicio cargada de forma positiva, como los aminosilanos o los aminosilanos cuaternarios6, 7, que actuarían además como co-agentes directores de la estructura y posibilitarían la síntesis en medio alcalino. Por otra parte, la utilización de moléculas surfactantes aniónicas-catiónicas con función de agentes directores de la estructura favorece la formación de fases mesoporosas de MCM-48 en condiciones de síntesis relativamente suaves8.
Como complemento a lo dicho, se han obtenido estructuras de sílice ordenadas mediante el auto-ensamblado de bio-copolímeros que emulan el proceso biológico de la silicificación7, 9. Por ejemplo, homopéptidos como la poli(lisina) y la poli(arginina) inducen la formación de estructuras mesoporosas de sílice10. Para estudiar la contribución de estas moléculas complejas (proteínas) en la bio-silicificación, se ha estudiado el papel que diferentes aminoácidos tienen como agentes de polimerización de sílice a pH11. También se han obtenido nanopartículas en soles no tamponados de Usina-sílice12, por ejemplo en condiciones de pH elevado, condiciones similares a las utilizadas en la síntesis de sílice mesoporosa mediante la utilización de moléculas con la función de agente directores de la estructura. Igualmente, se han obtenido sistemas de organización periódica constituidos por nano-esferas de sílice producidas a través de una modificación del denominado método de Stöber, utilizando aminoácidos con carácter básico (L-lisina o L-arginina) en lugar de amoniaco13.
Al igual que la secuencia de aminoácidos de una proteína determina su estructura secundaria y terciaria y, por tanto, le confiere unas determinadas propiedades biológicas, la incorporación de aminoácidos en la síntesis de sílice ordenada mesoporosa podría ser una buena estrategia para modificar su posible quiralidad o adecuarla a múltiples aplicaciones relacionadas con la biotecnología.
Explicación de la invención
La presente invención proporciona la síntesis, caracterización y aplicación de un nuevo material mesoporoso obtenido mediante la utilización de aminoácidos que transfieren su quiralidad a la sílice mesoporosa ordenada obtenida. Por ejemplo, una de sus posibles aplicaciones podría ser la separación de aminoácidos quirales.
Un primer aspecto de la presente invención se refiere a un proceso de obtención de una estructura de sílice mesoporosa de tamaño de poro nanométrico y cuyo ordenamiento espacial es de tipo hexagonal, mediante la utilización de aminoácidos para favorecer la condensación de las especies de sílice.
Como se presenta en los ejemplo, algunos materiales concretos de la presente invención se han obtenido en medio básico, combinando dos precursores de silicio (tetraetil ortosilicato (TEOS) y 3[3-(trimetoxisilil)propil]-N-octadecil-N,N-dimetilamonio (C18-TMS)), junto con cuatro aminoácidos diferentes (DL- y L-arginina, DL- y L-histidina, L-isoleucina y L-prolina).
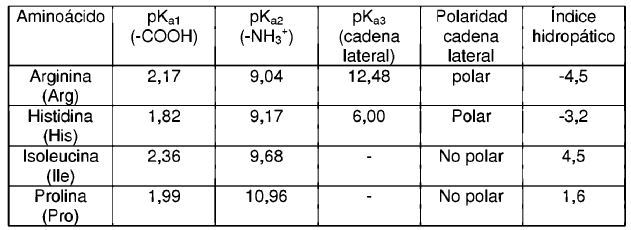
En el Esquema 1 se representan las fórmulas estructurales de TEOS y C18-TMS, mientras que en la Tabla 1 aparecen las propiedades más relevantes para la invención de los aminoácidos utilizados, y en el Esquema 2 pueden verse sus correspondientes fórmulas estructurales.
Esquema 1
Fórmulas estructurales del TEOS (izquierda) y de C18-TMS (derecha)
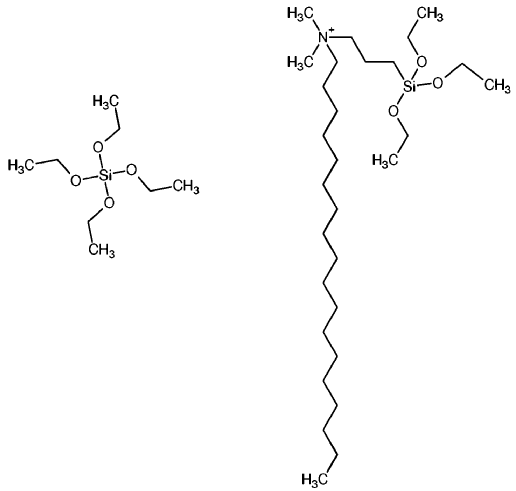
Por todo ello, un aspecto de la presente invención se refiere a un procedimiento para la obtención de un material mesoporoso, ordenado y quiral que comprende:
La temperatura de calcinación del paso (b) es preferiblemente mayor de 600ºC. Este paso se suele realizar en un periodo de entre 5 y 12 horas y a una velocidad de calentamiento de aproximadamente 10ºC/min, aunque todos estos parámetros se ajustan dependiendo del material obtenido en (a).
En una realización preferida, el precursor de silicio es TEOS, C18-TMS o cualquiera de sus combinaciones y más preferidamente el precursor de silicio es una combinación de TEOS y C18-TMS en una relación molar 3/0,5 con respecto al aminoácido (3/0,5/1 TEOS/C18-TMS/aminoácido).
Este procedimiento es lo suficientemente flexible como para ser aplicado a la mayoría de los aminoácidos típicos, así como a otras muchas moléculas orgánicas quirales, aunque de forma preferida el aminoácido se selecciona de entre arginina, histidina, isoleucina o prolina y más preferidamente de entre DL, o L-arginina, DL- o L-histidina, L-isoleucina o L-prolina.
La combinación de un precursor de silicio con un aminoácido esencial en el paso (a) se realiza en medio básico, que se puede obtener por ejemplo, pero sin limitarse, por adición de NaOH y/o TMAOH.
Se sugiere un mecanismo de síntesis que se basaría en la formación de micelas como la representada en el Esquema 3. Este mecanismo comprendería las siguientes etapas: (1) formación de enlaces covalentes Si-O-Si entre moléculas de surfactante C18-TMS (el dímero del Esquema 4 sería una representación factible de este proceso); (2) establecimiento de interacciones electrostáticas entre los aminoácidos y las partes polares de las moléculas de surfactante; y (3) condensación de la sílice sobre los silanos de la micela. Esto apunta, justificado por los experimentos de separación enantiomérica que se presentarán más adelante, que se produce una transferencia de quiralidad del aminoácido a la micela, y de ésta a la sílice. En definitiva los aminoácidos, incluso una vez eliminados junto a la demás materia orgánica al activar la porosidad de la sílice, dejan su impronta molecular en la mesofase sintetizada. Nótese que las moléculas del Esquema 1 para participar en los Esquemas 3 y 4 se habrían hidrolizado (el medio básico en el que se lleva a cabo todo el proceso cataliza esta hidrólisis), lo que haría que grupos hidroxilo reemplazasen a los correspondientes grupos etoxi y metoxi de TEOS y C18-TMS, respectivamente.
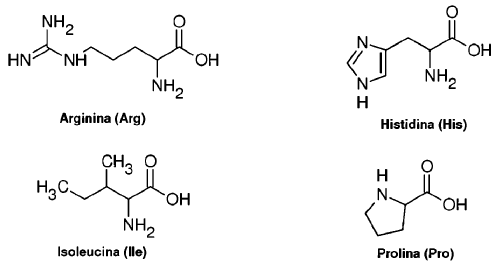
Esquema 2
Fórmulas estructurales de los aminoácidos arginina, histidina, isoleucina y prolina
 [Seguir leyendo]
[Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la obtención de un material me soporoso, ordenado y quiral que comprende:
2. Procedimiento según la reivindicación 1, donde el precursor de silicio se selecciona de entre TEOS, C18-TMS o cualquiera de sus combinaciones.
3. Procedimiento según la reivindicación 2, donde el precursor de silicio es una combinación de TEOS y C18-TMS en una relación molar 3/0,5 con respecto al aminoácido (3/0,5/1 TEOS/C18-TMS/aminoácido).
4. Procedimiento según cualquiera de las reivindicaciones 1 a 3, donde el aminoácido se selecciona de entre arginina, histidina, isoleucina o prolina.
5. Procedimiento según la reivindicación 4, donde el aminoácido se selecciona de entre DL, o L-arginina, DL- o L-histidina, L-isoleucina o L-prolina.
6. Procedimiento según cualquiera de las reivindicaciones 1 a 5, donde el medio básico del paso (a) se obtiene por adición de NaOH y/o TMAOH.
7. Material mesoporoso y ordenado obtenible por el procedimiento según cualquiera de las reivindicaciones 1 a 6.
8. Material mesoporoso según la reivindicación 7 cuyo área superficial específica (BET) es de entre 800 y 1000 m2/g, presenta un tamaño de poro (BJH) menor de 4 nm y un volumen de poros de entre 0,4 y 1 cm3/g.
9. Uso del material mesoporoso según las reivindicación 7 u 8, como catalizador o biocatalizador.
10. Uso del material mesoporoso según las reivindicación 7 u 8, para separación y/o purificación de sustancias ópticamente activas.
11. Uso del material mesoporoso según la reivindicación 10 donde las sustancias óptimamente activas son aminoácidos quirales.
12. Uso del material mesoporoso según las reivindicación 7 u 8, para obtener membranas sobre soportes inorgánicos porosos.
13. Uso del material mesoporoso según las reivindicación 7 u 8, para obtener membranas mixtas polímero-sílice.
14. Membranas inorgánicas o híbridas que incorporan el material mesoporoso según las reivindicaciones 7 u 8.
15. Uso de las membranas según la reivindicación 14 para separar por filtración mezclas de sustancias ópticamente activas.
16. Uso de las membranas según la reivindicación 14 en reactores de membrana.
Patentes similares o relacionadas:
Proceso de producción de un material zeolítico MFI que emplea precursores elementales, del 23 de Octubre de 2019, de BASF SE: Un proceso de producción de un material zeolítico que tiene una estructura de armazón de MFI que comprende YO2, en donde dicho proceso comprende preparar […]
Procedimiento para preparar zeolitas, del 26 de Febrero de 2019, de versalis S.p.A: Procedimiento para preparar zeolitas MFI/MEL o MEL que presentan la fórmula x TiO2 . (1-x) SiO2 en la que x presenta un valor comprendido entre 0,0005 […]
Procedimiento de preparación de materiales mesoporosos, del 18 de Abril de 2018, de Total Raffinage France: Procedimiento de fabricación de un material mesoporoso que comprende las etapas de: - (a) preparación de una solución acuosa de al menos un agente estructurante que presenta […]
Composición del material para el tamiz molecular SSZ-87 y su síntesis, del 14 de Junio de 2017, de CHEVRON U.S.A. INC.: Un tamiz molecular que tiene una relación molar de 10 o más de óxido de silicio con respecto a un óxido seleccionado de óxido de boro y óxido de aluminio y que tiene, […]
Uso de películas finas de sílices mesoporosas como materiales sensibles en sensores gravimétricos para la detección o el análisis de vapores de compuestos nitrados, del 12 de Abril de 2017, de COMMISSARIAT A L'ENERGIE ATOMIQUE ET AUX ENERGIES ALTERNATIVES: Uso de una película fina de sílice mesoporosa que se ha obtenido mediante un procedimiento sol-gel como material sensible en un sensor gravimétrico para […]
Composiciones y procedimientos para la síntesis de sílices mesoporosas cúbicas que tienen morfología de tipo "fideo", del 18 de Enero de 2017, de Dow Global Technologies LLC: Una composición que comprende una sílice mesoporosa que tiene una estructura de canales tridimensionales con entramado de tipo MCM-48, según define la Asociación Internacional […]
Material de tamiz molecular EMM-23, su síntesis y uso, del 4 de Enero de 2017, de EXXONMOBIL CHEMICAL PATENTS INC.: Un material de tamiz molecular que tiene, en su forma calcinada, un patrón de difracción de rayos X que incluye los siguientes picos indicados en la Tabla 1: **Tabla**
Materiales zeolíticos y métodos para su preparación usando compuestos de alqueniltrialquilamonio, del 9 de Noviembre de 2016, de BASF SE: Procedimiento para la preparación de un material zeolítico que tiene una estructura de armazón de tipo MFI, que comprende las etapas de: […]