Micobacterias inactivadas para su uso por vía oral en la prevención de la tuberculosis.
La presente invención se refiere a micobacterias inactivadas para su uso por vía oral en la prevención de la tuberculosis.
Dichas bacterias se administran según una pauta de administración de múltiples dosis, administradas con un intervalo temporal reducido entre las mismas, de modo que induce una respuesta tolerizante frente a la infección por el bacilo de la tuberculosis. La utilización de las bacterias inactivadas de acuerdo con dicha pauta permite controlar el progreso de la infección desde un estado latente a tuberculosis activa.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201200640.
Solicitante: FUNDACIÓ INSTITUT PER A LA INVESTIGACIÓ EN CIÈNCIES DE LA SALUT "GERMANS TRIAS I PUJOL" (IGTP) UNITAT DE TUBERCULOSI EXPERIMENTAL.
Nacionalidad solicitante: España.
Inventor/es: CARDONA IGLESIAS,PERE JOAN, VILAPLANA MASSAGUER,Cristina, MARZO ESCARTÍN,Elena.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/04 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Mycobacterium, p. ej. Mycobacterium tuberculosis.
Fragmento de la descripción:
MICOBACTERIAS INACTIVADAS PARA SU USO POR VíA ORAL EN LA PREVENCiÓN DE LA TUBERCULOSIS
Campo de la técnica La presente invención se enmarca en la provisión de medicamentos para ser administrados por vía oral para la prevención de la tuberculosis, en particular para controlar el paso de la infección latente a la infección activa de dicha enfermedad.
Estado de la técnica anterior
La tuberculosis es una enfermedad infecciosa crónica ocasionada por las bacterias pertenecientes al grupo Mycobacterium tuberculosis-complex (MTB-C) , que incluye actualmente los bacilos M. tuberculosis, M. bovis, M. micro ti y M. africanum, siendo el M. tuberculosis el agente más importante y frecuente en relación con la tuberculosis humana. Dicha enfermedad afecta principalmente a los pulmones, si bien en algunos casos puede extenderse también a otros órganos. Si no se trata adecuadamente, la tuberculosis puede resultar mortal.
Según el informe del 2011 de la Organización Mundial de la Salud, anualmente se registran 9 millones de nuevos casos a nivel mundial de personas que manifiestan la enfermedad y se contabilizan aproximadamente 1, 7 millones de fallecimientos. Se considera, así mismo, que en el mundo existen más de 2.500 millones de personas infectadas y que cada año se generan unos 100 millones de infectados nuevos.
La tuberculosis se transmite por el aire, de manera que los pacientes con una cavidad tuberculosa en sus pulmones son la principal fuente de la transmisión de esta enfermedad, tal como se describe, por ejemplo, en J. Grosset, Studies in shorl-course chemotherapy for tuberculosis. Basis for shorlcourse chemotherapy, Chest, 1981, 80, 719-720, Y en J. Grosset, Mycobacterium tuberculosis in the Extracellular Comparlment: an Underestimated Adversar y , Antimicrob. Agents Chemother., 2003, 47, 833-836.
Según se describe en dichos artículos, los pacientes expulsan,
mediante la tos o el estornudo, una gran cantidad de microgotas capaces de transportar bacilos, que pueden entrar en el espacio alveolar de la persona que los inhala.
Tras la inhalación, el bacilo es fagocitado por los macrófagos alveolares, y es dentro de esta célula donde el bacilo puede crecer, hasta causar la destrucción de la misma. De nuevo en el espacio extracelular, el bacilo es fagocitado por nuevos macrófagos y este proceso se va repitiendo hasta que, al ser drenados y generar una infección en los ganglios linfáticos hiliares, se genera una respuesta inmune basada en una inmunidad celular.
Unas 6 semanas después de la infección, el crecimiento bacilar cesa, el hospedador positiviza la prueba cutánea de la tuberculina, caracterizada por una respuesta de hipersensibilidad retardada (o DTH, del inglés Delayed Type Hypersensitivity) , y se genera la denominada necrosis caseosa en el punto de infección.
Una de las características principales de la infección tuberculosa, es el hecho de que M. tuberculosis es capaz de permanecer durante años en el tejido del hospedador sin desarrollar la enfermedad, en forma de infección tuberculosa "latente", pero manteniendo sus posibilidades de generar una tuberculosis activa.
Este estado latente de la infección está relacionado con la aparrclon de la denominada necrosis caseosa, que se genera en la lesión alveolar inicial y en el tejido pulmonar circundante, resultando en la destrucción de los macrófagos que contienen los bacilos que se están multiplicando, produciéndose una lesión necrótica sólida.
El origen de esta reacción necrótica no se conoce con exactitud, pero se relaciona con la reacción de tipo DTH. Esencialmente, la respuesta inmune que permite el control de la población bacilar es de tipo celular y mayoritariamente dirigida por linfocitos CD4 de tipo Th1, es decir, capaz de generar la respuesta de tipo DTH y también de identificar macrófagos infectados y de activarlos para destruir a los bacilos de su interior.
Aproximadamente en un 10% de los individuos infectados, dicha necrosis sólida se reblandece, siendo uno de los episodios más importantes en la infección tuberculosa, puesto que es entonces cuando la infección progresa a tuberculosis activa, o sea a enfermedad tuberculosa.
En la mayoría de los casos, el reblandecimiento se asocia con el drenaje del tejido reblandecido hacia el árbol bronquial, formándose una cavidad tuberculosa, y un crecimiento extracelular explosivo del bacilo, con la entrada de oxígeno a través del orificio bronquial. Con la tos, este caseum reblandecido y repleto de bacilos, es diseminado por otras partes de los bronquios, del pulmón y del exterior.
El tratamiento farmacológico de la tuberculosis se caracteriza por ser una terapia prolongada, cosa que dificulta su seguimiento a la vez que favorece la aparición de bacterias resistentes a los fármacos.
Se considera que la mejor estrategia para la contención de la tuberculosis se basa en un enfoque preventivo de la misma.
La vacuna actual, administrada por vía parenteral, que se emplea en el tratamiento preventivo contra la tuberculosis está basada en bacterias de la cepa denominada BCG (Bacilo de Calmette-Guerin) , una variante atenuada de M. bovis. Sin embargo, se ha observado que su eficacia disminuye con el tiempo y que es ineficaz para la prevención de la enfermedad en adultos, de hecho se considera que tan solo protege a los nichos del desarrollo de una enfermedad tuberculosa mortal (miliar o meníngea) .
Se han desarrollado otros tratamientos profilácticos de la tuberculosis basados principalmente en otras cepas de micobacterias vivas atenuadas, o bien en subunidades bacterianas.
Así mismo, en el estado de la técnica también se han explorado tratamientos profilácticos de la tuberculosis basados en micobacterias inactivadas, con el objeto de obtener una respuesta inmune análoga a la obtenida con las vacunas basadas en micobacterias atenuadas, es decir, del tipo Th1, generadora de interferón-y.
Así, por ejemplo, en el artículo Opie et al., Protective inoculation against human tuberculosis with heat-killed tubercle bacilli, Am. J. Hyg., 1939,
29, 155-164, se describe un estudio clínico en el que se administraron cinco dosis por vía intracutánea de bacilos de M. tuberculosis inactivados por calentamiento, con el objetivo de generar protección frente a la enfermedad.
Así mismo, en el artículo Agger et al. Specific acquired resistance in mice immunized with killed mycobacteria, Scand. J. Immunol., 2002, 56, 443447, se describe un estudio experimental con ratones que fueron vacunados con tres dosis administradas por vía subcutánea de 1000 I-Ig de bacilos M. tuberculosis inactivados por calentamiento, con un intervalo de 2 semanas entre cada dosis, observándose una inducción de inmunidad específica basada en linfocitos T.
También se han ensayado otras micobacterias inactivadas para inducir protección frente a la tuberculosis, habitualmente por vía parenteral.
Por ejemplo, en Gupta et al., Immunogenicity and protective efficacy of "Mycobacterium w" against Mycobacterium tuberculosis in mice Immunized with live versus heat-killed M. w by the aerosol or parenteral route,
Infect. Immun., 2009, 77 (1) , 223-231, se describe que se administraron micobacterias M. w vivas o inactivadas por calentamiento. Estas últimas fueron administradas como monodosis por vía subcutánea, y se observó una respuesta inmunitaria basada en la inducción de linfocitos Th1, que generaban interferonas.
Es particularmente deseable, disponer de un tratamiento profiláctico que sea efectivo por vía oral, ya que dicha vía facilita considerablemente la administración del fármaco y la adherencia al tratamiento.
En este sentido, existen algunos documentos en el estado de la técnica referidos a la administración por vía oral de bacterias inactivadas por el calor de otra micobacteria, Mycobacterium vacae, para conseguir un efecto terapéutico de la tuberculosis activa, según una pauta combinada con los fármacos habituales en quimioterapia.
A nivel experimental, en Hernández-Pando et al., Orally administered Mycobacterium vaccae modulates expression of immunoregulator y molecules in BALB/c mice with pulmonar y tuberculosis, Clin. Vaccine Immunol., 2008, 15 (11) , 1730-1736, se describe un ensayo realizado con ratones a los que se les administró por vía oral 5 dosis de 0, 1 IJg de M. vaccae inactivado por calentamiento, con un intervalo de 28 días entre cada administración, y induciéndose una infección con M. tuberculosis por vía intratraqueal 23 h después de la primera dosis. En dicho estudio se confirmó que se generaba una respuesta inmune de tipo celular aumentándose la secreción de linfocitos Th1, mientras que disminuía la...
Reivindicaciones:
1. Uso de micobacterias inactivadas del grupo denominado Mycobacterium tuberculosis complex (MTB-C) que se eligen de entre el grupo formado por M. tuberculosis, M. bovis, M. africanum, y M. microti, y M. bovis BCG para la preparación de un medicamento para la prevención de la tuberculosis.
2. Uso según la reivindicación 1, caracterizado porque: -las micobacterias se administran periódicamente por vía oral, -el intervalo entre las dosis no es superior a 5 días, y -el número de dosis administradas es de al menos 5.
3. Uso según la reivindicación 2, caracterizado porque las micobacterias inactivadas se eligen entre M. tuberculosis, M. bovis y M. bovis BCG.
4. Uso según cualquiera de las reivindicaciones 1 a 3, caracterizado porque las micobacterias se inactivan mediante un proceso de calentamiento.
5. Uso según cualquiera de las reivindicaciones 1 a 4, caracterizado porque el intervalo entre las dosis no es superior a 3 días.
6. Uso según la reivindicación 5, caracterizado porque el intervalo entre las dosis no es superior a 2 días.
7. Uso según cualquiera de las reivindicaciones 1 a 6, caracterizado porque el número de dosis administradas es de al menos 7.
8. Uso ~egún la reivindicación 7, caracterizado porque el número de dosis administradas es de al menos 9.
9. Uso según cualquiera de las reivindicaciones 1 a 8, caracterizado porque la cada dosis comprende entre 103 y 1010 micobacterias inactivadas.
10. Uso según cualquiera de las reivindicaciones 1 a 9, caracterizado porque las micobacterias se administran en forma de una composición farmacéutica que comprende las micobacterias inactivadas y al menos un excipiente farmacéutica mente aceptable.
11. Uso según la reivindicación 10, caracterizado porque la composición farmacéutica 5 está en forma de cápsulas.
12. Uso según la reivindicación 10, caracterizado porque la composición farmacéutica está en forma de comprimidos.
13. Uso según cualquiera de las reivindicaciones 1 a 12, caracterizado porque se administra a un individuo infectado por M. tuberculosis en el que la infección se encuentra en estado latente.
14. Uso según cualquiera de las reivindicaciones 1 a 12, caracterizado porque se 15 administra a un individuo no infectado por M. tuberculosis.
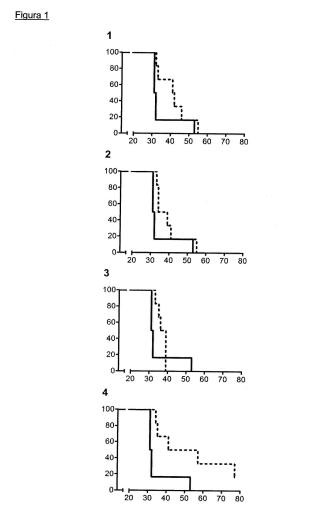
Figura 1
100 80
•
L••,
t
tI
,
L.
o 100 80 60 40 20 o 3
100 80 60 40 20 O
100 80 60 40 20 20 30 40 50 60 70 80
,
•.., , •
lo.,
,
t.•
•
60 70 80
••..,
•
t.•
L.
60 70 80
-, •ti
•t__
•
•
.. ----.
•1__ .... ___ •
O
60 70 80
Figura 2
100 80 60 40 20
o 100 80 60 40 20 O
60 40 20 O
100 80 60 40 20 O
-
••a. __•
•
•
L ......
•
•
"
I
60 70 80
._---.
•
L.....
L.I __
,
I••
L•••••
•
60 70 80
-,
'., , •
..... ...
•
, . I I
60 70 80
. ., •• , l•••
L,
, •I •
60 70 80
Figura 3
Figura 4
- ---.
•--e_..
... _--..
!. •••I
o 45
100 80 ' •••• 60 40 20
o i I 35 40 45 50
Figura 5
100 80 60 40 20
80 60 40 20
___ e'
O
.'--.....
, ,
-.
I
30 32 34 36 38 40 42
Figura 6
2
66 O
O
ti O
tP 00
~
O
~
~
D 8
~
O
6L -----6
Patentes similares o relacionadas:
Composiciones inmunogénicas de PCV2 multivalentes y métodos para producir dichas composiciones, del 27 de Mayo de 2020, de Boehringer Ingelheim Animal Health USA Inc: Una vacuna combinada multivalente para uso en un método para (i) la prevención de una infección por PCV2, o de reinfección por PCV2 o (ii) la reducción o eliminación […]
Arginina desiminasa con reactividad cruzada reducida hacia anticuerpos para ADI - PEG 20 para el tratamiento del cáncer, del 6 de Mayo de 2020, de TDW Group: Una composición terapéutica que comprende una arginina desiminasa (ADI) aislada y un vehículo farmacéuticamente aceptable, en donde la ADI aislada comprende la secuencia de […]
Mycobacterium recombinante como vacuna para uso en seres humanos, del 18 de Marzo de 2020, de VAKZINE PROJEKT MANAGEMENT GMBH: Una célula de Mycobacterium bovis recombinante de la cepa Danesa subtipo Praga que es deficiente en ureasa y que comprende una molécula de ácido nucleico […]
VACUNA MULTIVALENTE PARA EL TRATAMIENTO Y PREVENCIÓN DE LA TUBERCULOSIS, LISTERIOSIS Y NEUMONÍA, del 26 de Diciembre de 2019, de FUNDACIÓN INSTITUTO DE INVESTIGACIÓN MARQUÉS DE VALDECILLA: La presente invención se refiere a una vacuna sintética multivalente eficaz en el tratamiento y/o prevención de la tuberculosis, listeriosis y neumonías. Las vacunas terapéuticas […]
VACUNA MULTIVALENTE PARA EL TRATAMIENTO Y PREVENCIÓN DE LA TUBERCULOSIS, LISTERIOSIS Y NEUMONÍA, del 23 de Diciembre de 2019, de FUNDACIÓN INSTITUTO DE INVESTIGACIÓN MARQUÉS DE VALDECILLA: Vacuna multivalente para el tratamiento y prevención de la tuberculosis, listeriosis y neumonía. La presente invención se refiere a una vacuna sintética […]
 Composición antigénica de micobacterias, del 31 de Julio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunogénica que comprende un antígeno relacionado con M72, en la que el antígeno relacionado con M72 comprende una secuencia […]
Composición antigénica de micobacterias, del 31 de Julio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunogénica que comprende un antígeno relacionado con M72, en la que el antígeno relacionado con M72 comprende una secuencia […]
 Vacunas antimicobacterianas, del 31 de Julio de 2019, de UNIVERSITE DE GENEVE: Una partícula de virus infeccioso de la coriomeningitis linfocítica deficiente en la replicación para uso como una vacuna en un método para tratar o prevenir una infección […]
Vacunas antimicobacterianas, del 31 de Julio de 2019, de UNIVERSITE DE GENEVE: Una partícula de virus infeccioso de la coriomeningitis linfocítica deficiente en la replicación para uso como una vacuna en un método para tratar o prevenir una infección […]
Vacuna TB contra la tuberculosis para impedir la reactivación, del 28 de Mayo de 2019, de STATENS SERUM INSTITUT: Vacuna para la utilización en el bloqueo de la reactivación de la tuberculosis en individuos con infección latente por M. tuberculosis, que comprende […]