Un método para la síntesis de feroxihita de manganeso tetravalente para la eliminación de arsénico del agua.
Un método para la síntesis de una feroxihita de manganeso tetravalente (δ
-Fe(1-x)MnxOOH), caracterizado por el hecho de que tiene lugar en un reactor de flujo continuo, en condiciones ácidas débiles y rédox controlado, y se aplica mediante las siguientes etapas:
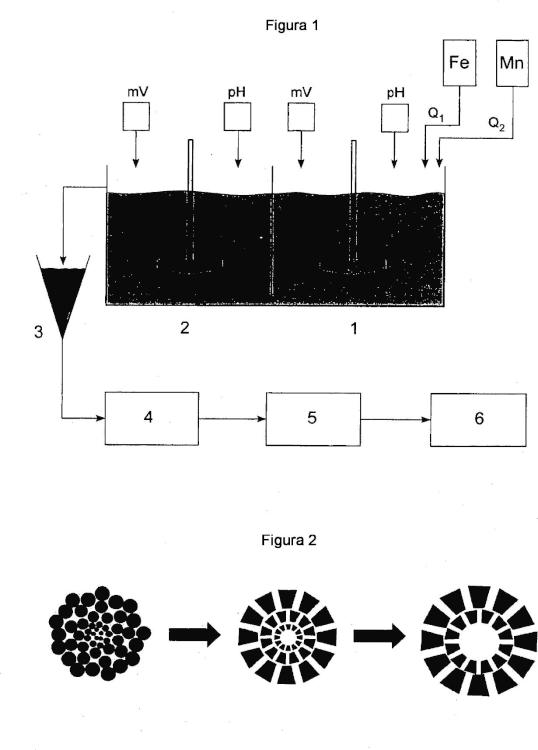
i) En el reactor (1) se añade FeSO4 o FeCl2 como fuente de hierro, se añade KMnO4 o MnSO4 o MnCl2 o Mn(NO3)2 como fuente de manganeso con una concentración de 1-100 g/l. Para la reacción, el pH se ajusta en el intervalo ácido débil 4-7 añadiendo uno o más de los reactivos NaOH, NaHCO3, Na2CO3, KOH, KHCO3, K2CO3. Al mismo tiempo, el rédox se ajusta en el intervalo 300-800 mV añadiendo uno o una combinación de más de uno de los reactivos KMnO4, NaClO2, ClO2, 2KHSO5·KHSO4·K2SO4, Na2S2O8, K2S2O8.
ii) Después, la reacción se termina en el reactor (2). El valor del pH en el reactor (2) también se ajusta en el intervalo ácido débil 4-7 añadiendo uno o una combinación de más de uno de los reactivos NaOH, NaHCO3, Na2CO3, KOH, KHCO3, K2CO3, y al mismo tiempo el rédox se ajusta en el intervalo 300-800 mV añadiendo uno o más de los reactivos KMnO4, NaClO2, ClO2, 2KHSO5·KHSO4·K2SO4, Na2S2O8, K2S2O8.
El tiempo de retención debería ser al menos 30 min. en cada uno de los dos reactores.
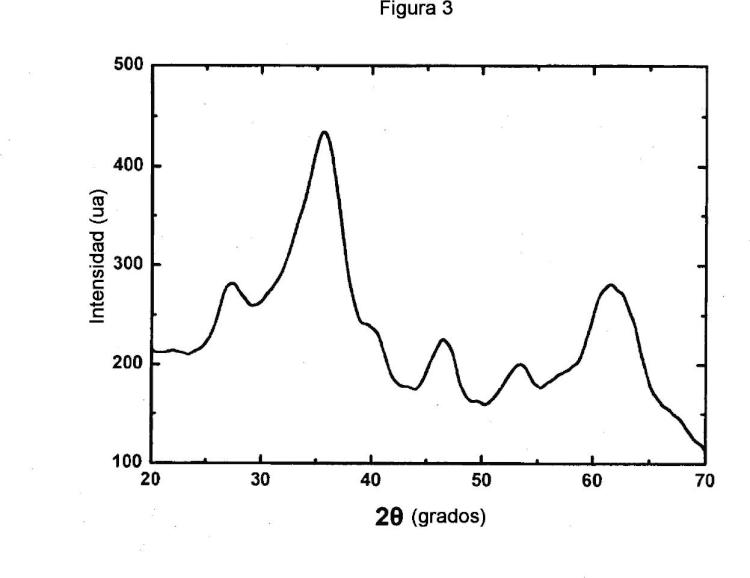
iii) A continuación, el producto que sale del reactor (2) entra en el tanque (3) de espesamiento, en el que, por agitación lenta durante 1-48 h, la geometría del grano se controla entre esferas irregulares y esferas huecas, y el área específica entre 100 m2/g y 300 m2/g.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GR2011/000042.
Solicitante: Loufakis Chemicals S.A.
Inventor/es: MITRAKAS,MANASSIS, SYMEONIDIS,KONSTANTINOS, TRESINTSI,SOFIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B01J20/06 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 20/00 Composiciones absorbentes o adsorbentes sólidas o composiciones que facilitan la filtración; Absorbentes o adsorbentes para cromatografía; Procedimientos para su preparación, regeneración o reactivación. › conteniendo óxidos o hidróxidos de metales no previstos en el grupo B01J 20/04.
- B01J20/28 B01J 20/00 […] › caracterizados por su forma o sus propiedades físicas.
- C01G49/00 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01G COMPUESTOS QUE CONTIENEN METALES NO CUBIERTOS POR LAS SUBCLASES C01D O C01F (hidruros metálicos C01B 6/00; sales de oxácidos de halógenos C01B 11/00; peróxidos, sales de los perácidos C01B 15/00; tiosulfatos, ditionitos, politionatos C01B 17/64; compuestos que contienen selenio o teluro C01B 19/00; compuestos binarios del nitrógeno con metales C01B 21/06; azidas C01B 21/08; amidas metálicas C01B 21/092; nitritos C01B 21/50; fosfuros C01B 25/08; sales de los oxácidos del fósforo C01B 25/16; carburos C01B 32/90; compuestos que contienen silicio C01B 33/00; compuestos que contienen boro C01B 35/00; compuestos que tienen propiedades de tamices moleculares pero que no tienen propiedades de cambiadores de base C01B 37/00; compuestos que tienen propiedades de tamices moleculares y de cambiadores de base, p. ej. zeolitas cristalinas, C01B 39/00; cianuros C01C 3/08; sales del ácido ciánico C01C 3/14; sales de cianamida C01C 3/16; tiocianatos C01C 3/20; procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; obtención a partir de mezclas, p. ej. a partir de minerales, de compuestos metálicos que son los compuestos intermedios de un proceso metalúrgico para la obtención de un metal libre C21B, C22B; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › Compuestos de hierro.
- C02F1/28 C […] › C02 TRATAMIENTO DEL AGUA, AGUA RESIDUAL, DE ALCANTARILLA O FANGOS. › C02F TRATAMIENTO DEL AGUA, AGUA RESIDUAL, DE ALCANTARILLA O FANGOS (procedimientos para transformar las sustancias químicas nocivas en inocuas o menos perjudiciales, efectuando un cambio químico en las sustancias A62D 3/00; separación, tanques de sedimentación o dispositivos de filtro B01D; disposiciones relativas a las instalaciones para el tratamiento del agua, agua residual o de alcantarilla en los buques, p. ej. para producir agua dulce, B63J; adición al agua de sustancias para impedir la corrosión C23F; tratamiento de líquidos contaminados por radiactividad G21F 9/04). › C02F 1/00 Tratamiento del agua, agua residual o de alcantarilla (C02F 3/00 - C02F 9/00 tienen prioridad). › por absorción o adsorción (utilizando cambiadores de iones C02F 1/42; composiciones absorbentes o adsorbentes B01J).
PDF original: ES-2520645_T3.pdf
Fragmento de la descripción:
Un método para la síntesis de feroxihita de manganeso tetravalente para la eliminación de arsénico del agua La invención pertenece al campo de la ingeniería química, y específicamente en la tecnología de tratamiento del agua mediante adsorbentes sólidos. En el actual estado de la técnica, los adsorbentes sólidos se usan como medios de relleno en un lecho de columna para la eliminación mediante adsorción de metales pesados, y especialmente arsénico, de agua potable y residuos.
La presencia de arsénico (As) en agua potable es uno de los problemas de contaminación más importantes y más ampliamente extendidos del agua. Se demuestra que el consumo a gran escala de agua con mayores concentraciones de arsénico está relacionado con el riesgo de enfermedades cardiovasculares, diabetes, así como cáncer de piel, de pulmón, de vejiga, y, como consecuencia, con el incremento de mortalidad. El límite para la concentración total de arsénico en agua potable se fijó en 10 ï?g/l desde 2001 en los Estados Unidos de América y desde 1998 en la Unión Europea. La aparición de arsénico es principalmente un problema que se produce en agua subterránea que se origina mediante fuentes naturales (sedimentos aluviales y lavado de minerales) o actividad antropogénica. Habitualmente se encuentra en forma de oxianiones [H2AsO4-/HAsO42-] de As (V) pentavalente o en forma no cargada H3AsO3 de As (III) trivalente, en una relación determinada por el rédox del entorno y la acidez (pH) . Específicamente, en condiciones oxidantes, la presencia de oxianiones negativos de As (V) está favorecida, mientras que en un entorno reductor predomina la forma no cargada de As (III) . El estado de oxidación del arsénico está directamente relacionado con su toxicidad, puesto que As (III) es 60 veces más tóxico que As (V) .
Los procedimientos de eliminación del arsénico se categorizan en relativamente selectivos y no selectivos. El no selectivo (nanofiltración, ósmosis inversa) no es preferible debido a su coste elevado y a la alteración de la composición del agua. Entre los métodos relativamente selectivos de eliminación del arsénico, los predominantes son la coprecipitación con hierro trivalente y la adsorción. Más específicamente, aunque la coprecipitación tiene un coste de operación relativamente pequeño, exige una supervisión muy especializada de la operación, incluyendo la adición controlada de un reactivo químico de hierro trivalente, así como el espesamiento y el tratamiento deshidratante del lodo producido que contiene el arsénico eliminado. Por esta razón, el uso de adsorbentes consumibles es, actualmente, la tendencia predominante, puesto que es de lejos el método de eliminación de arsénico más simple.
Los principales procedimientos de adsorción de arsénico se refieren al uso de lechos activados de alúmina (Al2O3) o de óxido de titanio (TiO2) o de oxihidróxidos de hierro en columnas. Durante los últimos años, el uso de oxihidróxidos de hierro en un lecho de adsorción se prefiere generalmente debido a:
ï· la capacidad satisfactoria de adsorción que presentan, ï· la reducción de la concentración de arsénico por debajo de 1 ï?g/l, ï· el procedimiento demanda una atención mínima durante la operación, y ï· el cumplimiento de requisitos de lixiviación para la eliminación segura de los oxihidróxidos saturados en los vertederos como un residuo inerte.
Sin embargo, los oxihidróxidos de hierro son capaces de eliminar eficientemente sólo las formas iónicas de As (V) [H2AsO4-/HAsO42-], mientras que su rendimiento con respecto a la forma no cargada H3AsO3 de As (III) es muy limitado. La demanda de eliminación de As (III) hace a los oxihidróxidos de hierro menos competitivos, puesto que el coste del tratamiento se hace significativamente mayor debido a la baja capacidad de adsorción para el As (III) , así como a la necesidad de adición de una etapa de oxidación extra para As (III) .
Generalmente, hay dos enfoques para superar el problema de la eliminación de As (III) usando adsorbentes:
1. el uso de dos compuestos en el que el primero (MnO2) oxida As (III) a As (V) , y el segundo (oxihidróxido de hierro) sorbe el As (V) producido,
2. el uso de un compuesto mixto (oxihidróxido de hierro/manganeso trivalente) que actúa como reactivo oxidante del As (III) y, al mismo tiempo, como medio adsorbente para el As (V) formado.
En el primer enfoque, para la eliminación eficiente de As (III) y As (V) igualmente, se usan adsorbentes bifásicos, un oxihidróxido de hierro y un dióxido de manganeso (MnO2) . El papel del MnO2 es oxidar As (III) a As (V) , que entonces es adsorbido y unido al oxihidróxido de hierro. El procedimiento de producción para tales materiales es la precipitación de manganeso como MnO2 por la reducción de KMnO4 en un entorno alcalino (pH > 7) y su fijación al oxihidróxido de hierro.
En consecuencia, el documento EP 2.168.677 describe el procedimiento sintético y la aplicación para la eliminación de As (III) de un óxido bifásico de hierro y manganeso. El desarrollo de este material tiene lugar en el sitio sobre un soporte a través de la reacción del sulfato de hierro (FeSO4) o tricloruro de hierro (FeCl3) o sulfato de manganeso
(MnSO4) y permanganato potásico (KMnO4) . Esta patente se refiere a la síntesis de una mezcla de dos materiales distintos: el hidróxido de hierro y MnO2. Este adsorbente tiene éxito oxidando As (III) mediante MnO2, y adsorbe el As (V) obtenido mediante una fase de hidróxido de hierro. En las publicaciones G. Zhang et al., Water Research 41 (2007) 1921 y G. Zhang et al., Journal of Hazardous Materials 168 (2009) 820, en las que se describe el procedimiento para una síntesis de óxido bifásico de hierro y manganeso mediante adición de disolución FeSO4 a una disolución de KMnO4 a un pH 7-8 en un reactor discontinuo, se da información adicional por el mismo investigador. La estructura del producto se caracteriza como una mezcla de oxihidróxido de hierro y MnO2 en un estado amorfo. La capacidad oxidante de MnO2 permite la mejora de la adsorción de As (III) por el oxihidróxido de hierro, aunque parece que la capacidad máxima de adsorción para As (V) es mucho menor que aquella para As (III) . En conclusión, los materiales dados a conocer en los tres documentos anteriores contienen MnO2, que tiene una capacidad muy baja de adsorción para As (V) y, como resultado, el incremento de su porcentaje en la síntesis del óxido bifásico es la causa de la disminución de la capacidad total de adsorción y el mayor coste del tratamiento.
La patente CN101024160 es una aproximación muy cercana a las publicaciones de G. Zhang et al., Water Research 41 (2007) 1921 y G. Zhang et al., Journal of Hazardous Materials 168 (2009) 820, pero se usa un pH muy alcalino en el intervalo de 9-11, en lugar de las condiciones alcalinas suaves (pH 7-8) , añadiendo una base, principalmente NaOH, a una disolución de KMnO4. En estas condiciones, la reacción de la disolución de FeSO4 gradualmente añadida a la disolución de KMnO4 da como resultado la formación, bajo pH arbitrario y alteración rédox, de un material compuesto férrico-manganeso que consiste en MnO2 y oxihidróxido de hierro. La reacción de síntesis es seguida por la inserción de diatomita, a fin de proporcionar un sustrato para la deposición del precipitado y obtener un gránulo adsorbente final, apropiado para uso en un lecho de adsorción. Sin embargo, el uso de sustrato implica la presencia de un porcentaje bajo de materiales activos, así como un tiempo de vida bajo y un incremento del coste del tratamiento, ya sea por la sustitución del material o por su regeneración. La capacidad de adsorción del material para As (III) (0, 5 ï?g/ml a una concentración en el equilibrio de 10 ï?g/l, pH 6, 7 y matriz de agua destilada) es incluso menor que aquella para oxihidróxidos de hierro comerciales (1, 5-3 ï?g/mg) , cuya insuficiencia para eliminar As (III) se pretende cubrir.
De forma similar, la publicación H. Zeng et al., Water Research, 42 (2008) 4629, presenta el estudio de un adsorbente de oxihidróxido de hierro que contiene alrededor de 20% de manganeso. El material consiste en dos fases separadas: oxihidróxido de hierro (ferrihidrita) y MnO2 con estructura de bimesita. Además, la fase de manganeso se sitúa en el interior del material, lejos de la superficie, y por lo tanto el contacto con el agua tratada, así como la acción oxidante esperada, es limitado.
En el documento US 2010/0051555 se describe un procedimiento de eliminación de As (III) que usa como primera etapa un lecho en columna de MnO2 para la oxidación de As (III) a As (V) , seguido de una etapa de precipitación con Fe (III) , en la que se captura As (V) . Sin embargo,... [Seguir leyendo]
Reivindicaciones:
1. Un método para la síntesis de una feroxihita de manganeso tetravalente (ï?-Fe (1-x) MnxOOH) , caracterizado por el hecho de que tiene lugar en un reactor de flujo continuo, en condiciones ácidas débiles y rédox controlado, y se aplica mediante las siguientes etapas:
i) En el reactor (1) se añade FeSO4 o FeCl2 como fuente de hierro, se añade KMnO4 o MnSO4 o MnCl2 o Mn (NO3) 2 como fuente de manganeso con una concentración de 1-100 g/l. Para la reacción, el pH se ajusta en el intervalo ácido débil 4-7 añadiendo uno o más de los reactivos NaOH, NaHCO3, Na2CO3, KOH, KHCO3, K2CO3. Al mismo tiempo, el rédox se ajusta en el interval.
30. 800 mV añadiendo uno o una combinación de más de uno de los reactivos KMnO4, NaClO2, ClO2, 2KHSO5·KHSO4·K2SO4, Na2S2O8, K2S2O8.
ii) Después, la reacción se termina en el reactor (2) . El valor del pH en el reactor (2) también se ajusta en el intervalo ácido débil 4-7 añadiendo uno o una combinación de más de uno de los reactivos NaOH, NaHCO3, Na2CO3, KOH, KHCO3, K2CO3, y al mismo tiempo el rédox se ajusta en el interval.
30. 800 mV añadiendo uno o más de los reactivos KMnO4, NaClO2, ClO2, 2KHSO5·KHSO4·K2SO4, Na2S2O8, K2S2O8.
El tiempo de retención debería ser al menos 30 min. en cada uno de los dos reactores.
iii) A continuación, el producto que sale del reactor (2) entra en el tanque (3) de espesamiento, en el que, por agitación lenta durante 1-48 h, la geometría del grano se controla entre esferas irregulares y esferas huecas, y el área específica entre 100 m2/g y 300 m2/g.
2. Un método para la síntesis de una feroxihita de manganeso tetravalente (ï?-Fe (1-x) MnxOOH) según la reivindicación 1, caracterizado por el hecho de que se observa la aplicación óptima del método cuando el pH de la reacción se ajusta a 5, 5 con una variabilidad de 0, 5, y el rédox se ajusta a 600 mV con una variabilidad de 50 mV.
3. Un método para la síntesis de una feroxihita de manganeso tetravalente (ï?-Fe (1-x) MnxOOH) según las reivindicaciones 1 y 2, caracterizado por el hecho de que el producto producido tras la aplicación del método se deshidrata mecánicamente (4) , se conforma en granos con un tamaño preferiblement.
25. 2500 ï?m (5) , y se seca .
10. 200º C (6) .
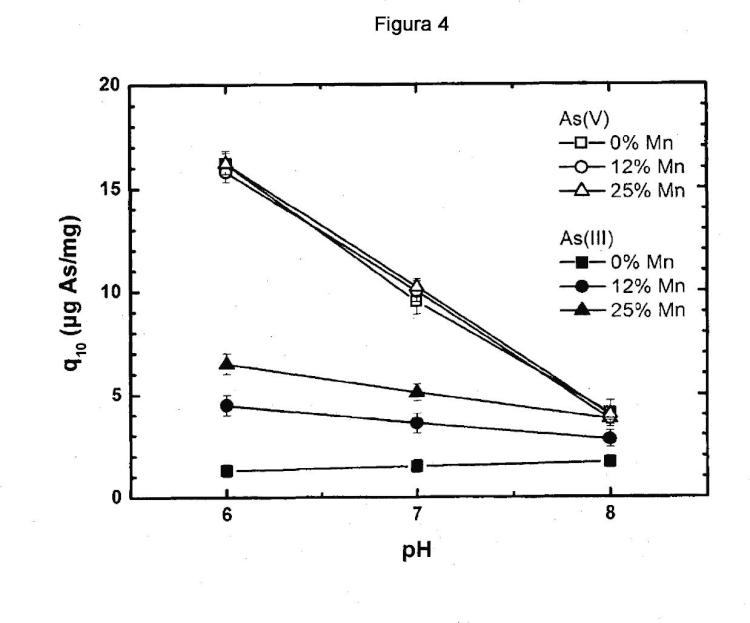
4. Material adsorbente producido según el método de las reivindicaciones 1 a 3, que se caracteriza por el hecho de que consiste en feroxihita de manganeso tetravalente de una sola fase (ï?-Fe (1-x) MnxOOH) , en el que un porcentaje de 0, 05-25% de hierro se ha sustituido isomórficamente por átomos de manganeso, con una geometría esférica irregular a esférica hueca y una superficie específica entre 100 m2/g y 300 m2/g y un tamaño de granos preferiblement.
25. 2500 ï?m.
5. Uso del material adsorbente de la reivindicación 4 producido según el método de las reivindicaciones 1 a 3, para la eliminación de arsénico trivalente o/y pentavalente, así como de vanadio, antimonio, mercurio, níquel, plomo, del agua en un lecho de columna o dispersiones de polvo.
Patentes similares o relacionadas:
Desulfuración y procedimientos novedosos para la misma, del 17 de Junio de 2020, de CHINA PETROLEUM & CHEMICAL CORPORATION: Procedimiento para la producción de una composición que comprende: (a) mezclar: 1) un líquido, 2) un compuesto que contiene cinc, 3) un material […]
Material de cubrimiento de contaminantes reactivos, dispersable, del 15 de Abril de 2020, de AMCOL INTERNATIONAL CORPORATION: Un material de cubrimiento subacuático para cubrir sedimento contaminado, que comprende una pluralidad de partículas compactadas de un material […]
Procedimiento para la desorción de metales que se unen a hierro y oxoaniones a partir de nanopartículas de óxido de hierro superparamagnéticas (SPION), del 17 de Febrero de 2020, de UNIVERSITAT AUTONOMA DE BARCELONA: Procedimiento para la desorción de metales que se unen a hierro y oxoaniones a partir de filtros adsorbentes a base de nanopartículas de óxido de […]
Método de procesamiento de desechos radiactivos líquidos, del 12 de Febrero de 2020, de Eksorb Ltd: Método de procesamiento y uso de desechos radiactivos líquidos, LRW, que implica la oxidación de los LRW y la retirada de radionucleidos de una fase líquida […]
Purificación de corrientes de hidrocarburos líquidas por medio de sorbentes que contienen cobre, del 10 de Septiembre de 2019, de EVONIK DEGUSSA GMBH: Procedimiento para la purificación de mezclas de hidrocarburos, en el que una mezcla de hidrocarburos contaminada que contiene hidrocarburos con de tres a ocho […]
Composiciones para la eliminación de hidrocarburos e hidrocarburos halogenados de entornos contaminados, del 21 de Agosto de 2019, de Remediation Products, Inc: Un método para preparar un catalizador en soporte que comprende: a. mezclar un carbón activado capaz de absorber contaminantes hidrocarbonados halogenados con […]
Catalizador de nano hierro altamente activo para la absorción de sulfuro de hidrógeno, del 7 de Agosto de 2019, de NEW TECHNOLOGY VENTURES, INC: Un sorbente útil para retirar compuestos de azufre de las corrientes de fluidos que comprende: un compuesto de hierro (II) seleccionado del grupo que consiste en óxidos, hidróxidos […]
Tratamiento de agentes de extracción degradados con oxima en soluciones orgánicas de proceso, del 26 de Junio de 2019, de Outotec (Finland) Oy: Un método para regenerar una solución de extracción orgánica con base en hidroxioxima degradada utilizada en la recuperación de metales mediante extracción líquido-líquido, […]