Dispositivo de cierre vascular.
Un dispositivo adecuado para un procedimiento de tratamiento de un sitio de compromiso vascular para sellaruna punción o abertura,
y para tratar, suprimir o prevenir una respuesta tisular en dicho sitio, en el que eldispositivo comprende:
una cantidad reguladora de respuesta tisular de rapamicina como agente terapéutico y un material o dispositivohemostático, caracterizado por que
el material o dispositivo hemostático comprende una lámina de colágeno que está impregnada, absorbida,adsorbida, saturada, dispersada o inmovilizada con rapamicina en una cantidad de aproximadamente 0,2 μg/cm2a 2 mg/cm2 del material de matriz de colágeno, que en forma seca está en una lámina que tiene 0,3-3,0 mm degrosor,
y en el que el dispositivo hemostático está configurado para aplicarse de forma perivascular alrededor de lasuperficie externa del vaso objetivo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/019468.
Solicitante: VASCULAR THERAPIES, LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 201 EAST 87TH STREET, APT. 14C NEW YORK, NY 10128 ESTADOS UNIDOS DE AMERICA.
Inventor/es: IYER,SRIRAM, KIPSHIDZE,NICHOLAS, NIKOLAYCHIK,VICTOR, ROUBIN,GARY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B17/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › Instrumentos, dispositivos o procedimientos quirúrgicos, p. ej. torniquetes (A61B 18/00 tiene prioridad; dispositivos anticonceptivos, pesarios, dispositivos para su introducción A61F 6/00; cirugía ocular A61F 9/007; cirugía otorrina A61F 11/00).
- A61K31/4745 A61 […] › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con sistemas cíclicos teniendo el nitrógeno como heteroátomo de un ciclo, p. ej. fenantrolinas (derivados de la yohimbina, vinblastina A61K 31/475; derivados de la ergolina A61K 31/48).
PDF original: ES-2452731_T3.pdf
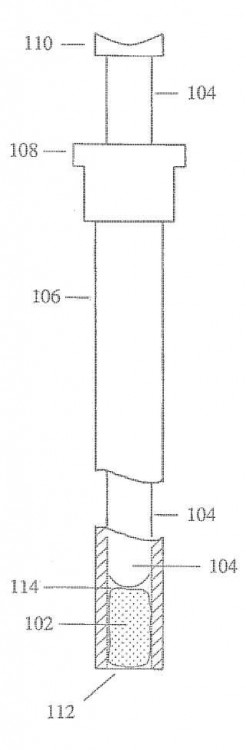
Fragmento de la descripción:
Dispositivo de cierre vascular
Antecedentes La presente invención se refiere, en general, a implantes terapéuticos, dispositivos, útiles para prevenir, suprimir, o tratar los fallos en los injertos de acceso vascular para hemodiálisis y otros procedimientos vasculares. La invención también se refiere a implantes terapéuticos que comprenden un material de matriz y un agente terapéutico, en los que la composición situada en contacto externo con un vaso sanguíneo (implante perivascular de la composición) se puede usar para lograr la hemostasis, por ejemplo, para sellar una ruptura en la pared vascular y administrar un agente terapéutico que puede regular la cantidad de respuesta tisular a la matriz implantada.
El documento US6554851 describe procedimientos de sellado de un sitio de inyección.
Se llevan a cabo procedimientos vasculares tales como la construcción de injertos de acceso para hemodiálisis y angioplastia para proporcionar un acceso vascular en pacientes con insuficiencia renal que necesitan hemodiálisis disfunción y para tratar afecciones tales como ateroesclerosis. Se pueden construir injertos de acceso vascular para hemodiálisis como una fístula arterio-venosa (por ejemplo, Brecisa-Cimino) , o como un injerto de interposición de material prostético (por ejemplo, politetrafluoroetileno "PTFE") o bien de tejido biológico (por ejemplo, vena) entre una arteria y una vena.
Normalmente, dichos injertos se construyen usando un segmento tubular o cilíndrico de material sustancialmente inerte y adecuadamente biocompatible tal como PTFE, el material más común usado para el acceso prostético de diálisis. En un enfoque, se interpone quirúrgicamente un segmento de PTFE entre una arteria y una vena en el brazo, antebrazo o muslo. A continuación, el injerto está disponible para repetidos accesos vasculares en la realización de hemodiálisis.
Después de la colocación del injerto, las zonas suturadas en la arteria y la vena sufren una curación. Sin embargo, el 60 por ciento de estos injertos fallan, normalmente debido al estrechamiento luminal, o estenosis, en el extremo venoso. Se desarrollan lesiones similares en injertos sintéticos de PTFE colocados en la circulación arterial, aunque la estenosis en injertos arteriales se desarrolla más lenta que en los extremos venosos. Es bien conocido el fallo o la disfunción de los injertos usados en la derivación quirúrgica de la arteria coronaria o en cirugía vascular periférica (por ejemplo, aorta-ilíaca, femoral-femoral, femoral-poplítea, femoral-tibial) . El fallo de los injertos vasculares o reconstrucción arterial resulta del estrechamiento luminal del vaso o conducto protésico, en o lejos del sitio anastomótico, del trombo intraluminal o una respuesta vasculoproliferativa, o de otras patologías, por ejemplo, infección del injerto protésico.
La hiperplasia de la neoíntima, una manifestación de la respuesta vasculoproliferativa, afecta al vaso y al orificio de injerto adyacente. La pared del vaso se espesa y la luz se estrecha debido a la migración y proliferación de células del músculo liso. La etiología de los fallos de injertos se puede relacionar con una variedad de estímulos físicos (por ejemplo, tensión de corte que provoca una interrupción hemodinámica) , químicos o biológicos, así como infección o rechazo de cuerpo extraño, lo que puede explicar por qué las fístulas que no implican un cuerpo extraño (por ejemplo, PTFE) permanecen patentes más tiempo que los injertos de acceso vascular que implican la interposición de un injerto de PTFE. Como la estenosis en el injerto se vuelve progresivamente más grave, el injerto se vuelve disfuncional y el acceso para procedimientos médicos subóptimo. Finalmente, la estenosis que se deja sin tratar da lugar a oclusión y a fallo de injerto.
Los extremos venosos de los injertos son propensos al estrechamiento por múltiples motivos. Esta localización está expuesta únicamente a presiones arteriales y tasas del flujo arterial, disipación de energía acústica o vibratoria en la pared del vaso y tejido circundante, punción repetida del injerto, e infusión de la sangre procesada. Además, en el ejemplo de hemodiálisis, el extremo venoso del injerto puede estar bañado en mitógenos liberados durante el paso de la sangre a través del tubo de diálisis o durante la activación de plaquetas en el sitio de la punción de la aguja.
Las muestras de tejido recogidas del sitio de anastomosis injerto-vena de los injertos estenósicos de PTFE durante una revisión quirúrgica muestran un estrechamiento significativo de la luz y se caracterizan por la presencia de células del músculo liso, acumulación de la matriz extracelular, angiogénesis dentro de la neoíntima y adventicia, y en presencia de una capa celular de macrófagos activos que cubre el material de injerto de PTFE. Se expresan una gran variedad de citocinas y factores estimuladores del crecimiento celular como el factores de crecimiento derivado de plaquetas (PDGF) , factor de crecimiento fibroblástico básico (bFGF) , y factor de crecimiento endotelial vascular (VEGF) por las células del músculo liso o miofibroblastos dentro de la neoíntima venosa, macrófagos que cubren ambos lados del injerto de PTFE, y recipientes dentro de la neoíntima y adventicia. Se ha sugerido que los macrófagos, citocinas específicas (PDGF, bFGF, y VEGF) , y la angiogénesis dentro de la neoíntima y adventicia probablemente contribuyen a la patogénesis de la hiperplasia de la neoíntima venosa.
En el ejemplo de hemodiálisis, la hiperplasia de la neoíntima venosa caracterizada por estenosis y posterior trombosis representa la inmensa mayoría de las patologías que dan como resultado el fallo en el injerto de diálisis de PTFE, que evita la hemodiálisis, dando lugar a una insuficiencia renal, deterioro clínico, y muerte. La disfunción de acceso vascular es la causa más importante de morbilidad y de hospitalización en la población con hemodiálisis. Sin embargo, a pesar de la magnitud del problema y de los costes asociados, actualmente no existen tratamientos eficaces para la prevención o el tratamiento de hiperplasia de la neoíntima venosa en injertos de diálisis de PTFE.
Una vez que se ha producido la estenosis, el tratamiento consiste en una reconstrucción vascular adicional. Un procedimiento actual de tratamiento implica la reducción u obliteración del estrechamiento y la restauración del flujo sanguíneo a través del injerto por tratamientos no quirúrgicos, basados en catéter percutáneo tales como angioplastia con balón. Este procedimiento implica hacer uso de un catéter con balón en el sitio del bloqueo e inflar el balón para incrementar el diámetro luminal mínimo del vaso comprimiendo el material lo que provoca la restricción contra el interior de la pared del vaso. Dependiendo de la longitud y la gravedad de la restricción, se puede repetir el procedimiento varias veces inflando y desinflando el balón. Cuando se completa, se retira el catéter con balón del sistema.
Aunque se puede usar la angioplastia con balón como un procedimiento "independiente", se acompaña frecuentemente con la utilización de una endoprótesis. Una endoprótesis es un dispositivo de soporte o estructura expandible que se sitúa dentro de la vasculatura para evitar el retroceso mecánico y para reducir la posibilidad de reestrechamiento o reestenosis, en el sitio de la restricción original. Las endoprótesis son "expandibles con balón" o "autoexpansibles" y cuando se utilizan de forma endovascular, contiguas a la pared interna del vaso. Esté o no colocada una endoprótesis, esta forma de tratamiento tiene un alto riesgo de fallo, es decir, un alto riesgo de reestenosis en el sitio del tratamiento. A menos que la estenosis se trate de forma eficaz y permanente, el fallo de injerto tiende a seguir.
En el acontecimiento de fallo de injerto, el paciente debe sufrir un procedimiento endovascular, es decir, un procedimiento no quirúrgico, percutáneo basado en catéter o cirugía vascular de repetición tal como una trombectomía para "descoagular" el injerto o para colocar otro injerto de acceso vascular o una derivación en un sitio diferente, a menos que el paciente reciba un trasplante de riñón. Dados los problemas obvios de las cirugías de repetición y la disponibilidad limitada de los trasplantes, se necesita un tratamiento que sea tanto eficaz y duradero para prevenir y tratar la estenosis.
La gran mayoría de los enfoques actuales para tratar la respuesta vasculoproliferativa que se cree que es la base fisiopatológica de la estenosis y reestenosis se basan en el tratamiento dentro de la luz vascular o del injerto. Un enfoque actual utiliza endoprótesis recubiertas con fármaco o impregnadas... [Seguir leyendo]
Reivindicaciones:
1. Un dispositivo adecuado para un procedimiento de tratamiento de un sitio de compromiso vascular para sellar una punción o abertura, y para tratar, suprimir o prevenir una respuesta tisular en dicho sitio, en el que el dispositivo comprende:
una cantidad reguladora de respuesta tisular de rapamicina como agente terapéutico y un material o dispositivo hemostático, caracterizado por que el material o dispositivo hemostático comprende una lámina de colágeno que está impregnada, absorbida, adsorbida, saturada, dispersada o inmovilizada con rapamicina en una cantidad de aproximadamente 0, 2 μg/cm2 a 2 mg/cm2 del material de matriz de colágeno, que en forma seca está en una lámina que tiene 0, 3-3, 0 mm de grosor,
y en el que el dispositivo hemostático está configurado para aplicarse de forma perivascular alrededor de la superficie externa del vaso objetivo.
2. El dispositivo de la reivindicación 1, en el que el colágeno es colágeno bovino tipo I.
3. El dispositivo de acuerdo con la reivindicación 2, en el que el colágeno está seleccionado del grupo que consiste 15 en tipo I, tipo II, tipo III II, tipo IV, tipo XI, y mezclas de los mismos.
4. El dispositivo de la reivindicación 1, en el que la rapamicina está presente en una cantidad de aproximadamente 0, 02 μg a 100 mgs/mg en peso de la lámina de combinación de colágeno.
5. El procedimiento de la reivindicación 1, en el que el material hemostático está seleccionado del grupo que consiste en colágeno, y mezclas de colágeno y fibrina y/o quitosano.
6. El dispositivo de la reivindicación 5, en el que el material hemostático comprende además fibrina.
7. El dispositivo de la reivindicación 5, en el que el material hemostático comprende además quitosano.
8. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 1-7, en el que el material hemostático es biodegradable.
9. El dispositivo de acuerdo con la reivindicación 1, en el que el dispositivo hemostático comprende un coadyuvante. 25 10. El dispositivo de acuerdo con la reivindicación 9, en el que el coadyuvante inhibe la calcificación.
11. El dispositivo de acuerdo con la reivindicación 10, en el que el coadyuvante es vitamina K.
Angiogramas de seguimiento de cuatro semanas
La flechas con círculo en la cola indican sitio de anastomosis
Histopatología a las 4 semanas
La región entre las flechas pequeñas indica engrosamiento de la neoíntima
El tratamiento con rapamicina Induce ARNm p21
Se obtuvieron tejidos de animales tratados y no tratados, se preparó ARN y se transcribió de forma inversa a ADNc, que se amplificó para el gen constitutivo b-actina y p21 por PCR. Los resultados demuestran que la expresión de ARNm p21 sólo se observó en tejidos tratados con rapamicina.
ARNm p21 ARNm β-actina 1 = tratado con rapamicina 2 = no tratado Fig 20
Patentes similares o relacionadas:
 Método para usar una cubierta de sonda, del 29 de Julio de 2020, de SABAN VENTURES PTY LIMITED: Un método para prevenir la contaminación de una sonda ultrasónica descontaminada que comprende el paso de, inmediatamente después de la desinfección, […]
Método para usar una cubierta de sonda, del 29 de Julio de 2020, de SABAN VENTURES PTY LIMITED: Un método para prevenir la contaminación de una sonda ultrasónica descontaminada que comprende el paso de, inmediatamente después de la desinfección, […]
Sistemas para el tratamiento de enfermedades del ojo, del 22 de Julio de 2020, de ALCON, INC: Un dispositivo para tratar un ojo de mamífero que tiene un párpado , que comprende: un escudo escleral que puede posicionarse cerca de una superficie […]
Herramienta de pinza de agarre, del 22 de Julio de 2020, de COLOPLAST A/S: Herramienta de pinza de agarre para extraer una endoprótesis desde un paciente, que comprende: una carcasa de mango que forma una parte […]
Adaptadores quirúrgicos para usar entre el conjunto de mango quirúrgico y las unidades de carga quirúrgica, del 22 de Julio de 2020, de Covidien LP (100.0%): Un conjunto adaptador para interconectar selectivamente una unidad de carga quirúrgica y un conjunto de mango que tiene al menos un […]
Aparatos de grapado quirúrgico, del 15 de Julio de 2020, de Covidien LP (100.0%): Un aparato de grapado quirúrgico , que comprende: una carcasa que tiene un actuador ; un miembro alargado que se extiende desde la carcasa; […]
Aplicadores que tienen sujetadores implantables para braquiterapia, del 15 de Julio de 2020, de Covidien LP (100.0%): Un aplicador de sujetadores que comprende: una porción de cuerpo que incluye un conjunto de mango ; un conjunto […]
Interfaz de manipulador robótico para herramientas quirúrgicas articuladas, del 8 de Julio de 2020, de Microsure B.V: Interfaz de manipulador robótico para acoplar una herramienta quirúrgica articulada a un manipulador de un robot quirúrgico, comprendiendo […]
Implante quirúrgico para la reparación de la pared muscular, del 1 de Julio de 2020, de JOHNSON & JOHNSON MEDICAL GMBH: Un implante quirúrgico adaptado para reparar un defecto del tejido o de la pared muscular, que comprende una sección exterior y una sección interior (6; […]