Procedimiento de obtención de condroitina sulfatada en las posiciones 4 o 6 de restos de N-acetil galactosamina.
Procedimiento de producción de sulfato de condroitina, en el que los restos N-acetil galactosamina sulfatados en las posiciones 4 o 6 están presentes en la misma cadena de polisacárido;
caracterizado poque comprende las siguientes etapas de reacción:
a) preparación del derivado de 4,6-bencilideno en los restos de la N-acetilgalactosamina en forma ácida;
b) acilación de los grupos hidroxilo 2 y 3 de los restos de ácido glucurónico;
c) apertura oxidativa del ciclo del bencilideno;
d) sulfatación de los grupos hidroxilo 4 o 6 de los restos de N-acetilgalactosamina;
e) eliminación del grupo protector de benzoílo de las posiciones 4 o 6 de los restos de N-acetilgalactosamina, y de los grupos protectores de acilo de los grupos hidroxilo 2 y 3 de los restos de ácido glucurónico;
f) purificación del sulfato de condroitina 4 o 6 obtenido de esta manera.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2011/069972.
Solicitante: ALTERGON S.A..
Nacionalidad solicitante: Suiza.
Dirección: Via Dogana Vecchia 2 6900 Lugano SUIZA.
Inventor/es: DE ROSA, MARIO, BEDINI,EMILIANO, DE CASTRO,CRISTINA, DI NOLA,ANNALIDA, PARRILLI,MICHELANGELO, RESTAINO,ODILE FRANCESCA, SCHIRALDI,CHIARA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C08B37/00 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21).
PDF original: ES-2534393_T3.pdf
Fragmento de la descripción:
Procedimiento de obtención de condroitina sulfatada en las posiciones 4 o 6 de restos de n-acetil galactosamina Campo de la invención La presente invención se refiere al campo de los procedimientos para la modificación estructural de polisacáridos.
Estado de la técnica El sulfato de condroitina pertenece a la familia más amplia de glicosaminoglicanos denominada GAG. Estos polisacáridos, unidos covalentemente a proteínas, tales como proteoglicanos, son constituyentes ubicuos de la matiz extracelular de todos los tejidos conectivos, en la que llevan a cabo numerosas funciones.
El sulfato de condroitina es un polisacárido lineal natural formando por restos alternantes de N-acetil-Dgalactosamina β 1→4 y D-glucuronato β 1→3. En los vertebrados, la condroitina está presente en formas sulfatadas de diversa manera; los restos implicados en la sulfatación son los grupos hidroxilo 4 y 6 de la N-acetilD-galactosamina, y en algunos casos también los grupos hidroxilo 2 y 3 del ácido glucurónico.
El peso molecular de la condroitina, y la cantidad y sitios de sulfatación, dependen de la especie, la edad y el tipo de tejido.
El sulfato de condroitina se utiliza como medicamento condrioprotector y antirreumático, con aplicaciones en el tratamiento de la osteoartritis tibiofibular de la rodilla y osteoartritis del cartílago de la articulación.
Actualmente, el sulfato de condroitina se obtiene mediante técnicas de extracción a partir de diversas fuentes animales, tales como cartílago de cerdo, cartílago de aleta de tiburón y de teleósteos. La escasez de la materia prima y la complejidad del procedimiento de purificación posterior restringe la disponibilidad de este principio activo a nivel mundial; su mercado está controlado por tanto por la imposibilidad de satisfacer la actual demanda de crecimiento. Además, las regulaciones cada vez más severas que controlan la seguridad de los medicamentos de origen animal que se aprueban frecuentemente pueden excluir del mercado farmacéutico en el futuro el sulfato de condroitina extraído.
En consecuencia existe un creciente interés en el desarrollo de estrategias de fabricación alternativas basadas en la biotecnología y en la síntesis química para obtener este tipo de polisacáridos o sus precursores.
La literatura científica (Rodriguez ML y col., Eur. J. Biochem., 1988, 177, 117-24; Manzoni M y col., Biotechnology Letters, 1996, 18, 383-6) y la literatura de patentes (documento WO 01/02597 A1) informan de la posibilidad de producir mediante fermentación, utilizando cepas de E. coli K4 naturales o recombinantes que producen un derivado de condroitina, el polisacárido K4, cuya estructura básica de carbono es idéntica a la de la condroitina, excepto por el injerto de ácido glucurónico procedente de restos de α-fructofuranosa en C3. La condroitina se puede obtener a partir del polisacárido K4 mediante hidrólisis ácida controlada de los restos de fructosa.
Los elevados rendimientos de fabricación, la simplicidad del procedimiento de purificación posterior desarrollado, los bajos costes globales del procedimiento y su bajo impacto ambiental hacen a dicha síntesis superior a las estrategias de biotecnología anteriormente descritas.
Dicho procedimiento de fermentación, si se suplementa adecuadamente por una estrategia de sulfatación química regioselectiva de la condroitina, puede por tanto hacer que el método biotecnológico sea competitivo en comparación con procedimientos convencionales para extraer sulfato de condroitina de materias primas de origen animal, que pueden quedar eliminadas del mercado farmacéutico por recientes desarrollos de la normativa relativa a la seguridad del producto.
La sulfatación de polisacáridos estructuralmente relacionados con la condroitina, tales como los polisacáridos K4 y K5, que están formados, como se ha indicado, por secuencias repetitivas de ácido glucurónico y N-acetilglucosamina en el caso de K5, y ácido glucurónico y N-acetil-glucosamina en el caso de K4, en las que se han injertado restos de fructosa, en este caso, en la posición 2 del ácido glucurónico, se describe en una serie de artículos y patentes, pero ninguno de esos documentos implica procedimientos de sulfatación regioselectiva que produzcan un sulfato de condroitina con las mismas características estructurales que la variedad humana.
Un esquema de síntesis para la sulfatación regioselectiva de la condroitina que conduce a un modelo de sulfatación similar al característico de la condroitina humana, y de la condroitina de origen extractivo usada actualmente de forma amplia como un medicamento condrioprotector y antirreumático en el tratamiento de enfermedades de las articulaciones sigue siendo por tanto tópico, pero no resuelto.
Sumario Se divulga un procedimiento que, por medio de la síntesis química, a partir de la condroitina obtenida mediante un procedimiento biotecnológico, produce un modelo de sulfatación similar al del que caracteriza a la condroitina humana y a la condroitina de origen extractivo, utilizando soluciones de síntesis compatibles con un escalado industrial.
Descripción detallada de la invención La presente invención, al eliminar los problemas presentes en los procedimientos conocidos de acuerdo con la técnica anterior, produce, mediante síntesis química, condroitina sulfatada en la que los restos de N-acetilgalactosamina están sulfatados en las posiciones 4 o 6 en la propia cadena de polisacárido, como se ha observado en el sulfato de condroitina humano y en el sulfato de condroitina obtenido actualmente mediante extracción a partir de fuentes naturales.
La presente invención se refiere en consecuencia a un procedimiento para la producción de sulfato de condroitina en el que están presentes restos de galactosamina sulfatados en las posiciones 4 o 6 en la propia cadena de polisacárido, caracterizado por las siguientes etapas: a) formación del correspondiente derivado de 4, 6
bencilideno en los restos de la N-acetil-galactosamina de la condroitina en forma ácida; b) acilación de los grupos hidroxilo 2 y 3 de los restos de ácido glucurónico; d) apertura oxidativa del ciclo del bencilideno; d) sulfatación de los grupos hidroxilo 4 o 6 de los restos galactosamina; e) eliminación del grupo protector de benzoílo de las posiciones 4 o 6 de los restos de N-acetil-galactosamina y de los grupos protectores de acetilo en los hidroxilos 2 y 3 de los restos de ácido glucurónico; f) purificación de condroitina 4 o 6 sulfatada.
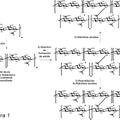
El procedimiento de acuerdo con la invención se ilustra esquemáticamente a continuación.
El elemento clave del procedimiento de síntesis de acuerdo con la invención es la apertura oxidativa del ciclo de bencilideno, que permite la protección selectiva de las posiciones 4 o 6 de la N-acetil-galactosamina con un grupo benzoílo. De esta forma, tras solo 3 etapas de protección, la cadena de polisacárido presenta unidades de disacáridos que tienen una única función alcohol aún libre, y solo en la posición 4 o 6 del resto N-acetilgalactosamina. La sulfatación completa de un polisacárido protegido de esta manera produce fácilmente un sulfato de condroitina, en el que los restos de N-acetil galactosamina sulfatada en las posiciones 4 o 6 están presentes en la misma cadena de polisacárido. La escisión hidrolítica de los grupos protectores produce un sulfato de condroitina con peso molecular y modelo de sulfatación característicos similares a los de la condroitina humana. El esquema de reacción reivindicado, caracterizado por un único procedimiento de purificación final basado en procedimientos de membranas que se puede escalar industrialmente de forma sencilla, produce sulfato de condroitina 4 o 6 con buenos rendimientos a costes compatibles con el escalado industrial.
Los ejemplos siguientes describen la producción de condroitina sulfatada, en la que los restos de N-acetilgalactosamina están sulfatados en las posiciones 4 o 6 en la propia cadena de polisacárido, una característica estructural recurrente en el sulfato de condroitina humano y en el sulfato de condroitina obtenido actualmente mediante extracción a partir de fuentes naturales.
Ejemplo 1 -Síntesis de 4, 6-bencilideno derivado de condroitina. Preparación de condroitina ácida Se disolvieron 50 gramos de condroitina obtenidos mediante fermentación tal como se ha descrito en la solicitud de patente italiana Nº 1.312.984, que tenía un peso molecular de 38 kDa y una pureza > 90 %, en 1, 5 l de agua MilliQ y se mantuvieron con agitación durante aproximadamente 2 h a temperatura ambiente con 250 g de FLUKA Dowex 50 WX8 H+ en forma de resina de intercambio catiónico, malla 50-100, lavada y neutralizada... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento de producción de sulfato de condroitina, en el que los restos N-acetil galactosamina sulfatados en las posiciones 4 o 6 están presentes en la misma cadena de polisacárido; caracterizado poque comprende las siguientes etapas de reacción: a) preparación del derivado de 4, 6-bencilideno en los restos de la N-acetilgalactosamina en forma ácida; b) acilación de los grupos hidroxilo 2 y 3 de los restos de ácido glucurónico; c) apertura oxidativa del ciclo del bencilideno; d) sulfatación de los grupos hidroxilo 4 o 6 de los restos de N-acetilgalactosamina; e) eliminación del grupo protector de benzoílo de las posiciones 4 o 6 de los restos de N-acetilgalactosamina, y de los grupos protectores de acilo de los grupos hidroxilo 2 y 3 de los restos de ácido glucurónico; f) purificación del sulfato de condroitina 4 o 6 obtenido de esta manera.
2. El procedimiento de acuerdo con la reivindicación 1, en el que la etapa a) se obtiene haciendo reaccionar condroitina en forma ácida con α, α-dimetoxitolueno en presencia de un catalizador ácido en fase heterogénea durante 10-30 h .
7. 90 º C.
3. El procedimiento de acuerdo con la reivindicación 1, en el que se obtiene la etapa b) , para la inserción de grupos protectores de acilo en los grupos hidroxilo 2 y 3 de los restos de ácido glucurónico del derivado de 4, 6-bencilideno de la condroitina, haciendo reaccionar el producto de la etapa a) en fase heterogénea a temperatura ambiente durante 10-30 h con un anhídrido de ácido carboxílico en presencia de trietilamina y 4 (dimetilamina) -piridina.
4. El procedimiento de acuerdo con la reivindicación 1, en el que la etapa c) , para la apertura oxidativa del anillo de bencilideno, se lleva a cabo haciendo reaccionar el producto de la etapa b) en fase heterogénea, a baja temperatura, en presencia de luz visible, durante 10-30 h con bromato de sodio y ditionito de sodio.
5. El procedimiento de acuerdo con la reivindicación 1, en el que la etapa d) , para la sulfatación en 4 o 6 de los restos de N-acetil-galactosamina, se lleva a cabo haciendo reaccionar el producto de la etapa c) en fase heterogénea, a temperaturas comprendidas entre 10 y 100 º C, durante 10-60 h con un complejo de piridinaanhídrido sulfúrico.
6. El procedimiento de acuerdo con la reivindicación 1, en el que la etapa e) , para la eliminación del grupo protector de benzoílo de las posiciones 4 o 6 de los restos de N-acetil-galactosamina y de los grupos protectores de acilo en los hidroxilos 2 y 3 de los restos de ácido glucurónico, implica hidrólisis ácida para eliminar cualquier resto de bencilideno aún presente en las posiciones 4-6 de la N-acetil-galactosamina, seguido por hidrólisis alcalina para eliminar los grupos acilo.
7. El procedimiento de acuerdo con la reivindicación 6, en el que la hidrólisis ácida se lleva a cabo disolviendo el producto de la etapa d) en agua y calentando este a 50 º C durante 0, 1-10 h, y la posterior hidrólisis básica se lleva a cabo ajustando la solución de hidrólisis ácida a pH 13 con NaOH y manteniéndola a temperatura ambiente durante 1-20 h.
8. El procedimiento de acuerdo con la reivindicación 1, en el que la etapa f) , que comprende la purificación de la condroitina 4 o 6 sulfatada de los restos de N-acetil-galactosamina, implica la ultrafiltración/diafiltración en membranas con un corte de 2-20 kDa y el secado del retentato.
9. El procedimiento de acuerdo con la reivindicación 8, en el que ultrafiltración/diafiltración se lleva a cabo con membranas con un corte de 10 kDa.
10. Sulfato de condroitina, obtenido de acuerdo con las reivindicaciones 1 a 9, en el que los restos de N-acetilgalactosamina en cada cadena de polisacárido se sulfatan en las posiciones 4 o 6 en un porcentaje comprendido entre 20 y 95 %.
11. El sulfato de condroitina de acuerdo con la reivindicación 10, en el que la relación entre la sulfatación en las posiciones 4 y 6 de los restos de galactosamina está comprendido entre 0, 1 y 10.
12. El sulfato de condroitina de acuerdo con las reivindicaciones 10 y 11, que tiene un peso molecular comprendido entre 5 y 50 kDa.
13. El sulfato de condroitina de acuerdo con la reivindicación 12, que tiene un peso molecular comprendido entre 12 y 30 kDa.
14. El sulfato de condroitina de acuerdo con la reivindicación 13, que tiene un peso molecular comprendido entre 15 y 25 kDa.
Patentes similares o relacionadas:
Separación de contaminantes de polisacárido de Streptococcus pneumoniae por manipulación del pH, del 17 de Junio de 2020, de WYETH LLC: Un procedimiento de reducción del contenido de proteínas y preservar el contenido de polisacárido capsular en un caldo de lisado celular complejo de Streptococcus pneumoniae, […]
Compuestos y sus efectos sobre el control del apetito y la sensibilidad a la insulina, del 10 de Junio de 2020, de IMPERIAL COLLEGE INNOVATIONS LIMITED: Un éster de propionato de inulina para su uso en la terapia para la reducción del apetito, ingesta de alimentos y/o ingesta de calorías y/o para mejorar […]
Evaluación de preparaciones de heparina, del 10 de Junio de 2020, de MOMENTA PHARMACEUTICALS, INC: Un procedimiento para identificar si se utilizó un procedimiento que incluye oxidación u oxidación seguido de tratamiento con un ácido para elaborar […]
Preparación de poli(ésteres de alfa-1,3-glucano) usando anhídridos orgánicos cíclicos, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un compuesto de poli(éster de alfa-1,3-glucano) representado por la estructura **(Ver fórmula)** en donde (i) n es al menos […]
Composiciones detergentes, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un derivado de polisacárido, en donde el derivado de polisacárido comprende un polisacárido sustituido con: a) uno o más grupos de poliamina; […]
 Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Reticulante de carbohidratos, del 6 de Mayo de 2020, de GALDERMA S.A.: Un producto de hidrogel que comprende moléculas de glucosaminoglucano como el polímero hinchable, en donde las moléculas de glucosaminoglucano se reticulan covalentemente […]
Hidrogeles polimerizables fluorados para vendajes de heridas y procedimientos para hacerlos, del 18 de Marzo de 2020, de THE UNIVERSITY OF AKRON: Un hidrogel que comprende: polímeros reticulados, los polímeros tienen cadenas principales de polisacáridos, donde las cadenas principales […]