COMPOSICIONES INYECTABLES GELIFICANTES A BASE DE PARTICULAS DE POLIMEROS RETICULADOS Y DE POLIMEROS NO RETICULADOS Y SUS APLICACIONES.
Composición inyectable gelificante a base de polímeros para la implantación intra-tisular y/o intra-vascular,
caracterizada por que comprende:
- al menos un polímero lineal insoluble en agua y soluble en al menos un disolvente miscible en agua,
- al menos un polímero reticulado hidrófilo e insoluble en agua,
- al menos un disolvente biocompatible miscible en agua; y por que se presenta en forma de una suspensión de partículas de dicho polímero reticulado hidrófilo en una solución de dicho polímero lineal
Tipo: Resumen de patente/invención. Número de Solicitud: W04000003FR.
Solicitante: ASSISTANCE PUBLIQUE - HOPITAUX DE PARIS
UNIVERSITE PARIS SUD XI.
Nacionalidad solicitante: Francia.
Dirección: 3 AVENUE VICTORIA,75004 PARIS.
Inventor/es: LAURENT, ALEXANDRE, LABARRE, DENIS, HONIGER, JIRI, LABSKY,JIRI, CHAPOT,RENE, WASSEF,MICHEL, SERON,AYMERIC.
Fecha de Publicación: .
Fecha Concesión Europea: 5 de Agosto de 2009.
Clasificación Internacional de Patentes:
- A61K47/32 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Compuestos macromoleculares obtenidos por reacciones en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. carbómeros (resinas de carbopol).
- A61K9/00M5
- A61L24/00H7
- A61L24/04M
- A61L27/26 A61 […] › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › Mezclas de materiales macromoleculares.
- A61L27/52 A61L 27/00 […] › Hidrogeles o hidrocoloides.
- A61L31/04B
- A61L31/14F
Clasificación PCT:
Clasificación antigua:
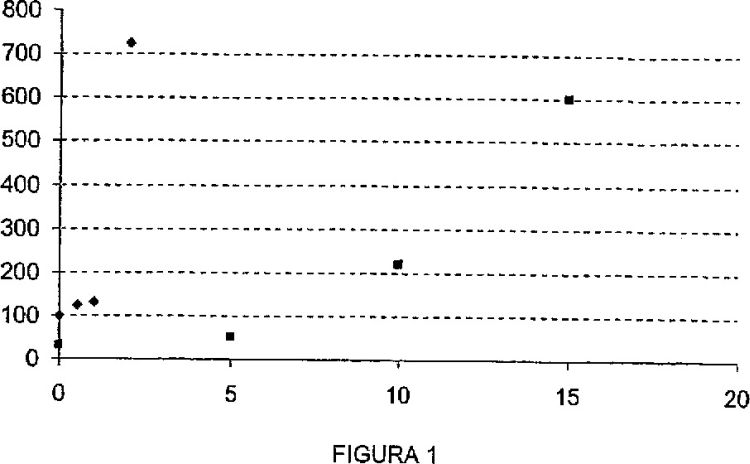
Fragmento de la descripción:
Composiciones inyectables gelificantes a base de partículas de polímeros reticulados y de polímeros no reticulados y sus aplicaciones.
La presente invención se refiere a composiciones inyectables gelificantes que contienen una asociación de polímeros lineales y polímeros reticulados, así como a sus aplicaciones, particularmente para realizar oclusiones terapéuticas (embolizaciones), el relleno de conductos y cavidades o la implantación por vía percutánea.
En el entorno médico es frecuente el uso de biomateriales reabsorbibles o no reabsorbibles. Estos biomateriales pueden presentarse de diferentes formas y utilizarse por ejemplo para realizar oclusiones vasculares terapéuticas (embolizaciones), para la reconstrucción tisular, el tratamiento del reflujo gastro-esofágico, la incontinencia urinaria, la implantación percutánea, la reducción de arrugas y en general el relleno de conductos y cavidades.
En este contexto, es normal utilizar materiales inyectables que se presentan en forma gelificada y que se solidifican in situ inmediatamente después de la inyección.
De este modo ya se han propuesto colas y cementos acrílicos inyectables, por ejemplo, a base de isobutilcianoacrilato, N-butilcianoacrilato o también poli(metacrilato de metilo) (PMMA). Estos materiales presentan sin embargo el inconveniente de ser tóxicos y difíciles de manipular en la medida en que pueden ocasionar que se adhiera el catéter utilizado para la inyección. Es más difícil controlar in situ el tiempo de polimerización de estos materiales.
Del mismo modo ya se ha propuesto sustituir las colas y los cementos acrílicos, particularmente en las patentes de Estados Unidos 5.580.568, 5.695.480 y 5.851.508, por soluciones gelificantes compuestas principalmente por un polímero insoluble en agua en solución en un disolvente biocompatible y miscible en agua como por ejemplo dimetilsulfóxido (DMSO). De acuerdo con estos documentos, el polímero en solución se solidifica in situ tras la inyección de acuerdo con un fenómeno de extracción del disolvente que es miscible en agua y por consiguiente miscible en el medio fisiológico naturalmente acuoso.
Sin embargo, estas soluciones gelificantes presentan un determinado número de inconvenientes:
- - el tiempo necesario de salida del disolvente condiciona el tiempo de gelificación del polímero. De este modo, a mayor cantidad de disolvente presente en la solución, mayor es el tiempo de gelificación;
- - durante la gelificación in situ la solución posee una resistencia mecánica reducida frente al flujo circulante. La capa externa en contacto con la sangre se gelifica en primer lugar, mientras que el interior del depósito permanece líquido. La deformabilidad del depósito bajo flujo es considerable mientras que no finalice la fase de gelificación del polímero. Este tiempo puede ser demasiado largo para que se produzca la solidificación del polímero antes de que la solución se transporte por el flujo sanguíneo. En la práctica, la utilización de dichas soluciones gelificantes requiere una inyección muy lenta para que la solución pueda gelificarse in situ a medida que sale del catéter. Si la inyección no se realiza de manera suficientemente lenta, la solución gelificante se deforma para estirarse y transportarse a través del flujo sanguíneo como un líquido viscoso, o formar una placa contra la pared vascular de una capa más o menos espesa;
- - durante la solidificación del polímero, se produce una disminución de volumen del orden del 20 al 80% (fenómeno de retracción), debido a la extracción del disolvente por el flujo circulante y poco compensado por la entrada del líquido fisiológico en el polímero durante la solidificación (precipitación), lo que produce menor depósito de polímero que de solución inyectada. No es posible compensar esta pérdida de volumen aumentando la concentración de polímero en la solución gelificante ya que esto produciría un aumento considerable de la viscosidad de la solución gelificante que obstaculizaría o impediría la inyección a través de agujas o microcatéteres por ejemplo;
- - los disolventes biocompatibles miscibles en agua utilizados para disolver los polímeros, en particular el DMSO, tienen una toxicidad vascular local y sistémica considerable (Mottu F et al., PDA J. Pharm. Sci. Technol., 2000, 54 (6), 456-469), que por supuesto es proporcional a la dosis liberada en el flujo sanguíneo. Además, con dicho disolvente, la inyección de las soluciones gelificantes requieren el uso de catéteres especiales, diseñados para resistir el disolvente. No obstante, incluso en este caso, el disolvente puede sin embargo dañar los microcatéteres por los que se inyecta.
Con el fin de solucionar todos estos problemas los inventores han detallado lo que se considera el objeto de la invención.
La presente invención tiene por tanto como objeto una composición inyectable gelificante a base de polímeros para la implantación intra-tisular y/o intra-vascular, caracterizada por que comprende:
- - al menos un polímero lineal insoluble en agua y soluble en al menos un disolvente miscible en agua,
- - al menos un polímero reticulado hidrófilo e insoluble en agua, teniendo dicho polímero reticulado una afinidad por dicho polímero lineal y
- - al menos un disolvente biocompatible miscible en agua; y/o por que se presenta en forma de una suspensión de partículas de dicho polímero reticulado hidrófilo en una solución de dicho polímero lineal.
La composición inyectable gelificante de acuerdo con la invención presenta las siguientes ventajas y características físico-químicas:
- - permite obtener, para un mismo volumen de composición gelificante inyectado que con las soluciones gelificantes descritas en el estado de la técnica anterior, una cantidad final de polímero depositado comparativamente mayor por unidad de volumen inyectado;
- - presenta una viscosidad inferior a la de las soluciones inyectables descritas en el estado de la técnica anterior conteniendo la misma masa de polímero soluble;
- - conduce a una cohesión más fuerte del gel depositado en el lumen vascular;
- - permite disminuir la cantidad de disolvente inyectado al paciente;
- - permite acortar el tiempo de solidificación del polímero lineal con respecto a una solución gelificante clásica, ya que, aunque la cantidad de disolvente es menor, la cinética de salida del disolvente de la mezcla es más rápida.
Cuando la composición inyectable gelificante de acuerdo con la invención se inyecta en un líquido fisiológico, que por naturaleza es acuoso, el disolvente abandona la mezcla de polímeros, lo que produce la precipitación y la solidificación del polímero lineal que atrapa entonces el polímero reticulado hidrófilo. La cantidad total y el volumen del material aumentan por la presencia del polímero reticulado hidrófilo que, debido a su afinidad por el agua, se hincha en medio acuoso.
En el sentido de la presente invención, el término "afinidad" utilizado para calificar el polímero reticulado presente en la composición inyectable gelificante se entiende como cualquier causa que requiera que el polímero reticulado se combine con el polímero lineal y que los mantenga unidos cuando se realice la combinación. Como ejemplo, esta afinidad puede ser particularmente química.
De acuerdo con la invención, el o los polímeros lineales se seleccionan preferentemente entre los polímeros neutros o poco cargados.
Entre dichos polímeros, pueden citarse particularmente los poli(acrilatos de alquilo), poli(metacrilatos de alquilo), poli(cianoacrilatos de alquilo), poli(acetato de vinilo), poli(butirato de vinilo), poli(vinil formal), poli(vinil acetal), poli(vinil butiral), poli(oxipropileno), poli(oxitetrametileno), ésteres de celulosa insolubles en agua, ésteres de quitosano u otros polisacáridos insolubles en agua, poliláctidos, poliglicólidos, policaprolactona, ésteres de poli(ácido málico), ésteres de poli(ácido maleico), ésteres de poli(ácido fumárico), y los copolímeros o derivados lineales insolubles en agua que comprende estos compuestos.
Entre estos polímeros, pueden citarse más particularmente...
Reivindicaciones:
1. Composición inyectable gelificante a base de polímeros para la implantación intra-tisular y/o intra-vascular, caracterizada por que comprende:
- - al menos un polímero lineal insoluble en agua y soluble en al menos un disolvente miscible en agua,
- - al menos un polímero reticulado hidrófilo e insoluble en agua,
- - al menos un disolvente biocompatible miscible en agua; y por que se presenta en forma de una suspensión de partículas de dicho polímero reticulado hidrófilo en una solución de dicho polímero lineal.
2. Composición inyectable gelificante de acuerdo con la reivindicación 1, caracterizada por que el o los polímeros lineales se seleccionan entre los poli(acrilatos de alquilo), poli(metacrilatos de alquilo), poli(cianoacrilatos de alquilo), poli(acetato de vinilo), poli(butirato de vinilo), poli(vinil formal), poli(vinil acetal), poli(vinil butiral), poli(oxipropileno), poli(oxitetrametileno), ésteres de celulosa insolubles en agua, ésteres de quitosán u otros polisacáridos insolubles en agua, poliláctidos, poliglicólidos, policaprolactona, ésteres de poli(ácido málico), ésteres de poli(ácido maleico), ésteres de poli(ácido fumárico), y copolímeros o derivados lineales insolubles en agua que contienen estos compuestos.
3. Composición inyectable gelificante de acuerdo con la reivindicación 2, caracterizada por que el o los polímeros lineales se seleccionan entre el polihidroxietilmetacrilato, poli(metacrilato de metilo), polihidroxipropilmetacrilato, copolímeros de hidroxietilmetacrilato o de hidroxipropilmetacrilato y de acrilonitrilo, copolímeros de hidroxietilmetacrilato o de hidroxipropilmetacrilato y de N-terc-butilacrilamida, copolímeros de hidroxietilmetacrilato o de hidroxipropilmetacrilato y de acetoacetoxietilmetacrilato, poli-(N-acriloil-2-amino-2-hidroximetil-1,3-propanodiol), poli-(n-2-hidroxipropil metacrilamida), y sus derivados.
4. Composición inyectable gelificante de acuerdo con la reivindicación 3, caracterizada por que el o los polímeros lineales se seleccionan entre los copolímeros de hidroxipropilmetacrilato y acrilonitrilo, copolímeros de hidroxipropilmetacrilato y N-terc-butilacrilamida y los copolímeros de hidroxipropilmetacrilato y acetoacetoxietilmetacrilato.
5. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que el o los polímeros lineales representan del 3 al 25% (m/V).
6. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que el o los polímeros reticulados hidrófilos se seleccionan entre los polímeros obtenidos por reticulación de polímeros lineales insolubles en agua como se definen en la reivindicación 2.
7. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones 1 a 5, caracterizada por que el o los polímeros reticulados hidrófilos se seleccionan entre los polímeros obtenidos por reticulación de polímeros lineales solubles en agua.
8. Composición inyectable gelificante de acuerdo con la reivindicación 7, caracterizada por que los polímeros lineales solubles en agua se seleccionan entre los alginatos; derivados de almidón; éteres de celulosa; acetatos de celulosa con un grado de sustitución comprendido entre 0,6 y 0,8; sulfatos de celulosa, polisacáridos hidrosolubles; sales de quitosanos; polímeros acrílicos y metacrílicos; poliacrilamidas y polimetacrilamidas sustituidas o no; derivados hidrolizados de poli(vinilacetatos); polímeros derivados de poli(oxietileno), poli(etilenimina); sales solubles de poli(vinilpiridina), poli(vinilpirrolidona); poliuretanos; sus sales y sus copolímeros.
9. Composición inyectable gelificante de acuerdo con la reivindicación 6, caracterizada por que el o los polímeros reticulados se seleccionan entre los polímeros reticulados de hidroxietilmetacrilato, hidroxipropilmetacrilato o poli-(N acriloil-2-amino-2-hidroximetil-1,3 propanodiol) así como entre los copolímeros reticulados de hidroxietilmetacrilato y poli-(N-acriloil-2-amino-2-hidroximetil-1,3-propanodiol) o hidroxipropilmetacrilato y poli-(N-acriloil-2-amino-2-hidroximetil-1,3-propanodiol).
10. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que el índice de reticulación del polímero reticulado está comprendido entre 0,5 y el 12% (m/V).
11. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que el o los polímeros reticulados representan del 1 al 30% (m/V).
12. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que el tamaño de las partículas de polímero (o polímeros) reticulado (o reticulados) está comprendido entre 1 y 1000 µm.
13. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que comprende al menos un polímero lineal de hidroxietilmetacrilato o hidroxipropilmetacrilato o un copolímero lineal a base de hidroxietilmetacrilato o hidroxipropilmetacrilato y partículas de polímero reticulados de hidroxietilmetacrilato, hidroxipropilmetacrilato o poli-(N-acriloil-2-amino-2-hidroximetil-1,3-propanodiol), y/o copolímeros reticulados de hidroxietilmetacrilato y poli-(N-acriloil-2-amino-2 hidroximetil-1,3-propanodiol) o hidroxipropilmetacrilato y poli-(N-acriloil-2-amino-2-hidroximetil-1,3-propanodiol).
14. Composición inyectable gelificante de acuerdo con la reivindicación 13, caracterizada por que comprende:
- - al menos un copolímero lineal a base de hidroximetiletilmetacrilato o hidroxipropilmetacrilato, y
- - al menos partículas de copolímeros reticulados de hidroxietilmetacrilato o hidroxipropilmetacrilato y poli-(N-acriloil-2-amino-2-hidroximetil-1,3-propanodiol).
15. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que el o los disolventes biocompatibles miscibles en agua se seleccionan entre la N-metil-pirrolidona, dimetiletilamida, dimetiléter de dietilenglicol, etil-lactato, etanol, dimetoxietano, dimetilsulfóxido, glicofurol y sus mezclas.
16. Composición inyectable gelificante de acuerdo con la reivindicación 16, caracterizada por que dichos disolventes se seleccionan entre etanol y N-metil-pirrolidona.
17. Composición inyectable gelificante de acuerdo con una cualquiera de las reivindicaciones anteriores, caracterizada por que incluye además uno o varios adyuvantes seleccionados entre colorantes, marcadores de imágenes, agentes anti-inflamatorios, agentes angiogénicos, agentes anti-mitóticos, inhibidores de la angiogénesis, factores del crecimiento, vitaminas, hormonas, proteínas, vacunas, péptidos, antisépticos y antimicrobianos.
18. Composición inyectable gelificante como se define en una cualquiera de las reivindicaciones 1 a 17, para usar en el relleno de conductos y cavidades.
19. Composición inyectable gelificante como se define en una cualquiera de las reivindicaciones 1 a 17, para usar en la realización de oclusiones vasculares terapéuticas, en la reconstrucción tisular, en el tratamiento del reflujo gastro-esofágico o de la incontinencia urinaria, en la implantación percutánea o en la reducción de arrugas.
20. Solución intermedia a base de copolímero lineal caracterizada por que comprende:
- - al menos un copolímero lineal de hidroxipropilmetacrilato y acrilonitrilo, y/o al menos un copolímero de hidroxipropilmetacrilato y N-terc-butilacrilamida y/o al menos un copolímero de hidroxipropilmetacrilato y acetoacetoxietilmetacrilato, y
- - al menos un disolvente biocompatible miscible en agua; entendiéndose que cuando dicha solución intermedia contiene un copolímero lineal de hidroxipropilmetacrilato y acrilonitrilo el disolvente no es dimetilsulfóxido ni dimetilformamida.
Patentes similares o relacionadas:
Preparaciones de hidrogel térmico reversible para su uso en el tratamiento de trastornos del urotelio, del 15 de Julio de 2020, de UroGen Pharma Ltd: Una composición de hidrogel termorreversible mucoadhesiva biocompatible que incorpora toxina botulínica y que comprende al menos un agente de gelificación […]
Producto para el tratamiento de lesiones y verrugas cutáneas y dispositivo para la aplicación de dicho producto, del 15 de Julio de 2020, de SIXTEM LIFE S.R.L: Producto a base de ácido salicílico para el uso en el tratamiento de lesiones cutáneas y verrugas, caracterizado porque comprende: - ácido salicílico; […]
Formulaciones de azalida acuosas concentradas, del 8 de Julio de 2020, de Sun Pharma Global FZE: Una composición farmacéutica tópica para su uso en el tratamiento de una infección ocular que comprende administrar a un paciente en necesidad del mismo, una cantidad […]
Forma de dosificación para su inserción en la boca, del 17 de Junio de 2020, de Nal Pharmaceutical Group Limited: Composición farmacéutica para aplicación a la mucosa oral que comprende: una matriz soluble en agua que comprende una cantidad eficaz de un agente farmacéuticamente […]
Polimerosomas de gradiente de pH transmembrana y su uso en la eliminación del amoníaco y sus análogos metilados, del 27 de Mayo de 2020, de ETH ZURICH: Un polimerosoma que comprende (a) una membrana, que comprende un copolimero en bloque de poli(estireno) (PS) y poli(oxido de etileno) (PEO), en […]
Composición intranasal que comprende betahistina, del 22 de Abril de 2020, de Otolanum AG: Una composición farmacéutica para administración intranasal a un paciente humano, que comprende una solución o suspensión de una cantidad […]
Composiciones farmacéuticas acuosas que contienen complejos de borato-poliol, del 15 de Abril de 2020, de NOVARTIS AG: Una composición oftálmica multidosis, que comprende: brinzolamida, brimonidina o una combinación de estas; un polímero aniónico; […]
Composición de suspensión oftálmica, del 1 de Abril de 2020, de BAUSCH & LOMB INCORPORATED: Una suspension oftalmica que comprende un ingrediente activo oftalmico suspendido en un vehiculo de la formulacion, en donde el ingrediente activo oftalmico es loteprednol […]