Procedimiento de preparación de biosensor amperométrico de lactato, biosensor obtenido mediante ese procedimiento y su uso en medios complejos.
Procedimiento de preparación de un biosensor amperométrico para la determinación de lactato basado en la enzima lactato oxidasa (LOD) que comprende las siguientes etapas:
dispersión de un biopolímero en disolvente orgánico; preparación de disolución mediadora añadiendo un mediador y nanotubos de carbono; preparación de disolución enzimática con al menos la enzima LOD; adición de la disolución mediadora y enzimática sobre una plataforma serigrafiada desechable; y secado del biosensor. También son objeto de la presente invención, el biosensor obtenido mediante este procedimiento, donde el biopolímero está basado en polisacáridos de glucosa y amilosa con grupos funcionales hidroxilo, amino, acetilo o carboxílicos y presenta enlaces glicosídicos; y su uso en medios complejos como medios celulares embrionarios, medios alimentarios o muestras de sangre.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201431875.
Solicitante: UNIVERSIDAD DE ALICANTE.
Nacionalidad solicitante: España.
Inventor/es: MONTIEL LEGUEY,VICENTE, INIESTA VALCÁRCEL,Jesús, HERNÁNDEZ IBÁÑEZ,Naiara, BANKS,Craig Edward.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12Q1/25 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen enzimas que no pueden ser clasificarsse en los grupos C12Q 1/26 - C12Q 1/70.
- G01N27/00 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R).
Fragmento de la descripción:
Procedimiento de preparación de biosensor amperométrico de lactato, biosensor obtenido mediante ese procedimiento y su uso en medios complejos.
CAMPO DE LA INVENCIÓN
La presente invención se enmarca en el campo de los sensores amperométricos de uso en reproducción asistida, cuya finalidad más concretamente se centra en la detección y determinación de lactato/ácido láctico en medios complejos como los medios de cultivos 10 celulares, empleados en el desarrollo y crecimiento de células de embriones humanos.
ESTADO DE LA TÉCNICA ANTERIOR
La mayoría de las investigaciones para el desarrollo de biosensores electroquímicos de lactato se centran en mejorar:
(i) la inmovilización de la enzima empleada sobre el material del electrodo,
(ii) la mejora de la transferencia electrónica, 20
(iii) el tipo de mediadores y coenzimas,
(iv) la mejora de la estabilidad del sensor, y
(v) la miniaturización del biosensor.
Teniendo en cuenta estas premisas, durante las últimas tres décadas han ido creciendo las 25 investigaciones sobre el desarrollo de biosensores de lactato debido a su importancia en distintas áreas de aplicación. En la mayoría de estudios que se pueden encontrar en la actualidad, se opta por la fabricación de biosensores amperométricos basados en dos tipos de enzimas: la lactato oxidasa y la lactato deshidrogenasa. Esta última requiere de la presencia del cofactor nicotinamida adenina dinucleótido oxidado (NAD+) que es reducido a 30 NADH, lo que conlleva la fabricación de un biosensor sofisticado, caro y con un tiempo de vida limitado [L. Agüí, M. Eguílaz, C. Peña-Farfal, P. Yáñez-Sedeño, J.M. Pingarrón, Electroanalysis 21 (2009) 386; A.C. Pereira, M.R. Aguiar, A. Kisner, D.V. Macedo, L.T. Kubota, Sensors and Actuators, B: Chemical 124 (2007) 269]. Por el contrario la enzima lactato oxidasa contiene el cofactor Flavín adenín dinucleótido (FAD) en su estructura, que 35 cataliza la conversión de lactato a piruvato en presencia de O2 generándose al mismo tiempo H2O2 como producto [V.P. Zanini, B. López De Mishima, V. Solís, Sensors and Actuators, B: Chemical 155 (2011) 75]. Por tanto y, debido fundamentalmente a que el cofactor NADH se encuentra presente en medios de cultivo embrionario, lo que interferiría en la medida si se utilizara un biosensor basado en la lactato deshidrogenasa, es necesario 40 desarrollar biosensores electroquímicos de lactato en los cuales sea empleada como enzima la lactato oxidasa.
Los biosensores amperométricos de lactato, que emplean lactato oxidasa como biocatalizador para la reacción de oxidación de lactato a piruvato generando peróxido de 45 hidrógeno, funcionan cuando se les somete a un potencial entre +0.5 y +0.65 V frente al electrodo de referencia AgCl/Ag (cloruro 3 M) . Este es el rango de potenciales necesario para oxidar el H2O2 sobre la superficie del electrodo y, por consiguiente, establecer una respuesta cuantificable que relaciona la intensidad de corriente obtenida con la cantidad de lactato presente en disolución de estudio [L. Rassaei, W. Olthuis, S. Tsujimura, E.J.R. 50 Sudhölter, A. Van Den Berg, Analytical and Bioanalytical Chemistr y 406 (2013) 123]. El problema de estos biosensores amperométricos de lactato es el elevado potencial al cual se debe realizar la medida cuando el medio en el que se encuentra el lactato puede contener a otras sustancias que también pueden contribuir a la lectura de la corriente registrable a estos potenciales (son los denominados interferentes) . Para evitar esta circunstancia, debemos encontrar un rango de potenciales dónde dichas sustancias no contribuyan a la lectura de corriente que sólo debe ser debida a la presencia del lactato. Por tanto, es necesario el desarrollo de biosensores amperométricos de lactato que puedan operar a 5 potenciales de trabajo del electrodo bajos y, consecuentemente, se puedan evitar interferencias debidas a esas especies electroactivas que pueden oxidarse a potenciales más elevados.
La estrategia elegida hasta el momento en la bibliografía relacionada es la búsqueda de 10 mediadores que favorezcan la disminución del potencial de oxidación del H2O2 producido por la especie enzima lactato oxidasa. De esta forma el proceso de oxidación no se lleva a cabo directamente sobre la superficie del sensor sino a través de un mediador anclado a ésta y ello se produce a un potencial sensiblemente inferior al descrito habitualmente [
Costa Eric D
, Electrochemical biosensor stability. Patent Number: EP546019-A; WO9204466-A1; 15 AU9184377-A]. En la literatura se pueden encontrar mediadores redox de distinta naturaleza, entre los más utilizados se encuentran la ftalocianina de cobalto [F.J. Rawson, W.M. Purcell, J. Xu, R.M. Pemberton, P.R. Fielden, N. Biddle, J.P. Hart, Talanta 77 (2009) 1149], el ferroceno [S. Pérez, E. Fàbregas, Analyst 137 (2012) 3854] o derivados de éste como el ferroceno metanol (FcMe) [V.P. Zanini, B. López De Mishima, V. Solís, Sensors and 20 Actuators, B: Chemical 155 (2011) 75, X. Li, J. Zang, Y. Liu, Z. Lu, Q. Li, C.M. Li, Analytica Chimica Acta 771 (2013) 102]. A potenciales de +0.19 V el ferroceno metanol se oxida a ferrocinio (1) , el ferrocinio oxida posteriormente al H2O2 (2) formado tras la oxidación del lactato por la enzima lactato oxidasa (en adelante LOD) , finalmente detectándose la posterior señal electroquímica a un potencial formal de +0.19 V frente a un electrodo de 25 referencia AgCl/Ag (3 M KCl) (3) . Como se puede observar, el potencial se reduce notablemente de +0.65 V a +0.19 V, pudiéndose evitar la interferencia de otras sustancias electroactivas presentes en el medio de estudio.
( 1 )
( 2 )
( 3 )
El grupo de Fábregas y Pérez [S. Pérez, E. Fàbregas, Analyst 137 (2012) 3854] inmovilizan simultáneamente la enzima lactato oxidasa junto con la enzima peroxidasa de rábano silvestre (HRP) . En este sistema bienzimático la oxidación de lactato está catalizada por la enzima lactato oxidasa dando como subproducto peróxido de hidrógeno que posteriormente se reduce a H2O por la acción catalítica de la enzima HRP en su forma reducida, dando 35 lugar a la enzima HRP en su forma oxidada. Finalmente, la enzima HRP en su forma oxidada se reduce por el FcMe dando lugar a la especie ferrocinio metanol (FcMe+) , que posteriormente se reduce electroquímicamente a un potencial de -200 mV frente a un electrodo pseudoreferencia de pasta de plata / cloruro de plata.
Por otra parte y para que estos sistemas puedan funcionar correctamente, es necesario inmovilizar la enzima LOD sobre la superficie del biosensor. Entre los distintos procedimientos referenciados algunos autores apuestan por el empleo de matrices de sol-gel [J. Huang, J. Li, Y. Yang, X. Wang, B. Wu, J.i. Anzai, T. Osa, Q. Chen, Materials Science and Engineering C 28 (2008) 1070; J. Weber, A. Kumar, S. Bhansali, Sensors and Actuators, 45 B: Chemical 117 (2006) 308] por ser inertes químicamente, por la posibilidad de modificar la porosidad y por permitir trabajar a bajas temperaturas. Un ejemplo de lo anterior es el biosensor fabricado por Huang y colaboradores, quienes emplearon una matriz de sílice sol-gel mediante la mezcla de Tetraetil ortosilicato (TEOS) , H2O y HCl que adicionaron sobre un electrodo de carbón vítreo modificado con nanotubos de carbón de pared múltiple (MWCNT) 50
y nanopartículas de platino, obteniendo un biosensor para la medida de muestras de sangre con una sensibilidad de 6.36 A/mM, un rango de linealidad de (0.2~2) x 10-3 M, pero con una estabilidad de 4 semanas [J. Huang, J. Li, Y. Yang, X. Wang, B. Wu, J.i. Anzai, T. Osa, Q. Chen, Materials Science and Engineering C 28 (2008) 1070].
Otros autores han preferido como sustrato la combinación de una matriz de sílice y un biopolímero, de modo que la matriz de sílice aportaba el carácter hidrofílico, el biopolímero mejoraba la inmovilización de la proteína y, con ello, el biosensor amperométrico mejoraba la transferencia iónica, proporcionando estabilidad mecánica y buena adhesión. Un ejemplo sobre la estrategia anterior corresponde al biosensor realizado por Zanini y col., quienes 10 emplearon un hidrogel de laponita en presencia de quitosano sobre un sustrato masivo de carbón vítreo para la medida de lactato en alimentos presentando una sensibilidad de 0.326 ± 0.003 A cm-2 M-1 y un límite de detección de (3.8 ± 0.2) x 10-3 M [V.P. Zanini, B. López De Mishima, V. Solís, Sensors and Actuators, B: Chemical 155 (2011) 75; X. Li, J. Zang, Y. Liu, Z. Lu, Q. Li, C.M. Li, Analytica Chimica Acta 771 (2013) 102]. Sin embargo el biosensor fue 15 probado únicamente para la determinación de lactato en bebidas alcohólicas y productos lácteos. No obstante,...
Reivindicaciones:
1. Procedimiento de preparación de un biosensor amperométrico de lactato basado en la enzima lactato oxidasa (LOD) que comprende las siguientes etapas:
1. Dispersión del biopolímero en disolvente orgánico.
2. A la dispersión anterior se adicionan un mediador y nanotubos de carbono, para dar lugar a la disolución mediadora.
3. Preparación de la disolución enzimática disolviendo al menos la enzima LOD en una disolución tampón a pH neutro. 10
4. Adición de la disolución mediadora obtenida en la etapa 2 sobre una plataforma serigrafiada.
5. Adición de la disolución enzimática obtenida en la etapa 3 sobre la plataforma serigrafiada y la disolución mediadora.
6. Secado del biosensor para la eliminación del disolvente. 15
2. Procedimiento de preparación de un biosensor amperométrico de lactato según la reivindicación 1, donde el biopolímero utilizado es quitosano.
3. Procedimiento de preparación de un biosensor amperométrico de lactato según la 20 reivindicación 1, donde el biopolímero utilizado está basado en polisacáridos de glucosa o amilosa, funcionalizados con grupos hidroxilo, amino, acetilo o carboxílico, que contienen enlaces glucosídicos, como son el almidón, la quitina, el ácido hialurónico, el glucógeno y la celulosa.
4. Procedimiento de preparación de un biosensor amperométrico de lactato según la reivindicación 1, donde el disolvente orgánico es dimetilformamida o una combinación de dimetilformamida y etanol.
5. Procedimiento de preparación de un biosensor amperométrico de lactato según la 30 reivindicación 4, donde la combinación de dimetilformamida y etanol es en proporción 1:3 (v:v) .
6. Procedimiento de preparación de un biosensor amperométrico de lactato según la 35 reivindicación 1, donde el mediador utilizado es el ferroceno metanol.
7. Procedimiento de preparación de un biosensor amperométrico de lactato según la reivindicación 1, donde los nanotubos de carbono utilizados son de pared múltiple y están funcionalizados con grupos oxigenados. 40
8. Procedimiento de preparación de un biosensor amperométrico de lactato según la reivindicación 1, donde la disolución enzimática se prepara con la enzima lactato oxidasa (LOD) , junto a la enzima peroxidasa de rábano silvestre (HRP) .
9. Procedimiento de preparación de un biosensor amperométrico de lactato según la reivindicación 1, donde la plataforma serigrafiada es de grafito desechable, de tipo convencional, microelectrodo, array, microarray, microbanda o microbanda en serie, para conferir versatilidad y rapidez al sistema.
10. Procedimiento de preparación de un biosensor amperométrico de lactato según la reivindicación 1, donde el secado se realiza a 2-5 ºC o a 25 ºC bajo condiciones de alto vacío durante 1 hora y después se almacena a 2-5 ºC al aire.
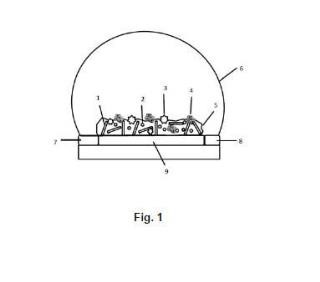
11. Biosensor amperométrico de lactato basado en la enzima lactato oxidasa (LOD) obtenido por el procedimiento descrito en la reivindicación 1, formado por un sustrato de grafito serigrafiado soportado sobre un polímero aislante flexible, una matriz carbonosa conductora formada por la combinación de un sistema enzimático que 5 contiene al menos la enzima LOD, nanotubos de carbono funcionalizados y el biopolímero para la inmovilización de la enzima.
12. Uso del biosensor amperométrico de lactato basado en la enzima lactato oxidasa (LOD) descrito en la reivindicación 11 en medios complejos, incluidos los medios de 10 cultivo embrionario utilizados en técnicas de reproducción asistida humana y otros medios utilizados en el desarrollo celular.
13. Uso del biosensor amperométrico de lactato basado en la enzima lactato oxidasa (LOD) descrito en la reivindicación 11 en muestras alimentarias provenientes del 15 sector vinícola y cervecero.
14. Uso del biosensor amperométrico de lactato basado en la enzima lactato oxidasa (LOD) descrito en la reivindicación 11 en la determinación de los niveles de lactato en sangre. 20
Patentes similares o relacionadas:
MÉTODO PARA PREDECIR O PRONOSTICAR LA RESPUESTA AL TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE CON INTERFERÓN BETA., del 9 de Abril de 2020, de SERVICIO ANDALUZ DE SALUD: Método para predecir o pronosticar la respuesta de los individuos con esclerosis múltiple al tratamiento con INF-beta que comprende medir los niveles […]
Uso de HE4 y otros marcadores bioquímicos para la evaluación de cánceres de ovario, del 18 de Septiembre de 2019, de FUJIREBIO DIAGNOSTICS, INC: Un método para evaluar si una paciente padece cáncer de ovario en estadio I, el método comprende evaluar al menos dos marcadores, que incluyen […]
Métodos para medir actividad enzimática, útiles para determinar la viabilidad celular en muestras no purificadas, del 24 de Julio de 2019, de Momentum Bioscience Limited: Un kit de ensayo para uso en un método para la detección de la actividad de la polimerasa como un indicador de la presencia de un microrganismo […]
Composiciones y métodos relacionados con la argininosuccinato sintetasa, del 5 de Junio de 2019, de Bioregency, Inc: Una cantidad terapéuticamente eficaz de argininosuccinato sintetasa para uso en un método para tratar la exposición de un sujeto a una endotoxina bacteriana.
Un método para medir la actividad proteasa de C3 y C5 convertasa de la vía de complemento alternativa, del 20 de Febrero de 2019, de ALEXION PHARMACEUTICALS, INC.: Un método para medir la actividad proteasa de C3 convertasa que comprende las etapas de: a. unir covalentemente biotina a C3b para producir C3b biotinilado […]
Método que utiliza sustratos de enzimas que producen productos fluorescentes insolubles y cromógenos, y el uso en combinación con sustratos de enzimas que producen productos solubles, del 14 de Marzo de 2018, de Roth, Geoffrey N: Un método para detectar organismos objetivo específicos que comprende las etapas: a) obtener una muestra que contiene dichos organismos objetivo específicos; […]
Detección de dinoflagelados productores de saxitoxina, del 28 de Febrero de 2018, de NEWSOUTH INNOVATIONS PTY LIMITED: Un método para detectar un dinoflagelado productor de saxitoxina en una muestra, comprendiendo el método: obtener una muestra para su uso en el método; y analizar […]
Uso de proteínas de tipo DJ-1 para caracterizar la sequedad de la piel, del 20 de Diciembre de 2017, de L'OREAL: Uso de al menos un polipéptido con una secuencia de aminoácidos codificada por una secuencia de ácido nucleico representada completamente o parcialmente […]