ESTABILIZACION DE LOS CONJUGADOS DE PEROXIDASA.
La presente invención se refiere a un proceso para la estabilización de compuestos inmunológicamente activos que tienen actividad de peroxidas añadiéndoles una cantidad efectiva de al menos un compuesto de un ácido arílico bórico.
La presente invención también se refiere a reactivos estabilizados que comprenden un compuesto activo inmunológicamente que tienen actividad de peroxida y al menos un compuesto de ácido arílico bórico
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E99307443.
Solicitante: ORTHO-CLINICAL DIAGNOSTICS.
Nacionalidad solicitante: Reino Unido.
Dirección: MANDEVILLE HOUSE, 62 THE BROADWAY,AMERSHAM, BUCKINGHAMSHIRE HP7.
Inventor/es: DAWKES, ADRIAN CHARLES, EDWARDS, JOHN, YEARWOOD,GRAHAM DE LISLE, KILMARTIN,PATRICK, MANN,VEROUKA ZSUZSANNA, HOURD,PAUL.
Fecha de Publicación: .
Fecha Solicitud PCT: 21 de Septiembre de 1999.
Fecha Concesión Europea: 9 de Junio de 2010.
Clasificación Internacional de Patentes:
- C12N9/08 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › actúan sobre el peróxido de hidrógeno como aceptor (1.11).
- C12N9/96 C12N 9/00 […] › Estabilización de una enzima por formación de un aducto o de una composición; Formación de conjugaciones de enzimas.
Clasificación PCT:
- C07K14/80 C […] › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Citocromos.
- C07K14/805 C07K 14/00 […] › Hemoglobinas; Mioglobinas.
- C12N9/08 C12N 9/00 […] › actúan sobre el peróxido de hidrógeno como aceptor (1.11).
- C12N9/96 C12N 9/00 […] › Estabilización de una enzima por formación de un aducto o de una composición; Formación de conjugaciones de enzimas.
Clasificación antigua:
- C07K14/80 C07K 14/00 […] › Citocromos.
- C07K14/805 C07K 14/00 […] › Hemoglobinas; Mioglobinas.
- C12N9/08 C12N 9/00 […] › actúan sobre el peróxido de hidrógeno como aceptor (1.11).
- C12N9/96 C12N 9/00 […] › Estabilización de una enzima por formación de un aducto o de una composición; Formación de conjugaciones de enzimas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Estabilización de los conjugados de peroxidasa.
Campo de la invención
La presente invención se refiere a un procedimiento para estabilizar peroxidasas conjugadas con otras moléculas biológicamente activas y a una solución que comprende y estabiliza un conjugado de peroxidasa, para usar en procedimientos analíticos.
Antecedentes de la invención
Las peroxidasas, en particular la peroxidasa de rábano (HRP), son enzimas que normalmente se usan en procedimientos analíticos, incluidos inmunoensayos. Se conocen muchos formatos y se usan ampliamente para la medición de antígenos, anticuerpos, haptenos y otros analitos. Algunos ejemplos son ensayos competitivos e inmunométricos. En inmunoensayos competitivos, un analito marcado compite con el analito en una muestra para unirse a una especie de unión a analito inmovilizada. Por tanto, el incremento de la concentración del analito en la muestra reduce el analito marcado que pasa a estar inmovilizado. En ensayos inmunométricos, un ligante de analito marcado forma complejo con un analito en la muestra y un ligante del analito inmovilizado. En este tipo de ensayo, el incremento de la concentración del analito en la muestra tiene como resultado un incremento del ligante del analito marcado que pasa a estar inmovilizado. En ambos tipos de inmunoensayo, el analito marcado inmovilizado se separa del analito marcado no unido y se mide la actividad de HRP inmovilizada o sin unir.
Los reactivos para usar en los procedimientos analíticos, tales como inmunoensayos, deben permanecer activos tras la fabricación, envío y periodos de almacenamiento. Durante estos periodos pueden estar sujetos a temperaturas relativamente altas o bajas que afectan a la actividad. Por tanto, es una ventaja comercial proporcionar un reactivo que contiene el material marcado con peroxidasa u otros componentes biológicos activos.
Esto no se consigue fácilmente para muchos materiales biológicos. Por ejemplo, las moléculas marcadas con enzima y otras biomoléculas complejas se usan ampliamente en inmunoensayos y se ha observado que la actividad de la enzima o de la biomolécula activa puede disminuir con el tiempo, especialmente a las bajas concentraciones usadas en los procedimientos de inmunoensayo. Se encuentra que la actividad biológica disminuye con más rapidez a medida que la temperatura de almacenamiento aumenta. Una forma de ralentizar o prevenir una disminución de la actividad de una enzima o enzima conjugada con una molécula activa es añadir un agente estabilizante a la enzima en solución en una cantidad suficiente para alcanzar estabilización.
Los procedimientos para la estabilización de las peroxidasas o HRP incluyen la adición de polietilenglicol y sales de calcio (patente de EE.UU. 4.728.023); la adición de ácido 8-anilino-1-naftaleno sulfónico (patente FGR 3.100.076); la adición de fenol y fenoles sustituidos con uno o más sustituyentes de alquilo C1-C3 inferior, cloro y bromo (patente de EE.UU. 4.764.468); la adición de 4-aminoantipirina (patente europea 070.992); la adición de iones polivalentes del grupo III y del grupo IV (patente de EE.UU. 4.169.012 y la adición de una 4-hidroxi o 4-alcoxiarilacetamida (patente de EE.UU. 5.372.932). La estabilización tanto de HRP como de otras biomoléculas se ha alcanzado mediante la adición de un compuesto que tiene un anillo benceno sustituido con al menos un grupo hidroxilo y un grupo de valor sigma Hammett (sp) - 0,20
Aunque los aditivos conocidos en la actualidad mejoran la estabilidad de la peroxidasa y otras moléculas biológicas, sigue habiendo la necesidad de mejoras adicionales. En particular, se desean formulaciones reactivas que tengan mejor estabilidad a temperatura ambiente y a las elevadas temperaturas experimentadas durante el transporte de reactivos. Algunos de los aditivos conocidos pueden interaccionar con proteínas y otros componentes que se usan con frecuencia en formulaciones reactivas analíticas y, en algunos casos, pueden afectar a las reacciones inmunológicas que se utilizan en los inmunoensayos. También se desean aditivos que estabilizan los componentes activos de las formulaciones y que no tienen efectos perjudiciales sobre otros componentes.
Los compuestos de organoboro en soluciones acuosas interaccionan fuertemente con muchas moléculas. La interacción, que puede realizarse mediante una serie de mecanismos diferentes, se ha explotado en la purificación de varios materiales. Por ejemplo, en el fraccionamiento de glicoproteínas se usa ácido 3-aminofenilborónico fijado a un soporte sólido. Los organoboratos pueden inhibir muchas enzimas, afectar al metabolismo animal y son bacterostáticos reconocidos (véase Boronate Ligands in Biochemical Separations, Amicon Corporation, Danvers, Publicación 507, 1981, para una revisión exhaustiva). También se ha encontrado que los compuestos de organoboro incrementan la emisión de luz de reacciones quimioluminiscentes catalizadas por la HRP (publicación PCT nº WO 93/16195) solos o en combinación con un potenciador fenólico o de amina aromática (publicación PCT nº WO 94/23060).
Los compuestos de organoboro también se han usado en los electrodos de transferencia de electrones (publicación PCT nº WO 85/02861).
Los ácidos arilborónicos son una familia de compuestos dentro del grupo de organoboro. Los ácidos arilborónicos se han usado en formulaciones de detergentes líquidos que contienen enzimas proteolíticas (publicación PCT nº WO 92/19707). A concentraciones elevadas de ácido arilborónico, se evita que las enzimas proteolíticas degraden otros componentes proteicos de la formulación detergente. En la dilución posterior en agua de lavado, las enzimas proteolíticas se reactivan.
El uso de derivados de ácido borónico o de ácido borínico como estabilizantes de enzimas se describe en el documento WO 95/02046.
Nagasaki, T. y col. (Chem. Lett. 1994, 1945-1948) indica que la mioglobina sustituida con ácido fenilborónico (una peroxidasa) es más estable que la mioglobina no sustituida.
Liu, X. y col. (J. Mol. Recogn., vol. 9, Nº 5-6, 1996, 462-467) describe que se puede usar catecol[2-(dietilamino)carbonil-4-bromometil]fenilboronato para inmovilizar la peroxidasa de rábano.
Sorprendentemente, los inventores han encontrado que los compuestos de ácido arilborónico se pueden añadir como agente estabilizante para ralentizar o prevenir una disminución de la actividad de la peroxidasa o la peroxidasa que se ha conjugado con otra molécula (en lo sucesivo conjugado marcado con peroxidasa o conjugado), particularmente HRP o HRP-conjugado destinado para su uso en un inmunoensayo.
Resumen de la invención
Por tanto, un objeto de la presente invención es proporcionar un procedimiento tal como se cita en la reivindicación 1. Es notable el hecho de que dicho procedimiento abarca estabilizar un conjugado marcado con peroxidasa mediante la adición de al menos un compuesto de ácido arilborónico al reactivo conjugado. Las composiciones estabilizadas son útiles en los procedimientos analíticos. Son particularmente útiles en inmunoensayos enzimáticos.
Una forma de realización de la presente invención es una solución tal como se cita en la reivindicación 9, en la que la solución tiene un pH de 7,0 o inferior a 7,0 y en la que un conjugado de peroxidasa se estabiliza con al menos un ácido arilborónico.
Una forma de realización preferida es la composición o procedimiento anterior, en el que la peroxidasa es peroxidasa de rábano.
Descripción detallada
La presente invención se refiere al uso de compuestos de ácido arilborónico como estabilizantes de HRP. El estabilizante es un ácido arilborónico de la fórmula ArB(OH)2, en el que Ar es fenilo o naftilo.
La estructura arilo puede estar insustituida o sustituida con uno o más sustituyentes seleccionados del grupo constituido por: alquilo, alquilo sustituido, arilo, arilo sustituido excluida la sustitución con hidroxilo, éter, amina, amina sustituida, azo, amida, halógeno, nitro, tiol, derivado de tiol, aldehído, ácido, sal ácida, éster, sulfonato, fosfonato, trimetilsililo. Algunos ejemplos de compuestos sustituidos e insustituidos son:
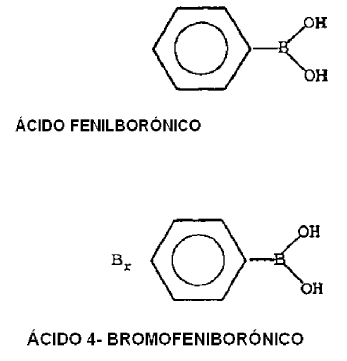
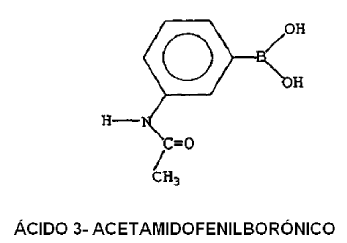
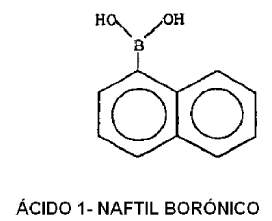
Reivindicaciones:
1. Un procedimiento para estabilizar en una solución que tiene un pH de 7,0 o inferior a 7,0 un compuesto inmunológicamente activo que tiene actividad peroxidasa y conjugado con una molécula activa seleccionada del grupo constituido por: un anticuerpo o un fragmento del mismo, un antígeno, un hapteno, una proteína, una glicoproteína, un péptido, un mimético proteico, una molécula de ácido nucleico, un esteroide, una hormona, o un derivado de cualquiera de los anteriores, en el que dicho procedimiento comprende: añadir una cantidad eficaz para estabilizar dicho compuesto conjugado que tiene actividad peroxidasa de al menos un compuesto de ácido arilborónico de fórmula ArB(OH)2 en la que Ar es fenilo o naftilo que está insustituido o está sustituido con uno o más sustituyentes seleccionados del grupo constituido por alquilo, alquilo sustituido, arilo, arilo sustituido, éter, amina, amina sustituida, azo, amida, halógeno, nitro, tiol, derivado de tiol, aldehído, ácido, sal ácida, éster, sulfonato, fosfonato y trimetilsililo, en la que cuando el compuesto de ácido borónico está sustituido con un arilo sustituido, el sustituyente en el arilo sustituido no es hidroxilo.
2. El procedimiento de la reivindicación 1, en el que el compuesto ácido arilborónico es ácido 4-bromofenilborónico.
3. El procedimiento de la reivindicación 1, en el que el compuesto ácido arilborónico es ácido 3-acetamidofenilborónico.
4. El procedimiento de una cualquiera de las reivindicaciones 1 a 3, en el que el compuesto inmunológicamente activo es mioglobina.
5. El procedimiento de una cualquiera de las reivindicaciones 1 a 3, en el que el compuesto inmunológicamente activo es una peroxidasa.
6. El procedimiento de la reivindicación 5, en la que la peroxidasa es peroxidasa de rábano.
7. El procedimiento de una cualquiera de las reivindicaciones 1 a 6, en el que la solución es una solución acuosa.
8. El procedimiento de la reivindicación 7, en la que la cantidad de compuesto de ácido arilborónico añadido es de 0,01 por ciento a 0,5 por ciento, preferentemente de aproximadamente 0,1 por ciento, en peso por volumen.
9. Una solución que tiene un pH de 7,0 o inferior a 7,0, en la que la solución comprende un compuesto inmunológicamente activo que tiene actividad peroxidasa y conjugado a una molécula activa seleccionada del grupo constituido por un anticuerpo o un fragmento del mismo, un antígeno, un hapteno, una proteína, una glicoproteína, un péptido, un mimético proteico, una molécula de ácido nucleico, un esteroide, una hormona, o un derivado de cualquiera de los anteriores, en el que dicha solución comprende adicionalmente al menos un compuesto de ácido arilborónico de fórmula ArB(OH)2 en la que Ar es fenilo o naftilo que está insustituido o está sustituido con uno o más sustituyentes seleccionados del grupo constituido por alquilo, alquilo sustituido, arilo, arilo sustituido, éter, amina, amina sustituida, azo, amida, halógeno, nitro, tiol, derivado de tiol, aldehído, ácido, sal ácida, éster, sulfonato, fosfonato y trimetilsililo, en la que cuando el compuesto de ácido borónico está sustituido con un arilo sustituido, el sustituyente en el arilo sustituido no es hidroxilo.
10. La solución de la reivindicación 9, en la que el compuesto ácido arilborónico es ácido 4-bromofenilborónico.
11. La solución de la reivindicación 9, en el que el compuesto ácido arilborónico es ácido 3-acetamidofenilborónico.
12. La solución de una cualquiera de las reivindicaciones 9 a 11, en la que el reactivo además comprende un agente conservante.
13. La solución de una cualquiera de las reivindicaciones 9 ó 12, en el que el compuesto inmunológicamente activo es mioglobina.
14. La solución de una cualquiera de las reivindicaciones 9 a 12, en el que el compuesto inmunológicamente activo es una peroxidasa.
15. La solución de la reivindicación 14, en la que la peroxidasa es peroxidasa de rábano.
16. La solución de una cualquiera de las reivindicaciones 9 a 15, en el que la solución es una solución acuosa.
17. La solución de la reivindicación 16, en la que el compuesto de ácido arilborónico añadido está presente en una cantidad que es de 0,01 por ciento a 0,5 por ciento, preferentemente de aproximadamente 0,1 por ciento, en peso por volumen.
Patentes similares o relacionadas:
Procesamiento para recuperación y purificación de una fosfatasa alcalina, del 1 de Julio de 2020, de AM-PHARMA B.V.: Un método para producir una composición físicamente estable que comprende una fosfatasa alcalina (AP) aislada comprendiendo el método - la disolución o dilución […]
Composiciones enzimáticas líquidas estabilizadas, del 6 de Mayo de 2020, de NOVOZYMES A/S: Aldehído peptídico con la fórmula B2-B1-B0-H, donde: H es hidrógeno; B0 es un residuo de Tyr; B1 es un residuo de aminoácido de alanina, cisteína, glicina, […]
 Método para la mejora de la estabilidad de fitasa con ácido fítico, y composiciones que comprenden fitasa y ácido fítico, del 25 de Marzo de 2020, de DANISCO US INC: Método para aumentar la estabilidad de fitasa en una composición de gránulos, comprendiendo el método la introducción de al menos 10 milimolal de ácido fítico […]
Método para la mejora de la estabilidad de fitasa con ácido fítico, y composiciones que comprenden fitasa y ácido fítico, del 25 de Marzo de 2020, de DANISCO US INC: Método para aumentar la estabilidad de fitasa en una composición de gránulos, comprendiendo el método la introducción de al menos 10 milimolal de ácido fítico […]
Método para obtener una biomasa de una microalga de la especie Tetraselmis chuii enriquecida en superóxido dismutasa (SOD), del 1 de Enero de 2020, de Fitoplancton Marino S.L: Un método para obtener una biomasa de una microalga de la especie Tetraselmis chuii enriquecida en superóxido dismutasa (SOD) que comprende cultivar dicha […]
Edición genómica usando nickasas Cas9, del 25 de Diciembre de 2019, de The Broad Institute, Inc: Una composición que no es de origen natural o que está manipulada para su uso en tratamiento, por manipulación de una primera y segunda secuencia diana en hebras […]
Composiciones líquidas estables para lavado manual de vajilla que contienen enzimas, del 31 de Mayo de 2019, de Ecolab USA Inc: Una composición enzimática líquida estabilizada que comprende: un agente estabilizador de enzimas, en donde dicho agente es un tensioactivo anfótero; y una combinación […]
Agentes de lavado o detergentes líquidos con estabilidad mejorada de las enzimas, del 17 de Abril de 2019, de HENKEL AG & CO. KGAA: Agente de lavado o detergente líquido que contienen acetato de potasio y por lo menos una enzima, caracterizado porque la cantidad de iones potasio en la totalidad de la composición […]
Conjugados de Fc-histidil-ARNt sintetasa, del 10 de Abril de 2019, de Atyr Pharma, Inc: Un polipéptido de fusión histidil-ARNt sintetasa (HRS)-Fc, que comprende una secuencia de aminoácidos al menos un 98 % idéntica a la SEQ ID NO:337, donde el […]