SISTEMA Y MÉTODO DE ESTIMACIÓN DE GLUCOSA EN PLASMA.
Sistema y método de estimación de glucosa en plasma.
Se proporciona un sistema de estimación de glucosa en plasma que comprende un sensor que genera una señal a partir de una concentración de glucosa medida en un medio,
unos medios de filtrado y un estimador glucémico. También un método que comprende: i) generar una señal que represente la concentración de glucosa medida en el medio; ii) filtrar la señal generada; iii) aplicar un conjunto de modelos de estimación locales, a la señal anterior, obteniendo un conjunto de estimaciones locales de glucosa en plasma; iv) aplicar una ponderación a cada una de las estimaciones locales obtenidas anteriormente; v) estimar una concentración de glucosa en plasma mediante la suma de las estimaciones locales ponderadas obtenidas en el paso anterior; vi) corregir la señal obtenida del paso anterior a partir de medidas de referencia de glucemia, y obtener la estimación final de glucosa en plasma.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201130811.
Solicitante: UNIVERSIDAD POLITECNICA DE VALENCIA.
Nacionalidad solicitante: España.
Inventor/es: BONDÍA COMPANY,Jorge, BARCELÓ RICO,Fátima, DÍEZ RUANO,José Luís, ROSSETTI,Paolo, VEHI CASELLAS,Josep, LEAL MONCADA,Yenny Teresa.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B5/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › Medidas encaminadas a establecer un diagnóstico (diagnóstico por medio de radiaciones A61B 6/00; diagnóstico por ondas ultrasónicas, sónicas o infrasónicas A61B 8/00 ); Identificación de individuos.
- G06F19/00
Fragmento de la descripción:
SISTEMA Y METODO DE ESTIMACIÓN DE GLUCOSA EN PLASMA.
OBJETO DE LA INVENCIÓN
La presente invención, tal y como se expresa en el enunciado de esta memoria
5 descriptiva se refiere a un sistema y a un método de estimación de glucosa en plasma
cuyo objeto es proporcionar un sistema y un método de monitorización continua de
glucosa cuya exactitud de resultados representa un avance substancial respecto de los
sistemas y métodos del estado de la técnica.
El campo de aplicación de la presente invención es la monitorización continua de
10 glucosa en diabetes y otros estados de alteración de metabolismo glucídico (por ejemplo
pacientes críticos) . Dentro de este campo cabe señalar: la monitorización en tiempo real,
la monitorización retrospectiva, la monitorización para control de infusión de insulina
en terapias actuales, la monitorización en sistemas en lazo semi-cerrado y en lazo
cerrado en combinación con bomba de insulina y algoritmo de control (páncreas
15 artificial) y la monitorización con sensores mínimamente invasivos y no invasivos. Otro
campo de aplicación de la presente invención es la monitorización continua de otros
analitos medidos en compartimentos alternativos al "gold standard" y que, por tanto,
requieran una forma (sistema y/o método) de estimación (p.e. saturación de oxígeno en
hemoglobina) .
20 ANTECEDENTES DE LA INVENCIÓN
La monitorización de la glucemia capilar es un pilar del tratamiento de los
pacientes diabéticos. En los últimos años se ha ido difundiendo la monitorización
continua de la glucosa en tejido subcutáneo como herramienta adicional para la mejora
del control glucémico. Este tipo de monitorización, llamado mínimamente invasivo, se
2 5 basa en la medición de la concentración de glucosa en el fluido intersticial, es decir, en
un compartimento distinto al que tradicionalmente se usa como referencia (el plasma) .
También se están desarrollando tecnologías de monitorización no invasiva que analizan
en un determinado compartimento las variaciones producidas por los cambios de la
concentración de glucosa en determinadas propiedades o señales. El análisis de estas
3 O variaciones permite estimar la concentración de glucosa en plasma ("glucemia") . Las
prestaciones de estos monitores son aún muy pobres en comparación con los
mínimamente invasivos, con lo que las agencias reguladoras no han permitido todavía su
comercialización.
La medición directa o indirecta de la concentración de glucosa en compartimentos alternativos al plasma implica la necesidad de métodos para la estimación de glucosa en plasma, que es la variable de interés. Estos métodos son conocidos como "métodos de calibración", contribuyendo a la exactitud de la estimación. Dicha exactitud se mide comúnmente mediante la desviación absoluta relativa media o mediana (MARD) respecto a medidas en sangre venosa, arterial o capilar ("gold standard") . En la siguiente tabla se muestran algunos monitores continuos actualmente en el mercado, todos ellos mínimamente invasivos, junto con la exactitud reportada.
Monitor continuo MARD (media/mediana) Glucosa de referencia Fuente
Abbott Freestyle Navigator 12.8%/9.3% V en osa (YSI) W einstein et al. (2007)
Medtronic Guardian REAL-Time 19.9%/16.7% V en osa (YSI) Mazze et al. (2009)
Medtronic Paradigm VEO 15.89%/11.56% Capilar (glucómetro) Keenan et al. (2010)
DexCom SEVEN 16.7%/13.2% V en osa (YSI) Zisser et al. (2009)
SexCom SEVEN Plus 15.9%/13% V en osa (YSI) Bailey et al. (2009)
10
Los inconvenientes que presentan los sistemas y métodos del estado de la
técnica son relativos a que los métodos de calibración de los anteriormente mencionados
monitores se basan en técnicas de regresión lineal, con la consideración de un retardo
puro entre glucosa intersticial y plasmática. Por tanto, la información de la dinámica
15 entre los distintos compartimentos biológicos es ignorada y consecuentemente puede
justificar, al menos parcialmente, errores tan elevados. Esto se demuestra en Facchinetti
et al. JDST, 1 (5) , 2007 mediante técnicas de recalibración y deconvolución de un
modelo dinámico plasma-intersticio (no aplicables en tiempo real) . En Facchinetti et al.,
DTT, 12 (5) , 2010 se emplea un filtro de Kalman extendido en serie con el algoritmo de
2 O calibración estándar del monitor continuo para la consideración en tiempo real de la
dinámica y mejora de la precisión, aunque se presentan resultados en simulación no
extrapolables al uso clínico. En Leal et al., JDST, 4 (2) , 2010, se demuestra, aunque en
un estudio limitado, cómo la consideración del comportamiento dinámico expresadomediante un modelo autorregresivo permite meJorar la exactitud, consiguiendo un
MARD de 9.6% (media) 16.7% (mediana) . Sin embargo, dicha exactitud empeora en el
rango hipoglucémico con errores de 8.1 mg/dL (media) y 6.0 mg/dL (mediana) y un
valor ISO de 86.7%. Esto es debido a que la relación plasma-intersticio es compleja y
5 posiblemente dependiente del estado metabólico del paciente, con lo que la descripción
de dicha relación mediante un único modelo (de ámbito global) puede resultar
insuficiente.
Es precisamente la magnitud del error de los sistemas actuales la que ha
condicionado la aprobación por parte de las agencias reguladoras de la monitorización
1 O continua de glucosa únicamente como herramienta complementaria, y no sustitutiva, a la
medición capilar. Adicionalmente, la inexactitud de la monitorización continua de
glucosa es hoy en día el mayor limitante en el desarrollo del páncreas artificial para la
automatización del control glucémico en pacientes con diabetes. La importancia de
mejorar la exactitud de los monitores continuos queda patente en los requerimientos del
15 ICT cal14 del FP7, donde se plantea el objetivo de reducir el MARD por debajo del 5%.
No es conocido en el estado actual de la técnica ningún sistema ni método de
monitorización continua de la glucosa con la exactitud con la que la realiza la presente
invención.
DESCRIPCIÓN DE LA INVENCIÓN
2 O Los monitores continuos, tanto los mínimamente invasivos como los no invasivos,
proporcionan una medida indirecta de la concentración de glucosa en plasma. Los
monitores mínimamente invasivos actualmente en el mercado se fundamentan en
sensores electroquímicos basados en reacciones enzimáticas (glucosa oxidasa) que
proporciOnan una señal eléctrica (intensidad de corriente) representativa de la
2 5 concentración de glucosa en el líquido intersticial, que posteriormente es filtrada y
procesada por el sistema de calibración para estimar la glucosa en plasma. En el caso de
monitores no invasivos, la señal proveniente del sensor puede ser de otra naturaleza, así
como el compartimento directamente medido. La presente invención tiene, por tanto,
como objetivo transformar la salida del sensor (posiblemente filtrada) en estimaciones lo
3 O más exactas posibles de la glucosa en plasma.
Para lograr los objetivos y evitar los inconvenientes indicados en anteriores
apartados, la invención consiste en un sistema de estimación de glucosa en plasma que
comprende: un sensor que genera una señal de monitorización seleccionada entre unaseñal de intensidad de corriente y señal alternativa a partir de una concentración de
glucosa medida en un medio seleccionado entre un líquido intersticial y un
compartimento remoto del que pueda obtenerse una señal equivalente a la mencionada
intensidad de corriente con su correspondiente sensor adaptado, unos medios de filtrado
5 que filtran la señal de monitorización, y un estimador glucémico. El estimador
glucémico a su vez, comprende al menos: dos módulos de estimación locales (estáticos o
dinámicos) , donde cada módulo de estimación local calcula una estimación local de
glucosa en plasma a partir de unas medidas de referencia de glucemia (capilares,
arteriales, venosas o cualquier combinación de las mismas) y de la señal de
1 O monitorización generada por el sensor previamente filtrada por los medios de filtrado; un
módulo de ponderación local por cada módulo de estimación local conectados en serie,
donde cada módulo de ponderación local pondera la estimación local de glucosa en
plasma calculada por el módulo de estimación local al que se encuentra conectado; y, un
sumador que comprende una entrada por cada módulo de ponderación local conectada a
15 cada salida de cada módulo de ponderación local. Tal que el estimador glucémico...
Reivindicaciones:
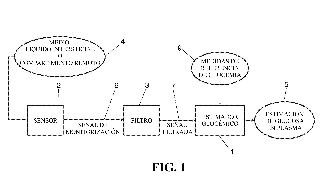
1. Sistema de estimación de glucosa en plasma que comprende:
• un sensor (2) que genera una señal de monitorización (6) seleccionada entre una señal de intensidad de corriente y una señal alternativa a partir de una concentración de glucosa medida en un medio (4) seleccionado entre un líquido intersticial y un compartimento remoto ( 4) ;
• unos medios de filtrado (3) que filtran la señal de monitorización (6) ; y,
• un estimador glucémico (1) que comprende al menos:
o dos módulos de estimación locales (llA, llB, llC) , donde cada módulo de estimación local calcula una estimación local de glucosa en plasma a partir de unas medidas de referencia de glucemia (9) y de la señal de monitorización generada por el sensor (2) previamente filtrada por los medios de filtrado (3) ;
o un módulo de ponderación local (12, 12A, 12B, 12C) por cada módulo de estimación local conectados en serie, donde cada módulo de ponderación local pondera la estimación local de glucosa en plasma calculada por el módulo de estimación local al que se encuentra conectado; y,
o un sumador que comprende una entrada por cada módulo de ponderación local conectada a cada salida de cada módulo de ponderación local;
tal que el estimador glucémico calcula una estimación global de glucosa en plasma resultado de la suma de las ponderaciones llevadas a cabo por los módulos de 2 5 ponderación local.
2. Sistema de estimación de glucosa en plasma, según la reivindicación 1,
caracterizado por que el estimador glucémico (1) adicionalmente comprende un módulo corrector (10) de al menos dos entradas y una salida, donde dicho módulo corrector
O recibe por una de sus entradas unas medidas de referencia de glucemia (9) y por la otra entrada, la salida del sumador; donde la medida de referencia de glucemia está seleccionada entre una medida capilar, una medida arterial, una medida venosa y cualquier combinación de las mismas.
3. Sistema de estimación de glucosa en plasma, según la reivindicación 1 ó 2,
caracterizado por que cada uno de los al menos dos módulos de estimación locales
(llA, llB, llC) comprende unos medios de procesamiento de un modelo de estimación
5 local, el cual está seleccionado entre un modelo de estimación local estático y un modelo
de estimación local dinámico (14) , y a su vez, el modelo de estimación local estático
está seleccionado entre un modelo de estimación local estático individual y un modelo
de estimación local estático poblacional, y el modelo de estimación local dinámico está
seleccionado entre un modelo de estimación local dinámico individual y un modelo de
1 O estimación local dinámico poblacional.
4. Sistema de estimación de glucosa en plasma, según una cualquiera de las
reivindicaciones 1 a 3, caracterizado por que el módulo de ponderación local
(12, 12A, 12B, 12C) comprende unos medios de procesamiento de un modelo de
15 ponderación (15) .
5. Sistema de estimación de glucosa en plasma, según una cualquiera de las
reivindicaciones 1 a 4, caracterizado por que el estimador glucémico (1) adicionalmente
comprende unas señales de entrada adicionales (8) .
20
6. Sistema de estimación de glucosa en plasma, según una cualquiera de las
reivindicaciones 2 a 5, caracterizado por que el estimador glucémico (1) adicionalmente
comprende un módulo de normalización de la señal filtrada (17 A) , un módulo de
normalización de las entradas adicionales (17B) , un módulo de normalización de las
2 5 medidas de referencia de glucemia (17C) y un módulo de desnormalización (18) que
normalizan la señal filtrada (7) , las entradas adicionales (8) , las medidas de referencia de
glucemia (9) y desnormaliza la salida del módulo corrector (1 0) , respectivamente.
7.Sistema de estimación de glucosa en plasma, según la reivindicación 6,
3 O caracterizado por que el estimador glucémico (1) adicionalmente comprende un filtro
adaptativo (16) conectado al módulo de normalización de la señal filtrada (17 A) , al
módulo de normalización de las entradas adicionales (17B) y al módulo de
normalización de las medidas de referencia de glucemia (17C) para ajustar en tiemporeal unos parámetros de normalización comprendidos en dichos módulos de
normalización; y donde dicho filtro adaptativo está adicionalmente conectado al módulo
de desnormalización (18) para ajustar en tiempo real unos parámetros de
desnormalización comprendidos en dicho módulo de desnormalización.
5
8.Sistema de estimación de glucosa en plasma, según la reivindicación 5,
caracterizado por que las señales de entrada adicionales (8) están seleccionadas entre: a)
señales binarias: insulinemia alta/baja, estado de hipoglucemia/no-hipoglucemia, estado
de hiperglucemia/no-hiperglucemia, estado postprandial/no-postprandial; b) señales
1 O continuas de insulinemia estimadas mediante modelos farmacocinéticos de insulina a
partir de información proveniente de una bomba de infusión de insulina; e) señales
externas provenientes de sensores externos; y e) combinación de las anteriores.
9. Sistema de estimación de glucosa en plasma, según una cualquiera de las
15 reivindicaciones anteriores, caracterizado por que los medios de filtrado (3) están
seleccionados entre filtros analógicos y filtros digitales, donde dichos medios de filtrado
(3) eliminan ruido de medida, medidas erróneas y medidas fuera de un rango
preestablecido de la señal de monitorización (6) generada por el sensor (2) .
20 10. Método de estimación de glucosa en plasma que comprende:
i) generar (20) una señal de monitorización seleccionada entre una señal de
intensidad de corriente y una señal alternativa, que represente una
concentración de glucosa medida en un medio seleccionado entre un
líquido intersticial y un comportamiento remoto;
25 ii) filtrar (21) la señal de monitorización generada;
iii) aplicar (22) un conjunto de modelos de estimación locales, estáticos o
dinámicos, a la señal de monitorización anteriormente generada y filtrada,
obteniendo un conjunto de estimaciones locales de glucosa en plasma;
iv) aplicar (23) una ponderación a cada una de las estimaciones locales
30 obtenidas del paso anterior en función de la validez de cada modelo de
estimación local;
v) estimar (25) una concentración de glucosa en plasma mediante la suma de
las estimaciones locales ponderadas obtenidas del paso anterior;vi) corregir la señal obtenida del paso anterior a partir de medidas de referencia de glucemia, la cual está seleccionada entre capilar, arterial, venosa y cualquier combinación de las mismas, obteniendo la estimación final de glucosa en plasma.
11. Método de estimación de glucosa en plasma, según la reivindicación 10, caracterizado por que el paso iii) adicionalmente comprende aplicar el conjunto de modelos de estimación locales a la señal de monitorización generada y filtrada por el paso i) y a al menos una señal de entrada adicional.
12. Método de estimación de glucosa en plasma, según la reivindicación 11, caracterizado por que el paso iii) adicional y previamente comprende normalizar la señal de monitorización generada y filtrada; el paso vi) adicional y previamente comprende normalizar la medida de referencia de glucosa; y el paso v) adicionalmente comprende desnormalizar la estimación de la concentración de glucosa en plasma.
13. Método de estimación de glucosa en plasma, según la reivindicación 12, caracterizado por que el paso iii) adicional y previamente comprende normalizar la al menos una señal de entrada adicional.
14. Método de estimación de glucosa en plasma, según la reivindicación 10, caracterizado por que el modelo de estimación local es dinámico de la forma: ELMi (xk; Pi) = Pit · xk1 + Piz · Xkz + ... + Pid · xkd +Po donde Xk es el vector de datos de entrada y ~¡ es el vector de parámetros de regresión.
15. Método de estimación de glucosa en plasma, según la reivindicación 14, caracterizado por que el modelo de ponderación es de la forma:
ELMPi =Vi x ELMi
donde ELM¡ es el modelo dinámico local i, y donde V¡ es el factor de ponderación tal que:H
d -~ ( (xkr:ii) )
n
e aij
j=1
donde Xk representa al valor actual del vector de entrada, Xkj son cada una de sus componentes y p¡j y Ciij la media y desviación estándar, respectivamente, de la función gaussiana correspondiente al modelo local i-ésimo, para cada dimensión del vector de entradas, y Hes un factor que define la zona de tránsito entre los valores O y l.
Patentes similares o relacionadas:
Procedimiento y aparato para proporcionar el procesamiento y control de datos en un sistema de comunicación médica, del 29 de Julio de 2020, de ABBOTT DIABETES CARE INC: U procedimiento, que comprende: ejecutar, en una unidad receptora , una rutina predeterminada asociada con una operación de un dispositivo de monitorización […]
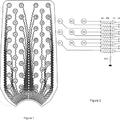 Dispositivo sensor para detección de señales bioeléctricas, del 29 de Julio de 2020, de CorTec GmbH: Dispositivo sensor para detectar senales bioelectricas y para implantar dentro o fuera de un cerebro, el dispositivo sensor que comprende […]
Dispositivo sensor para detección de señales bioeléctricas, del 29 de Julio de 2020, de CorTec GmbH: Dispositivo sensor para detectar senales bioelectricas y para implantar dentro o fuera de un cerebro, el dispositivo sensor que comprende […]
Sistema y procedimiento para evaluar el riesgo asociado con un estado de glucosa, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un dispositivo informático configurado para realizar un procedimiento de análisis de un estado de glucosa, comprendiendo el procedimiento: identificar, […]
FUNDA ELECTRÓNICA PARA ADAPTACIÓN DE DISPOSITIVOS MÓVILES CON INSTRUMENTOS DE DIAGNÓSTICO MÉDICO MULTIDISCIPLINAR, del 27 de Julio de 2020, de RUESGA DELGADO,OSCAR: Funda electrónica para adaptación de dispositivos móviles con instrumentos de diagnóstico médico multidisciplinar que comprende una funda de uso electrónico […]
Cama eléctrica, del 8 de Julio de 2020, de Keeson Technology Corporation Limited: Una cama eléctrica, que comprende una estructura de cama, una pluralidad de láminas de cama, un dispositivo de despertador, un reloj y una caja de control […]
SÍSTEMA Y MÉTODO PARA EL TRATAMIENTO DE ADICCIONES DE UN INDIVIDUO QUE LO NECESITE, CON BAJAS TASAS DE RELAPSO, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención corresponde a un sistema, más particularmente a un sistema NFB, y método, que permite el tratamiento de adicciones en las que está […]
Aparato y método de algometría humana, del 1 de Julio de 2020, de The Children's Research Institute: Un método implementado por el procesador para medir objetivamente el dolor que comprende: aplicar estimulación eléctrica de una intensidad específica […]
MAMÓGRAFO ÓPTICO QUE UTILIZA INFRARROJO CERCANO EN GEOMETRÍA DE REFLECTANCIA DIFUSA, del 25 de Junio de 2020, de CONSEJO NACIONAL DE INVESTIGACIONES CIENTIFICAS Y TECNICAS (CONICET) (33.3%): Un dispositivo formador de imágenes mamográficas para análisis y detección de posibles inhomogeneidades en el tejido mamario de una paciente usando […]