Método y aparato para medir el gasto de flujo cardíaco.
El método para estimar el gasto cardíaco Q, que comprende
una primera etapa para recibir una presión sanguínea,
que se ha adquirido por medio de un sensor, y convertir la presiónsanguínea recibida a una señal de presión p(t) expresada en mmHg;
una segunda etapa para calcular una estimación de un volumen sistólico del ventrículo izquierdo LSV, tal estimación secalcula como una función de una impedancia hidráulica de la arteria;
una tercera etapa para calcular una estimación del gasto cardíaco Q como un producto del volumen sistólico delventrículo izquierdo LSV multiplicado por un valor de frecuencia cardíaca actual HR:
Q≥ LSV*HR
el método está caracterizado porque la impedancia hidráulica de la arteria se calcula por medio de un análisis de laprimera y segunda derivadas con respecto al tiempo de la señal de presión p(t) sobre la base del punto de resonancia, elpunto sistólico, el punto diastólico y el punto dícroto de la señal de presión p(t).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2000/003697.
Solicitante: ROMANO, SALVATORE.
Nacionalidad solicitante: Italia.
Dirección: VIA BOITO, 33 50144 FIRENZE ITALIA.
Inventor/es: ROMANO,SALVATORE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B5/0245 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › A61B 5/00 Medidas encaminadas a establecer un diagnóstico (diagnóstico por medio de radiaciones A61B 6/00; diagnóstico por ondas ultrasónicas, sónicas o infrasónicas A61B 8/00 ); Identificación de individuos. › utilizando captadores que generan señales eléctricas.
- A61B5/029 A61B 5/00 […] › Medida del volumen de eyección cardiaco, p. ej. volumen evacuado por minuto.
PDF original: ES-2438726_T3.pdf
Fragmento de la descripción:
Método y aparato para medir el gasto de flujo cardíaco Campo de la invención La presente invención se refiere a un método y un aparato para determinar el volumen sistólico - es decir, el volumen de sangre expulsado del ventrículo izquierdo (LSV) , el volumen de sangre expulsado del ventrículo derecho (RSV) -y por lo tanto el gasto cardíaco Q - es decir, el volumen sistólico multiplicado por la frecuencia cardíaca (HR) -, de manera continua,
usando técnicas indirectas invasivas y no invasivas, a fin de permitir la adquisición de este importante parámetro hemodinámico en diversas situaciones clínicas y no clínicas, así como también en el transcurso de las pruebas ergométricas.
Técnica anterior
Para la medición del gasto cardíaco Q, los métodos invasivos que son usados en la actualidad más ampliamente son el método de termodilución (TDM) , método de Fick (FM) , y un método que usa la señal de la presión arterial p (t) medida en la aorta o en la arteria pulmonar, denominado como el método de contorno de pulso (PCM) .
Este método que usa la presión de la señal no es muy confiable y por esta razón es necesario hacer una calibración. Este es usualmente el TDM. En la actualidad no se han alcanzado resultados fiables por este método.
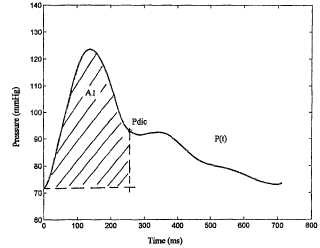
Este método PCM se deriva de una idea original de Herd [Herd J.A. y otros., 1864] y de la teoría denominada como la teoría de Windkassel (alemán para "cámara de aire") de Franck (Franck O., 1930) , y se basa en la existencia de una relación entre el volumen de sangre expulsado por el ventrículo izquierdo (LSV) o el volumen de sangre expulsado por el ventrículo derecho (RSV) , y el área bajo la curva de presión p (t) . La relación fundamental usada para calcular el volumen sistólico es SV=A/Z0 donde A, expresada en [mmHg t], es el área bajo la curva de presión p (t) (ver Figura A1) , y Z0, expresada en [mmHg/cm/t], es la impedancia hidráulica que depende de las resistencias dinámicas y de la distensibilidad de la pared arterial. El LSV se mide en [cm3], por lo tanto Q = LSV*HR es el gasto cardíaco expresado en litros por minuto si la frecuencia cardíaca se mide en latidos por minuto. A este respecto recordaremos que la línea de la presión arterial con respecto al tiempo se determina por la magnitud del LSV y por la impedancia vascular. Por consiguiente, el método de contorno de pulso procura separar y analizar estas dos contribuciones; sin embargo, el método es incapaz de determinar las dos contribuciones como variables independientes en el tiempo.
Aplicando la teoría de Windkassel, muchos estudios han intentado determinar el LSV solamente a partir de la forma de onda de presión y a partir de las características vinculadas a la transmisión de la onda en la aorta o en la arteria pulmonar (Remington J.W. y otros, 1948; Warner H.R. y otros., 1953; Herd J.A. y otros., 1966; Kouchoukos N.T. y otros., 1970]. La idea original de Franck se ha aplicado posteriormente con los años y ha hecho posible estimar el LSV de manera continua a partir de la medición de la señal de presión en la aorta o en la arteria pulmonar [McDonald D.A. y otros., 1974;
Wesseling K.H. y otros., 1976; Tajimi T. y otros., 1983; Wesseling K.H. y otros., 1993].
Sin embargo, en la aplicación concreta a las diversas situaciones clínicas posibles, el método de contorno de pulso requiere actualmente una "calibración" para el cálculo de la impedancia hidráulica. Para la calibración, se usa generalmente uno de los otros dos métodos mencionados anteriormente, es decir, el método de termodilución y el método de Fick, o regresiones 45 lineales de parámetros aórticos, tales como el diámetro de la aorta, y la edad, sexo, altura y peso del paciente.
Desafortunadamente, los factores de calibración y regresión están sujetos a errores, dado que los métodos a partir de los cuales se obtienen a su vez son imprecisos y que las regresiones en cualquier caso se obtienen en un número limitado de sujetos, y son por lo tanto aceptables solamente como un medio y no como una verdadera medida de la cantidad
investigada.
De hecho, el gasto cardíaco estimado usando el método de termodilución y el método de Fick no siempre está de acuerdo con los parámetros clínicos obtenidos usando otras técnicas de diagnóstico, y esto ocurre principalmente en pacientes que sufren de ciertas formas de enfermedades del corazón, tales como las enfermedades que implican la dilatación del corazón,
cardiopatía valvular, y fibrilación cardíaca.
Para proporcionar un ejemplo, considere dos señales posibles en la aorta estudiada entre los puntos de apertura y cierre del ventrículo. Estas señales presentarán generalmente la misma área pero de diferentes formas, con diferentes tiempos de consecución del punto sistólico.
El método tradicional de contorno de pulso producirá por lo tanto la misma medición exacta (misma integrante) evaluada sobre la base de la impedancia de calibración. Sin embargo, es evidente que a partir de una forma diferente de la señal debe derivarse una impedancia diferente, que no se puede evaluar. La patente de Estados Unidos núm. US 5 647 369 describe un método que calcula una medida del gasto cardíaco basado en la presión sanguínea del paciente. Por lo tanto, los límites de las técnicas invasivas en uso actualmente son: a) la deficiente precisión alcanzable en la estimación del gasto cardíaco a causa de enfermedades clínicas; b) la no aplicabilidad generalmente a causa de la condición patológica del paciente; y c) la imposibilidad de aplicar las dichas técnicas invasivas, por ejemplo durante una prueba ergométrica.
Alcance de la invención
Un primer alcance de la invención es obtener las mediciones de manera continua que son más fiables que las obtenidas usando las técnicas invasivas y no invasivas aplicadas actualmente. Un segundo alcance es interpretar la medición independiente sustancialmente del punto de aplicación del sensor mediante la introducción de variaciones en las fórmulas específicas, sin ninguna necesidad de calibración previa de la medición.
Resumen de la invención
Los propósitos anteriores se han alcanzado de acuerdo con la invención usando un método que obtiene directamente el gasto cardíaco a partir de la señal de presión medida de una manera invasiva, en la aorta ascendente, en la arteria pulmonar y en la braquial femoral y radial, o medida de una manera no invasiva, por ejemplo de la arteriola del dedo usando un medidor de brazalete. De acuerdo con el método, la impedancia de la señal de presión se calcula sobre la base de los puntos de resonancia de la señal mediante la asimilación de la señal a la de un flujo en un tubo elástico y asumiendo la constancia del módulo de Young, que se toma particularmente para tener un valor de la unidad. De esta manera, es posible calcular el gasto cardíaco sin ya tener que usar diferentes calibraciones, pero exclusivamente a partir de un análisis de la onda de presión y de sus características.
La impedancia hidráulica se calcula por medio de un análisis de la primera y segunda derivadas con respecto al tiempo de la señal de presión registrada.
De acuerdo con un aspecto adicional de la invención, se hace por otra parte, una corrección del valor de la presión media que se usa para el cálculo de LSV a fin de tomar en cuenta las atenuaciones de dicho valor en los diversos puntos de posible registro de la señal.
De acuerdo con un aspecto adicional de la invención, a partir de la señal registrada en el dedo (desde algún otro punto de una manera no invasiva) , el método hace posible una reconstrucción directa de la señal en la aorta y en la arteria pulmonar, y desde la última señal de una reconstrucción del gasto cardíaco.
Más específicamente, de acuerdo con la invención a fin de obtener la estimación SV hemos tomado en consideración la presión de onda en la aorta ascendente y/o en la arteria pulmonar, la distensibilidad de la arteria (E) y la resistencia periférica (R) . Por lo tanto hemos tomado en consideración que: 1) el SV depende de la variación de presión obtenida en la apertura de la válvula ventricular (que es la diferencia entre la presión sistólica y diastólica dividida por el tiempo necesario para pasar entre la sistólica y la diastólica) y 2) el SV está condicionado por E y R.
A fin de obtener estas contribuciones hemos tomado en cuenta el valor de la presión dícrota y los otros puntos característicos entre la presión dícrota sistólica (estos valores de presión se deben dividir por el tiempo. Este tiempo es la diferencia entre el final del ritmo cardíaco y el momento en que se toma... [Seguir leyendo]
Reivindicaciones:
1. El método para estimar el gasto cardíaco Q, que comprende una primera etapa para recibir una presión sanguínea, que se ha adquirido por medio de un sensor, y convertir la presión sanguínea recibida a una señal de presión p (t) expresada en mmHg; una segunda etapa para calcular una estimación de un volumen sistólico del ventrículo izquierdo LSV, tal estimación se calcula como una función de una impedancia hidráulica de la arteria; una tercera etapa para calcular una estimación del gasto cardíaco Q como un producto del volumen sistólico del
ventrículo izquierdo LSV multiplicado por un valor de frecuencia cardíaca actual HR:
Q= LSV*HR
el método está caracterizado porque la impedancia hidráulica de la arteria se calcula por medio de un análisis de la 15 primera y segunda derivadas con respecto al tiempo de la señal de presión p (t) sobre la base del punto de resonancia, el punto sistólico, el punto diastólico y el punto dícroto de la señal de presión p (t) .
2. El método de acuerdo con la reivindicación 1, caracterizado porque la estimación del volumen sistólico del ventrículo izquierdo LSV se calcula de acuerdo con la siguiente formula
LSV = (K/1000000) *[B (Pm) /K1] * (a/Ztot) ]
donde: -K es una primera constante igual a 1: K=1;
-Pm = (psist+2pdias) /3 es un valor de presión medio, con psist = p (tsist) es la presión sistólica en el tiempo de pulso sistólico tsist, y pdias = p (tdias) es la presión diastólica en el tiempo de pulso diastólico tdias, -en donde B (Pm) se da, cuando dicha presión sanguínea se toma en una aorta ascendente, por
de otra manera, cuando dicha presión sanguínea se toma en una arteria pulmonar, por
de otra manera, cuando dicha presión sanguínea no se registra de manera invasiva desde el dedo arterial o se registra de manera invasiva desde la arteria femoral o desde otro punto periférico tal como la arteria braquial o radial, por
- K1 es una segunda constante, igual a:
100, cuando dicha presión sanguínea se toma en una aorta ascendente o se registra de manera invasiva desde una arteria femoral o desde otro punto periférico tal como la arteria braquial o radial, de otra manera 12, cuando dicha presión sanguínea es una toma en la arteria pulmonar, de otra manera 90, cuando dicha presión sanguínea no se registra de manera invasiva desde el dedo arterial,
- A es un área bajo la totalidad de la señal de presión p (t) dada por la integral de la señal de presión p (t) entre el tiempo tdias en el pulso diastólico y el tiempo tdíc en la presión dícrota pdíc, y
- Ztot es un factor de división que es igual a Z1 + Z2 - Z3,
cuando dicha presión sanguínea se toma en una aorta ascendente y la señal de presión p (t) es del tipo que se muestra en la Figura 4, y la primera y segunda derivadas de la señal de presión p (t) son como las que se muestran en las Figuras 5 y 6 así como también cuando dicha presión sanguínea se registra o no de manera invasiva desde el dedo arterial o se registra de manera invasiva desde una arteria femoral o desde otro punto periférico tal como la arteria braquial o radial, y la señal de presión p (t) es del tipo que se muestra en la Figura 11, y las correspondientes primera y segunda derivadas de la señal de presión p (t) son como las que se muestran en la Figura 12 y 13, o Z1 + Z2 - 2*Z3, cuando dicha presión sanguínea no se registra de manera invasiva desde el dedo arterial o se registra de manera invasiva desde una arteria femoral u otro punto periférico tal como la arteria braquial o radial y la señal de presión p (t) es del tipo que se muestra en la Figura 14, y las correspondientes primera y segunda derivadas de la señal de presión p (t)
son como las que se muestran en las Figuras 15 y 16, o Z1 +Z2 - 2*Z3 - Z5, cuando dicha presión sanguínea no se registra de manera invasiva desde el dedo arterial o se registra de manera invasiva desde una arteria femoral u otro punto periférico tal como la arteria braquial o radial y la señal de presión p (t) es del tipo que se muestra en la Figura 17, y las correspondientes primera y segunda derivadas de la señal de presión p (t)
son como las que se muestran en las Figuras 18 y 19,
donde:
- Z1 = (psist-pdias) /tsist, -Z2 = pdíc/ (tfinal-tdíc) , con tfinal es el tiempo del final del ciclo cardíaco,
-Z3 = P3/ (tfinal-t3) , con t3 es el tiempo del valor mínimo de la segunda derivada de la señal de presión p (t) entre el tiempo tsist y el tiempo tdíc, y P3=p (t3) es la presión correspondiente, y -Z5 = P5/ (tfinal-t5) , con t5 es el tiempo del primer valor máximo de la segunda derivada de la señal de presión p (t) entre el tiempo tsist y el tiempo tdíc, y P5=p (t5) es la presión correspondiente.
3. El método de acuerdo con la reivindicación 1, en que la presión se adquiere de una manera no invasiva desde la arteriola del dedo, y se lleva a cabo una reconstrucción de la señal de presión en la aorta ascendente por medio de una regresión múltiple lineal.
4. El aparato para estimar el gasto cardíaco Q, caracterizado porque comprende: -el medio sensor de presión para sensar una presión sanguínea; y -el medio de procesamiento para llevar a cabo los métodos de acuerdo con cualquiera de las reivindicaciones 1-3.
5. El aparato de acuerdo con la reivindicación 4, caracterizado porque el medio sensor de presión es un pequeño 20 brazalete para mediciones no invasivas, que se envuelve alrededor de un dedo.
6. El programa de computadora que se puede cargar en una unidad de computadora, caracterizado porque se adapta para ejecutarse, cuando se ejecuta en la unidad de computadora, el método para estimar el gasto cardíaco Q de acuerdo con cualquiera de las reivindicaciones anteriores 1-3.
7. Un medio legible por computadora que almacena un programa de computadora, caracterizado porque el programa es el programa de computadora de acuerdo con la reivindicación 6.
=i (Eca E;v
=i (Eca E;v
=i (Eca E;v
=i (Eca E;v
=i (Eca E;v
o"iEa . (!. i>a =i (Eca E;v
=i (Eca E;v
=i (Eca E;v
Eºa; o"iEa; . (!. i>a;
=i (Eca E;v
=i (Eca E;v
Patentes similares o relacionadas:
PECHERA ENVOLVENTE PARA MONITOREO E.C.G., del 23 de Mayo de 2019, de ALEGRE, Gastón Gabriel: Pechera envolvente para monitoreo E.C.G. constituida por una primera lámina y una segunda lámina adosada a la primera, ambas flexibles e inelásticas. […]
Métodos para la detección de una convulsión a partir de los datos cardiacos, del 24 de Abril de 2019, de Cyberonics, Inc: Un producto de programa informático codificado con instrucciones que, cuando son ejecutadas por un ordenador, hacen que un dispositivo médico lleve a cabo un método de […]
Un traje de baño, del 27 de Marzo de 2019, de Roka Sports Inc: Un traje de baño, que comprende: una porción de cintura que se extiende alrededor de la cintura de un usuario; una correa de cintura […]
Selección de vectores de detección en un dispositivo de estimulación cardiaca con evaluación postural, del 26 de Noviembre de 2018, de CAMERON HEALTH, INC.: Un sistema de estimulación cardiaca implantable que comprende: un dispositivo médico implantable que incluye un receptáculo que aloja circuitos operativos […]
Diseño de traje de buceo, del 5 de Septiembre de 2018, de Roka Sports Inc: Un traje de buceo, que comprende: una primera región central que comprende un primer material y que tiene un primer grosor; […]
Contador de pulsos para recién nacidos, del 13 de Julio de 2016, de LAERDAL MEDICAL AS: Contador de pulsos que comprende un primer electrodo y un segundo electrodo adaptados para estar dispuestos en contacto con una parte […]
Sistema de monitorización continua del estado de conducción aurículo-ventricular (AV) mediante detección lejana de la actividad ventricular con un marcapasos monocameral, del 26 de Mayo de 2014, de QUESADA DORADOR, Aurelio: Se describe un sistema de monitorización continua del estado de conducción aurículo-ventricular del corazón de un paciente mediante el que resulta posible […]
 DISCRIMINACION ENTRE ARRITMIAS VENTRICULAES Y SUPRAVENTRICULARES, del 16 de Abril de 2009, de CAMERON HEALTH, INC.: Un cardioversor/desfibrilador implantable que comprende: un conjunto de electrodos conductores que incluye cierto número de electrodos (18, 20, […]
DISCRIMINACION ENTRE ARRITMIAS VENTRICULAES Y SUPRAVENTRICULARES, del 16 de Abril de 2009, de CAMERON HEALTH, INC.: Un cardioversor/desfibrilador implantable que comprende: un conjunto de electrodos conductores que incluye cierto número de electrodos (18, 20, […]