Péptidos inhibidores de la fusión del VIH con propiedades biológicas mejoradas.
Un péptido aislado que comprende una secuencia de aminoácidos de SEC ID N.º: 9.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/002990.
Solicitante: Synageva BioPharma Corp.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 128 Spring Street, Suite 520 Lexington, MA 02421 ESTADOS UNIDOS DE AMERICA.
Inventor/es: FRIEDRICH, PAUL, E., DWYER,John, BRAY,Brian L, SCHNEIDER,Stephen E, ZHANG,Huyi, TVERMOES,Nicolai A, JOHNSTON,Barbara E.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/16 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › VIH-1.
PDF original: ES-2381631_T3.pdf
Fragmento de la descripción:
Péptidos inhibidores de la fusión del VIH con propiedades biológicas mejoradas.
Campo de la invención
La presente invención se refiere a un péptido sintético derivado de la secuencia de aminoácidos de gp41 del Virus de la Inmunodeficiencia Humana (VIH) . Más específicamente, la presente invención se refiere a un péptido inhibidor de la fusión del VIH que tiene ciertas diferencias de aminoácidos, en comparación con la secuencia de adición de aminoácidos naturales de la gp41 del VIH, que confiere propiedades biológicas beneficiosas al péptido inhibidor de la fusión del VIH.
Antecedentes de la invención
Ahora se conoce bien que las células se pueden infectar por el VIH a través de un procedimiento por el que tiene lugar fusión entre la membrana celular y la membrana vírica. El modelo generalmente aceptado de este proceso es que el complejo glicoproteico de la cubierta vírica (gp120/gp41) interacciona con los receptores de superficie celular en las membranas de las células objetivo. Tras la unión de gp120 a los receptores celulares (por ejemplo, CD4 en combinación con un co-receptor de quimiocinas tal como CCR-5 o CXCR-4) , se induce un cambio conformacional en el complejo gp120/gp41 que permite a gp41 insertarse dentro de la membrana de la célula objetivo y mediar la fusión transmembrana.
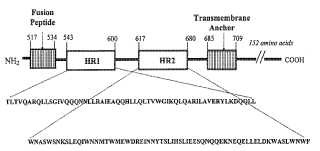
La secuencia de aminoácidos de la gp41 y su variación entre diferentes cepas de VIH, se conoce bien. La figura 1 es una representación esquemática de los dominios funcionales generalmente aceptados de gp41 (nótese que los números de secuencia de aminoácidos pueden variar ligeramente dependiendo de la cepa de VIH) . El dominio fusogénico se cree que está implicado en la inserción dentro de y en la disrupción de la membrana de la célula objetivo. El dominio transmembrana, que contiene la secuencia de ancla transmembrana, se sitúa en el extremo Cterminal de la proteína. Entre el dominio fusogénico y el ancla transmembrana están dos regiones distintas, conocidas como regiones de iteración de héptada (HR) , teniendo cada región una pluralidad de héptadas. La secuencia de aminoácidos que comprende la región HR1 y la secuencia de aminoácidos que comprende la región HR2 son cada una regiones altamente conservadas en la proteína de la cubierta del VIH-1. La región HR2 se ha descrito generalmente como que comprende residuos de aminoácidos de SEC ID N.º: 1, o polimorfismos de los mismos (véase, por ejemplo, la figura 2) . Como se muestra en la figura 1, las regiones HR tienen una pluralidad de tramos de 7 residuos de aminoácidos o "héptadas" (los 7 aminoácidos en cada héptada designados de "a" a "g") , con un predominio de los residuos hidrófobos en las posiciones primera ("a") y cuarta ("d") y residuos cargados frecuentemente en las posiciones quinta ("e") y séptima ("g") . También están presentes en la secuencia de aminoácidos de gp41 del VIH restos similares a cremalleras de leucina que comprenden una secuencia de 8 aminoácidos que se inicia con, y que finaliza con, bien una isoleucina o bien una leucina. Como se ilustra en la figura 1, la región HR2 tiene justo un resto similar a cremalleras de leucina, mientas que la región HR1 tiene cinco restos similares a cremalleras de leucina. Las héptadas y un resto similar a cremallera de leucina son características de secuencias de aminoácidos que se piensa que contribuyen a la formación de la estructura de superhélice encontrada para gp41.
Se descubrió que los péptidos derivados de la secuencia natural de la región HR1 ("péptidos HR1") o de la región HR2 ("péptidos HR2") de la gp41 del VIH inhiben la transmisión de VIH a células huésped tanto en ensayos in vitro como en estudios clínicos in vivo. Por ejemplo, los péptidos HR2, según se ejemplifican por DP176 (también conocido como T20, enfuvirtida y Fuzeon®; SEC ID N.º: 2) , T651 (SEC ID N.º: 3) , T649 (SEC ID N.º: 4) , bloquearon infección de células objetivo con potencias de 0, 5 ng/ml (CE50 frente a VIH-1LAI) , 5 ng/ml (CI50; VIH-1 IIIB) y 2 ng/ml (CI50; VIH-1 IIIB) , respectivamente. Se han realizado esfuerzos para mejorar la actividad biológica de los péptidos derivados de gp41 de VIH, tales como tratar de estabilizar la estructura del péptido helicoidal. Por ejemplo, péptidos sintéticos que tienen estabilización de la hélice se describen por los autores de la presente invención en la publicación PCT WO2005/067960 y se ejemplifican como SEC ID N.º: 5-7 en el presente documento. Péptidos sintéticos que pueden inhibir la fusión del VIH (un procedimiento por el que el gp41 del VIH media fusión entre la membrana vírica y la membrana de la célula durante el proceso de la infección por VIH de una célula objetivo) son una clase de péptidos a menudo referidos como péptidos inhibidores de fusión de VIH-1.
Otro inconveniente asociado con péptidos sintéticos se refiere a la solubilidad y estabilidad en vehículos farmacéuticamente aceptables de base acuosa, en cuanto se relaciona con el procedimiento de fabricar una formulación de solución inyectable de un péptido inhibidor de fusión del VIH. Por ejemplo, es difícil lograr una solución inyectable acuosa que contenga un péptido sintético que tenga una secuencia de aminoácidos de SEC ID N.º: 2 en una concentración de más de 100 mg/ml sin encontrar problemas de solubilidad (en los que la formulación se asemeja a un gel, más que a una solución, o el péptido precipita aparte de la solución durante un periodo de tiempo predeterminado) y de estabilidad (degradándose el péptido durante un periodo de tiempo predeterminado) y sin añadir componentes adicionales a la formulación para promover estabilidad y/o solubilidad. También sería deseable desarrollar un péptido inhibidor de fusión de VIH que tenga solubilidad y estabilidad mejoradas, teniendo mientras propiedades farmacológicas mejoradas.
Por tanto, existe una necesidad de un péptido inhibidor de la fusión del VIH, que: (a) cuando se añada en una cantidad eficaz, pueda interferir con el procedimiento de fusión vírica mediado por gp41 del VIH y más preferentemente, interferir con los cambios conformacionales de gp41 necesarios para efectuar fusión, inhibiendo de este modo la fusión de gp41 de VIH a una membrana celular objetivo; (b) demuestre solubilidad y estabilidad incrementadas en una solución acuosa; y (c) demuestre propiedades farmacológicas mejoradas. La presente invención trata de estas necesidades.
Sumario de la invención
La presente invención se refiere a péptidos aislados que son péptidos inhibidores de fusión del VIH.
En un aspecto, la presente invención se refiere a un péptido inhibidor de fusión del VIH que comprende una secuencia de aminoácidos de SEC ID N.º: 9 derivada de una secuencia de aminoácidos de base ("secuencia base") que tiene una secuencia de aminoácidos de SEC ID N.º: 5, pero en la que el péptido inhibidor de la fusión del VIH difiere de la secuencia base por tener dos restos similares a cremalleras de leucina en su secuencia de aminoácidos y por tener una leucina adicional presente en su secuencia de aminoácidos distinta de aquella necesaria para formar un resto similar a cremalleras de leucina (es decir, un aminoácido en la secuencia distinto de una posición de aminoácidos 1 a 8 de un resto similar a cremalleras de leucina sustituyendo isoleucina por leucina en una posición aminoacídica 21 de la SEC ID N.º: 5) .
La presente invención también se refiere a un péptido inhibidor de fusión de VIH, en el que el péptido inhibidor de fusión de VIH: (a) contiene la secuencia de aminoácidos de SEC ID N.º: 9 (b) tiene una secuencia de aminoácidos que tiene 2 restos similares a cremalleras de leucina; (c) que tiene una leucina adicional (por ejemplo, comparada con una secuencia de base de una cualquiera o de más SEC ID N.ºs: 5-7) en su secuencia de aminoácidos distinta de en la posición aminoacídica 1 a 8 de un resto similar a cremalleras de leucina; y (d) preferentemente demuestra una mejora de una o más propiedades biológicas. En ciertas realizaciones, el péptido inhibidor de la fusión del VIH está entre 15 y 60 residuos aminoacídicos de longitud. En una realización, el péptido inhibidor de la fusión del VIH comprende adicionalmente un grupo N-terminal o un grupo C-terminal, o ambos; aquellos grupos terminales pueden incluir, pero no están limitados a: un grupo amino o un grupo acetilo en el extremo N-terminal; y un grupo carboxilo o un grupo amido en el extremo C-terminal. En una realización, el péptido inhibidor de la fusión del VIH puede autoasociarse para formar un multímero, por ejemplo, un trímero o sintetizarse en forma multimérica,... [Seguir leyendo]
Reivindicaciones:
1. Un péptido aislado que comprende una secuencia de aminoácidos de SEC ID N.º: 9.
2. El péptido de la reivindicación 1, que comprende adicionalmente una o más funcionalidades reactivas.
3. El péptido de la reivindicación 1, en el que el péptido es de hasta 60 aminoácidos de longitud.
4. Una molécula de ácido nucleico aislado que comprende una secuencia de nucleótidos que codifica un péptido de acuerdo con la reivindicación 1.
5. Un vector que comprende la molécula de ácido nucleico de la reivindicación 4.
6. El vector de la reivindicación 5, en el que el vector es un vector de expresión.
7. Una célula aislada que comprende el vector de la reivindicación 5 ó 6.
8. Una composición que comprende: (i) el péptido de la reivindicación 1 ó 2; y (ii) un vehículo farmacéuticamente aceptable, un vehículo macromolecular, o una combinación de los mismos.
9. La composición de la reivindicación 8, en la que la composición es estéril.
10. Una combinación de agentes antirretrovirales para su uso durante el tratamiento de VIH-I, la combinación que comprende el péptido de la reivindicación 1 ó 2 y uno o más agentes antirretrovirales seleccionados del grupo constituido por un inhibidor de la entrada del VIH, un inhibidor de la integrasa del VIH, un inhibidor de la transcriptasa reversa, un inhibidor de proteasa, un inhibidor del vif, un inhibidor del factor de transcripción específico del virus, un inhibidor de procesamiento viral y un inhibidor de maduración del VIH.
11. El uso del péptido de la reivindicación 1 para la preparación de una composición farmacéutica para la inhibición de la transmisión del VIH a una célula, en el que la composición farmacéutica es para poner en contacto el virus en presencia de una célula, con una cantidad del péptido de la reivindicación 1 eficaz para inhibir la infección de la célula por el VIH.
12. El uso del péptido de la reivindicación 1 para la preparación de una composición farmacéutica para inhibir la fusión del VIH, que comprende poner en contacto el virus, en presencia de una célula, con una cantidad del péptido de la reivindicación 1 eficaz para inhibir la fusión del VIH.
13. Uso del péptido de la reivindicación 1 para la preparación de una composición farmacéutica para tratar un individuo infectado por VIH, en el que la composición farmacéutica es para administrar al individuo una cantidad del péptido de la reivindicación 1 efectiva para lograr, en el individuo tratado, un resultado terapéutico seleccionado del grupo constituido por: una reducción en la carga viral del VIH, un incremento en la población de células CD4+ circulantes y una combinación de las mismas.
14. Un procedimiento de sintetizar el péptido de SEC ID N.º: 9, en el que un conjunto de los tres fragmentos peptídicos se produce por síntesis en fase sólida, el conjunto comprende:
a. SEC ID N.º: 17, SEC ID N.º 18, SEC ID N.º: 19, y un resto de leucina; o
b. SEC ID N.º: 17, SEC ID N.º: 18 y SEC ID N.º: 20;
en el que los miembros del grupo se combinan después usando un enfoque de condensación de fragmentos para producir el péptido SEC ID N.º: 9.
15. Un conjunto de péptidos, en el que el conjunto comprende:
a. TTWEAWDRAIAE (SEC ID N.º: 17) YAARIEALLRALQE (SEC ID N.º: 18) , QQEKNEAALRE (SEC ID N.º: 19) ;
b. TTWEAWDRAIAE (SEC ID N.º: 17) YAARIEALLRALQE (SEC ID N.º: 18) , QQEKNEAALREL (SEC ID N.º: 20) ;
c. TTWEAWDRAIAEYAARIEAL (SEC ID N.º: 29) , LRALQEQQEKNEAALRE (SEC ID N.º: 30) ;
d. TTWEAWDRAIAEYAARIEAL (SEC ID N.º: 29) , LRALQEQQEKNEAALREL (SEC ID N.º: 31) ;
e. TTWEAWDRAIA (SEC ID N.º: 21) , EYAARIEALLRALQE (SEC ID N.º: 22) , QQEKNEAALRE (SEC ID N.º: 19) ;
f. TTWEAWDRAI (SEC ID N.º: 23) , AEYAARIEALLRALQE (SEC ID N.º: 24) , QQEKNEAALRE (SEC ID N.º: 19) ;
g. TTWEAWDRA (SEC ID N.º: 25) , IAEYAARIEALLRALQE (SEC ID N.º: 26) , QQEKNEAALRE (SEC ID N.º: 19) ; h) TTWEAWDR (SEC ID N.º: 27) , AIAEYAARIEALLRALQE (SEC ID N.º: 28) , QQEKNEAALRE (SEC ID N.º: 19) ;
i. TTWEAWDRAIA (SEC ID N.º: 21) , EYAARIEALLRALQE (SEC ID N.º: 22) , QQEKNEAALREL (SEC ID N.º: 20) ;
j. TTWEAWDRAI (SEC ID N.º: 23) , AEYAARIEALLRALQE (SEC ID N.º: 24) , QQEKNEAALREL (SEC ID N.º: 20) ;
k. TTWEAWDRA (SEC ID N.º: 25) , IAEYAARIEALLRALQE (SEC ID N.º: 26) , QQEKNEAALREL (SEC ID N.º: 20) ;
l. TTWEAWDR (SEC ID N.º: 27) , AIAEYAARIEALLRALQE (SEC ID N.º: 28) , QQEKNEAALREL (SEC ID N.º: 20) ;
m. TTWEAWDRAIAEYAARIE (SEC ID N.º: 32) , ALLRALQEQQEKNEAALRE (SEC ID N.º: 33) ;
n. TTWEAWDRAIAEYAARIE (SEC ID N.º: 32) , ALLRALQEQQEKNEAALREL (SEC ID N.º: 34) ;
o. TTWEAWDRAIAEYAARIEALLRALQE (SEC ID N.º: 40) , QQEKNEAALRE (SEC ID N.º: 19) ; o
p. TTWEAWDRAIAEYAARIEALLRALQE (SEC ID N.º: 40) , QEKNEAALREL (SEC ID N.º: 20) .
16. El grupo de péptidos de la reivindicación 15, en el que una o más cadenas laterales de al menos un péptido están protegidas con un grupo protector.
17. El grupo de péptidos de la reivindicación 16, en el que el grupo protector se selecciona del grupo constituido por 9-fluoroenilmetoxi-carbonilo (Fmoc) , t-butilo (t-Bu) , tritilo (trt) , butiloxicarbonilo (Boc) , carbobenzoxilo, dansilo y un grupo éster de para-nitrobencilo.
18. El péptido de la reivindicación 1, en el que el péptido comprende adicionalmente un grupo N-terminal o Cterminal.
19. El péptido de la reivindicación 1, en el que la secuencia de aminoácidos consiste en la SEC ID N.º: 9.
20. El péptido de la reivindicación 19, en el que el péptido consiste en la secuencia de aminoácidos de SEC ID N.º: 9 y un grupo N-terminal o un grupo C-terminal.
21. El péptido de la reivindicación 19 ó 20, en el que el grupo N-terminal es un grupo amino o un grupo acetilo; y el grupo C-terminal es un grupo carboxilo o un grupo amido.
22. El péptido de la reivindicación 21, en el que el grupo N-terminal es un grupo acetilo.
23. El péptido de la reivindicación 21, en el que el grupo C-terminal es un grupo amido.
24. El péptido de la reivindicación 21, en el que el grupo N-terminal es un grupo acetilo y el grupo C-terminal es un grupo amido.
25. El péptido de la reivindicación 24, en el que el péptido consiste en la secuencia de aminoácidos de SEC ID N.º: 9, un grupo N-terminal que es un grupo acetilo y un grupo C-terminal que es un grupo amido.
26. Un dímero, un trímero o un multímero del péptido de la reivindicación 1, 19, o 24.
27. El trímero de la reivindicación 26.
28. Una composición que comprende el péptido de la reivindicación 19 ó 24 y un vehículo farmacéuticamente aceptable.
29. La composición de la reivindicación 28, en el que dicho vehículo farmacéuticamente aceptable es agua, agua tamponada, solución salina, glicina al 0, 3 %, alcoholes acuosos, o solución acuosa isotónica.
30. Una combinación de agentes antirretrovirales para su uso durante el tratamiento de VIH-1, la combinación que comprende el péptido de la reivindicación 1 ó 2 y uno o más agentes antirretrovirales seleccionados del grupo constituido por un inhibidor de la entrada del VIH, un inhibidor de la integrasa del VIH, un inhibidor de la transcriptasa inversa, un inhibidor de proteasa, un inhibidor del vif, un inhibidor del factor de transcripción específico del virus, un inhibidor de procesamiento viral y un inhibidor de maduración del VIH.
31. El uso del péptido de la reivindicación 1, 2 ó 19 para la preparación de una preparación farmacéutica para el
tratamiento del VIH-1, en combinación con uno o más agentes antirretrovirales seleccionados del grupo constituido por un inhibidor de la entrada del VIH, un inhibidor de la integrasa del VIH, un inhibidor de la transcriptasa inversa, un inhibidor de proteasa, un inhibidor del vif, un inhibidor del factor de transcripción específico del virus, un inhibidor de procesamiento viral y un inhibidor de maduración del VIH.
32. Un procedimiento de síntesis del péptido de la reivindicación 20, dicho procedimiento comprende la condensación de fragmentos peptídicos que tienen las secuencias de aminoácidos de SEC ID N.º: 19 y SEC ID N.º:
40.
33. El procedimiento de la reivindicación 32 en el que el fragmento peptídico que tiene la secuencia de aminoácidos de SEC ID N.º: 19 se acopla covalentemente con un residuo de aminoácido leucina antes de la condensación de los fragmentos peptídicos.
34. Un conjunto de fragmentos peptídicos para la síntesis del péptido de la reivindicación 20, que comprende un conjunto de fragmentos peptídicos que tienen las secuencias aminoacídicas seleccionadas del grupo constituido por:
a. SEC ID N.º: 40 y SEC ID N.º: 19;
b. SEC ID N.º: 40 y SEC ID N.º: 20;
c. SEC ID N.º: 17, SEC ID N.º: 18, SEC ID N.º: 19 y Leu;
d. SEC ID N.º: 17, SEC ID N.º: 18 y la SEC ID N.º: 20; o
e. SEC ID N.º: 7 y SEC ID N.º: 35.
35. Uso de una combinación de agentes antivirales para la preparación de una preparación farmacéutica para el tratamiento de VIH, la combinación que comprende el péptido de la reivindicación 1, 2, 20 ó 25 y uno o más agentes antivirales seleccionados del grupo constituido por un inhibidor de la entrada del VIH, un inhibidor de la integrasa del VIH, un inhibidor de la transcriptasa inversa, un inhibidor de proteasa, un inhibidor del vif, un inhibidor del factor de transcripción específico del virus, un inhibidor de procesamiento viral y un inhibidor de maduración del VIH.
FIG. 2
FIG. 3
FIG. 4
Patentes similares o relacionadas:
Uso de una proteína accesoria derivada del VIH para la reactivación del VIH latente, del 27 de Mayo de 2020, de Janssen Sciences Ireland Unlimited Company: Una proteína que consiste en los primeros 66 aminoácidos N-terminales (T66) de la proteína accesoria Tat derivada del virus de inmunodeficiencia humana […]
Sal de cloruro de Tat-NR2B9c, del 29 de Enero de 2020, de NoNO Inc: Una sal de cloruro de un péptido que es TAT-NR2B9c (SEQ ID NO:6) o difiere de TAT-NR2B9c en hasta 5 sustituciones, inserciones o deleciones de […]
Direccionamiento de factores de coagulación al TLT-1 en plaquetas activadas, del 23 de Octubre de 2019, de NOVO NORDISK HEALTH CARE AG: Una proteína procoagulante que comprende (i) al menos un factor de coagulación, que es un polipéptido de FVII o un polipéptido de FIX, unido covalentemente […]
Vector dual para la inhibición del virus de la inmunodeficiencia humana, del 16 de Octubre de 2019, de Calimmune Inc: Una célula hospedadora preparada transduciendo una célula hematopoyética con un vector de expresión lentiviral, comprendiendo el vector de expresión lentiviral una primera […]
Antígenos del virus de la inmunodeficiencia humana, vectores, composiciones y métodos de uso de los mismos, del 28 de Agosto de 2019, de Janssen Vaccines & Prevention B.V: Un ácido nucleico que codifica una proteína de la envoltura del VIH sintética que comprende la secuencia de aminoácidos de la SEQ ID NO: 8, o la SEQ ID […]
Procedimiento novedoso y composiciones, del 12 de Junio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Uno o más primeros polipéptidos inmunógenos para su uso en un procedimiento de generación de una respuesta inmunológica frente a Mycobacterium spp., en los […]
 Producción rápida de virus de título elevado, del 29 de Mayo de 2019, de ALEXION PHARMACEUTICALS, INC.: Procedimiento de producción de partículas virales, que comprende:
introducir de forma transitoria en una línea celular DF-1 una secuencia de nucleótidos […]
Producción rápida de virus de título elevado, del 29 de Mayo de 2019, de ALEXION PHARMACEUTICALS, INC.: Procedimiento de producción de partículas virales, que comprende:
introducir de forma transitoria en una línea celular DF-1 una secuencia de nucleótidos […]
Vectores y construcciones de liberación de antígenos de virus de la gripe, del 8 de Mayo de 2019, de ALTIMMUNE UK LIMITED: Una construcción de vector fluorocarbonado-antígeno de estructura CmFN--CyHx-(Sp)-R, donde m = 3 a 30, n <= 2m + 1, y = 0 a 15, x <= 2y, […]