COMBINACIÓN DE ESTEROIDES QUE TIENEN ACTIVIDAD CORTICOSTEROIDEA MEJORADA POR TRANSPORTADORES.
Una combinación que comprende: (a) un compuesto que tiene la fórmula:
en la que: R1 es alquilo C1-C7; Z es carbonilo o p-hidroximetileno; X es Cl o F; y la línea punteada en el anillo A indica que la unión 1,2 está saturada o insaturada; y (b) un compuesto que tiene la fórmula: en la que: Z1 es carbonilo, p-hidroximetileno o metileno; R2 es H, -OH o -OCOR3 donde R3 es alquilo C1-C5; Y es -OH, -SH o -OCOR4, donde R4 es alquilo C1-C5, ciclopentiletilo o dietilaminometilo; y la línea punteada se define como anteriormente; en una cantidad antiinflamatoria combinada, sinérgicamente eficaz; siendo la cantidad de compuesto de fórmula (II) suficiente para potenciar la actividad antiinflamatoria o la duración de la acción, o ambas, de dicho compuesto de fórmula (I), donde dicha cantidad de dicho compuesto de fórmula (II) sola es insuficiente como para tener actividad antiinflamatoria; con la salvedad de que la combinación excluye cualquier compuesto de fórmula: en la que: R es H o alquilo C1-C4; Z2 es carbonilo o ß-hidroximetileno; X1 es -O- o -S-; R5 es -OH, -OR6, -OCOOR6 o -OCOR7 donde R6 es alquilo C1-C4 y R7 es alquilo C1-C4, fluorometilo o clorometilo; y la línea punteada es como se ha definido anteriormente; con la salvedad de que cuando R es alquilo C1-C4, entonces R5 es -OH
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/012304.
Solicitante: BODOR, NICHOLAS S.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 10225 COLLINS AVENUE, UNIT 1002/1004 BAL HARBOUR, FL 33154 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BODOR, NICHOLAS, S..
Fecha de Publicación: .
Fecha Solicitud PCT: 24 de Mayo de 2007.
Clasificación Internacional de Patentes:
- A61K31/568 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › sustituidos en posición 10 y 13 por una cadena que tiene al menos un átomo de carbono, p. ej. androstano, testosterona.
- C07J3/00B
- C07J5/00C1
Clasificación PCT:
- A61K31/568 A61K 31/00 […] › sustituidos en posición 10 y 13 por una cadena que tiene al menos un átomo de carbono, p. ej. androstano, testosterona.
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2356946_T3.pdf
Fragmento de la descripción:
ANTECEDENTES DE LA INVENCIÓN
CAMPO TÉCNICO DE LA INVENCIÓN
La invención se refiere a potenciar la actividad y/o la duración de la acción de esteroides antiinflamatorios 5 particulares para aplicación tópica u otra aplicación local.
TÉCNICA ANTERIOR:
La aplicación tópica u otra aplicación local de potentes glucocorticoides puede producir efectos tóxicos 10 graves tales como rasgos de Cushingoid, supresión pituitaria-suprarrenal, atrofia dérmica, inmunosupresión, aumento de peso e inhibición de la cicatrización de heridas. Se han producido otras clases de respuestas tóxicas, incluyendo alergias y cataratas, como consecuencia 15 del uso de fármacos de este tipo a largo plazo.
La aplicación oftálmica de glucocorticosteroides presenta problemas adicionales. Los mecanismos protectores incorporados al ojo permiten que se apliquen solamente pequeñas dosis al ojo para alcanzar los sitios diana dentro 20 de éste; en general, más del 90% de la dosis total traspasa a la circulación general. A su vez, esto conduce a graves efectos colaterales sistémicos del tipo anteriormente descrito. Además, existe un efecto colateral más grave y específico cuando estos fármacos se utilizan en el ojo: un 25 aumento de la presión intraocular (IOP). El glaucoma crónico o agudo inducido por corticosteroides se ha reportado, de hecho, desde principios de los años sesenta. En general, el corticosteroide es necesario solo tópicamente para controlar la inflamación. No obstante, el 30 esteroide absorbido es responsable de los efectos colaterales graves antes mencionados. Se cree que el efecto del corticosteroide sobre la vía de flujo acuoso y los
glucosaminoglicanos del tejido adyacente (GAG) es importante en el desarrollo de hipertensión ocular inducida por glucocorticoides.
Los glucocorticosteroides naturales y muchos de sus derivados comercializados son Δ4 y Δ1,4 pregnenos que tienen 5 sustituyentes 21-hidroxi. Existen, no obstante, una serie de antiinflamatorios Δ4 y Δ1,4 androstenos que se describen en la bibliografía; obsérvense, por ejemplo, la memoria de patente británica No. 1,384,372; Phillipps et al, la patente estadounidense No. 3,828,080 y Kalvoda et al. y la 10 patente estadounidense No. 4,285,937.
En los últimos años, se han desarrollado esteroides suaves en un intento de proveer compuestos que tengan actividad antiinflamatoria potente con mínima actividad sistémica. Una serie de esteroides suaves que se describe 15 que tiene potente actividad antiinflamatoria con mínima actividad sistémica consiste en los 17-carbonatos de la patente estadounidense de Bodor No. 4,996,335. Estos compuestos incluyen, como realizaciones preferidas, haloalquil 17α-alcoxicarboniloxi-11β-hidroxiandrost-4-en-3-20 ona-17β-carboxilatos y los correspondientes compuestos Δ1,4, que opcionalmente portan sustituyentes 6α- y/o 9α-flúor y 16α- o 16α-metilo. Uno de estos compuestos es 17α-etoxicarboniloxi-11β-hidroxiandrosta-1,4-dien-3-ona-17β-carboxilato de clorometilo, también conocido como 25 loteprednol etabonato. El loteprednol etabonato actualmente es comercializado en los Estados Unidos por Bausch & Lomb Pharmaceuticals, Inc. como Alrex® y Lotemax® y combinado con tobramicina como Zylet® para uso oftálmico. Otros usos del loteprednol etabonato se encuentran actualmente bajo 30 estudios clínicos (para la rinitis y diversas afecciones dermatológicas).
A pesar del desarrollo de esteroides que tienen menos toxicidad sistémica, existe una gran necesidad de mejorar las aplicaciones tópicas y otras aplicaciones locales. Los compuestos local y tópicamente activos más nuevos y menos tóxicos son más costosos de sintetizar que los compuestos 5 ya consolidados. Asimismo, los esteroides antiinflamatorios más potentes son aquellos que tienen sustitución en las posiciones 6, 9 y/o 16 y, por lo tanto, no solo son los más eliminados estructuralmente de los corticosteroides naturales sino que además son los que poseen la mayor 10 toxicidad. Por lo tanto, existe la necesidad de potenciar la actividad o la duración de la acción, o ambas, de los androstenos suaves del tipo 17α-carbonato que carecen del patrón de sustitución 6-, 9- y/o 16. Además, sería conveniente permitir que estos esteroides se sometan a un 15 metabolismo más simple y se concentren en el sitio de acción deseado.
Uno de los principales metabolitos inactivos de la hidrocortisona es el ácido cortiénico, es decir, ácido 11β,17β-dihidroxiandrost-4-en-3-ona-17β-carboxílico. El 20 ácido cortiénico y el correspondiente ácido Δ1,4 ya se han descrito como intermedios sintéticos útiles en la preparación de los esteroides suaves descritos en las patentes estadounidenses de Bodor No. 4,710,495 y No. 4,996,335. Los ésteres 17β-metilo, etilo e isopropilo de 25 ácido Δ1-cortiénico se han descrito como metabolitos inactivos putativos de los derivados de androsteno del documento WO 97/42214 y de la patente estadounidense de Bodor No. 5,981,517. La patente '517 también describe el uso de ácido A1-cortiénico como competidor (con [3H]-30 triamcinolona acetonida como marcador) para estudios in vitro de unión a los receptores de los derivados de androsteno de esa patente y menciona estudios similares de
loteprednol etabonato. Druzgala et al., J. Steroid Biochem. Mole. Biol., Vol. 38, No. 2, pág. 149-154 (1991) describe estudios anteriores de unión a receptores in vitro de loteprednol etabonato y dos metabolitos putativos, ácido Δ1-cortiénico y el correspondiente carbonato de 17α-etilo, 5 en un medio que contiene 10-5M ácido cortiénico como competidor, junto con [3H]-triamcinolona acetonita como marcador. Druzgala et al. también explican que el loteprednol propiamente dicho es activo desde el punto de vista intrínseco, mientras que los metabolitos putativos 10 son en realidad inactivos. Ni estos ácidos ni sus ésteres han sido indicados como ingredientes activos para uso en composiciones farmacéuticas para el tratamiento de la inflamación, ya que no son activos en sí mismos como agentes antiinflamatorios. 15
No obstante, se ha descrito que dichos metabolitos inactivos potencian la actividad antiinflamatoria y la duración de la acción del loteprednol etabonato y los esteroides suaves relacionados en la publicación de solicitud de patente estadounidense de Bodor No. 20 2005/0026892A1 (correspondiente al documento WO2005/000317), publicada el 3 de febrero de 2005. Dichos metabolitos inactivos también se han descrito como potenciadores de la actividad antiinflamatoria y la duración de la acción de otros corticosteroides 25 seleccionados, por ejemplo, hidrocortisona; véase la publicación de solicitud de patente estadounidense de Bodor No. 2005/0020351A1, publicada el 27 de enero de 2005 (correspondiente al documento WO2004/112800).
No obstante, aún existe la necesidad de métodos y 30 composiciones alternativos para potenciar la actividad antiinflamatoria y la duración de la acción del loteprednol etabonato y los esteroides suaves relacionados.
RESUMEN Y OBJETOS DE LA INVENCIÓN
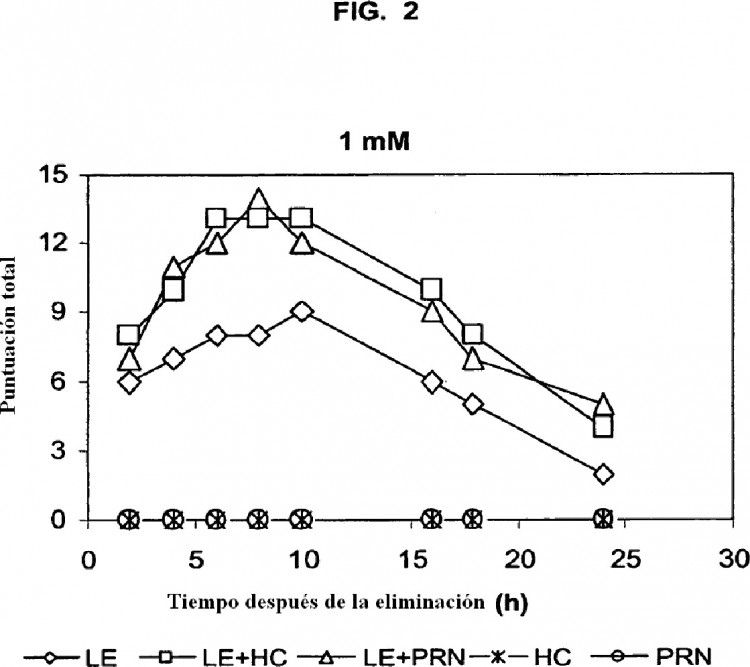
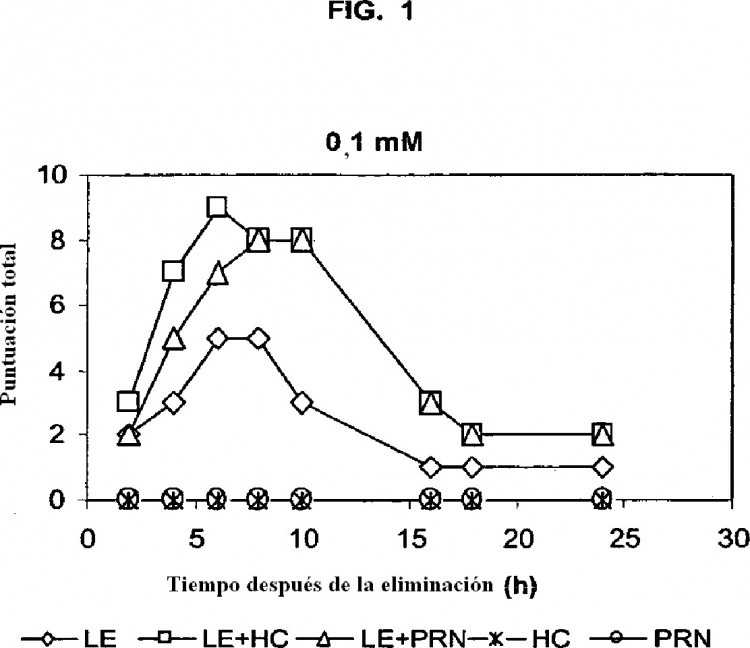
Se ha descubierto ahora que la hidrocortisona, la prednisolona y compuestos asociados potencian la actividad tópica u otra actividad local, o la duración de la acción, de esteroides antiinflamatorios suaves seleccionados, como 5 el loteprednol etabonato. Por consiguiente, en un aspecto, la presente invención provee una combinación que comprende:
(a) un compuesto que tiene la fórmula:
en la que: 10
R1 es alquilo C1-C7;
Z es carbonilo o p-hidroximetileno; X es Cl o F;
y la línea punteada en el anillo A indica que la unión 1,2 es saturada o insaturada;
y 15
(b) un compuesto que tienen la fórmula:
en la que:
Z1 es carbonilo, p-hidroximetileno o metileno;
R2 es H, -OH o -OCOR3 donde R3 es alquilo C1-C5; 20
Y es -OH, -SH o -OCOR4, donde R4 es alquilo C1-C5, ciclopentiletilo o dietilaminometilo;
y la línea punteada en el anillo A indica que la unión 1,2 está saturada o insaturada; en una cantidad antiinflamatoria eficaz, combinada y sinérgica; 5
donde la cantidad de compuesto de formula (II) es suficiente para potenciar la actividad antiinflamatoria o la duración de la acción, o ambas, de dicho compuesto de fórmula (I), siendo... [Seguir leyendo]
Reivindicaciones:
1. Una combinación que comprende:
(a) un compuesto que tiene la fórmula:
en la que: 5
R1 es alquilo C1-C7;
Z es carbonilo o p-hidroximetileno;
X es Cl o F;
y la línea punteada en el anillo A indica que la unión 1,2 está saturada o insaturada; y 10
(b) un compuesto que tiene la fórmula:
en la que:
Z1 es carbonilo, p-hidroximetileno o metileno;
R2 es H, -OH o -OCOR3 donde R3 es alquilo C1-C5; 15
Y es -OH, -SH o -OCOR4, donde R4 es alquilo C1-C5, ciclopentiletilo o dietilaminometilo;
y la línea punteada se define como anteriormente;
en una cantidad antiinflamatoria combinada, sinérgicamente eficaz;
siendo la cantidad de compuesto de fórmula (II) suficiente para potenciar la actividad antiinflamatoria o la duración de la acción, o ambas, de dicho compuesto de fórmula (I), 5 donde dicha cantidad de dicho compuesto de fórmula (II) sola es insuficiente como para tener actividad antiinflamatoria;
con la salvedad de que la combinación excluye cualquier compuesto de fórmula: 10
en la que:
R es H o alquilo C1-C4;
Z2 es carbonilo o β-hidroximetileno;
X1 es -O- o -S-; 15
R5 es -OH, -OR6, -OCOOR6 o -OCOR7 donde R6 es alquilo C1-C4 y R7 es alquilo C1-C4, fluorometilo o clorometilo;
y la línea punteada es como se ha definido anteriormente;
con la salvedad de que cuando R es alquilo C1-C4, entonces R5 es -OH. 20
2. Una combinación según la reivindicación 1, en la que el compuesto de fórmula (I) es:
(a) 17α-etoxicarbonilox-11β-hidroxiandrosta-1,4-dien-3-ona-17β-carboxilato de clorometilo;
(b) 11β-hidroxi-17α-metoxicarboniloxiandrost-4-en-3-ona-25 17β-carboxilato de clorometilo;
(c) 17α-etoxicarbonilox-11β-hidroxiandrost-4-en-3-ona-17β-carboxilato de clorometilo;
(d) 17α-butoxicarboniloxi-11β-hidroxiandrost-4-en-3-ona-17β-carboxoliato de clorometilo;
(e) 11β-hidroxi-17α-isopropoxicarboniloxiandrost-4-en-3-5 ona-17β-carboxilato de clorometilo;
(f) 11β-hidroxi-17α-isopropoxicarboniloxiandrosta-1,4-dien-3-ona-17β-carboxilato de clorometilo;
(g) 11β-hidroxi-17α-isobutoxicarboniloxiandrost-4-en-3-ona-17β-carboxilato de clorometilo; 10
(h) 11β-hidroxi-17α-propoxicarboniloxiandrost-4-en-3-ona-17β-carboxilato de clorometilo;
(i) 11β-hidroxi-17α-isopropoxicarboniloxiandrost-4-en-3-ona-17β-carboxilato de fluoroxnetilo;
(j) 11β-hidroxi-17α-n-propoxicarboniloxiandrosta-1,4-dien-15 3-ona-17β-carboxilato de clorometilo; o
(k) 11β-hidroxi-17α-metoxicarboniloxiandrosta-1,4-dien-3-ona-17β-carboxilato de clorometilo.
3. Una combinación según la reivindicación 1, en la que, en el compuesto de fórmula (I), 20
(a) R1 es metilo, etilo, n-propilo, isopropilo, n-butilo o isobutilo, X es cloro y Z es p-hidroximetileno, y/o
(b) la unión 1,2 está insaturada.
4. Una combinación según la reivindicación 1, en la que el compuesto de fórmula (I) es loteprednol etabonato. 25
5. Una combinación según una cualquiera de las reivindicaciones 1 a 4, en la que el compuesto de fórmula (II) es cortisona, acetato de cortisona, hidrocortisona, acetato de hidrocortisona, hidrocortisona aceponato, hidrocortisona butirato, cortisona 21-30 ciclopentanopropionato, hidrocortisona 21-cipionato, hidrocortisona valerato, prednisolona, prednisolona, acetato, prednisolona tebutato, prednisolona 21-pivalato,
prednisolamato, prednival, prednisona, prednisona 21-acetato, corticosterona, tixocortol, corticosterona 21-acetato, hidrocortamato, 11-desoxicorticosterona, 11-desoxihidrocortisona, prednicarbato o hidrocortisona tebutato, especialmente acetato de hidrocortisona, 5 hidrocortisona butirato, prednisolona, prednisolona acetato, prednisona, corticosterona, 11-desoxicorticosterona u 11-desoxihidrocortisona.
6. Una composición farmacéutica que comprende:
(1) una combinación según una cualquiera de las 10 reivindicaciones 1 a 5, y
(2) un vehículo no tóxico, farmacéuticamente aceptable para ello, adecuado para aplicación tópica u otra aplicación local.
7. Una composición farmacéutica que comprende: 15
(1) una cantidad antiinflamatoria combinada sinérgicamente eficaz de:
(a) loteprednol etabonato; y
(b) un compuesto que tiene la fórmula:
20
en la que Z1 es carbonilo, β-hidroximetileno o metileno; R2 es H, -OH o -OCOR3 donde R3 es alquilo C1-C5; Y es -OH, -SH o -OCOR4 donde R4 es alquilo C1-C5; y la línea punteada en el anillo A indica que la unión 1,2 está saturada o insaturada, donde la cantidad de compuesto de fórmula (II) 25 es suficiente para potenciar la actividad antiinflamatoria
o la duración de la acción, o ambas, del loteprednol etabonato, donde dicha cantidad de dicho compuesto de fórmula (II) sola es insuficiente como para tener actividad antiinflamatoria; y
(2) un vehículo no tóxico, farmacéuticamente aceptable para 5 aplicación tópica u otra aplicación local;
con la salvedad de que la composición excluye cualquier compuesto que tenga la fórmula:
10
en la que:
R es H o alquilo C1-C4;
Z2 es carbonilo o β-hidroximetileno;
X1 es -O- o-S-;
R5 es -OH, -OR6, -OCOOR6 o -OCOR7 donde R6 es alquilo C1-C4 y 15 R7 es alquilo C1-C4, fluorometilo o clorometilo;
y la línea punteada es como se ha definido anteriormente;
con la salvedad de que cuando R es alquilo C1-C4, entonces R5 es -OH.
8. Una composición según la reivindiación 7, en la que 20 la relación molar del compuesto de fórmula (II) al loteprednol etabonato oscila entre aproximadamente 2:1 y aproximadamente 0,05:1.
9. Una composición según una cualquiera de las reivindicaciones 6 a 8, en la que: 25
(a) el vehículo es aceptable desde el punto de vista oftálmico y la composición es una composición oftálmica; o
(b) la composición está formulada como: un ungüento, gel, loción o crema; un polvo; gotas o una pulverización; un supositorio, enema de retención o espuma; un comprimido o 5 miniesfera masticable o para chupar; un aerosol; una formulación nebulizada o en polvo para inhalación oral; una forma de dosificación parenteral u otra forma inyectable; una forma de dosificación oral que libera los ingredientes activos en los intestinos grueso o delgado. 10
10. Una composición según una cualquiera de las reivindicaciones 6 a 9, formulada en un parche dérmico o transdérmico, donde la composición se usa opcionalmente en el tratamiento de inflamación dérmica.
11. Una combinación según una cualquiera de las 15 reivindicaciones 1 a 5 o una composición según una cualquiera de las reivindicaciones 6 a 9, para uso en el tratamiento de inflamación tópica u otra aplicación localizada, p. ej., para administración al ojo u ojos de un animal de sangre caliente para tratar una respuesta 20 inflamatoria oftálmica; a la mucosa nasal de un animal de sangre caliente para tratar una respuesta inflamatoria nasal; por inhalación oral a un animal de sangre caliente para tratar una respuesta inflamatoria asmática; a la mucosa rectal de un animal de sangre caliente para tratar 25 la inflamación del intestino grueso o el intestino delgado, o del recto; oralmente a un animal de sangre caliente para tratar una respuesta inflamatoria de los intestinos grueso o delgado; al oído u oídos de un animal de sangre caliente para tratar una respuesta inflamatoria ótica; por inyección 30 a la articulación o articulaciones de un animal de sangre caliente para tratar una respuesta artrítica; a la piel de un animal de sangre caliente para tratar una respuesta
inflamatoria dérmica; u oralmente a un animal de sangre caliente para tratar una respuesta inflamatoria oral, gingival o de garganta.
12. Uso de una combinación según una cualquiera de las reivindicaciones 1 a 5 o una composición según una 5 cualquiera de las reivindicaciones 6 a 9 en la preparación de un medicamento para tratar la inflamación tópica u otra inflamación localizada, p. ej., para administración al ojo u ojos de un animal de sangre caliente para tratar una respuesta inflamatoria oftálmica; a la mucosa nasal de un 10 animal de sangre caliente para tratar una respuesta inflamatoria nasal; por inhalación oral a un animal de sangre caliente para tratar una respuesta inflamatoria asmática; a la mucosa rectal de un animal de sangre caliente para tratar la inflamación del intestino grueso o 15 el intestino delgado, o del recto; oralmente a un animal de sangre caliente para tratar una respuesta inflamatoria de los intestinos grueso o delgado; al oído u oídos de un animal de sangre caliente para tratar una respuesta inflamatoria ótica; por inyección a la articulación o 20 articulaciones de un animal de sangre caliente para tratar una respuesta artrítica; a la piel de un animal de sangre caliente para tratar una respuesta inflamatoria dérmica; u oralmente a un animal de sangre caliente para tratar una respuesta inflamatoria oral, gingival o de garganta. 25
13. Uso de una composición según la reivindicación 10 en la preparación de un medicamento para tratar la inflamación dérmica.
14. Uso de:
(a) un compuesto que tiene la fórmula: 30
en la que:
Z1 es carbonilo, p-hidroximetileno o metileno;
R2 es H, -OH o -OCOR3 donde R3 es alquilo C1-C5;
Y es -OH, -SH o -OCOR4, donde R4 es alquilo C1-C5, 5 ciclopentiletilo o dietilaminometilo;
y la línea punteada es como se define a continuación; o
(b) un compuesto de fórmula (II) según se ha definido en la reivindicación 5,
en la preparación de un medicamento para potenciar la 10 actividad antiinflamatoria tópica o local o la duración de la acción, o ambas, de:
(i) un compuesto que tiene la fórmula:
en la que: 15
R1 es alquilo C1-C7;
Z es carbonilo o β-hidroximetileno;
X es Cl o F;
y la línea punteada en el anillo A indica que la unión 1,2 está saturada o insaturada; o
(ii) un compuesto de fórmula (I) según se ha definido en la reivindicación 2 o en la reivindicación 4,
después de la administración tópica u otra administración 5 local de dicho compuesto a un animal de sangre caliente que necesita tratamiento para aliviar una respuesta inflamatoria tópica u otra respuesta inflamatoria localizada;
donde la cantidad de compuesto de fórmula (II) en dicho 10 medicamento es sinérgica y suficiente para potenciar la actividad antiinflamatoria o la duración de la acción, o ambas, de dicho compuesto de fórmula (I), pero insuficiente sola para tener actividad antiinflamatoria; donde la relación molar del compuesto de fórmula (II) al compuesto 15 de fórmula (I) es opcionalmente entre aproximadamente 2:1 y aproximadamente 0,05:1,
con la salvedad que ni el medicamento ni el tratamiento utilizan ningún compuesto de la fórmula:
20
en la que:
R es H o alquilo C1-C4;
Z2 es carbonilo o β-hidroximetileno;
X1 es -O- o -S-;
R5 es -OH, -OR6, -OCOOR6 o -OCOR7 donde R6 es alquilo C1-C4 y 25 R7 es alquilo C1-C4, fluorometilo o clorometilo;
y la línea punteada es como se ha definido anteriormente;
con la salvedad de que cuando R es alquilo C1-C4, entonces R5 es -OH.
15. Un compuesto que tiene la fórmula:
5
en la que:
Z1 es carbonilo, β-hidroximetileno o metileno; R2 es H, -OH o -OCOR3 donde R3 es alquilo C1-C5;
Y es -OH, -SH o -OCOR4, donde R4 es alquilo C1-C5, ciclopentiletilo o dietilaminometilo; y la línea punteada 10 es como se define a continuación;
para uso en potenciar, en una cantidad que sola es insuficiente como para tener actividad antiinflamatoria, la actividad antiinflamatoria tópica u otra actividad antiinflamatoria local o la duración de la acción, o ambas, 15 de un compuesto que tiene la fórmula:
en la que:
R1 es alquilo C1C7;
Z es carbonilo o β-hidroximetileno;
X es Cl o F;
y la línea punteada en el anillo A indica que la unión 1,2-está saturada o insaturada; 5
con la salvedad de que el uso no implica ningún compuesto que tenga la fórmula:
en la que:
R es H o alquilo C1-C4; 10
Z2 es carbonilo o β-hidroximetileno;
X1 es -O- o-S-;
R5 es -OH, -OR6, -OCOOR6 o -OCOR7 donde R6 es alquilo C1-C4 y R7 es alquilo C1-C4, fluorometilo o clorometilo;
y la línea punteada es como se ha definido anteriormente; 15
con la salvedad de que cuando R es alquilo C1-C4, entonces R5 es -OH.
Patentes similares o relacionadas:
Preparado de rocuronio que causa menos dolor vascular, método para producirlo y método para reducir y/o aliviar el dolor vascular al usarlo, del 8 de Abril de 2020, de MARUISHI PHARMACEUTICAL CO., LTD.: Un preparado de rocuronio que contiene rocuronio y una solución tampón y que tiene una acidez químicamente valorable de 100 mEq o menos y un pH de 2,5 a 4,5, con la condición […]
Sistema de administración de fármacos por vía transmucosa oral, del 1 de Abril de 2020, de Abon Pharmaceuticals, LLC: Una forma de dosificación transmucosa oral que comprende (a) un vehículo primario monofásico que comprende (i) un agente de inhibición […]
Formulaciones de 15-hidroxiestearato de macrogol, del 25 de Diciembre de 2019, de ALLERGAN, INC.: Composición oftálmica que comprende un principio activo farmacéutico en una cantidad suficiente para contribuir al tratamiento, la prevención o reducción […]
Formulaciones estables de undecanoato de testosterona, del 24 de Julio de 2019, de Merck Sharp & Dohme B.V: Una formulación farmacéutica que comprende: undecanoato de testosterona; propilenglicol, aceite de ricino polietoxilado, monocaprilato de propilenglicol […]
Modulación terapéutica de la lubricación de la superficie ocular, del 10 de Julio de 2019, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Una composición farmacéutica para el uso en el tratamiento de la deficiencia de lubricación ocular o los síntomas asociados a ella que comprende […]
Formulaciones de testosterona, del 12 de Junio de 2019, de FERRING B.V.: Una formulación transdérmica que comprende: - el 2% en peso de testosterona, - alcanol de C2 a C4, - el 20,0% en peso de propilenglicol, […]
Combinaciones farmacéuticas que comprenden testosterona y tadalafilo en el tratamiento de la disfunción sexual femenina, del 5 de Junio de 2019, de EB IP Lybrido B.V: Uso de una combinación de testosterona o un análogo de la misma que tenga el mismo tipo de actividad y tadalafilo, en la preparación de un medicamento […]
Compuesto esteroideo para su uso en el tratamiento de encefalopatía hepática, del 29 de Mayo de 2019, de Umecrine Cognition AB: El compuesto oxima de 3α-etinil-3ß-hidroxiandrostan-17-ona**Fórmula** o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento de encefalopatía […]