POLIMERO BIOCOMPATIBLE.
Composición polímera biocompatible para un artículo que tiene una superficie destinada a quedar en contacto con sangre,
tejido, piel, capas epiteliales, heridas, células en fluidos de cultivo, fluidos corporales, fluidos de diálisis y/o fluidos terapéuticos para remoción o infusión, caracterizada por el hecho de que la composición polímera comprende un complejo de bismuto incorporado a la composición polímera en una cantidad que corresponde a un porcentaje de un 0,002 a un 0,08% en peso de bismuto con respecto a la composición polímera
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/SE2004/000804.
Solicitante: GAMBRO LUNDIA AB.
Nacionalidad solicitante: Suecia.
Dirección: BOX 10101,220 10 LUND.
Inventor/es: BECK, WERNER, DEPPISCH,REINHOLD, WITTNER,BERND, DIETRICH,RUTH, SCHNELL,ANDREA.
Fecha de Publicación: .
Fecha Concesión Europea: 21 de Julio de 2010.
Clasificación PCT:
- A61L27/34 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › Materiales macromoleculares.
- A61L28/00 A61L […] › Materiales para dispositivos de colostomía (adhesivos para dispositivos de colostomía A61L 24/00).
- A61L29/08 A61L […] › A61L 29/00 Materiales para catéteres o para su revestimiento (forma o estructura de los catéteres A61M 25/00). › Materiales para revestimientos.
- A61L31/10 A61L […] › A61L 31/00 Materiales para otros artículos quirúrgicos. › Materiales macromoleculares.
Clasificación antigua:
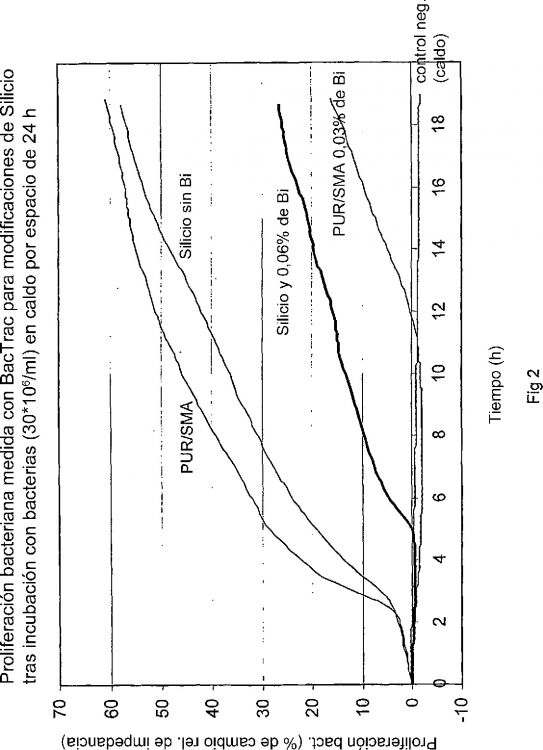
Fragmento de la descripción:
Polímero biocompatible.
Ámbito técnico de la invención
La presente invención se refiere a una composición polímera biocompatible para un artículo que tiene una superficie destinada a establecer contacto con sangre, tejido, piel, capas epiteliales, heridas, células en fluidos de cultivo, fluidos corporales, fluidos de diálisis y/o fluidos terapéuticos para remoción o infusión.
La invención también se refiere a un método para la preparación de la susodicha composición polímera biocompatible, a un artículo que comprende la composición polímera biocompatible y a un uso de la misma.
Antecedentes de la técnica
Muchos de los dispositivos médicos que se usan en contacto con sangre, tejido, piel, capas epiteliales, heridas, células en fluidos de cultivo, fluidos corporales, fluidos de diálisis y/o fluidos terapéuticos para remoción o infusión están hechos de materiales que no son biocompatibles. Así, en muchos sistemas los materiales generan reacciones adversas en el contexto de aplicación en el respectivo sistema biológico. Son distintos tipos de aplicación p. ej. la aplicación transcutánea, en la cavidad peritoneal, para tener acceso al sistema vascular o en líneas en las que se preparan fluidos de diálisis.
La falta de biocompatabilidad puede conducir a coagulación de la sangre, así como a inflamación y activación tisular, y adicionalmente puede establecerse infección microbiana en la superficie de los dispositivos. La colonización de bacterias y la formación de biopelículas sobre las superficies constituyen un problema médico básico. Los dispositivos que están destinados a quedar en contacto a largo plazo, como p. ej. dispositivos tales como stents implantados, sistemas de drenaje de fluidos corporales o catéteres residentes pueden servir de superficie para la adherencia de células huéspedes, permitiendo así que las células huéspedes lleguen a activarse, proliferen o alteren la función fisiológica normal y opongan resistencia a la función de un dispositivo o al uso previsto para el mismo. La formación de biopelículas o la colonización bacteriana sobre las superficies de los dispositivos médicos crea una situación inflamatoria crónica, lo cual da finalmente lugar al inicio del fallo del dispositivo y a que sean necesarias serias intervenciones médicas, o incluso a que se den situaciones que constituyen una amenaza para la vida.
La importancia de la actividad antimicrobiana y de la prevención de la formación de coágulos, p. ej. en un catéter, ha sido dada a conocer en un informe de Wang et al., "Staphylococcus Epidermis Adhesion to Hydrophobic Biomedical Polymer is Mediated by Platelets", J. of Infectious Diseases, 1993, 167:329-36, donde se describe una fuerte relación entre la deposición de plaquetas y la promoción del crecimiento bacteriano.
La GB-1 041 058 publica una composición y un método para proteger materiales contra el ataque de hongos o bacterias, donde un compuesto de bismuto es aplicado a una superficie, p. ej. mediante pulverización o aplicación de un postizo, o bien es incorporado al material a proteger durante la fabricación del mismo. El compuesto de bismuto se usa en aplicaciones con textiles, pinturas y desinfectantes, o bien para proteger a las plantas contra el ataque de hongos y otros microorganismos.
En la US-A-5 958 671 se da a conocer una serie de sales de bismuto que tienen actividad bactericida y bacteriostática para uso farmacológico, como agentes antisépticos, antimicrobianos y antibacterianos para impedir la infección y para la desinfección y la limpieza de superficies, como conservantes y para matar los organismos de las biopelículas e impedir la formación de biopelículas. La composición también se usa para tratar infecciones bacterianas del tracto gastrointestinal.
Una serie de complejos de bismuto, como p. ej. bismuto-propanoditiol o bismuto-piridiona, que tienen propiedades antimicrobianas y de inhibición de la formación de biopelículas, ha sido descrita por Domenico et al., "The potencial of bismuth-thiols for tretatment and prevention of Infection", Infect. Med., 17(2):123-127, 2000. Se propone el uso de dichos complejos para el recubrimiento de catéteres residentes, p. ej. Además, Domenico et al. han tratado acerca de las "Activities of bismuth thiols against Staphylococci and Staphylococcal biofilms", Antimicrobial Agents and Cemotherapy, May 2001, p. 1417-1421.
La WO 00/21585 publica policaprolactona, PDMS, como parte de una película polimérica mediante la adición de un componente adicional que ejerce actividad antimicrobiana y mantiene el perfil de alta biocompatibilidad del recubrimiento (ausencia de citotoxicidad, trombogenicidad mejorada y reducida promoción del crecimiento bacteriano).
La US-A-6.267.782 se refiere a una mezcla de una composición metálica y un material biocompatible en una solución para la preparación de un artículo médico que comprende metal antimicrobiano. El material biocompatible puede comprender un polímero biológico y el metal puede ser una composición de bismuto. Sin embargo, la composición metálica es depositada sobre la superficie del artículo, lo cual redunda en una liberación de bismuto desde el artículo.
La prevención de las infecciones derivadas de accesos a la sangre, p. ej. en catéteres, es de gran importancia desde la perspectiva de sanidad pública, es decir al aumentar la resistencia de las bacterias contra las estrategias antibióticas y con respecto a los costes relacionados con el posterior tratamiento médico tras infecciones de la corriente sanguínea y complicaciones sépticas. Por ejemplo, las infecciones de la corriente sanguínea relacionadas con los catéteres intravasculares son una importante causa de enfermedad y excesivos costes médicos. Muchas infecciones de la corriente sanguínea relacionadas con los catéteres se producen en unidades de cuidados intensivos a costa de muchas muertes y de altos costes.
Por consiguiente se han desarrollado muchas estrategias para impedir estas complicaciones. Como describen Donlan et al., ``Biofilms and Device-associated Infections, Emerging Infectious Diseases, 89, Vol. 7, Nº 2, marzo-abril, 2001, las de la mayoría de estas estrategias para impregnar materiales poliméricos p. ej. con plata u otros aditivos o incluso con antibióticos, redundan en un ineficaz control del crecimiento bacteriano y de la formación de biopelículas.
Está descrito por Mermel et al., "New Technologies to Prevent Intravascular Catheter Related Bloodstream Infections", Emerging Infectious Diseases, Vol. 7, Nº 2, marzo-abril, 2001, que no son eficaces las intervenciones tecnológicas en las que se impregnan materiales de catéteres con distintas clases de agentes bacterianos. Estudios in vitro han sugerido el potencial de resistencia bacteriana contra los agentes antimicrobianos que se usan para impregnar estos catéteres al ir extendiéndose más su uso clínico. Además de éstos, muy a menudo ayudan a reducir las infecciones relacionadas con los catéteres intervenciones no tecnológicas tales como el adiestramiento del personal de enfermería y el uso de ambientes estériles por medio de la utilización de máscaras estériles, ropas estériles, etc.
Sin embargo, en la actualidad no está disponible solución técnica alguna que impida en el sitio del catéter la formación de biopelículas por adherencia y proliferación bacteriana. De acuerdo con los conocimientos que figuran en los libros de texto farmacéuticos, en la práctica médica y/o farmacéutica se usan muchos compuestos de bismuto, como p. ej. carbonato de bismuto, nitrato de bismuto, citrato de bismuto y salicilato de bismuto. Las correspondientes formulaciones farmacológicas son conocidas como Angass-S-Ulcowics, Bismoflk-V, Jadrox-600, Ulcolind, etc. Las sales de bismuto y los bismuto-tioles son activos contra un amplio espectro de bacterias. La concentración inhibitoria está situada dentro de la gama de valores que va de 3 a 300 µmoles de bismuto-3+. Las de la mayoría de las cepas bacterianas conocidas son susceptibles a los compuestos de bismuto, y es importante observar que los mismos son sumamente eficaces contra Staphylococcus Aureus, incluyendo a la especie Staphylococcus Aureus resistente a la meticilina (MRSA) (Dominico et al.).
El principal problema es el de que los compuestos de bismuto, y especialmente los bismuto-tioles, son potencialmente tóxicos. No está completamente claro el mecanismo en virtud del cual el bismuto trabaja para impedir la proliferación bacteriana. Se demostró recientemente que el Bis-BAL...
Reivindicaciones:
1. Composición polímera biocompatible para un artículo que tiene una superficie destinada a quedar en contacto con sangre, tejido, piel, capas epiteliales, heridas, células en fluidos de cultivo, fluidos corporales, fluidos de diálisis y/o fluidos terapéuticos para remoción o infusión, caracterizada por el hecho de que la composición polímera comprende un complejo de bismuto incorporado a la composición polímera en una cantidad que corresponde a un porcentaje de un 0,002 a un 0,08% en peso de bismuto con respecto a la composición polímera.
2. Composición polímera biocompatible según la reivindicación 1, caracterizada por el hecho de que dicha composición polímera comprende adicionalmente nanopartículas que incluyen un complejo de bismuto.
3. Composición polímera biocompatible según la reivindicación 1 o 2, caracterizada por el hecho de que el complejo de bismuto se elige de entre los miembros del grupo que consta de citrato de bismuto y amonio, óxido de bismuto (III), hidrato de galato de bismuto (III), citrato de bismuto, oxicloruro de bismuto (III), tetrametilheptanodionato de bismuto (III), hexafluoroacetonato de bismuto (III), subsalicilato de bismuto (III), trifenilbismuto, bismuto (III) ciprofloxacina, cloruro de bismuto (III), dicloruro de trifenilbismuto, carbonato de trifenilbismuto, dihidróxido de trifenilbismuto, dinitrato de trifenilbismuto, disalicilato de trifenilbismuto, trifenilbismutina, bis(2-cloroacetoato) de trifenilbismuto, bis(4-aminobenzoato) de trifenilbismuto, bis(acetato-O) trifenilbismuto, dibromotrifenilbismuto y difluorotrifenilbismuto.
4. Composición polímera biocompatible según la reivindicación 1 o 2, caracterizada por el hecho de que el complejo de bismuto es trifenilbismuto o dicloruro de trifenilbismuto, y preferiblemente dicloruro de trifenilbismuto.
5. Composición polímera biocompatible según cualquiera de las reivindicaciones 1-3, caracterizada por el hecho de que la composición polímera comprende un componente polímero peliculígeno.
6. Composición polímera biocompatible según la reivindicación 5, caracterizada por el hecho de que el polímero peliculígeno es un polímero de siloxano y/o un oligómero de siloxano.
7. Composición polímera biocompatible según la reivindicación 5, caracterizada por el hecho de que la composición polímera comprende adicionalmente un bloque de polímero hidrofóbico que tiene grupos extremos reactivos.
8. Composición polímera biocompatible según la reivindicación 7, caracterizada por el hecho de que el polímero peliculígeno se selecciona de entre los miembros del grupo que consta de poliuretanos, poliolefinas, elastómeros, polietilenglicoles, policarbonatos, polietersulfonas, polisulfonas, polivinilpirrolidonas y cloruros de polivinilo, y el bloque hidrofóbico se selecciona de entre los miembros del grupo que consta de polímeros de siloxano, oligómeros de siloxano, fluoropolímeros, polietilenglicoles, copolímeros de polietilenglicol-polidimetilsiloxano, poliésteres de silicona y copolímeros tribloque de polilactona, polisiloxano-polilactona.
9. Composición polímera biocompatible según la reivindicación 8, caracterizada por el hecho de que el polímero peliculígeno es un poliuretano y el bloque de polímero hidrofóbico es un copolímero tribloque de polilactona-polisiloxano-polilactona que contiene mono-, bi- o múltiples grupos extremos reactivos.
10. Método para la preparación de una composición copolímera biocompatible, caracterizado por el hecho de que se incorpora a la composición polímera un complejo de bismuto en una cantidad que corresponde a un porcentaje de un 0,002 a un 0,08% en peso de bismuto con respecto a la composición polímera.
11. Método para la preparación de una composición copolímera biocompatible según la reivindicación 10, caracterizado por el hecho de que se incorporan a la composición polímera nanopartículas que contienen un complejo de bismuto.
12. Método para la preparación de una composición copolímera biocompatible según la reivindicación 10 u 11, caracterizado por el hecho de que el complejo de bismuto se elige de entre los miembros del grupo que consta de citrato de bismuto y amonio, óxido de bismuto (III), hidrato de galato de bismuto (III), citrato de bismuto, oxicloruro de bismuto (III), tetrametilheptanodionato de bismuto (III), hexafluoroacetonato de bismuto (III), subsalicilato de bismuto (III), trifenilbismuto, bismuto (III) ciprofloxacina, cloruro de bismuto (III), dicloruro de trifenilbismuto, carbonato de trifenilbismuto, dihidróxido de trifenilbismuto, dinitrato de trifenilbismuto, disalicilato de trifenilbismuto, trifenilbismutina, bis(2-cloroacetoato) de trifenilbismuto, bis(4-aminobenzoato) de trifenilbismuto, bis(acetato-O) trifenilbismuto, dibromotrifenilbismuto y difluorotrifenilbismuto.
13. Método para la preparación de una composición copolímera biocompatible según la reivindicación 10 u 11, caracterizado por el hecho de que el complejo de bismuto es trifenilbismuto o dicloruro de trifenilbismuto, y preferiblemente dicloruro de trifenilbismuto.
14. Método para la preparación de una composición copolímera biocompatible según cualquiera de las reivindicaciones 10-13, caracterizado por los pasos de combinar una composición polímera peliculígena y un complejo de bismuto en presencia de un solvente de forma tal que todos los componentes quedan disueltos en el solvente, incubar los componentes disueltos en el solvente bajo condiciones que permitan a los componentes reaccionar entre sí en solución, y formar una película extendiendo la solución sobre una superficie a recubrir bajo condiciones que permiten que se evapore el solvente.
15. Método para la preparación de una composición copolímera biocompatible según cualquiera de las reivindicaciones 10-14, caracterizado por el hecho de que el polímero peliculígeno es un polímero de siloxano y/o un oligómero de siloxano y el complejo de bismuto es dicloruro de trifenilbismuto.
16. Método para la preparación de una composición copolímera biocompatible según cualquiera de las reivindicaciones 10-13, caracterizado por los pasos de combinar una composición polímera peliculígena y un complejo de bismuto con un bloque de polímero hidrofóbico que tiene grupos extremos que reaccionan con el componente polímero peliculígeno en presencia de un disolvente de forma tal que todos los componentes quedan disueltos en el solvente, incubar los componentes disueltos en el solvente bajo condiciones que permiten a los componentes reaccionar entre sí en solución, y formar una película extendiendo la solución sobre una superficie a recubrir bajo condiciones que permiten que se evapore el disolvente.
17. Método para la preparación de una composición copolímera biocompatible según cualquiera de las reivindicaciones 10-13 y 16, caracterizado por el hecho de que el polímero peliculígeno es un poliuretano, el complejo de bismuto es dicloruro de trifenilbismuto y el bloque de polímero hidrofóbico es un copolímero tribloque de polilactona-polisiloxano-polilactona que contiene mono-, bi- o múltiples grupos extremos reactivos.
18. Artículo que tiene una superficie destinada a quedar en contacto con sangre, tejido, piel, capas epiteliales, heridas, células en fluidos de cultivo, fluidos corporales, fluidos de diálisis y/o fluidos terapéuticos para remoción o infusión, caracterizado por el hecho de que dicho artículo tiene al menos una película de una composición polímera que comprende un complejo de bismuto en una cantidad que corresponde a un porcentaje de un 0,002 a un 0,08% en peso de bismuto con respecto a la composición polímera, cubriendo dicha superficie.
19. Artículo según la reivindicación 18, caracterizado por el hecho de que dicho artículo tiene un recubrimiento multicapa de dicha composición polímera
20. Artículo según la reivindicación 18, caracterizado por el hecho de que dicho artículo tiene un recubrimiento de dicha composición polímera, y de que dicha composición polímera adicionalmente incluye nanopartículas que incluyen un complejo de bismuto.
21. Artículo según la reivindicación 20, caracterizado por el hecho de que dicha composición polímera comprende un componente polímero peliculígeno.
22. Artículo según la reivindicación 21, caracterizado por el hecho de que el polímero peliculígeno es un polímero de siloxano y/o un oligómero de siloxano.
23. Artículo según la reivindicación 21, caracterizado por el hecho de que dicha composición polímera adicionalmente comprende un bloque de polímero hidrofóbico que tiene uno o varios grupos extremos reactivos.
24. Artículo según la reivindicación 23, caracterizado por el hecho de que el polímero peliculígeno se selecciona de entre los miembros del grupo que consta de poliuretanos, poliolefinas, elastómeros, polietilenglicoles, policarbonatos, polietersulfonas, polisulfonas, polivinilpirrolidonas y cloruros de polivinilo, y el bloque hidrofóbico se selecciona de entre los miembros del grupo que consta de polímeros de siloxano, oligómeros de siloxano, fluoropolímeros, polietilenglicoles, copolímeros de polietilenglicol-polidimetilsiloxano, poliésteres de silicona y copolímeros tribloque de polilactona-polisilixano-polilactona.
25. Artículo según la reivindicación 24, caracterizado por el hecho de que el polímero peliculígeno es un poliuretano y el bloque de polímero hidrofóbico es un copolímero tribloque de polilactona-polisiloxano-polilactona que contiene mono-, bi- o múltiples grupos extremos reactivos.
26. Uso de una composición polímera biocompatible según la reivindicación 1 para un dispositivo médico destinado a quedar en contacto con sangre, tejido, tejido con heridas, células en fluidos de cultivo, fluidos corporales, fluidos de diálisis o fluidos terapéuticos para remoción o infusión a fin de acrecentar la biocompatibilidad e impedir el crecimiento bacteriano.
27. Uso de una composición polímera biocompatible según la reivindicación 1 sobre superficies en contacto con sangre, tejido, piel, capas epiteliales, heridas, células en fluidos de cultivo, fluidos corporales, fluidos de diálisis y/o fluidos terapéuticos para remoción o infusión.
28. Composición polímera biocompatible según la reivindicación 9, caracterizada por el hecho de que la liberación de bismuto desde dicha composición polímera a una solución acuosa es de menos de un 0,05% de la cantidad total de bismuto contenida en la composición polímera.
29. Artículo según la reivindicación 18, donde la película, que es al menos una, consta de una composición polímera biocompatible según la reivindicación 9, caracterizado por el hecho de que la liberación de bismuto desde la película que es al menos una a una solución acuosa es de menos de un 0,05% de la cantidad total de bismuto contenida en la composición polímera.
Patentes similares o relacionadas:
Películas de proteína de múltiples capas, métodos de preparación y dispositivos de suministro de fármacos e implantes biomédicos que emplean las películas, del 15 de Julio de 2020, de AddBIO AB: Un implante biomédico que comprende un sustrato de implante y una película de proteína de múltiples capas en al menos una porción de la superficie del sustrato de implante, […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composiciones y métodos para el tratamiento de huecos óseos y fracturas abiertas, del 22 de Abril de 2020, de Polypid Ltd: Una composición farmacéutica que comprende partículas de relleno óseo recubiertas y no recubiertas en una proporción entre aproximadamente 1:3 […]
Procedimiento de injerto de polímeros bioactivos sobre unos materiales metálicos, del 11 de Marzo de 2020, de Univ Paris XIII Paris-Nord Villetaneuse: Procedimiento de injerto directo de polímeros bioactivos sobre un material metálico protético de titanio o de aleación de titanio, que comprende las etapas siguientes: […]
Dispositivos médicos con trombogenicidad reducida, del 4 de Marzo de 2020, de Heart Research Institute Ltd: Un dispositivo médico vascular que comprende una superficie, que consiste en un polihexano o un poliacetileno biocompatibles polimerizados con plasma, […]
Emulsiones de copolímero de politetrafluoroetileno, del 12 de Febrero de 2020, de W.L. GORE & ASSOCIATES, INC.: Un método de preparación de una emulsión de agua en disolvente que comprende un copolímero de tetrafluoroetileno disuelto en un disolvente orgánico miscible […]
Revestimiento para una superficie, del 15 de Enero de 2020, de W.L. GORE & ASSOCIATES, INC.: Una superficie que tiene un revestimiento que comprende una mezcla de componentes A y B, en donde el componente A es un polímero formado mediante autopolimerización de una molécula […]
Administración inyectable de micropartículas y composiciones para ello, del 25 de Diciembre de 2019, de TEPHA, INC.: Un kit que comprende una composición inyectable de micropartículas que comprende una población de micropartículas, en donde las micropartículas comprenden […]