Procedimiento para la preparación de derivados de 1,1,2-trialquil-1H-indeno a partir de derivados de 2-(1,1,2-trialquil-3-oxopropil)benzaldehído.
Procedimiento para la preparación de derivados de 2-alquil-1H-indeno y 2,
3,4,4a-tetrahidro-1H-fluoreno a partir de derivados de 2-(2-alquil-3-oxopropil)benzaldehido y 2-(2-formilciclohexil)benzaldehido, respectivamente.
La presente invención describe un procedimiento para la preparación de derivados de 2-alquil-1H-indeno y de 2,3,4,4a-tetrahidro-1H-fluoreno, mediante tratamiento ácido de derivados de 2-(2-alquil-3-oxopropil)benzaldehído y 2-(2-formilciclohexil)benzaldehído, respectivamente.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201531158.
Solicitante: UNIVERSIDAD DE GRANADA.
Nacionalidad solicitante: España.
Inventor/es: ALVAREZ DE MANZANEDA ROLDAN,ENRIQUE, GUARDIA MONTEAGUDO,Juan José, CHANHBOUN KARIMI,Rachid.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C13/465 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 13/00 Hidrocarburos cíclicos conteniendo ciclos distintos a ciclos aromáticos de seis miembros, con o sin ciclos aromáticos de seis miembros. › Indenos; Indenos completamente o parcialmente hidrogenados.
- C07C13/567 C07C 13/00 […] › Fluorenos; Fluorenos completa o parcialmente hidrogenados.
- C07C4/18 C07C […] › C07C 4/00 Preparación de hidrocarburos a partir de hidrocarbonos que tienen mayor número de átomos de carbono. › Procesos catalíticos.
- C07C47/542 C07C […] › C07C 47/00 Compuestos que tienen grupos —CHO. › Benzaldehídos alquilados.
- C07C47/546 C07C 47/00 […] › policíclicos.
PDF original: ES-2547027_A1.pdf
Fragmento de la descripción:
PROCEDIMIENTO PARA LA PREPARACIÓN DE DERIVADOS DE 1,1,2- TRIALQUIL-1H-INDENO A PARTIR DE DERIVADOS DE 2-(1,1,2- TRIALQUIL-3-OXOPROPIL)BENZALDEHÍDO
CAMPO DE LA INVENCIÓN
La presente invención se encuadra dentro del campo de la sintesis orgánica, en particular, de compuestos con esqueleto de 1,1,2-trialquil-lií-indeno, a partir de derivados de 2-(1,1,2-trialquil-3-oxopropil)benzaldehido.
ANTECEDENTES DE LA INVENCIÓN
Se han descrito diversos procedimientos para la preparación de derivados de lií-indeno, siendo los más habituales aquellos que implican reacciones de acilación de Friedel-
| Crafts intramoleculares | [I. | Masao | et | al. 2 010, J. Chem. | ||
| Res. 325 | y referencias | que | alli | se | citan], | procesos de |
| delación | de o-alil | bencil | haluros y | compuestos |
relacionados, catalizados por Pd [G.-Z. Wu et al. 1989, J. Org. Chem. 54, 2507] y reacciones intramoleculares de
alquiliden carbenoides con aril carbaniones [H. Yanagisawa et al. 2003, Bull. Chem. Soc. Jpn. 76, 2009]. Más
recientemente se han descrito procesos de delación de 2- alquinil-arilepóxidos, catalizados por rutenio [L. Ming- Yuan et al. 2004, J. Org. Chem. 69, 7700].
**(Ver fórmula)** **(Ver fórmula)**1,2,2-tr¡alquil-1 H-indeno 4a-metil-2,3,4,4a-tetrahidro-1 H-fluoreno
La unidad de 1,1,2-trialquil-lií-indeno forma parte del fragmento de 4a-metil-2,3,4,4a-tetrahidro-lií-fluoreno,
presente en algunos terpenoides de gran interés, como los taiwaniaquinoides. Estos son un grupo de terpenoides que presentan un poco usual esqueleto reordenado 5 (6-^7) o 6-
nor-5 (6-^7) abeo-abietano, que han sido aislados de algunas especies de coniferas del Este de Asia, tales como Taíwania cryptomerioid.es, y poseen una prometedora actividad biológica [para un reciente review, ver G. Majetich et al.
2010, J. Nat. Prod. 73, 284]. Estos compuestos poseen un
anillo fenólico o quinónico, y un esqueleto de 4a- metiltetrahidrofluoreno, como taiwaniaquinona D (1) [W. Lin
et al. 1996, Phytochemistry 42, 1657], H (2)[C.-I. Chang et al. 2005, Planta Med. 71, 72], dicroanona (3) o dicroanal
B(4) [ K. Kawazoe et al. 1999, Phytochemistry, 50, 493].
También los hay con esqueleto de 4a-metilhexahidrofluoreno, y unión A/B cis, como taiwaniaquinol B (5) [W. Lin et al. 1995, Phytochemistry 40, 871] o dicroanal A (6)[K. Kawazoe
et al. 1999, Phytochemistry, 50, 493],y con unión A/B 15 trans, como taiwaniaquinona A (7) [W. Lin et al. 1995,
Phytochemistry 40, 871], F (8)[C. Chang et al., 2003, Chem. Pharm. Bull. 51, 1420] y G (9) [C.-I. Chang et al. 2005,
Planta Med. 71, 72].
**(Ver fórmula)** **(Ver fórmula)** **(Ver fórmula)**2 R: H
3 R: Me
**(Ver fórmula)** **(Ver fórmula)** **(Ver fórmula)**7 R: H; R': CHO
8 R: Me; R': CHO
9 R: Me; R': H
La novedosa estructura de este tipo de compuestos y la prometedora actividad biológica que exhiben algunos de
ellos ha motivado el desarrollo de métodos de síntesis por parte de diversos grupos. La aproximación AC-ABC es normalmente la estrategia más empleada. La construcción del esqueleto de 4a-metiltetra- (o 4-metilhexa-) fluoreno implica usualmente la utilización de un sintón
monoterpénico, como p-ciclocitral o ácido ciclogeránico, junto con un derivado fenólico. En otros casos, la elaboración del esqueleto de 4a-metiltetra (o hexa) hidro- líT-fluoreno de los taiwaniaquinoides se ha realizado mediante la contracción del anillo B de un sistema
tricíclico 6-6-6 ABC. Se han utilizado tres estrategias para lograr este propósito: 1) Un proceso en cascada que implica un reordenamiento del ácido bencílico / descarboxilación [K. Gademann et al. 2010, Chem. Eur. J. 16, 7692]; 2) La apertura y posterior cierre del anillo B
mediante ozonolisis / condensación aldólica [M. Node et al. 2007, Bioorg. Med. Chem. 15, 2736; E. Alvarez-Manzaneda et
al. 2010, Chem. Commun. 46, 9244; 2012, J. Org. Chem. 77, 573] y 3) Un reordenamiento de Wolff de la adecuada a- diazocetona [K. Gademann et al. 2013, Org. Lett. 15, 1390;
A. Li et al. 2013, Org. Lett. 15, 2022].
La mayoría de los procedimientos conocidos en el estado de la técnica para la síntesis de este tipo de compuestos comprenden numerosas etapas de reacción, y por ello sus costes son elevados, los rendimientos obtenidos totales son bajos, y no resultan de interés para ser llevados a escala industrial y comercial.
Por lo tanto, existe la necesidad en el estado de la técnica de proporcionar métodos de síntesis alternativos, que superen al menos parte de las desventajas de los procedimientos del estado de la técnica.
OBJETO DE LA INVENCIÓN
Para superar las desventajas de los procedimientos
conocidos, la presente invención permite obtener compuestos con estructura de 1,1,2-trialquil-lff-indeno a partir de derivados de 2-(1,1,2-trialquil-3-oxopropil)benzaldehido, mediante un nuevo y sencillo procedimiento que comprende una condensación aldólica intramolecular y el posterior reordenamiento del hemiacetal derivado del correspondiente aldol, con pérdida de ácido fórmico. Este nuevo
procedimiento permite disminuir el número de etapas de sintesis, su coste, asi como aumentar el rendimiento en producto final.
También son objeto de la invención los intermedios de sintes is (14) y (20).
DESCRIPCIÓN DE LA INVENCIÓN
La presente invención se refiere a un nuevo procedimiento de preparación de compuestos con estructura de 1,1,2- trialquil-lü-indeno a partir de derivados de 2(1,1,2 trialquil-3-oxopropil)benzaldehido.
El procedimiento, en adelante "procedimiento de la
invención", comprende la transformación de un derivado de 2 - (1,1,2-trialquil-3-oxopropil)benzaldehido (compuesto
inicial) mediante tratamiento en condiciones ácidas para obtener un compuesto con estructura 1, 1,2-trialquil-lü- indeno (compuesto final). Con este tratamiento en
condiciones ácidas se consigue someter a los compuestos de partida a una condensación aldólica intramolecular y posteriormente, al reordenamiento del hemiacetal derivado del correspondiente aldol.
En particular, el tratamiento en condiciones ácidas se lleva a cabo a partir de una disolución del correspondiente compuesto inicial en un disolvente inerte, que se trata con un ácido orgánico, inorgánico o resina catiónica.
El disolvente inerte puede ser un disolvente seleccionado del grupo formado por tolueno, xileno, dimetilformamida, diclorometano y cloroformo.
El tratamiento se realiza a temperatura superior a 20°C, preferentemente a una temperatura entre 25°C y la temperatura de ebullición del disolvente empleado.
En dos realizaciones particulares, el procedimiento de la invención comprende preparar un compuesto de fórmula general 10 o un compuesto de fórmula general 11,
**(Ver fórmula)**mediante tratamiento en condiciones ácidas de un dialdehido de fórmula general 12 o de fórmula general 13, respectivamente.
**(Ver fórmula)** **(Ver fórmula)**donde Ri, R2 y R3 representa un grupo seleccionado de entre - R, -CH20R, -COR,-COOH, -COOR, -CONR2, donde -R representa un hidrógeno o un grupo alquilo C1-C4 lineal o ramificado, o
arilo,
donde R4, R5, R6 y R7 representan independientemente un grupo seleccionado de entre H, -R, -CHO, -COR, -CN, -COOH, -COOR, -CONR2,-CF3, -CH2OH, -CH2CI, -CH2NR2, -CH2COOH, -ch=ch2, halógeno,-N02, -NR2, -OR,-S02R, donde -R representa un
hidrógeno o un grupo alquilo C1-C4 lineal o ramificado, o arilo.
En una realización particular, la transformación de los compuestos 12 o 13 en los derivados 10 o 11, respectivamente, comprende el tratamiento de una disolución del correspondiente dialdehido 12 o 13 en un disolvente inerte, tal como por ejemplo tolueno, xileno,
dimetilformamida, diclorometano o cloroformo, con un ácido orgánico, inorgánico o resina catiónica, a temperatura ambiente o en caliente.
En una realización particular, el procedimiento permite preparar derivados de 7-isopropil-l,1,4a-trimetil-2,3, 4,4a- tetrahidro-lH-fluoreno (30) , relacionados estructuralmente con taiwaniaquinoides, a partir de derivados de 2-(2- formil-1,3,3-trimetilciclohexil)-5-isopropilbenzaldehido (31).
**(Ver fórmula)**MODOS DE REALIZACIÓN
A continuación se describen algunos casos particulares... [Seguir leyendo]
Reivindicaciones:
1.- Procedimiento de obtención de compuestos con estructura
de 1,1,2-trialquil-lH-indeno mediante tratamiento en
condiciones ácidas de derivados de 2-(1,1,2-trialquil-3- oxopropil)benzaldehido.
2.- Procedimiento según reivindicación anterior
caracterizado porque el tratamiento en condiciones ácidas se lleva a cabo a partir de una disolución del derivados de un derivado de 2-(1,1,2-trialquil-3-oxopropil)benzaldehido en un disolvente inerte, que se trata con un ácido orgánico, inorgánico o resina catiónica.
3.- Procedimiento según reivindicación anterior
caracterizado porque el disolvente inerte se selecciona del grupo formado por tolueno, xileno, dimetilformamida,
diclorometano y cloroformo.
4.- Procedimiento según cualquiera de las reivindicaciones anteriores para obtener un compuesto de fórmula general 10
**(Ver fórmula)**mediante tratamiento en condiciones ácidas de un dialdehido de fórmula general 12
**(Ver fórmula)**donde Ri, R2 y R3 representa un grupo seleccionado de entre - R, -CH2OR, -COR,-COOH, -COOR, -CONR2, donde -R representa un hidrógeno o un grupo alquilo C1-C4 lineal o ramificado, o 5 arilo,
donde R4, R5, R6 y R7 representan independientemente un grupo seleccionado de entre H, -R, -CHO, -COR, -CN, -COOH, -COOR, -CONR2,-CF3, -CH2OH, -CH2CI, -CH2NR2, -CH2COOH, -CH=CH2, halógeno,-N02, -NR2, -OR,-S02R, donde -R representa un
hidrógeno o un grupo alquilo C1-C4 lineal o ramificado, o arilo.
5.- Procedimiento según cualquiera de las reivindicaciones 1 a 3 para obtener o un compuesto de fórmula general 11,
**(Ver fórmula)**Re
mediante tratamiento en condiciones ácidas de un dialdehido de fórmula general 13
**(Ver fórmula)**0Ach8ho
Rl R2
donde R2, R2 y R3 representa un grupo seleccionado de entre - R, -CH2OR, -COR,-COOH, -COOR, -CONR2, donde -R representa un hidrógeno o un grupo alquilo C1-C4 lineal o ramificado, o
arilo,
donde R4, R5, R6 y R7 representan independientemente un grupo seleccionado de entre H, -R, -CHO, -COR, -CN, -COOH, -COOR, -CONR2,-CF3, -ch2oh, -ch2ci, -ch2nr2, -ch2cooh, -CH=CH2, halógeno,-N02, -NR2, -OR,-S02R, donde -R representa un
hidrógeno o un grupo alquilo C1-C4 lineal o ramificado, o 10 arilo.
6.- Procedimiento según reivindicación 5 para preparar de derivados de 7-isopropil-l,1,4a-trimetil-2,3,4,4a-
tetrahidro-lH-fluoreno (30)
<
a partir de derivados de 2-(2-formil-l,3,3- trimetilciclohexil)-5-isopropilbenzaldehido (31)
**(Ver fórmula)** **(Ver fórmula)**7.- Compuesto intermedio de fórmula 25
**(Ver fórmula)**donde Ri es Me y R2 es H.
8.- Procedimiento según reivindicación 5 para obtener (R)-
7-Isopropil-1,1,4a-trimetil-2,3,4,4a-tetrahidro-1H-fluoreno (15) a partir de 2-((1S,2S)-2-formil-1,3,3-
trimetilciclohexil)-5-isopropilbenzaldehido (14).
9.- Procedimiento según reivindicación 5 para obtener (R)-
2- Isopropil-4b,8,8-trimetil-5,6,7,8-tetrahidro-4bH-fluoren-
3- ol (17) a partir de 2-((1S,2S)-2-formil-1,3,3- trimetilciclohexil)-4-hidroxi-5-isopropilbenzaldehido(16)
10.- Procedimiento según reivindicación 5 para obtener (R)-7-Isopropil-6-metoxi-1,1,4a-trimetil-2,3,4,4a- tetrahidro-1H-fluoreno (19) a partir de 2-((1S,2S)-2- formil-1,3,3-trimetilciclohexil)-5-isopropil-4- metoxibenzaldehido (18).
11.- Compuesto intermedio de fórmula
**(Ver fórmula)**donde R1 es COOMe y R2 es OMe.
12.- Procedimiento según reivindicación 5 para obtener
(1R,4aR)- 7-Isopropil-6-metoxi-1,4a-dimetil-2,3,4,4a-
tetrahidro-1H-fluoren-1-carboxilato de metilo (21) a partir de (1R,2R,3S)- 2-formil-3-(2-formil-4-isopropil-5-
metoxifenil)-1,3-dimetilciclohexancarboxilato de metilo 10 (20).
OFICINA ESPAÑOLA DE PATENTES Y MARCAS
N.° solicitud:
**(Ver fórmula)**ESPAÑA
Fecha de presentación de la solicitud: 04.08.2015 Fecha de prioridad:
INFORME SOBRE EL ESTADO DE LA TECNICA
(5) int. ci.: Ver Hoja Adicional
DOCUMENTOS RELEVANTES
Categoría
Documentos citados
Reivindicaciones
afectadas
KATOFI, T. et al. "Synthesis of DL-standishinal and its related compounds for the studies on structure-activity relatioship of inhibitory activity against aromatase". Bioorganic & Medicinal Chemistry 2007, Volumen 15, páginas 2736-2748. [Disponible en línea el 20.01.2007].
Ver página 2736, resumen; página 2737, figura 1; página 2739, tablas 1 y 2.
TAHARA, A. et al. "Diterpenoids. XII. Catalytic Hydrogenation of D5,6-and 6-Enol Acetoxy- hydrofluorene Derivatives. A Synthesis of Hydrofluorene Derivatives (cis-A/B-Ring Fusión (a C5- H)). Chemical and Pharmaceutical Bulletin 1969, Volumen 17, Número 1, páginas 68-74.
Ver página 69, cuadro 1.
KAKDE, B.N. et al. "Metal triflate-catalyzed cyclization of arylvinylcarbinols: formal synthesis of (±)-dichroanone and (±)-taiwaniaquinone H". RCS Advances 2013, Volumen 3, páginas 8176-8179. Ver página 8176, resumen; página 8177, tabla 1.
LIAO, X. et al. "Enantioselective Total Syntheses of (-)-Taiwaniaquinone H and (-)-Taiwaniaquinol B by Iridium-Catalyzed Borylation and Palladium-Catalyzed Asymmetric a-Arylation". Journal of the American Chemical Society 2011, Volumen 133, páginas 2088-2091. [Disponible en linea el 26.01.2011], Ver página 2088, resumen; página 2089, esquema 3.
KUMAR JANA, C. et al. "Connecting C19 Norditerpenoids to C2o Diterpenes: Total Syntheses of 6- Hydroxy-5,6-dehydrosugiol, 6-Hidroxysugiol, and Taiwaniaquinone H, and Formal Synthesis of Dichroanone". Synthesis 2010, Número 13, páginas 2223-2232. Ver página 2226, esquema 7, compuesto 28.
TANG, S. et al. "Application of a Domino Friedel-Crafts Acylation/Alkylation Reaction to the Formal Syntheses of (+)-Taiwaniaquinol B and (±)-Dichroanone". Organic Letters 2008,
Volumen 10, Número 9, páginasl 855-1858. [Disponible en línea el 08.04.2008]. Ver página 1857, esquema 3, compuesto 18; esquema 4.
MAJETICH, G. & SHIMKUS, J.M. "The Taiwaniaquinoids: A Review". Journal of Natural Products 2010, Volumen 73, Número 2, páginas 284-298. [Disponible en línea el 26.01.2010].
Ver página 284, figura 1; página 285, figura 2; página 287, esquema 4, compuesto 64.
1-12
1-12
1-12
1-12
1-12
1-12
1-12
Categoría de los documentos citados X: de particular relevancia
Y: de particular relevancia combinado con otro/s de la misma categoría A: refleja el estado de la técnica
O: referido a divulgación no escrita
P: publicado entre la fecha de prioridad y la de presentación de la solicitud
E: documento anterior, pero publicado después de la fecha
| de presentación de la solicitud | ||
| El presente informe ha sido realizado | ||
| IS para todas las reivindicaciones | para las reivindicaciones n°: | |
| Fecha de realización del informe | Examinador | Página |
| 21.09.2015 | G. Esteban García | 1/6 |
Patentes similares o relacionadas:
COMPUESTOS DE LA VITAMINA D CON MARCAJE ISOTÓPICO, del 12 de Marzo de 2020, de UNIVERSIDADE DE SANTIAGO DE COMPOSTELA: Compuestos de la vitamina D con marcaje isotópico. La invención se dirige a compuestos de fórmula I caracterizados por ser derivados de las vitaminas […]
Métodos de economía circular para preparar compuestos insaturados, del 27 de Noviembre de 2019, de INTERNATIONAL FLAVORS & FRAGRANCES INC.: Un método para preparar un compuesto insaturado, que comprende la deshidrogenación de un compuesto saturado correspondiente en presencia […]
Catalizadores, del 6 de Septiembre de 2017, de BOREALIS AG: Complejo racémico de fórmula (I) **(Ver fórmula)** en la que M es circonio o hafnio; cada X es un ligando sigma; L es un puente […]
Amino-1,3,5-triazinas N-sustituidas con radicales bicíclicos quirales, procedimiento para su preparación, composiciones de las mismas y su uso como herbicidas y reguladores del crecimiento de las plantas, del 5 de Marzo de 2014, de BAYER CROPSCIENCE AG: Un compuesto ópticamente activo de fórmula (I),**Fórmula** en la que: R1 es H, halógeno, alquilo (C1-C6), haloalquilo (C1-C6), [alcoxi (C1-C4)]alquilo (C1-C4), […]
COMPUESTOS QUIRALES, PROCEDIMIENTOS DE OBTENCIÓN Y USO, del 25 de Junio de 2012, de UNIVERSIDADE DE VIGO: La presente invención describe dos compuestos quirales, su procedimiento de síntesis y su uso como precursores para la obtención de análogos de tipo Gémini […]
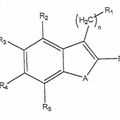 INDENO DERIVADOS, SU PREPARACION Y SU USO COMO MEDICAMENTOS, del 1 de Abril de 2008, de LABORATORIOS DEL DR. ESTEVE, S.A.: Indeno derivados, su preparación y su uso como medicamentos.#La presente invención hace referencia a nuevos indeno derivados de formula general (I), así como a su procedimiento […]
INDENO DERIVADOS, SU PREPARACION Y SU USO COMO MEDICAMENTOS, del 1 de Abril de 2008, de LABORATORIOS DEL DR. ESTEVE, S.A.: Indeno derivados, su preparación y su uso como medicamentos.#La presente invención hace referencia a nuevos indeno derivados de formula general (I), así como a su procedimiento […]
COMPUESTOS DE METALOCENO EN PUENTE COMO CATALIZADORES DE LA POLIMERIZACION DE OLEFINA., del 16 de Marzo de 2007, de POLIMERI EUROPA S.P.A.: Compuestos de metaloceno que presentan la fórmula general (I): en la que: - R1 y R2 pueden ocupar independientemente cualquiera de las posiciones […]
Actividad antitumoral de taiwaniaquinoides y compuestos relacionados, del 21 de Noviembre de 2013, de UNIVERSIDAD DE GRANADA: Actividad antitumoral de taiwaniaquinoides y compuestos relacionados. La invención define el uso de un compuesto de fórmula general (I) para la fabricación […]