Sistema de suministro para tapa de recipiente.
Un dispositivo de suministro (600) para reconstituir un producto farmacéutico en polvo con un diluyente de una jeringa antes de administrar el producto con un gradiente de concentración de manera que el producto más altamente concentrado se proporciona inicialmente,
el dispositivo que comprende:
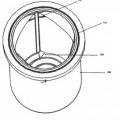
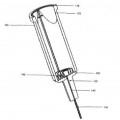
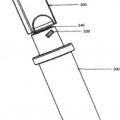
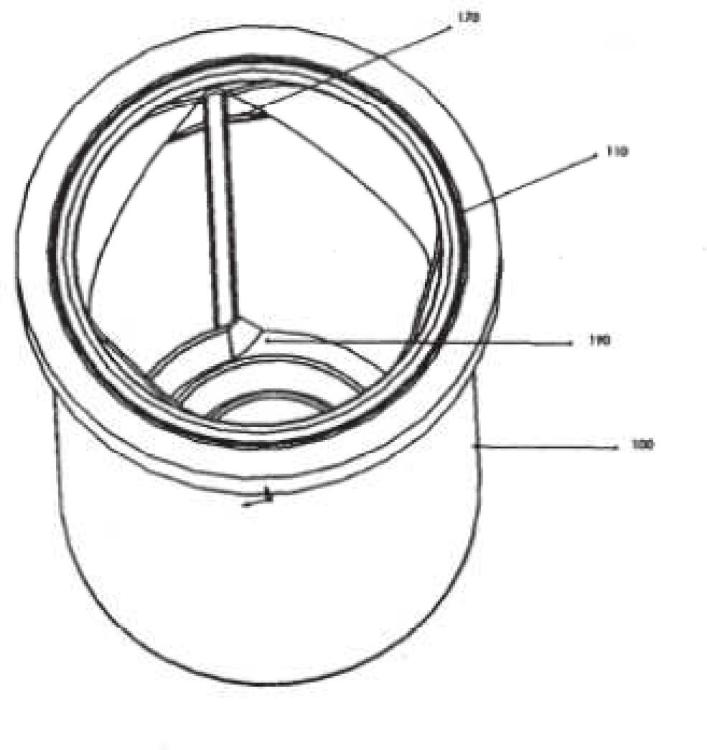
un ensamble de tapa de recipiente que tiene un recipiente de producto (100) para contener un medicamento liofilizado en polvo, dicho ensamble que tiene un orificio de expulsión (130) en un extremo y capaz de acoplar dicha jeringa en el extremo opuesto, dicho ensamble que comprende un ensamble de émbolo (500) que comprime el medicamento en polvo de manera que hay el mínimo espacio de aire entre una base inferior del recipiente de producto y el ensamble de émbolo, y en donde, al activar dicha jeringa, el ensamble de émbolo permite que el diluyente expulsado desde dicha jeringa entre en contacto con el polvo en dicho recipiente de producto (100) y reconstituya rápidamente el polvo a medida que el diluyente fluye hacia dicho orificio de expulsión (130) de dicho recipiente de producto; y
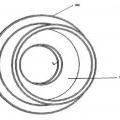
caracterizado porque un canal espiral de mezcla (190) que se integra en la base inferior del recipiente de producto (100), dentro del cual se localiza el medicamento en polvo, y en donde el diluyente entra en contacto con el medicamento en polvo y lo reconstituye a medida que fluye a través del canal espiral de mezcla hacia el orificio de expulsión (130), en donde los diluyentes reconstituyen el medicamento en polvo de manera que el producto se suministra a una concentración inicialmente más alta.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/003065.
Solicitante: CHANG, BYEONG.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1626 LANCASTER CIRCLE THOUSAND OAKS, CA 91360 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CHANG,BYEONG, LIU,ROGER.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B67D7/60 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B67 APERTURA Y CIERRE DE BOTELLAS, TARROS O RECIPIENTES ANALOGOS; MANIPULACION DE LIQUIDOS. › B67D DISTRIBUCION, SUMINISTRO O TRANFERENCIA DE LIQUIDOS, NO PREVISTA EN OTRO LUGAR (limpieza de conducciones o tubos o de sistemas de conducciones o tubos B08B 9/02; limpieza, vaciado o llenado de botellas, tarros, botes, cubas, barriles o recipientes similares no previstos en otro lugar B67C; suministros de agua E03; sistemas de tuberías F17D; sistemas de suministro de agua caliente para uso doméstico F24D; medidas de volúmenes, de caudales, de gasto másico o de niveles de líquidos, cómputo volumétrico G01F; aparatos accionados por monedas o similares G07F). › B67D 7/00 Aparatos o dispositivos para transferir líquidos desde recipientes de almacenaje a granel o depósitos en vehículos o en recipientes portátiles, p. ej. para fines de venta al por menor (disposición general de las estaciones de servicio para suministrar combustibles a los vehículos B60S 5/02; para llenar o vaciar los tanques de agua de las locomotoras, p. ej. columnas para suministro de agua B61K 11/00; para abastecimiento de aviones en vuelo B64D 39/00; instalaciones para manipulación de líquidos especialmente adaptados para el llenado de aeronaves estacionadas B64F 1/28). › que funcionan a mano.
- G01F11/00 FISICA. › G01 METROLOGIA; ENSAYOS. › G01F MEDIDA DEL VOLUMEN, FLUJO VOLUMETRICO, FLUJO MASICO O NIVEL DE LIQUIDOS; DOSIFICACION VOLUMETRICA. › Aparatos que requieren un accionamiento exterior adaptado a cada operación repetida e idéntica para medir y separar, independientemente del peso, un volumen predeterminado de fluido o de material sólido fluyente desde una línea de abastecimiento o recipiente y para suministrarlo.
PDF original: ES-2500494_T3.pdf
Fragmento de la descripción:
Sistema de suministro para tapa de recipiente Campo de la invención
El campo de la presente invención es un sistema de suministro para tapa de recipiente que es adecuado para productos farmacéuticos inyectables liofilizados y el cual facilita la inyección directa y fácil del producto liofilizado sin necesidad de una etapa de reconstitución/mezcla del polvo y un diluyente líquido.
Antecedentes de la invención
Debido a los avances continuos en las tecnologías de ingeniería genética y celular, las proteínas que se sabe que muestran diversas acciones farmacológicas in vivo son susceptibles de elaboración en grandes cantidades para aplicaciones farmacéuticas. No obstante, una de las tareas más demandantes en el desarrollo de sustancias farmacéuticas proteínicas es abordar las inestabilidades físicas y químicas inherentes de tales proteínas, especialmente en las formas de dosificación acuosa. Para tratar de entender y maximizar la estabilidad de las sustancias farmacéuticas proteínicas y cualquier otra proteína utilizable, se han llevado a cabo muchos estudios, especialmente en las últimas dos décadas. Estos estudios han abarcado muchas áreas, que incluyen el plegamiento y despliegue/desnaturalización de las proteínas, los mecanismos de inestabilidades químicas y físicas de las proteínas así como diversos medios para estabilizar proteínas en forma acuosa; véase, por ejemplo, Manning y otros Pharm Res., 1989, 6: 93- 918; Arakawa y otros, Adv Drug Deliv Rev., 21; 46: 37-326; Wang W., Int J Pharm., 1999; 185: 129-188; y Chen T., Drug Dev Ind Pharm., 1992; 18: 1311-1354.
Debido a los problemas de inestabilidad asociados con las formas de dosificación acuosa, las formulaciones en polvo generalmente se prefieren para obtener la estabilidad suficiente para la vida útil deseada del producto. En la industria farmacéutica y biotecnológica se han conocido, fundamentado y llevado a la práctica diversas técnicas para preparar polvos secos. Tales técnicas Incluyen llofilización, secado por pulverización, liofilizado por pulverización, cristalización masiva, secado al vacío y secado por espuma. La lioflllzación (secado por congelamiento) con frecuencia es un método preferido utilizado para preparar polvos secos (liofilizados) que contienen proteínas. Se conocen bien por los expertos en la técnica diversos métodos de lioflllzación; véase, por ejemplo, Pikal MJ., En: Cleland JL E. eds. Formularon and Delivery of Proteins and Peptides. Washington, DC: American Chemical Soclety; 1994: 12-133; y Wang W., Int J Pharm. 2; 23: 1-6.
El procedimiento de llofilización consiste de tres etapas: congelamiento, secado primario y secado secundarlo. Debido a que el producto proteínico se mantiene congelado durante el proceso de secado, la llofilización proporciona las siguientes ventajas con respecto a las técnicas alternativas: daño y pérdida mínimos de la actividad en materiales termolábiles delicados; velocidad y completltud de la rehidratación; la posibilidad de dosificación limpia y precisa en los recipientes del producto final de manera que se reduce la contaminación por partículas y bacterias; permite la reconstitución del producto a una concentración mayor que la que tenía en el momento de congelamiento; y permite el almacenamiento del producto a temperatura ambiente. Esto último puede ser particularmente útil para productos hospitalarios en áreas que no tienen acceso fácil a congeladores, especialmente congeladores ultrafríos.
Desafortunadamente, incluso en las formas de dosificación sólida, algunas proteínas pueden ser relativamente inestables y esta inestabilidad puede ser producto del método de llofilización utilizado para preparar las formas de dosificación sólida y/o la inestabilidad inherente de las mismas formulaciones de dosificación sólidas propiamente dichas. Por ejemplo, en ciertos casos, los eventos de procesamiento de llofilización pueden obligar a una proteína a experimentar cambios químicos y físicos significativos. Tales eventos de procesamiento incluyen concentración de sales, precipitación, cristalización, reacciones químicas, cizallamiento, pH, cantidad de humedad residual que permanece después de la llofilización y similares. Tales cambios químicos y físicos incluyen, por ejemplo, formación de dímeros u otros agregados de orden superior y despliegue de la estructura terciaria. Desafortunadamente, estos cambios pueden resultar en la pérdida de la actividad de la proteína o pueden resultar en que porciones significativas de los materiales activos en el medicamento se hayan transformado químicamente en un producto o productos de degradación los cuales en realidad pueden comprender un antagonista para el medicamento o los cuales pueden dar lugar a efectos secundarios adversos. Además de las inestabilidades provocadas en las proteínas debido a las etapas inherentes del proceso de liofilización, otras desventajas de la liofilización incluyen: tiempos de procesamiento prolongados y complejos; altos costos energéticos; y acondicionamiento y mantenimiento costosos de las instalaciones de liofilización. De esta manera, el uso de la liofilización habitualmente se limita a materiales termosensibles y delicados de alto valor. Además, los polvos liofilizados típicamente se conforman como tortas, las cuales requieren trituración y molienda adicionalmente y opcionalmente de etapas de procesamiento de tamizado para proporcionar polvos que fluyan. Para tratar de entender y optimizar la estabilidad de las proteínas durante la liofilización y después de la liofilización se han llevado a cabo muchos estudios; véase, por ejemplo, Gómez G. y otros, Pharm Res. 21; 18:9-97; Strambini GB., Gabellieri E., Biophys J., 1996; 7:971-976; Chang BS. y otros, J Pharm Sci., 1996; 85:1325-133, Pikal MJ., Biopharm, 199; 3:9, Izutsu K. y otros, Pharm. Res., 1994; 11-995, Overcashier DE., J Pharm Sci., 1999; 88:688, y Schmidt EA. y otros, J Pharm Sci., 1999, 88:291.
Con el fin de permitir la administración parenteral de estos medicamentos en polvo, los medicamentos deben ponerse primero en forma líquida. Para este fin, los medicamentos se mezclan o reconstituyen con un diluyente antes de suministrarse parenteralmente a un paciente. El procedimiento de reconstitución debe realizarse bajo condiciones estériles y en algunos procedimientos de reconstitución, es difícil mantener condiciones estériles. Una manera de reconstituir un medicamento en polvo es inyectar un diluyente líquido directamente en un frasco de medicamento que contiene el medicamento en polvo. Esto puede realizarse mediante el uso de una jeringa de combinación y una aguja de jeringa que contienen el diluyente y frascos de medicamento que incluyen un tapón de caucho perforable. El método de administración es el siguiente: 1) el tapón de caucho del frasco de medicamento se perfora por la aguja y se inyecta el líquido en la jeringa dentro del frasco; 2) el frasco se agita para mezclar el medicamento en polvo con el líquido; 3) después de que el líquido y el medicamento se han mezclado completamente, se extrae en la jeringa una cantidad medida del medicamento reconstituido; 4) la jeringa se retira después del frasco y el medicamento se inyecta después al paciente.
Para las personas que requieren de frecuente administración parenteral de medicamentos, es una práctica común que a esas personas se les proporcione kits de uso domiciliario los cuales pueden incluir cartuchos de inyección, jeringas llenas de antemano, Inyectores en forma de pluma y/o autoinyectores para utilizarse con el propósito de autoadministración. Los autoinyectores que Incorporan mecanismos de inyección con agujas se conocen bien y se considera que presentan varias ventajas en relación a las jeringas hipodérmicas sencillas. Tales autoinyectores con agujas generalmente Incluyen un cuerpo o alojamiento, una jeringa con aguja o dispositivo similar, y uno o más mecanismos Impulsores para Insertar una aguja en el tejido del sujeto y suministrar una dosis deseada de medicamento líquido a través de la aguja Insertada. Hasta ahora, todos los dispositivos autoinyectores conocidos se han utilizado con formulaciones líquidas. Aún existe la necesidad de un autoinyector que pueda utilizarse para suministrar formulaciones en polvo.
Otros métodos de administración de medicamentos en polvo incluyen el uso de cartuchos de inyección de cámara doble y/o sistemas de jeringa llenas previamente. Los cartuchos de inyección del tipo de cámara doble se conocen bien y han encontrado un uso amplio. Se utilizan junto con diversos tipos de aparatos de inyección los cuales sirven para contener el cartucho mientras se prepara para la inyección y mientras las inyecciones se administran subsiguientemente. Los cartuchos de inyección del tipo de cámara... [Seguir leyendo]
Reivindicaciones:
1. Un dispositivo de suministro (6) para reconstituir un producto farmacéutico en polvo con un diluyente de una jeringa antes de administrar el producto con un gradiente de concentración de manera que el producto más altamente concentrado se proporciona inicialmente, el dispositivo que comprende:
un ensamble de tapa de recipiente que tiene un recipiente de producto (1) para contener un medicamento liofilizado en polvo, dicho ensamble que tiene un orificio de expulsión (13) en un extremo y capaz de acoplar dicha jeringa en el extremo opuesto, dicho ensamble que comprende un ensamble de émbolo (5) que comprime el medicamento en polvo de manera que hay el mínimo espacio de aire entre una base inferior del recipiente de producto y el ensamble de émbolo, y en donde, al activar dicha jeringa, el ensamble de émbolo permite que el diluyente expulsado desde dicha jeringa entre en contacto con el polvo en dicho recipiente de producto (1) y reconstituya rápidamente el polvo a medida que el diluyente fluye hacia dicho orificio de expulsión (13) de dicho recipiente de producto; y
caracterizado porque un canal espiral de mezcla (19) que se Integra en la base Inferior del recipiente de producto (1), dentro del cual se localiza el medicamento en polvo, y en donde el diluyente entra en contacto con el medicamento en polvo y lo reconstituye a medida que fluye a través del canal espiral de mezcla hacia el orificio de expulsión (13), en donde los diluyentes reconstituyen el medicamento en polvo de manera que el producto se suministra a una concentración inicialmente más alta.
2. Un dispositivo de acuerdo con la reivindicación 1, que comprende además un saliente de bloqueo (17) Integrado en una pared lateral del recipiente de producto (1) de tal manera que después de la inserción completa del ensamble de émbolo (5), el ensamble de émbolo se acopla al saliente de bloqueo (17) y no puede retirarse.
3. Un dispositivo de acuerdo con la reivindicación 1, en donde el ensamble de émbolo (5) comprende:
un componente de copa superior (3) que tiene uno o más canales de transferencia de fluidos los cuales permiten que el diluyente de una jeringa fluya a través del ensamble de émbolo y entre en contacto con el medicamento en polvo en el canal espiral de mezcla del recipiente de producto;
un componente de tapón (4) que tiene uno o más canales de transferencia de fluidos los cuales permiten que el diluyente de una jeringa fluya a través de el ensamble de émbolo y entre en contacto con el medicamento en polvo en el canal espiral de mezcla del recipiente de producto;
y en donde el componente de copa superior (3) se acopla con el componente de tapón (4) con un acoplamiento firme para formar el ensamble de émbolo (5).
4. Un dispositivo de acuerdo con cualquiera de las reivindicaciones 1 a la 3, en donde el extremo del orificio de expulsión del recipiente de producto (1) que además comprende una base separable (195) la cual sirve para mantener y estabilizar el recipiente de producto (1) durante el llenado y durante el proceso de liofilización.
5. Un dispositivo de acuerdo con la reivindicación 1 en donde dicho ensamble de tapa de recipiente comprende:
un ensamble de émbolo (5) que comprende:
una cavidad de acoplamiento de una lengüeta tipo Luer-Lock para permitir el acoplamiento por fricción de una jeringa estándar tipo Luer-Slip;
una cavidad circular que puede albergar una jeringa típica tipo Luer-Lock; y
un canal de transferencia de fluido definido el cual facilita el flujo de fluido a través de dicho ensamble de émbolo ensamblado; y
un componente de recipiente de producto (1) que comprende:
un extremo abierto que tiene una cámara capaz de contener un ingrediente activo líquido para liofilizarlo y diseñado para recibir dicho ensamble de émbolo (5);
un saliente de bloqueo (17) integrado en la pared lateral de dicho recipiente de producto (1);
una base inferior opuesta que comprende un orificio de expulsión (13) coaxial y hueco; y
el canal espiral de mezcla (19) integrado en dicha base inferior en la cual reside el ingrediente activo líquido.
6. Un dispositivo de acuerdo con la reivindicación 1 en donde dicho ensamble de tapa de recipiente comprende:
un componente de tapón (4) que comprende:
un canal de transferencia de fluido que se extiende axialmente desde el extremo proximal hasta el extremo distal en el exterior del componente de tapón el cual permite el flujo de fluido a través de dicho componente de tapón;
un componente de copa superior (3) que comprende:
una cavidad de acoplamiento de una lengüeta tipo Luer-Lock para permitir el acoplamiento por fricción de una jeringa estándar tipo Luer-Slip; una cavidad circular que puede albergar una jeringa típica tipo Luer-Lock; un interior circular hueco capaz de recibir dicho componente de tapón para crear un ensamble de émbolo (5); y
un canal de transferencia de fluido definido el cual facilita el flujo de fluido a través de dicho ensamble de
émbolo ensamblado;
un componente de recipiente de producto (1) que comprende:
un extremo abierto que tiene una cámara capaz de contener un ingrediente activo líquido para liofilizarlo y 1 diseñada para recibir dicho ensamble de émbolo;
un saliente de bloqueo (17) integrado en la pared lateral de dicho recipiente de producto (1);
una base inferior opuesta que comprende un orificio de expulsión (13) coaxial hueco; y
el canal espiral de mezcla (19) integrado en dicha base inferior en el cual reside el ingrediente activo
líquido.
Patentes similares o relacionadas:
 Dispositivo de distribución de producto líquido o pastoso, del 26 de Febrero de 2020, de ERCA: Dispositivo de distribución de producto líquido o pastoso, que comprende un cuerpo de distribución que tiene una entrada , una primera salida y una […]
Dispositivo de distribución de producto líquido o pastoso, del 26 de Febrero de 2020, de ERCA: Dispositivo de distribución de producto líquido o pastoso, que comprende un cuerpo de distribución que tiene una entrada , una primera salida y una […]
Capuchón de dosificación para un recipiente, un elemento de dosificación para el capuchón de dosificación y un recipiente con el capuchón de dosificación, del 26 de Febrero de 2020, de Teamplast B.V: Un capuchón de dosificación para un recipiente para dosificar materiales sólidos de flujo libre, que comprende una placa de cubierta con una abertura […]
Aparato y método a prueba de fallos para aspirar y/o dispensar líquidos en instrumentos de laboratorio automatizados, del 4 de Diciembre de 2019, de BECKMAN COULTER, INC.: Aparato para impedir o bien la introducción de aire en un líquido aspirado desde un recipiente (C) a través de un tubo de aspiración que pasa a través de una tapa […]
Dispositivo de dosificación de cantidades mínimas, en particular para aplicaciones farmacéuticas, así como el proceso de dosificación de cantidades mínimas de polvo, del 28 de Mayo de 2019, de Fydec Holding SA: Dispositivo de dosificación de cantidades mínimas , en particular para aplicaciones farmacéuticas o químicas, para dosificar volúmenes de polvo de menos de 1cm3, que comprende […]
MAQUINA DOSIFICADORA DE MASA, del 6 de Julio de 2017, de GONZALEZ GIBERT, Daniel: 1. Máquina dosificadora de masa que, aplicable al sector de la fabricación de pan, para pequeños y medianos obradores, está caracterizada por comprender […]
DISPOSITIVO HIDRÁULICO DE ACCIONAMIENTO DE SINFINES PARA VACIADO DE DEPÓSITOS DE SUSTANCIAS GRANULADAS Y/O PULVERULENTAS, del 3 de Enero de 2017, de NAVES SOLDEVILA, Antonio Ramon: Dispositivo hidráulico de accionamiento de sinfines para vaciado de depósitos de sustancias granuladas y/o pulverulentas. Dispositivo hidráulico […]
Aparato de dosificación, del 6 de Julio de 2016, de I.M.A. INDUSTRIA MACCHINE AUTOMATICHE S.P.A.: Un aparato que comprende una unidad de dosificación , provisto con medios de carcasa para soportar […]
Sistema de puerto para la fijación de un recipiente a un sistema de conexión, del 26 de Noviembre de 2014, de NESTEC S.A.: Sistema de puerto para la fijación de un recipiente que comprende una vasija y una salida a un sistema de conexión que presenta una entrada, dicho sistema […]