Procedimiento para la preparación de metilen-difenil-diisocianatos.
Procedimiento para la preparación de metilen-difenil-diisocianatos,
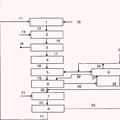
que comprende al menos las etapas
A1) reacción de anilina con formaldehído en presencia de ácido clorhídrico para dar una mezcla de reacción que contiene di- y poliaminas de la serie del difenilmetano ("MDA"), eventualmente al menos parcialmente con separación del agua introducida con los productos de partida o producida en la reacción de la mezcla de reacción,
A2) neutralización de la mezcla de reacción formada de acuerdo con la etapa A1) con disolución acuosa de hidróxido alcalino, obteniéndose una disolución acuosa que contiene cloruro alcalino y una fase orgánica que contiene la mezcla de las di- y poliaminas,
A3) separación de la fase orgánica de la etapa A2) de la fase acuosa y procesamiento de la fase orgánica para la obtención de la mezcla de las di- y poliaminas de la serie del difenilmetano,
A4) ajuste de la disolución que contiene cloruro alcalino que queda de acuerdo con la etapa A3) a un valor de pH< 8, purificación de la disolución que contiene cloruro alcalino de modo que ésta se lleve a un valor de COT< 200 ppm, preferentemente< 50 ppm, de manera muy especialmente preferente< 20 ppm, combinándose la disolución que contiene cloruro alcalino eventualmente al menos parcialmente con las fases acuosas eliminadas en la etapa A1) de la mezcla de reacción y/o con las fases acuosas que se producen en el procesamiento de la fase orgánica de acuerdo con la etapa A3),
B) reacción de la mezcla obtenida en la etapa A3) de las di- y poliaminas de la serie del difenilmetano con fosgeno para dar una mezcla de di- y poliisocianatos de la serie del difenilmetano (MDI) y cloruro de hidrógeno, caracterizado porque
C) la disolución que contiene cloruro alcalino purificada obtenida en la etapa A4) se alimenta al menos parcialmente a una oxidación electroquímica con formación de cloro, disolución de hidróxido alcalino y eventualmente hidrógeno, y
D) al menos una parte del cloro producido de acuerdo con la etapa C) se usa para la preparación del fosgenousado en la etapa B).
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09002178.
Solicitante: Bayer Intellectual Property GmbH.
Inventor/es: BULAN, ANDREAS, WEBER, RAINER, POHL, FRITZ, SIX, CHRISTIAN, BOHM,MATTHIAS, ADAMSON,RICHARD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C209/78 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 209/00 Preparación de compuestos que contienen grupos amino unidos a una estructura carbonada. › a partir de compuestos carbonilo, p. ej. a partir de formaldehído, y de aminas que tienen grupos amino unidos a átomos de carbono de ciclos aromáticos de seis miembros, con formación de metilendiarilaminas.
- C07C211/50 C07C […] › C07C 211/00 Compuestos que contienen grupos amino unidos a una estructura carbonada. › con al menos dos grupos amino unidos a átomos de carbono de ciclos aromáticos de seis miembros de la estructura carbonada.
- C07C263/10 C07C […] › C07C 263/00 Preparación de derivados del ácido isociánico. › por reacción de aminas con halogenuros de carbonilo, p. ej. con fosgeno.
- C07C265/14 C07C […] › C07C 265/00 Derivados del ácido isociánico. › que contienen al menos dos grupos isocianato unidos a la misma estructura carbonada.
- C25B1/26 C […] › C25 PROCESOS ELECTROLITICOS O ELECTROFORETICOS; SUS APARATOS. › C25B PROCESOS ELECTROLITICOS O ELECTROFORETICOS PARA LA PRODUCCION DE COMPUESTOS ORGANICOS O INORGANICOS, O DE NO METALES; SUS APARATOS (protección anódica o catódica C23F 13/00; crecimiento de monocristales C30B). › C25B 1/00 Producción electrolítica de compuestos inorgánicos o no metales. › Cloro; Sus compuestos (por producción simultánea de hidróxidos de metales alcalinos y de cloro, de sus oxiácidos o de sus sales C25B 1/34).
- C25B15/08 C25B […] › C25B 15/00 Funcionamiento o mantenimiento de las células. › Suministro o eliminación de reactivos o electrolitos; Regeneración de electrolitos.
PDF original: ES-2464287_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de metilen-difenil-diisocianatos La invención parte de un procedimiento para la preparación de metilen-difenil-diisocianatos (MDI) mediante reacción de anilina con formaldehído en presencia de ácido clorhídrico para dar una mezcla de di-y poliaminas de la serie del difenilmetano y reacción de la mezcla obtenida de las di-y poliaminas de la serie del difenil-metano con fosgeno para dar una mezcla de di-y poliisocianatos de la serie del difenilmetano.
Los diisocianatos aromáticos son materias primas importantes y versátiles para la química de poliuretano. A este respecto, el toluilendiisocianato (TDI) y el MDI son los isocianatos técnicos más importantes.
El término general “MDI” se usa en el campo específico y en el sentido de esta invención como término genérico para metilen (difenildiisocianatos) y polimetilen-polifenilen-poliisocianatos, los poliisocianatos de la serie del difenilmetano. Por los poliisocianatos de la serie del difenilmetano se entiende en particular compuestos y mezclas de compuestos del siguiente tipo:
en los que n representa un número natural ≥ 2.
El término metilen (difenildiisocianato) comprende los isómeros 2, 2’-metilen (difenildiisocianato) (2, 2’-MDI) , 2, 4’metilen (difenildiisocianato) (2, 4’-MDI) y 4, 4’-metilen (difenildiisocianato) (4, 4’-MDI) . En resumen se designan estos isómeros como “MDI monomérico”. El término polimetilen-polifenilen-poliisocianatos comprende el denominado “MDI polimérico” (PMDI) , que contiene MDI monomérico y homólogos superiores del MDI monomérico.
En todos los procedimientos de preparación relevantes a escala industrial se obtiene MDI mediante fosgenación de las correspondientes poliaminas de la serie del difenilmetano. La síntesis de MDI se realiza a este respecto habitualmente en un procedimiento de dos etapas. En primer lugar se condensa anilina con formaldehído para dar una mezcla de metilen (difenildiaminas) y polimetilenpoliaminas oligoméricas e isoméricas, la denominada MDA bruta. Esta MDA bruta se hace reaccionar a continuación en una segunda etapa con fosgeno de manera en sí conocida para dar una mezcla de los correspondientes metilen (difenildiisocianatos) y polimetilen-polifenilenpoliisocianatos oligoméricos e isoméricos, el denominado MDI bruto. A este respecto, la composición de isómeros y oligómeros permanece no modificada. En la mayoría de los casos se separa entonces una parte de los compuestos de 2 núcleos en otra etapa de procedimiento, por ejemplo mediante destilación o cristalización, permaneciendo el MDI polimérico (PMDI) como residuo.
La preparación continua, discontinua o semicontinua de poliaminas de la serie del difenilmetano, a continuación denominadas también de forma abreviada MDA, se ha descrito en numerosas patentes y publicaciones (véase por ejemplo H.J.Twitchett, Chem.Soc.Rev. 3 (2) , 209 (1974) , M.V. Moore en: Kirk-Othmer Encycl. Chem. Technol., 3ª Ed., Nueva York, 2, 338-348 (1978) . Habitualmente se realiza la preparación de MDA mediante reacción de anilina y formaldehído en presencia de catalizadores ácidos. Habitualmente se usa ácido clorhídrico como catalizador ácido, neutralizándose y por consiguiente consumiéndose el catalizador ácido de acuerdo con el estado de la técnica al final del procedimiento y antes de las etapas finales de procesamiento, por ejemplo de la separación destilativa de anilina en exceso, mediante adición de una base, normalmente disolución de hidróxido de sodio acuosa. Por regla general se realiza la adición del agente de neutralización de manera que la mezcla de neutralización obtenida puede separarse en una fase orgánica que contiene las poliaminas de la serie del difenilmetano y anilina en exceso y una fase acuosa que contiene además de cloruro de sodio aún restos de componentes orgánicos. La fase acuosa se desecha por regla general tras la separación de los componentes orgánicos como agua residual cargada de manera inorgánica.
Se sabe que puede variarse la composición de la MDA bruta preparada según el procedimiento descrito, por consiguiente del MDI bruto preparado a partir de ésta, en el contexto amplio mediante las condiciones de reacción usadas. Son especialmente importantes en este contexto la proporción en mol entre los componentes llevados a reacción anilina y formaldehído (a continuación denominada también de forma abreviada proporción A/F) como
también la cantidad de catalizador añadida, habitualmente indicada como grado de protonación (proporción en mol de catalizador añadido con respecto a anilina alimentada) .
Mediante altas proporciones A/F es accesible una MDA bruta con una alta proporción en monómeros, fomentando los altos grados de protonación a este respecto la formación de la 4, 4’-MDA especialmente significativa técnicamente como precursor para el correspondiente 4, 4’-MDI. Las dos medidas conducen, sin embargo, a una alta producción de sal que por un lado implica una alta pérdida económica, por otro lado una posible carga al medioambiente.
No han faltado intentos para desarrollar procedimientos en los que se reduzca claramente o se eviten completamente el agua residual producida en la preparación de MDA y la carga de sal que ha de desecharse a través del agua residual.
El documento DE 2 238 920 A1 da a conocer un procedimiento para la preparación de poliaminas de la serie del difenilmetano mediante condensación de anilina con formaldehído en presencia de agua y catalizadores ácidos, en el que la mezcla de condensación acuosa que ha reaccionado se extrae con un disolvente hidrófobo, la fase de disolvente así obtenida se procesa para dar las poliaminas y la fase acuosa tras la adición de anilina y formaldehído se reconduce al circuito al inicio del procedimiento. De acuerdo con al enseñanza del documento DE 2 238 920 A1, el agua de condensación producida en la reacción de los productos de partida y el agua en exceso que llega con los materiales de partida al sistema pueden descargarse del sistema en un punto adecuado. En el procedimiento se produce agua residual que contiene esencialmente sólo el agua introducida con los productos de partida así como el agua que se produce en la reacción de la anilina con el formaldehído, suprimiéndose el uso de disolución de hidróxido de sodio. Es desventajoso en este procedimiento el uso de un disolvente orgánico adicional, cuyo uso en una extracción así como la separación mediante destilación son costosos mecánica y energéticamente. Adicionalmente pueden conducirse grandes volúmenes de fase acuosa en el circuito de procedimiento y pueden procesarse igualmente de manera destilativa.
La reducción de las fases acuosas que van a procesarse con realimentación simultánea del catalizador homogéneo usado es objeto del documento DE 2 426 116 A1. Según la enseñanza del documento DE 2 426 116 A1 es especialmente ventajoso realizar la reacción de anilina con formaldehído en varias etapas, a este respecto hacer reaccionar anilina y formaldehído en una primera etapa en ausencia de un catalizador para dar un denominado precondensado (“aminal”) , separar tras finalizar la reacción el agua, entonces hacer reaccionar el precondensado en presencia de sales ácidas de la anilina o de sus productos de condensación con el formaldehído en presencia de disolventes polares, orgánicos, que permanecen indiferentes en las condiciones de reacción, y finalmente separar por lavado el catalizador usado con agua de la mezcla de reacción y reconducirlo a la etapa de reacción del precondensado. Son desventajosos también en este caso el uso de un disolvente orgánico adicional y el alto gasto mecánico y energético condicionado mediante esto para la extracción y destilación.
El documento DE 2 623 681 A1 da a conocer también la formación intermedia de un precondensado, adicionalmente al uso de un catalizador ácido heterogéneo a base de arcilla, zeolitas o tierras de diatomeas para la reacción de los precondensados para dar las poliaminas de la serie del difenilmetano, pudiéndose separar según la enseñanza del documento DE 2 623 681 A1 el catalizador tras finalizar la reacción mediante filtración o centrifugación de la mezcla de poliaminas y pudiéndose reconducir a la etapa de reacción del precondensado. Para la reacción de transposición debe secarse previamente el aminal sin embargo de manera costosa, siendo otro inconveniente del procedimiento la acumulación de productos de reacción en el catalizador, lo que tiene como consecuencia por regla general un tiempo de permanencia insuficiente del catalizador.
Es igualmente objeto de la enseñanza del documento EP 1 257... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de metilen-difenil-diisocianatos, que comprende al menos las etapas A1) reacción de anilina con formaldehído en presencia de ácido clorhídrico para dar una mezcla de reacción que contiene di-y poliaminas de la serie del difenilmetano (“MDA”) , eventualmente al menos parcialmente con separación del agua introducida con los productos de partida o producida en la reacción de la mezcla de reacción, A2) neutralización de la mezcla de reacción formada de acuerdo con la etapa A1) con disolución acuosa de hidróxido alcalino, obteniéndose una disolución acuosa que contiene cloruro alcalino y una fase orgánica que contiene la mezcla de las di-y poliaminas,
A3) separación de la fase orgánica de la etapa A2) de la fase acuosa y procesamiento de la fase orgánica para la obtención de la mezcla de las di-y poliaminas de la serie del difenilmetano, A4) ajuste de la disolución que contiene cloruro alcalino que queda de acuerdo con la etapa A3) a un valor de pH < 8, purificación de la disolución que contiene cloruro alcalino de modo que ésta se lleve a un valor de COT < 200 ppm, preferentemente < 50 ppm, de manera muy especialmente preferente < 20 ppm, combinándose la disolución que contiene cloruro alcalino eventualmente al menos parcialmente con las fases acuosas eliminadas en la etapa A1) de la mezcla de reacción y/o con las fases acuosas que se producen en el procesamiento de la fase orgánica de acuerdo con la etapa A3) , B) reacción de la mezcla obtenida en la etapa A3) de las di-y poliaminas de la serie del difenilmetano con fosgeno para dar una mezcla de di-y poliisocianatos de la serie del difenilmetano (MDI) y cloruro de hidrógeno,
caracterizado porque C) la disolución que contiene cloruro alcalino purificada obtenida en la etapa A4) se alimenta al menos parcialmente a una oxidación electroquímica con formación de cloro, disolución de hidróxido alcalino y eventualmente hidrógeno, y D) al menos una parte del cloro producido de acuerdo con la etapa C) se usa para la preparación del fosgeno usado en la etapa B) .
2. Procedimiento de acuerdo con la reivindicación 1, caracterizado porque al menos una parte de la disolución de hidróxido alcalino preparada de acuerdo con la etapa C) se reconduce a la neutralización de acuerdo con la etapa A) .
3. Procedimiento de acuerdo con una de las reivindicaciones 1 a 2, caracterizado porque al menos una parte del
cloruro de hidrógeno que se produce en la etapa B) se convierte en ácido clorhídrico y este ácido clorhídrico se usa al menos parcialmente en la reacción A1) de la anilina con formaldehído como catalizador.
4. Procedimiento de acuerdo con una de las reivindicaciones 1 a 3, caracterizado porque la concentración de cloruro alcalino de la disolución acuosa que contiene cloruro alcalino, que se obtiene de la etapa A4) , asciende a del 2 % al 24 % en peso, preferentemente del 5 % al 15 % en peso.
7. Procedimiento de acuerdo con una de las reivindicaciones 1 a 6, caracterizado porque la oxidación electroquímica de acuerdo con la etapa C) se realiza según una electrolisis de cloruro alcalino usando membranas 45 de intercambio iónico y/o usando electrodos de difusión de gas como cátodo.
8. Procedimiento según la reivindicación 7, caracterizado porque la electrolisis de cloruro alcalino se realiza según el procedimiento de electrolisis por membrana usando una membrana de intercambio iónico, siendo el cloruro alcalino de la disolución que contiene cloruro alcalino cloruro de sodio y la membrana de intercambio iónico presenta una capacidad de transporte de agua de > 3 mol de agua / mol de sodio, preferentemente > 4 mol de agua / mol de 50 sodio, de manera especialmente preferente > 5 mol de agua/ mol de sodio.
9. Procedimiento de acuerdo con la reivindicación 7 u 8, caracterizado porque las disoluciones de cloruro alcalino alimentadas a la electrolisis de cloruro alcalino están ajustadas antes de la electrolisis a un valor de pH < 7, preferentemente pH < 6.
10. Procedimiento de acuerdo con una de las reivindicaciones 7 a 9, caracterizado porque la concentración de 55 cloruro alcalino de la disolución que contiene cloruro alcalino que llega de la celda de electrolisis asciende a de 100
g/l a 280 g/l, preferentemente de 110 g/l a 220 g/l.
11. Procedimiento según una de las reivindicaciones 7 a 10, caracterizado porque la concentración de la disolución de hidróxido alcalino obtenida de la electrolisis asciende a del 13 % al 33 % en peso, preferentemente del 20 % al 30 % en peso.
Patentes similares o relacionadas:
Celda electrolítica para la producción de soluciones oxidantes, del 17 de Junio de 2020, de INDUSTRIE DE NORA S.P.A: Celda electrolítica para la producción de soluciones oxidantes, que comprende un compartimento anódico que contiene un ánodo […]
Método para producir un electrodo de difusión de gas, del 13 de Mayo de 2020, de INDUSTRIE DE NORA S.P.A: Un método para producir un electrodo de difusión de gas, comprendiendo dicho método las etapas de: revestir un tejido conductor sobre al menos un lado del mismo con un catalizador […]
Aparato de electrocloración, del 6 de Mayo de 2020, de Gaffey Technical Services Limited: Un aparato de electrocloración para generar una solución de hipoclorito de sodio que comprende una celda electrolítica ; un depósito de salmuera situado […]
 Electrodo, del 28 de Agosto de 2019, de Nouryon Chemicals International B.V: Un electrodo que comprende:
- un sustrato de electrodo de titanio ,
- una capa de TiOx con un grosor total en el intervalo de entre 40 - 200 μm […]
Electrodo, del 28 de Agosto de 2019, de Nouryon Chemicals International B.V: Un electrodo que comprende:
- un sustrato de electrodo de titanio ,
- una capa de TiOx con un grosor total en el intervalo de entre 40 - 200 μm […]
 Procedimientos de preparación de carbonato de litio altamente puro y de otros compuestos que contienen litio altamente puro, del 31 de Julio de 2019, de All American Lithium LLC: Un procedimiento de producción de un compuesto que contiene litio, que comprende las etapas de:
poner en contacto una salmuera acuosa que contiene […]
Procedimientos de preparación de carbonato de litio altamente puro y de otros compuestos que contienen litio altamente puro, del 31 de Julio de 2019, de All American Lithium LLC: Un procedimiento de producción de un compuesto que contiene litio, que comprende las etapas de:
poner en contacto una salmuera acuosa que contiene […]
 Procedimiento para la producción de cloro a partir de cloruro de hidrógeno y oxígeno, del 26 de Junio de 2019, de Covestro Deutschland AG: Procedimiento para la producción de cloro por medio de oxidación de múltiples etapas mediante
a) reacción térmica de cloruro de hidrógeno […]
Procedimiento para la producción de cloro a partir de cloruro de hidrógeno y oxígeno, del 26 de Junio de 2019, de Covestro Deutschland AG: Procedimiento para la producción de cloro por medio de oxidación de múltiples etapas mediante
a) reacción térmica de cloruro de hidrógeno […]
Procedimiento para la producción de electrodos de grafito para procesos electrolíticos, del 15 de Mayo de 2019, de Covestro Deutschland AG: Procedimiento para la producción de electrodos de grafito con un revestimiento predominantemente de metal noble para la electrólisis de ácido clorhídrico, en el que el electrodo […]
Revestimiento catalítico y método de fabricación del mismo, del 13 de Mayo de 2019, de INDUSTRIE DE NORA S.P.A: Sustrato de metal de de válvula revestida que tiene un revestimiento que comprende una primera capa catalítica que no contiene titanio y que consiste en una fase amorfa […]