Procedimiento para la estimación de la concentración de fosfatos en células vivas, colorante xanténico y síntesis del mismo.
Procedimiento para la estimación de la concentración de fosfatos en células vivas,
colorante xanténico y síntesis del mismo.
La presente invención describe un procedimiento de estimación de la concentración de fosfatos presente en células vivas a través de la medición del tiempo de decaimiento de fluorescencia de un colorante xanténico añadido a las células y sometido a una excitación mediante luz láser pulsada. También se describe un nuevo colorante xanténico derivado de la fluoresceína que posee mejores propiedades espectrales que los ya conocidos y un procedimiento de síntesis de dicho colorante.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201330861.
Solicitante: UNIVERSIDAD DE GRANADA.
Nacionalidad solicitante: España.
Inventor/es: ALVAREZ PEZ,JOSE MARIA, SALTO GONZALEZ,RAFAEL, GIRON GONZALEZ,MARIA DOLORES, JUSTICIA LADRON DE GUEVARA,JOSE, CUERVA CARVAJAL,JUAN MANUEL, CROVETTO GONZÁLEZ,Luis, ORTE GUTIÉRREZ,Ángel, RUEDAS RAMA,María José, TALAVERA RODRÍGUEZ,Eva María, MARTÍNEZ PERAGÓN,Ángela, PAREDES MARTÍNEZ,José Manuel.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D311/82 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 311/00 Compuestos heterocíclicos que contienen ciclos de seis miembros que contienen un átomo de oxígeno como único heteroátomo, condensados con otros ciclos. › Xantenos.
- C09B13/00 C […] › C09 COLORANTES; PINTURAS; PULIMENTOS; RESINAS NATURALES; ADHESIVOS; COMPOSICIONES NO PREVISTAS EN OTRO LUGAR; APLICACIONES DE LOS MATERIALES NO PREVISTAS EN OTRO LUGAR. › C09B COLORANTES ORGANICOS O COMPUESTOS ESTRECHAMENTE RELACIONADOS PARA PRODUCIR COLORANTES; MORDIENTES; LACAS (procesos de fermentación o procesos que utilizan enzimas para la síntesis de un compuesto dado C12P). › Colorantes de oxicetona.
- C09B57/02 C09B […] › C09B 57/00 Otros colorantes sintéticos de constitución conocida. › Colorantes cumarínicos.
- C09B57/14 C09B 57/00 […] › Colorantes benzoxanténicos; Colorantes benzotioxanténicos.
- G01N1/30 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 1/00 Muestreo; Preparación de muestras para la investigación (manipulación de materiales para un análisis automático G01N 35/00). › Tintura; Impregnación.
- G01N21/64 G01N […] › G01N 21/00 Investigación o análisis de los materiales por la utilización de medios ópticos, es decir, utilizando rayos infrarrojos, visibles o ultravioletas (G01N 3/00 - G01N 19/00 tienen prioridad). › Fluorescencia; Fosforescencia.
- G01N33/52 G01N […] › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Utilización de compuestos o de composiciones para investigaciones colorimétricas, espectrofotométricas o fluorométricas, p. ej. utilización de cintas de papel indicador.
Fragmento de la descripción:
PROCEDIMIENTO PARA LA ESTIMACIÓN DE LA CONCENTRACIÓN DE FOSFATOS EN CÉLULAS VIVAS, COLORANTE XANTÉNICO Y SÍNTESIS DEL
MISMO
SECTOR DE LA TÉCNICA
La presente invención se encuentra dentro del sector de la biomedicina, dentro de las técnicas relacionadas con sensores y microscopía de fluorescencia.
En particular, se trata de un procedimiento para cuantificar el fosfato soluble en el citoplasma de células vivas mediante la medida de tiempos de vida de fluorescencia y microscopía de imagen de fluorescencia.
Asimismo, la invención se enmarca también en el sector químico. En particular se describe la síntesis de una nueva sonda fluorescente derivada del xanteno que se utiliza en el procedimiento de cuantificación de fosfato mencionado.
ESTADO DE LA TÉCNICA
La fluoresceína y sus derivados constituyen una familia de colorantes muy empleada como sondas fluorescentes, por sus altos rendimientos cuánticos, solubilidad, fácil bio- conjugación y excitación con un láser de ión de argón (488 nm). La fluoresceína, en disolución acuosa se presenta bajo cuatro diferentes formas prototrópicas en función del pH, a saber; catión, neutro, monoanión y dianión. A su vez, la forma neutra se presenta bajo tres formas tautoméricas; lactona, cetona y züiterión. Los coeficientes de extinción y los rendimientos cuánticos de fluorescencia, son muy distintos para las diferentes especies prototrópicas. A pH cercano al fisiológico solo tiene lugar el equilibrio monoanión/dianión y ambas especies presentan espectros de absorción y de fluorescencia ligeramente diferentes. El dianión posee mayor coeficiente de extinción que el monoanión, medidos cada uno en su correspondiente máximo de absorción. Asimismo, el dianión tiene mayor rendimiento cuántico de fluorescencia, aunque el monoanión también fluoresce con relativa intensidad y con máximo de emisión casi coincidente en longitud de onda con el del dianión (Yguerabide, J.; Talavera, E.M.; Alvarez, J.M.; Quintero, B., Photochem. Photobiol. 1994, 60, 435-441). Debido a las favorables características espectrales de la fluoresceína, se ha sintetizado un número
importante de derivados de esta, que replican aproximadamente sus espectros y presentan características fotofísicas favorables para ciertos fines concretos.
Hace unos años, algunos de los inventores de esta patente, pusieron de manifiesto la existencia de una reacción de transferencia protónica en el estado excitado (ESPT) entre el monoanión y dianión de fluoresceína (Alvarez-Pez, J.M.; Ballesteros, L.; Talavera, E.M.; Yguerabide, J., J. Phys. Chem. A 2001, 105, 6320-6332), que modifica las características de emisión de fluorescencia de ambas especies. Propusieron un modelo en dos estados en presencia de un dador/aceptor protónico y dedujeron las expresiones teóricas derivadas del modelo que permitieron recuperar los parámetros cinéticos y espectrales del sistema estudiado. Además, se demostró la dependencia de estos dos tiempos de decaimiento con la concentración de fosfato, a distintos valores de pH. También se establecieron las ecuaciones teóricas y el software necesario para aplicar el análisis global compartimental (GCA), una herramienta de cálculo muy potente, a la obtención de los parámetros cinéticos y espectrales correspondientes a la citada reacción ESPT (Crovetto, L.; Orte, A.; Talavera, E.M.; Alvarez-Pez, J.M.; Cotlet, M.; Thielemans, J.; De Schryver, F.C.; Boens, N., J. Phys. Chem. B 2004, 108, 6082-6092).
En resumen, la presencia de la reacción de transferencia protónica en el estado excitado mediada por un buffer de fosfatos, modula los decaimientos de fluorescencia de la fluoresceína y de sus derivados. Dependiendo de factores experimentales como el pH y la longitud de onda de excitación, los valores de los dos tiempos de decaimiento pueden ser muy diferentes, pudiéndose tunear variando convenientemente los citados factores externos. Sin embargo, la naturaleza biexponencial de los decaimientos de fluorescencia de la fluoresceína, hace difícil su aplicación como sensor mediante la técnica de microscopia de imágenes de tiempos de vida de fluorescencia (FLIM).
En el año 2005 un grupo japonés sintetizó una serie de derivados de la fluoresceína, que denominaron como Tokyo Green (Urano, Y.; Kamiya, M.; Kanda, K.; Ueno, T.; Hirose, K.; Nagano, T., J. Am. Chem. Soc. 2005, 127, 4888-4894). Dos de los derivados en cuestión, el 9-[1-(2-Metoxi-5-metilfenil)]-6-hidroxi-3H-xanten-3-ona (2- OMe-5-Me TG) y el 9-[1-(2-Metil-4-metoxifenil)]-6-hidroxi-3H-xanten-3-ona (2-Me-4- OMe TG) tienen interesantes propiedades espectrales. En tales derivados se reemplazó el grupo carboxilo del ácido benzoico de la molécula de fluoresceína por un grupo metilo o metoxilo, lo que implica que solo puede existir una forma aniónica de estas moléculas. Esto disminuye el número de especies prototrópicas en disolución y simplifica el número de equilibrios entre ellas. Además, los derivados 2-OMe-5-Me TG
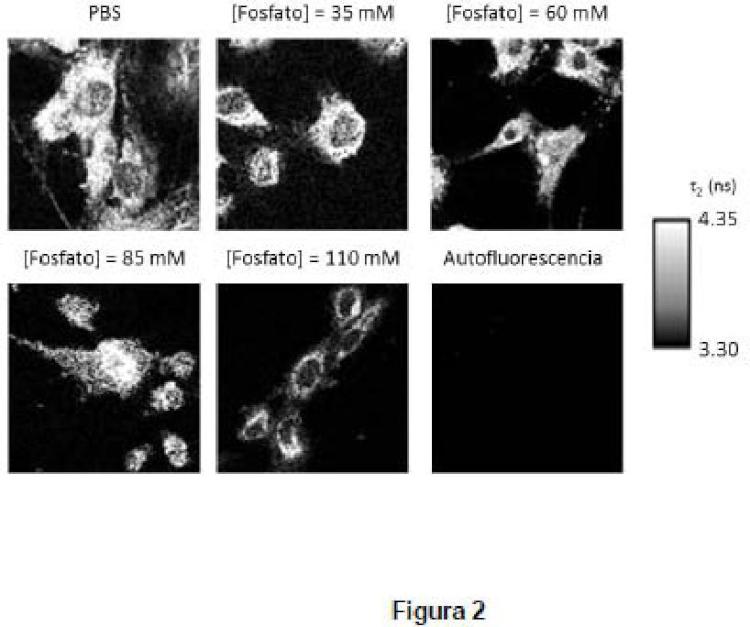
y 2-Me-4-OMe TG, se pueden considerar como sondas fluorescentes "ON/OFF". En efecto, cuando la mitad xanteno de los derivados está protonada (a pH ácido) el rendimiento cuántico de fluorescencia es igual o muy cercano a cero, mientras que, a pH alcalino, el rendimiento cuántico de la forma aniónica es similar al de la fluoresceína. Esta característica de sondas fluorescentes "ON/OFF" acompañadas de un bajo tiempo de vida de fluorescencia para la especie neutra, nos indicó la posibilidad de conseguir un decaimiento monoexponencial cuando se promueva la reacción ESPT entre la especie neutra y la aniónica, mediante la adición de una concentración suficiente de buffer de fosfatos, a valores de pH cercanos al fisiológico. Por esta razón, se abordó un estudio fotofísico en profundidad de ambos compuestos. Tal como se esperaba, la reacción ESPT entre las especies neutras y los correspondientes aniones solo tiene lugar en presencia de una concentración relativamente baja de un buffer de fosfatos, a pH alrededor de la neutralidad. Los tiempos cortos de ambos decaimientos son del orden del picosegundo y prácticamente se hacen nulos a concentraciones de fosfato mayores de 0,05 M, mientras que los tiempos de decaimiento más largos (entre 2 y 4 ns) resultan dependientes de la concentración de fosfato (Crovetto, L.; Paredes, J.M.; Ríos, R.; Talavera, E.M.; Alvarez-Pez, J.M., J. Phys. Chem. A 2007, 111, 13311-13320 y Paredes; J.M.; Crovetto, L.; Ríos, R.; Orte, A.; Alvarez-Pez, J.M.; Talavera, E.M., Phys. Chem. Chem. Phys. 2009, 11, 5400-5407). Además, las ventajosas características espectroscópicas del 2-Me-4-OMe TG motivó que con este colorante se extendiera el estudio fotofísico a nivel de moléculas individuales. Así, se obtuvieron los tiempos de decaimiento de fluorescencia recuperados a nivel de conjunto y de moléculas individuales, junto a los valores simulados con el modelo teórico establecido y las constantes cinéticas calculadas mediante GCA. La coincidencia de los tres conjuntos de valores fue excelente. Como resultado cuantitativo de interés se debe de destacar que la sensibilidad del tiempo de decaimiento frente al fosfato, se concreta en que un incremento de concentración de fosfatos desde 0 hasta 0.3 M decrece el tiempo de decaimiento desde 3.7 ns hasta 3.0 ns, a pH 6.5. Esta sensibilidad del tiempo de decaimiento a las condiciones ambientales hace de estos colorantes serios candidatos para sondar la concentración de fosfato a tiempo real en células vivas.
El reconocimiento selectivo de aniones de interés biológico ha recibido una gran atención por parte de químicos y biólogos. El ión fosfato juega un importante papel, no solo en el control del pH sanguíneo, sino también en la energética y metabolismo de las células. En este sentido, la regulación y control de la captación de fosfato en osteoblastos es particularmente importante. Asimismo, los aniones fosfato juegan un
papel importante en la transducción de señales y almacenamiento de energía en los sistemas biológicos y muchas de las enzimas comunes, tales como quinasas y fosfatasas, producen o consumen fosfato inorgánico que está también relacionado con la fosforilación de proteínas. De acuerdo con esto, la detección del aumento o disminución de la concentración de fosfato en los alrededores de estas enzimas es una forma común de monitorizar la actividad enzimática o el proceso de fosforilación proteica. Por este motivo, varios grupos de investigación han puesto su atención en la detección y discriminación de esos aniones. Sin embargo, hasta ahora se conocen muy pocos sensores no invasivos que muestren alta selectividad y sensibilidad en medios acuosos, pero ninguno que pueda detectar cuantitativamente y a tiempo real el anión fosfato en el citoplasma...
Reivindicaciones:
1.- Procedimiento de estimación de la concentración de fosfatos presente en células
vivas a través de la medición del tiempo de decaimiento de fluorescencia de un colorante xanténico añadido a las células y sometido a una excitación mediante luz láser pulsada.
2.- Procedimiento según reivindicación anterior, que comprende las siguientes etapas:
i) Añadir un colorante xanténico en disolución a la muestra de células.
ii) Excitar el colorante presente en la muestra mediante luz pulsada.
iii) Obtener, mediante microscopía de tiempos de vida de fluorescencia, una imagen de la muestra de células de X pixeles de ancho e Y pixeles de alto.
iv) Generar una matriz de dimensiones (X,Y), donde cada elemento (x,y) contiene el número de fotones detectados y el histograma de distribución de tiempos de detección de cada fotón individual que representa el decaimiento de fluorescencia.
v) Realizar el ajuste a una función multiexponencial de los decaimientos de fluorescencia recogidos en cada elemento, (x,y),
vi) Generar una matriz, de dimensiones (X,Y), en la que cada elemento contiene la estimación, a partir del modelo ajustado en la etapa anterior, del tiempo de vida de fluorescencia largo, t2, del colorante xanténico.
vii) Seleccionar el conjunto de pixeles de interés para el análisis, preferentemente los pixeles correspondientes al citoplasma celular, de una o varias células.
viii) Reconstruir y ajustar el decaimiento de fluorescencia global de la región de interés, en particular del citoplasma celular.
ix) Estimar la concentración total de fosfato mediante las ecuaciones procedentes de un modelo cinético de reacción entre los iones de fosfato y el colorante xanténico.
3.- Procedimiento según reivindicación anterior, caracterizado porque el colorante
xanténico se añade en disolución acuosa hasta alcanzar una concentración entre 10"3 4 5 mol x L-1 y 10"9 mol * L-1, preferentemente una concentración de 10"7 mol * L-1.
4.- Procedimiento según reivindicaciones 2 ó 3, caracterizado porque la luz pulsada
utilizada en la etapa ii) tiene una radiación monocromática con una longitud de
onda entre 400 y 500 nanometros, una frecuencia de repetición controlable en el rango de 1 a 20 Mhz y una anchura temporal del pulso preferentemente inferior a 500 picosegundos.
5.- Procedimiento según cualquiera de las reivindicaciones 2 a 4, caracterizado
porque los decaimientos se ajustan, en la etapa v), a un modelo de decaimiento no lineal, preferentemente mediante la función
w = A1 -e~^Tl + A2 e~^Tl + w0
siendo Xi un parámetro que representa las contribuciones de tiempo corto al decaimiento de fluorescencia; x2 representa el tiempo de decaimiento del colorante xanténico que es sensible a la concentración de fosfato; Ai y A2 los parámetros ajustables que representan las abundancias relativas de cada tiempo de decaimiento, y w0 un parámetro ajustable que representa el ruido de fondo.
6.- Procedimiento según reivindicación anterior, caracterizado porque el ajuste se
realiza suponiendo que x^ =1.5 ns.
7.- Procedimiento según cualquiera de las reivindicaciones 2 a 6, que además
comprende, tras la etapa vi), una etapa en la que se asocia una escala de color arbitrario a los valores contenidos en la matriz anterior para generar una imagen de forma que cada pixel esté coloreado según el valor del tiempo de vida del colorante xanténico, x2, calculado en la etapa vi)
8.- Procedimiento, según cualquiera de las reivindicaciones 1 a 7 caracterizado
porque el colorante xanténico utilizado es 2-Me-4-OMe TG
OMe
**(Ver fórmula)**9.- Colorante Xanténico 9-(4-ter-butil-2-metoxifenil)-6-hidroxi-3H-xanten-3-ona de fórmula 2-OMe-4-íBu GG.
**(Ver fórmula)**10.- Procedimiento, según cualquiera de las reivindicaciones 1 a 7, caracterizado 5 porque el colorante xanténico utilizado es el colorante 2-OMe-4-íBu GG.
11.- Programa de ordenador que comprende instrucciones de programa para hacer que un ordenador lleve a la práctica el procedimiento según cualquiera de las reivindicaciones 1 a 8 ó 10.
12.- Programa de ordenador de acuerdo con la reivindicación 11, que está
incorporado en unos medios de almacenamiento.
13.- Programa de ordenador de acuerdo con la reivindicación 11, que esta
soportado en una señal portadora.
14.- Procedimiento de síntesis del compuesto 2-OMe-4-íBu GG, que comprende las
siguientes etapas:
i) Transformar 2,2,4,4-tetrahidroxibenzofenona, I,
0
OH
en el compuesto con esqueleto xanténico II mediante tratamiento con agua en tubo de alta presión.
**(Ver fórmula)**O
**(Ver fórmula)**ii) Tratar el compuesto II con cloruro de tert-butildimetilsilano e imidazol en diclorometano para proteger sus dos grupos hidroxilo en forma de TBDMS (tert-butildimetilsilil) derivados y obtener el derivado III.
O
TBDMSO
**(Ver fórmula)**OTBDMS
III
iii) Tratar el compuesto V
**(Ver fórmula)**OMe
V
con NBS para obtener compuesto IV
**(Ver fórmula)**Br
IV
OMe
iv) Obtener un reactivo organometálico a partir del compuesto IV.
v) Hacer reaccionar el compuesto III con el reactivo organometálico obtenido en la etapa anterior.
vi) Tratar en ácido fuerte el crudo de la reacción entre III y reactivo organometálico obtenido en la etapa anterior para obtener el compuesto 2- OMe-4-fBu GG.
15.- Procedimiento de síntesis del compuesto 2-OMe-4-íBu GG según
reivindicación anterior en la que el reactivo organometálico es el litio derivado del compuesto IV obtenido por reacción del mismo con butil litio y usando THF como
disolvente.
16.- Procedimiento de síntesis del compuesto 2-OMe-4-tBu GG según
reivindicación anterior en la que el reactivo organometálico es un reactivo de Grignard VI,
tBu
OMe
MgBr
VI
obtenido al tratar el compuesto IV con Mg usando como disolvente THF o éter dietílico.
17.- Procedimiento de síntesis del compuesto 2-OMe-4-fBu GG según
reivindicación 15 caracterizado porque el butil litio empleado en la etapa iv) es
BuLi, en cualquier concentración y disolvente habitual de uso, preferentemente 2.5 M.
18.- Procedimiento de síntesis del compuesto 2-OMe-4-íBu GG según
reivindicación 16, caracterizado porque el disolvente empleado en la generación
del reactivo de Grignard VI es THF o éter dietílico.
**(Ver fórmula)**
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
Nanoparticulas de AG2S súper fluorescentes en la región del infrarrojo cercano y metódo de obtención, del 15 de Julio de 2020, de UNIVERSIDAD COMPLUTENSE DE MADRID: Nanopartículas de Ag2S súper fluorescentes en la región del infrarrojo cercano y método de obtención. El marcaje con sondas fluorescentes […]
DISPOSITIVO DE MONITORIZACIÓN DE SUSTANCIAS TÓXICAS EN AGUA Y SISTEMA QUE LO COMPRENDE, del 7 de Julio de 2020, de UNIVERSITAT ROVIRA I VIRGILI: Dispositivo de monitorización de sustancias tóxicas en agua y sistema que lo comprende. El dispositivo incorpora una cámara de referencia con un filtro depurativo […]
Ensayo de toxina botulínica con sensibilidad mejorada, del 1 de Julio de 2020, de BioMadison, Inc: Un método para aumentar la sensibilidad de la detección basada en células de una toxina botulínica, que comprende: (i) proporcionar una célula […]
Kit, su uso y procedimiento para la calibración de un sistema de medición de fotoluminiscencia, del 24 de Junio de 2020, de BAM BUNDESANSTALT FUR MATERIALFORSCHUNG UND -PRUFUNG: Kit para la calibracion trazable de un sistema de medicion de fotoluminiscencia, que comprende: a) al menos en cada caso uno de los siguientes patrones de fluorescencia (i) […]
Monitor de aerosol en tiempo real, del 17 de Junio de 2020, de Wuxi Maitong Scientific Instrument Co., Ltd: Un monitor de aerosol en tiempo real, que comprende: un conjunto de fuente de luz láser , configurado para emitir un rayo láser y generar […]
Un sistema óptico integrado para el examen de materiales de muestra, del 10 de Junio de 2020, de Iris Technology Solutions SL: Un sistema óptico que comprende: una fuente de luz ; un sistema de suministro de luz que comprende un reflector de una primera abertura […]
Dispositivo de soporte de elementos cromóforos, del 3 de Junio de 2020, de Genewave: Dispositivo de tipo biochip que comprende un sustrato cuya capa superficial forma una guía de onda plana , llevando dicha capa superficial elementos […]