PEPTIDO NEUROPROTECTOR ASI COMO SU USO EN EL TRATAMIENTO DE ENFERMEDADES CEREBROVASCULARES Y OTRAS PATOLOGIAS DEL SNC.
La presente invención hace referencia a un péptido neuroprotector,
caracterizado por comprender los 11 aminoácidos C-terminales de TrkB-T1 (residuos 466-476) (SEQ ID NO: 1) y ser capaz de interferir y/o inhibir la unión entre TrkB-T1 y sus moléculas interaccionantes en una neurona y/o célula glial. Así mismo, en la presente invención se protege el uso de dicho péptido neuroprotector para prevenir y/o tratar el daño neuronal en mamíferos causado por una enfermedad cerebrovascular o isquemia cerebral y/o por otra patología del SNC asociada a excitotoxicidad, y/o daño traumático cerebral y/o medular. También se protege una composición farmacéutica o medicamento caracterizado por comprender dicho péptido neuroprotector, así como el uso de los mismos en el tratamiento de enfermedades cerebrovasculares y otras patologías del SNC. Finalmente, se protege el método de obtención de dicho péptido neuroprotector.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201232015.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Inventor/es: DÍAZ-GUERRA GONZÁLEZ,Margarita, SÁNCHEZ TEJEDA,Gonzalo, GÓMEZ VIDAURRE,Oscar.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K7/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 5 a 11 aminoácidos.
PDF original: ES-2479815_A1.pdf
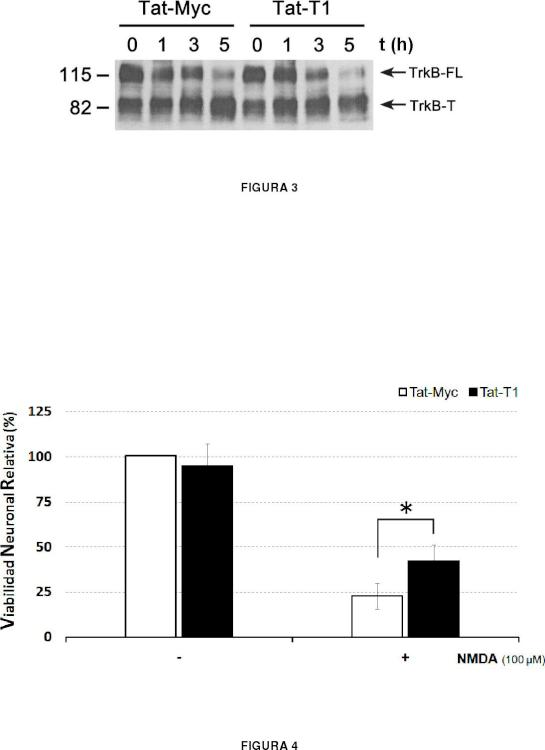
Fragmento de la descripción:
Péptido neuroprotector así como su uso en el tratamiento de enfermedades cerebrovasculares y otras patologías del snc
Sector de la técnica
La presente invención se engloba en el sector farmacéutico, y en el sector de servicios públicos, sociales y colectivos. En concreto, la presente invención se dirige a compañías farmacéuticas que trabajan en el campo de la neuroprotección, tanto referida a daños agudos (isquemia, trauma agudo) como crónicos (enfermedades neurodegenerativas).
Estado de la técnica anterior
La industria farmacéutica tiene gran interés en las patologías humanas de alta incidencia y de prevalencia creciente debido a los cambios demográficos y las mayores expectativas de vida. Las enfermedades cerebrovasculares (ECV) representan la segunda causa de muerte mundial, con 6,15 millones de defunciones y un 10,8% del total (según datos recientes de la OMS del año 2011). Así mismo, la isquemia cerebral es la segunda causa de demencia tras la enfermedad de Alzheimer, y el primer motivo de incapacidad en adultos.
La isquemia cerebral o ictus es un fenómeno que caracteriza a las ECVs y se define como la reducción por diferentes causas del aporte sanguíneo hasta unos niveles insuficientes para mantener el metabolismo y funcionamiento normales de las células cerebrales. Existen dos tipos de ictus según su origen: ictus hemorrágico, generado por la ruptura de un vaso cerebral, el espasmo vascular asociado a una hemorragia subaracnoidea y la hipertensión intracraneal, y el ictus isquémico, producido por la falta de riego sanguíneo en una región del cerebro debido a la presencia de un trombo o placa aterosclerótica. En el tejido afectado podemos diferenciar dos áreas: el núcleo del infarto, que sufre la reducción más severa de flujo sanguíneo y experimenta un daño irreversible, y la zona de penumbra isquémica, caracterizada por ser funcionalmente silente pero intacta desde el punto de vista estructural. Sin embargo, si el flujo sanguíneo no se recupera en un periodo de tiempo denominado ventana terapéutica, esta región puede sufrir procesos de degeneración neuronal secundaria que provocan la expansión del núcleo del infarto hacia la zona de penumbra isquémica.
El único tratamiento aprobado en la práctica clínica frente al ictus isquémico es la trombólisis con el activador tisular del plasminógeno (tPA), que contribuye a la restauración del flujo sanguíneo cerebral mediante la disolución del coágulo que obstruye la arteria. No obstante, la terapia trombolítica da lugar con relativa frecuencia a hemorragias intracerebrales sintomáticas y, además, el tPA presenta una toxicidad asociada que incrementa la degeneración neuronal en modelos experimentales. Estos efectos adversos conllevan la existencia de numerosas contraindicaciones para este tipo de terapia, lo cual ocasiona un problema adicional: la ventana terapéutica en la que los beneficios del tratamiento son superiores a los riesgos se estrecha considerablemente, estando dentro de las 3-4 horas tras el comienzo de los síntomas. Esto supone que en España únicamente un 4% de los pacientes de un ictus isquémico puede beneficiarse del uso de compuestos trombolíticos. Por tanto, aún mejorando la evolución de algunos pacientes, el uso del tPA no está exento de riesgos, tiene un uso muy limitado y solo es eficaz en una estrecha ventana terapéutica.
Entre las alternativas terapéuticas que se están tratando de desarrollar está la interferencia de las cascadas de señalización bioquímica inducidas por la ECV que conducen al daño isquémico y la muerte neuronal secundaria de la zona de penumbra. Reducir esta muerte neuronal secundaria sería extremadamente beneficioso porque permitiría atenuar el daño neurológico y el grado de discapacidad de los pacientes. El mecanismo fundamental de la muerte neuronal secundaria es la excitotoxicidad, el cual es un proceso inducido por el aumento de la concentración del neurotransmisor excitatorio glutamato en el espacio extracelular y la sobreactivación de sus receptores específicos, principalmente los de tipo N-metil-D-aspartato (NMDARs) (Olney, J.W. 1986). Por ello, la excitotoxicidad es una diana fundamental en la búsqueda de estrategias de neuroprotección. En el pasado, como primera aproximación, se utilizaron sobre todo fármacos que al unirse directamente a los NMDARs (antagonistas) o de manera indirecta (por ejemplo, inhibidores de la liberación de glutamato, antagonistas de los canales de calcio dependientes de voltaje) disminuían la sobreactivación del NMDAR. Sin embargo, estos fármacos mostraron resultados esperanzadores en modelos experimentales de isquemia pero fueron ineficaces en el tratamiento de la isquemia cerebral en humanos y, por tanto, no superaron los ensayos clínicos (Ikonomidou, C. & L. Turski. 2002). Un defecto común a la mayoría de estos fármacos es su falta de selectividad, motivada fundamentalmente por el desconocimiento de la naturaleza dual de los NMDARs, receptores que son críticos a un tiempo en procesos de supervivencia y de muerte celular (Hardingham, G.E., et al. 2002). Además, los NMDARs juegan también un papel preponderante en la transmisión sinóptica y la comunicación neuronal del SNC, tanto durante el desarrollo como en su vida adulta, y son críticos en procesos vitales como el aprendizaje, la memoria, la plasticidad sinóptica y la sinaptogénesis. Debido a ello, los fármacos desarrollados anteriormente en general bloquean tanto la activación fisiológica del NMDAR como la patológica y, por tanto, tienen efectos secundarios sobre el aprendizaje y producen somnolencia, alucinaciones o incluso coma.
El interés por desarrollar nuevos fármacos capaces de reducir el proceso excitotóxico va mucho más allá de las ECVs, ya que las alteraciones funcionales del NMDAR son también causantes de la degeneración o muerte neuronal en un gran número de patologías neurológicas, como son la hipoglucemia, epilepsia y el trauma agudo (Choi, D.W. et al, 1988). Además, la excitotoxicidad también aparece asociada a ciertas enfermedades neurodegenerativas como las enfermedades de Alzheimer, Parkinson, Huntington y la esclerosis lateral amiotrófica (ALS). En general, todas estas enfermedades carecen de tratamientos etiológicos y las terapias utilizadas son sintomáticas o paliativas. Así, por ejemplo, en casos moderados o graves de la enfermedad de Alzheimer se está utilizando un antagonista no-competitivo del NMDAR de desarrollo más reciente, la memantina, que presenta cierta eficacia en la reducción de la excitotoxicidad asociada a dicha enfermedad (Chen, H.S. & S.A. Lipton. 2006). Por último, la excitotoxicidad también es crítica en trastornos neurológicos caracterizados por hiperexcitabilidad o hipersensibilización neuronal (algunos tipos de disquinesias, dolor neuropático), y patologías oculares (glaucoma, retinopatía diabética, neuropatía óptica isquémica y traumatismos del nervio óptico).
Las regiones citoplásmicas C-terminales de las subunidades del NMDAR son necesarias para su reclutamiento y agrupamiento correcto en la densidad posináptica (PSD) y su funcionalidad. Son particularmente importantes los 4 aminoácidos C-terminales de las subunidades GluN2A y GluN2B, que constituyen un ligando capaz de interaccionar con los dominios PDZ presentes en diversas proteínas de la PSD, como PSD-95. Esta proteína de andamiaje es muy abundante en la PSD y presenta diversos dominios de interacción proteína-proteína incluyendo 3 secuencias PDZ. Mediante la conexión entre receptores de membrana, como el NMDAR, y múltiples proteínas efectoras, como la
enzima óxido nítrico sintasa neuronal (nNOS), PSD-95 organiza la puesta en marcha de distintas vías de señalización intracelular así como la interacción del NMDAR con el citoesqueleto neuronal. En isquemia cerebral, PSD-95 acopla la sobreactivación del NMDAR con la activación de la nNOS y la formación de NO, molécula crítica para la neurotoxicidad.
Partiendo de la hipótesis de que los NMDARs formados por subunidades GluN2B están implicados mayoritariamente en la señalización hacia la muerte neuronal, mientras que los constituidos por subunidades GluN2A facilitan la supervivencia (Liu etal., 2007), se ha tratado de disociar específicamente los complejos GluN2B-PSD-95-nNOS como una forma de reducir el daño neuronal en modelos de isquemia cerebral. Para ello, se ha generado un péptido de 20 aminoácidos que contiene los últimos 9 aminoácidos del extremo C-terminal de las subunidades GluN2B fusionado al dominio de transducción de la proteína Tat del virus de la inmunodeficiencia humana (VIH) (Aarts, M., et al. 2002). Esta pequeña secuencia de la proteína Tat es capaz de conferir la permeabilidad a través de la membrana plasmática y la barrera... [Seguir leyendo]
Reivindicaciones:
1. Un péptido neuroprotector caracterizado por comprender la secuencia SEQ ID NO: 1, capaz de impedir la unión entre TrkB-T1 y sus moléculas interaccionantes en células neuronales y/o gliales.
2. El péptido neuroprotector según la reivindicación 1, caracterizado por comprender un agente de internalización.
3. El péptido neuroprotector según la reivindicación 2, caracterizado por que el agente de internalización es la secuencia SEQ ID NO: 3.
4. El péptido neuroprotector según las reivindicaciones 1-3, caracterizado por que comprende un linker o una molécula de unión.
5. El péptido neuroprotector según la reivindicación 4, caracterizado por que la secuencia de dicho péptido es SEQ ID NO: 2.
6. El péptido neuroprotector según la reivindicación 4, caracterizado por que la secuencia de dicho péptido es SEQ ID NO: 9.
7. Una secuencia nucleotídica que codifica para el péptido neuroprotector descrito en las reivindicaciones 1-6.
8. Un vector de expresión o plásmido caracterizado por comprender al menos una secuencia nucleotídica descrita en la reivindicación 7.
9. Una célula hospedadora caracterizada por expresar el vector de expresión descrito en la reivindicación 8.
10. Una composición farmacéutica o medicamento caracterizado por comprender el péptido neuroprotector descrito en las reivindicaciones 1-6, o la secuencia nucleotídica descrita en la reivindicación 7, o el vector de expresión o plásmido descrito en la reivindicación 8, o la célula hospedadora descrita en la reivindicación 9.
11. Uso del péptido neuroprotector descrito en las reivindicaciones 1-6 en la fabricación de una composición farmacéutica o medicamento.
12. Uso según la reivindicación 11, caracterizado por que la composición farmacéutica o medicamento es para la prevención y/o tratamiento del daño neuronal.
13. Uso según la reivindicación 12, caracterizado por que el daño neuronal es causado por una patología del SNC asociada a excitotoxicidad en la que la vía de supervivencia BDNF/TrkB se encuentra alterada o inhibida.
14. Uso según la reivindicación 12, caracterizado por que el daño neuronal es causado por una enfermedad cerebrovascular en la que la vía de supervivencia BDNF/TrkB se encuentra alterada o inhibida.
15. Uso según la reivindicación 12, caracterizado por que el daño neuronal es causado por un traumatismo cerebral y/o medular en el que la vía de supervivencia BDNF/TrkB se encuentra alterada o inhibida.
16. Uso según la reivindicación 11, caracterizado por que la composición farmacéutica o medicamento se emplea sólo o en combinación con otros medicamentos para terapia trombolítica o para prevenir y/o tratar el daño isquémico.
17. La composición farmacéutica descrita en la reivindicación 10, para su uso en medicina.
18. La composición farmacéutica según la reivindicación 17, caracterizado para su 10 uso en la prevención y/o tratamiento del daño neuronal.
19. La composición farmacéutica según la reivindicación 18, caracterizado por que el daño neuronal es causado por una patología del SNC asociada a excitotoxicidad en la que la vía de supervivencia BDNF/TrkB se encuentra alterada o inhibida.
20. La composición farmacéutica según la reivindicación 18, caracterizado por que el daño neuronal es causado por una enfermedad cerebrovascular en la que la vía de supervivencia BDNF/TrkB se encuentra alterada o inhibida.
21. La composición farmacéutica según la reivindicación 18, caracterizado por que el
daño neuronal es causado por un traumatismo cerebral y/o medular en el que la vía de supervivencia BDNF/TrkB se encuentra alterada o inhibida.
22. La composición farmacéutica según la reivindicación 17, caracterizado por que la 25 composición farmacéutica o medicamento se emplea sólo o en combinación con otros medicamentos para terapia trombolítica o para prevenir y/o tratar el daño isquémico.
Patentes similares o relacionadas:
Péptido basado en colágeno tipo II alfa-1 útil para el tratamiento de una enfermedad de la superficie ocular, del 15 de Julio de 2020, de EYEBIO KOREA: Un péptido que consiste en una secuencia de aminoácidos representada por SEQ ID NO: 1.
Péptido que tiene actividad antiinflamatoria, y uso del mismo, del 8 de Julio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en una secuencia de aminoácidos de SEQ ID NO: 1, SEQ ID NO: 2 o SEQ ID NO: 3.
Péptido que tiene actividades antiinflamatoria, osteogénica y promotora del crecimiento del cabello, y uso del mismo, del 24 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que tiene actividad antiinflamatoria, que consiste en la secuencia de aminoácidos SEQ ID NO: 2.
Nueva inmunoterapia contra diversos tumores como el cáncer gastrointestinal y gástrico, del 24 de Junio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido seleccionado del grupo siguiente: a) péptido consistente en la secuencia conforme a la SEQ ID N.º 86, b) el péptido conforme a a), en la […]
Inmunoterapia WT1 para enfermedad angiogénica intraocular, del 17 de Junio de 2020, de INTERNATIONAL INSTITUTE OF CANCER IMMUNOLOGY, INC.: Una composición farmacéutica que comprende un péptido WT1 o péptido WT1 variante para su uso en el tratamiento y/o prevención de una enfermedad […]
Anticuerpos monoclonales humanizados y quiméricos para CD99, del 17 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un anticuerpo monoclonal humanizado aislado que se une específicamente a CD99 humano, y comprende: (a) una cadena ligera que comprende la secuencia de aminoácidos expuesta […]
Péptido con eficacia antiobesidad y antidiabética y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de SEQ ID NO: 1 o SEQ ID NO: 2.
Péptido que tiene actividades antiinflamatoria, osteogénica y de fomento del crecimiento del pelo, y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Péptido que tiene actividad antiinflamatoria, que consiste en secuencias de aminoácidos de SEQ ID NO: 3.