Método para la obtención de espumas de tántalo para sustitucion de tejidos duros.
Método para la obtención de espumas de tántalo para sustitución de tejidos duros.
Se presenta un método para obtener estructuras de tántalo (Ta) poroso a través del proceso de sinterización de polvos de Ta en combinación con partículas denominadas espaciadoras, adhesivos o agentes para la formación de poros. El principal objetivo de las espumas metálicas obtenidas es la aplicación para implantes sustitutivos de tejidos duros.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201230937.
Solicitante: UNIVERSITAT POLITECNICA DE CATALUNYA.
Nacionalidad solicitante: España.
Inventor/es: RUPÉREZ DE GRACIA,Elisa, MANERO PLANELLA,José María, GIL MUR,Francisco Javier, RICCARDI,Kiara, FERNÁNDEZ-FAIRÉN,Mariano.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61L27/04 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › Metales o aleaciones.
- A61L27/56 A61L 27/00 […] › Materiales porosos o celulares.
- B22F3/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B22 FUNDICION; METALURGIA DE POLVOS METALICOS. › B22F TRABAJO DE POLVOS METALICOS; FABRICACION DE OBJETOS A PARTIR DE POLVOS METALICOS; FABRICACION DE POLVOS METALICOS (fabricación de aleaciones mediante metalurgia de polvos C22C ); APARATOS O DISPOSITIVOS ESPECIALMENTE ADAPTADOS PARA POLVOS METALICOS. › Fabricación de piezas a partir de polvos metálicos, caracterizada por el modo de compactado o sinterizado; Aparatos especialmente concebidos para esta fabricación.
Fragmento de la descripción:
MÉTODO PARA LA OBTENCIÓN DE ESPUMAS DE TÁNTALO PARA SUSTITUCION DE TEJIDOS DUROS
ANTECEDENTES DE LA INVENCIÓN
La presente invención se basa en la fabricación de estructuras metálicas porosas, concretamente estructuras de Ta, destinadas a la producción de implantes o andamios para la ingeniería de tejidos. El Titanio (Ti) y algunas de sus aleaciones han sido ampliamente utilizadas como materiales para implantes ortopédicos bajo condiciones de carga debido a sus excepcionales propiedades mecánicas y biocompatibilidad. Sin embargo, la diferencia entre el módulo de Young del hueso (0.3-30 GPa) y del Ti y sus aleaciones (90-110 GPa) provoca una severa relajación de tensiones (stress shielding) lo cual conduce a la reabsorción del hueso. Para solucionar este inconveniente, es necesario reducir el módulo de Young de los biomateriales fabricados a partir de dichos metales a través de la formación de una estructura porosa, y de esta manera minimizar o eliminar el fenómeno de apantallamiento de cargas de los tejidos adyacentes al implante y eventualmente prolongar la vida útil del implante. Una estructura porosa fomenta la osteointegración entre sus poros aumentando la fijación mecánica del implante al ser los poros colonizados por el hueso neoformado. El tántalo (Ta) es un metal de transición (número atómico 73, peso atómico 180, 05) , altamente maleable y dúctil, el cual se mantiene relativamente inerte en vivo. Se ha demostrado que los implantes de Ta para aplicaciones ortopédicas presentan buena biocompatibilidad y osteointegración. Concretamente los componentes porosos de Ta, ofrecen un bajo módulo de elasticidad, un alto coeficiente de fricción y excelentes propiedades de osteointegración (por ej. bioactividad, biocompatibilidad y crecimiento) . Las propiedades mecánicas de andamios porosos de Ta (módulo de elasticidad ~3GPa) son comparables con las del hueso esponjoso, Ti, CoCr, aleaciones de acero inoxidable y otros biomateriales ortopédicos. El Ta poroso está disponible comercialmente y ha sido usado en un amplio rango de aplicaciones ortopédicas desde su introducción en 1997 incluyendo reemplazo de articulaciones, cirugía reconstructiva por tumores, fusión de la columna y para tratamiento de la necrosis avascular de la cabeza del fémur.
Dichos implantes son fabricados a través de un proceso de pirólisis de una espuma de poliuretano para crear un andamio (scaffold) de carbono vítreo seguido de la deposición química del metal. Normalmente este proceso resulta en un recubrimiento compuesto por un 99% de Ta y un 1% de carbono vítreo en peso, con un espesor variable entre 40 a 50μm y con un tamaño de poro entre 500 y 600 μm y una porosidad de 75-80% en volumen. La porosidad y tamaño de poro es superior a los recubrimientos porosos convencionales (30-40%) . Adicionalmente hay interconectividad entre los poros de la estructura 3D de Ta. Sin embargo, dentro de las limitaciones de dicho método de fabricación se encuentran el alto coste de producción asociado y la incapacidad para producir un implante completamente modular de Ta. Es por ello que en la presente patente se propone la obtención de estructuras porosas de Ta, empleando un método de pulvimetalurgia (PM) el cual es más económico y permite obtener espumas metálicas constituidas en su totalidad por Ta.
DESCRIPCIÓN DE LA INVENCIÓN
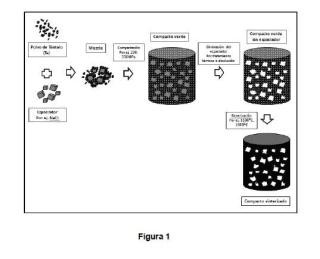
El método de PM basado en el uso de un ?space holder? o espaciador, es un proceso de fabricación en el cual se producen muestras metálicas de gran porosidad. Inicialmente se mezclan los polvos metálicos con el espaciador seleccionado, y luego esta mezcla se compacta, por ej. de forma uniaxial o isostática, para formar lo que se llama el compacto o cuerpo en verde. Posteriormente, se debe eliminar el espaciador con un tratamiento a bajas temperaturas, lo cual conlleva a una etapa inicial del sinterizado de las partículas de metal que están en contacto. Como resultado se tiene la formación inicial del cuello, seguido del sinterizado a altas temperaturas donde ocurre el crecimiento del cuello. En esta última etapa se produce la densificación de la estructura y una mejora de la integridad estructural de la pieza. Una representación esquemática del método de fabricación que se propone en la presente invención se puede observar en la Fig. 1. Partículas de polvo de Ta se mezclan con las partículas del espaciador, con o sin ayuda de una sustancia aglomerante para fomentar la unión entre partículas. Posteriormente, la mezcla de Ta y el espaciador es compactada a diferentes presiones para obtener un cuerpo en verde que luego será sometido a la eliminación del espaciador y de la sustancia aglomerante. Por último, se procede a la sinterización de la pieza.
El tamaño de las partículas de Ta que se seleccionó fue en base a la disponibilidad en el mercado de Ta de alta pureza para aplicaciones médicas. El tamaño promedio de las partículas de Ta disponible está entre 2 y 150 μm. En la aplicación de implantes para sustitución de hueso los poros son necesarios para la formación de tejido óseo ya que éstos permiten la migración y proliferación de los osteoblastos y de las células mesenquimales, así como el proceso de vascularización. De acuerdo con lo reportado en la literatura, el tamaño ideal de los poros para la formación de hueso mineralizado se encuentra entre 50 y 400 μm. De ahí que el tamaño promedio requerido del espaciador sea de (50-2000) μm, cercano al tamaño de poro que se desee obtener por réplica en la estructura metálica. Se pueden utilizar como espaciadores: NaCl, urea, carbonato de amonio de hidrógeno, polímeros como el PMMA, compuestos orgánicos, etc. Uno de los espaciadores que propone el presente método es el NaCl, el cual tiene como ventaja su alta solubilidad en agua (359 g/l a temperatura ambiente) lo cual permite eliminarlo fácilmente del compacto de Ta por medio de sucesivos lavados en agua, previos a la sinterización. Además, tiene una toxicidad muy baja, lo cual es de gran importancia si pequeñas cantidades del espaciador se quedan dentro de las espumas que serán empleadas como biomateriales en aplicaciones de implantes. Se propone también el uso de urea y partículas orgánicas como agentes espaciadores y adhesivos. La ventaja de la utilización de urea es que ésta puede ser eliminada del cuerpo en verde mediante su disolución en agua o por tratamiento térmico. Las partículas orgánicas por su parte, tienen la ventaja de que pueden ser eliminadas a temperaturas muy por debajo de la temperatura de sinterización del Ta, por ej. 400ºC. Se puede incorporar o no, un agente aglomerante (?binder?) para favorecer la unión entre las partículas de Ta previo al mezclado con el agente espaciador. Estas sustancias pueden ser: PVA, PEG, poliolefinas, parafina. El proceso de compactación, para la obtención del cuerpo en verde, puede realizarse en prensa uniaxial o isostática y a unas presiones de compactación comprendidas entre 200 y 450 MPa. Para asegurar un compacto uniforme es necesario partir de una mezcla homogénea de polvo de tántalo, espaciador y aglomerante.
Antes del proceso de sinterización se procede a eliminar el espaciador y, en su caso, el aglomerante, mediante disolución o por tratamiento térmico a bajas temperaturas, dependiendo del tipo de espaciador que se utilice. En la siguiente etapa el compacto es sinterizado para conseguir las propiedades mecánicas requeridas en un implante poroso metálico. El tratamiento térmico de sinterización se puede llevar a cabo en alto vacío (
5x10-2 Pa) . o en atmósfera inerte de argón o helio y a unas temperaturas comprendidas entre 1300ºC y 2000ºC El tiempo de sinterización puede oscilar entre 1 y 10h, dependiendo de las propiedades mecánicas requeridas. Las espumas de Tántalo pueden ser funcionalizadas superficialmente mediante la unión covalente de biomoléculas sobre el metal. Dicha funcionalización puede llevarse a cabo gracias a la fina capa de óxido metálico (3-6nm) que permite una fácil modificación química. El protocolo para la unión covalente de las biomoléculas seleccionadas al Tántalo consiste en: 1. Limpieza de la superficie en ultrasonidos con diferentes baños de ciclohexano, isopropanol y agua.
2. Activación de la superficie metálica mediante plasma de oxígeno y /o ataque ácido para producir grupos hidroxilos en superficie.
3. Proceso de silanización. Se utilizan moléculas del tipo, X-R-Si- (OR1) 3 siendo (-Si-OR1) los grupos siloxanos que se unen al metal, R la cadena alifática y X el grupo funcional que permitirá la posterior unión de las secuencias peptídicas. En este caso se utilizarán las moléculas: 3-aminopropil (trietoxi) silano (APTES) , 3cloropropil (trietoxi) silano (CPTES) y 3-glicidiloxipropil (dimetoxi)...
Reivindicaciones:
1. Un método para la elaboración de espumas metálicas de Ta que comprende las siguientes etapas:
a. Mezclado de partículas de Ta con un tamaño de partícula entre 2 y 150 μm, de pureza superior al 99, 9% y un agente espaciador (que es el causante de obtener la estructura porosa) de un tamaño medio de partícula entre 50 μm y 2.000 μm en una relación entre el 50% y el 80% de agente espaciador, preferentemente, entre un 60% y un 70% de espaciador
b. Compactación de la mezcla a presiones entre 200 y 450 MPa (obtención de los compactos en verde)
c. Eliminación del espaciador por tratamiento térmico o disolución
d. Sinterización del cuerpo en verde a una temperatura comprendida entre 1.300ºC y 2.000ºC durante, al menos, 1 hora en atmósfera inerte
o en alto vacio (
5x10-2 Pa) .
2. El método según la reivindicación 1 se caracteriza por la adición de un agente aglomerante en la etapa previa al mezclado con el agente espaciador, donde dicho agente aglomerante será del tipo PVA, PEG, poliolefinas o parafina.
3. El método según la reivindicación 1 se caracteriza porque las partículas del espaciador son del tipo: NaCl, urea o almidón.
4. El método según la reivindicación 1 permite obtener espumas de tántalo, con porosidades comprendidas entre el 50 y 80 % y caracterizadas por una estructura de poros interconectados.
5. Uso de las espumas metálicas de Ta como caja intersomática en columna vertebral.
6. El método según la R 1, caracterizado porque las espumas metálicas de Tántalo obtenidas se modifican superficialmente para ser funcionalizadas comprendiendo las siguientes etapas:
a. Limpieza de la superficie en ultrasonidos con diferentes baños de ciclohexano, isopropanol y agua.
b. Activación de la superficie metálica mediante plasma de oxígeno y /o ataque ácido para producir grupos hidroxilos en superficie.
c. La etapa de silanización en la que se utilizan moléculas del tipo, X-RSi- (OR1) 3 siendo (-Si-OR1) los grupos siloxanos que se unen al metal, R la cadena alifática y X el grupo funcional que permitirá la posterior unión de las secuencias peptídicas, que en este caso se
utilizarán las moléculas: 3-aminopropil (trietoxi) silano (APTES) , 3cloropropil (trietoxi) silano (CPTES) y 3glicidiloxipropil (dimetoxi) metilsilano (GPTES)
d. Unión covalente de secuencias cortas peptídicas con diferentes espaciadores (del tipo ácido aminohexanoico o cadenas de polietilenglicol, PEG) , unidades de ramificación para presentar varias secuencias al mismo tiempo (del tipo lisinas) y grupos de anclaje del tipo tioles.
7. El método según la reivindicación 6, caracterizado porque la unión de moléculas al producto sinterizado incluyen: péptidos, oligonucleótidos terapéuticos, antibióticos, factores de crecimiento celular, factores antiflamatorios y osteoactivos.
Figura 1
Figura 2
Patentes similares o relacionadas:
Método para producir bloques de carbonato de calcio, del 8 de Julio de 2020, de GC CORPORATION: Un método para producir un bloque de carbonato de calcio de no menos de 0,1 cm de diámetro y espesor, útil como material para proporcionar […]
Materiales cerámicos osteoinductivos moldeables e inyectables, del 24 de Junio de 2020, de NuVasive Netherlands B.V: Un material cerámico moldeable, maleable, amasable y/o inyectable que comprende fosfato de calcio poroso que tiene un tamaño de cristal de entre 0,1 y […]
Procedimiento de fabricación de un material metálico poroso para aplicaciones biomédicas, del 17 de Junio de 2020, de ALEACIONES DE METALES SINTERIZADOS, S.A: Procedimiento de obtención de una pieza de titanio poroso, caracterizado porque el polvo de titanio de partida es de pureza de calidad 2, con un tamaño de […]
Métodos y dispositivos para trasplante celular, del 10 de Junio de 2020, de Sernova Corporation: Un dispositivo para implantar células en un cuerpo huésped, que comprende: un andamio poroso que comprende al menos una cámara que tiene un extremo proximal y un extremo […]
Método para producir una matriz biocompatible con un diseño estructural dirigido, del 22 de Abril de 2020, de MedSkin Solutions Dr. Suwelack AG: Un método para la producción de una matriz biocompatible, donde el método comprende: a) proveer una composición que comprende al menos un biopolímero; […]
Estructuras para trasplante celular, del 15 de Abril de 2020, de PRESIDENT AND FELLOWS OF HARVARD COLLEGE: Un dispositivo que comprende una composición de estructura que presenta macroporos abiertos e interconectados, y que es capaz de controlar en el tiempo […]
Espumas de fibroína de seda inyectables y usos de la misma, del 1 de Abril de 2020, de TRUSTEES OF TUFTS COLLEGE: Un aplicador de inyección que comprende una composición inyectable, la composición inyectable comprende una espuma de fibroína de seda comprimida que tiene […]
Válvula cardíaca protésica que comprende compuestos polímeros duraderos de elevada resistencia adecuados para implantar, del 1 de Abril de 2020, de W.L. GORE & ASSOCIATES, INC.: Una válvula, que comprende: una estructura de soporte, y estando soportada al menos una valva sobre la estructura de soporte y móvil entre las posiciones […]