Procedimiento e instrumento de medición no invasiva de la oxigenación/saturación de tejido biológico.
Un procedimiento para la medida no invasiva del estado de la oxigenación/saturación de un tejido humano o animal (TS) que tiene una concentración de agua dada,
tal como, el cerebro o un músculo, que comprende, tras la elección del tejido a analizar, las etapas:
-proporcionar un instrumento para la medición no invasiva de la oxigenación/saturación de tejido biológico que comprende al menos una fuente óptica (OS) que genera radiaciones luminosas de intensidad continua, una sonda óptica (OP) que comprende un emisor (E) para llevar las radiaciones de luz generadas por al menos una fuente óptica (OS) en una parte del tejido (TS) y un receptor (R) para recibir las radiaciones retrodispersadas del tejido, una unidad receptora (RU) usada para convertir y amplificar una señal óptica procedente de dicho receptor (R) en una señal eléctrica de salida (MIS), en el que la unidad receptora (RU) es un subsistema electrónico para detectar señales ópticas de bajo nivel y comprende un fotodetector (PD) para la conversión de radiaciones ópticas que proceden del tejido al receptor (R) en una señal de corriente proporcional a ellas, un preamplificador (PREAMPLI) para convertir y amplificar la corriente en una señal de tensión, y un bloque de procesamiento analógico (SHAPER) adaptado para filtrar y maximizar la proporción de señal frente a ruido y suministrar una señal de salida proporcional a la intensidad óptica retrodispersada del tejido y que comprende un circuito de ajuste de ganancia para el ajuste automático de la ganancia para adaptar el instrumento para medir tejidos con diferentes niveles de absorción, y un circuito de compensación adaptado para minimizar el efecto de luz externa en tiempo real añadiendo una señal igual a ella, pero de signo opuesto, y una etapa de integración sincronizada con la propia señal, una unidad de control electrónica (CU) adaptada para gestionar las temporizaciones, señales medidas y una interfaz de un ordenador personal externo (PC) a través de un software para el procesamiento de las señales eléctricas recibidas
para obtener niveles absolutos de la oxigenación del tejido;
- configurar y ajustar el instrumento de acuerdo con el tipo de tejido:
- poner el emisor (E) y receptor (R) de la sonda óptica (OP) en contacto con el tejido (TS);
- comenzar el ciclo de medida usando una señal apropiada;
- el emisor (E) que emite radiaciones luminosas a una intensidad óptica dada y al menos a tres diferentes longitudes de onda en el espectro de infrarrojo cercano, donde al menos una es 980 nm, correspondiente a un pico de absorción de agua para una iluminación localizada del tejido;
- el circuito de ajuste de ganancia que ajusta automáticamente la ganancia electrónica por medio de un potenciómetro digital, para adaptar la sensibilidad del instrumento al nivel de absorción del tejido examinado, y compensar el desplazamiento por medio de dicho circuito de compensación, para minimizar la intensidad de luz externa añadiendo una señal igual a esta, pero de signo opuesto,
- el receptor (R) que recibe las radiaciones luminosas retrodispersadas del tejido a una distancia establecida de la zona iluminada;
- transformar la radiación retrodispersada detectada en una señal eléctrica por medio de dicho fotodetector (PD) y amplificar la señal eléctrica por medio de dicho preamplificador de bajo nivel de ruido (PREAMPLI); la unidad de control electrónica (CU):
- calcular la absorción óptica, expresada en densidad óptica, para cada longitud de onda dependiendo de la intensidad óptica incidente sobre el tejido y
retrodispersar la intensidad óptica;
- calcular la reflectancia para cada longitud de onda de la radiaciones emitidas;
- multiplicar cada reflectancia por una constante dependiendo del tipo de receptor;
- calcular el coeficiente de absorción a los 980 nm de longitud de onda, de acuerdo con la concentración y coeficiente de absorción específicos del agua;
- calcular el nivel de reflectancia de acuerdo con la teoría migración de fotones en tejidos y con dependencia de su dispersión en el interior del tejido;
- invertir el procedimiento de calcular la reflectancia en base al coeficiente y la reflectancia medida a la longitud de onda de 980 nm para recuperar el coeficiente de difusión (dispersión) en el tejido a dicha longitud de onda;
- usar el coeficiente de dispersión calculado para deducir el coeficiente de dispersión de las demás longitudes de onda también;
invertir el procedimiento de cálculo de la reflectancia sobre la base del coeficiente de dispersión calculado y la reflectancia medida para cada longitud de onda para recuperar el coeficiente de absorción para cada longitud de onda;
- calcular las concentraciones absolutas de oxihemoglobina y desoxihemoglobina, de acuerdo con la ley de Lambert-Beer usando el coeficiente de absorción calculado previamente;
- calcular la concentración absoluta de hemoglobina total como una suma de las concentraciones de oxígeno en hemoglobina y desoxihemoglobina y el índice de oxigenación del tejido como la proporción de la concentración de oxihemoglobina frente a la concentración de hemoglobina total;
- memorizar y posiblemente visualizar en tiempo real en la pantalla de un ordenador personal (PC) las concentraciones calculadas.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IT2008/000649.
Solicitante: NIROX S.R.L.
Nacionalidad solicitante: Italia.
Dirección: PIAZZA MARTIRI DELLA RESISTENZA 2 25010 ACQUAFREDDA (BS) ITALIA.
Inventor/es: ROVATI, LUIGI, DONINI,MAURIZIO, BANDERA,ANDREA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B5/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › Medidas encaminadas a establecer un diagnóstico (diagnóstico por medio de radiaciones A61B 6/00; diagnóstico por ondas ultrasónicas, sónicas o infrasónicas A61B 8/00 ); Identificación de individuos.
PDF original: ES-2541500_T3.pdf
Fragmento de la descripción:
Procedimiento e instrumento de medición no invasiva de la oxigenación/saturación de tejido biológico Campo de la invención
La presente invención se refiere al sector de equipos de diagnóstico y, en particular, se refiere a un instrumento no invasivo para medir la oxigenación, que es la relación entre la concentración de oxihemoglobina y desoxihemoglobina en tejido biológico, en particular en el cuerpo humano.
Estado de la técnica
En general, para evaluar el estado del tejido humano, tal como, por ejemplo, el cerebro o un músculo, también es Importante conocer el nivel de oxigenación. En este sentido, ya se encuentran disponibles Instrumentos para medir la oxigenación de tejidos.
El factor Importante reside en que el examen a llevar a cabo no sea Invasivo. Una técnica de medida está representada mediante la NIRS (espectroscopia de infrarrojo cercano), que consiste en ¡luminar un tejido con una fuente de luz con longitudes de onda en el intervalo espectral en el infrarrojo cercano (6-1 OOOnm), en detectar la luz difundida por el tejido por medio de un receptor y procesar estos datos para calcular la concentración de oxihemoglobina, hemoglobina desoxigenada y, de esta manera, obtener el estado de oxigenación de un tejido. Esta técnica está basada en la transparencia natural de los tejidos frente a la luz en la región NIR, combinada con el hecho de que los tejidos contienen una serie de cromóforos, que son sustancias que absorben la intensidad de la luz, de interés fisiológico con características de absorción óptica que son diferentes entre sí. En particular, los cromóforos de gran interés son agua, lípidos, oxihemoglobina y desoxihemoglobina. Mientras que algunos de estos, al parecer, son constantes durante un breve periodo, hemoglobina, tanto desoxihemoglobina como oxihemoglobina, tiene una concentración fuertemente relacionada con el metabolismo de tejidos. La luz que incide penetra en los tejidos y experimenta dos procesos principales: difusión (dispersión) y absorción, dependiendo ambos de la longitud de onda de la luz. En la banda espectral de NIR, es dominante la dispersión en comparación con la absorción, lo que se debe principalmente a la hemoglobina.
Sin embargo, la oxihemoglobina y desoxihemoglobina tienen diferentes espectros de absorción en el NIR, lo que posibilita a las dos formas de hemoglobina medirse de manera independiente; una vez que se ha cuantificado la hemoglobina, se puede determinar el nivel de oxigenación del tejido.
Dado lo anterior, la elección del algoritmo correcto a utilizar para interpretar los datos y, por consiguiente, los procedimientos de calibración y ejecución de los instrumentos, es muy importante.
Los instrumentos de NIRS, dependiendo del enfoque tecnológico, difieren en las siguientes tipologías:
Intensidad continua (CW): el tejido se ilumina a diferentes longitudes de onda y/o diferentes distancias fuente-receptor que mantienen constante la potencia emitida (Fig. 1 a);
Intensidad modulada o dominio-frecuencia (FD): la luz incidente sobre el tejido se modula en amplitud a frecuencias de entre 1-2 MHz (Fig. 1 b);
Tiempo-dominio (TD): el tejido se ilumina mediante impulsos que tiene una duración temporal del orden de picosegundos (Fig. 1c).
Las elecciones tecnológicas TD y FD, que permiten incluso llevar a cabo una medida directa de los coeficientes de absorción y dispersión y una medida cuantitativa de las concentraciones de oxihemoglobina, desoxihemoglobina e índice de oxigenación del tejido, están caracterizadas por una gran complejidad de ejecución.
La instrumentación para CW, por otro lado, no permite por sí misma la medición directa del coeficiente de absorción y dispersión; sin embargo, puesto que este enfoque es el más fácil de llevar a cabo, a fin de lograr una medida cuantitativa han aparecido diferentes enfoques; tales como:
sistemas multidistancia, que usa más distancias desde la fuente y el receptor para medir nivel de oxigenación,
sistemas de derivadas, que realizan las segundas derivadas en el espectro de absorción para eliminar la contribución de dispersión.
Sin embargo, el primer enfoque está sometido a errores debido a la heterogénea estructura de los tejidos, mientras que con el segundo enfoque no es posible medir la concentración absoluta de oxihemoglobina y desoxihemoglobina.
También se conoce el procedimiento del pico de absorción que está basado en el hecho de que la absorción de la luz que entra en el tejido y tiene determinadas longitudes de onda, por ejemplo, 98 nm, está principalmente dominado por agua. Sin embargo, este procedimiento se ha teorizado para calcular únicamente los cambios de concentraciones de oxihemoglobina y desoxihemoglobina y no su cuantificación.
El documento US-A-5 72 284 aborda un aparato para medir hemoglobina en el que la luz de diversas longitudes de onda emitida desde fuentes de luz se transmite, sin embargo, a través de tejidos vitales y se convierte en señales eléctricas para calcular los valores de términos de tejido y la concentración de hemoglobina.
El documento US26/214 A1 da a conocer un procedimiento para mediciones ópticas de parámetros deseados de la sangre del paciente efectuado, sin embargo, creando un estado de cese de flujo sanguíneo dentro de la región de medida, durante un periodo de tiempo, y continuando, en dicho periodo de tiempo, con sesiones de medición, cada una de las cuales al menos incluye dos mediciones con diferentes longitudes de onda de luz incidente.
El objeto de la presente invención es proponer un instrumento y un procedimiento para la cuantificación no invasiva de la concentración de oxihemoglobina y hemoglobina desoxigenada; proporcionando, de esta manera, una medición de la oxigenación/saturación de tejidos biológicos de una manera precisa y a un coste reducido.
Un objetivo adicional es proponer un instrumento particularmente, pero no únicamente, para medir la oxigenación de un músculo, que puede ofrecer una medición cuantitativa del curso de dicha oxigenación, más indicaciones con respecto a la acumulación de ácido láctico.
Dichos objetivos y ventajas implícitas que derivan de ellos se logran por medio de un instrumento no invasivo para la medida de la oxigenación/saturación de un tejido biológico de acuerdo con la reivindicación 2 por un procedimiento de medida de acuerdo con la reivindicación 1.
Breve descripción de los dibujos
Sin embargo, la invención se ilustrará en más detalle en la descripción que sigue, hecha en referencia a los dibujos adjuntos indicativos y no restrictivos, en los que:
Las fig. 1a, b y c son indicativas de la tecnología del estado de la técnica mencionado anteriormente;
La Fig. 2 es un diagrama de flujo de los instrumentos de medida de acuerdo con la invención;
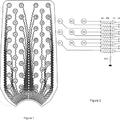
La Fig. 3 es un diagrama de flujo de la fuente óptica;
La Fig. 4 es una vista esquemática de la sonda óptica;
La Fig. 5 es un diagrama de flujo de la unidad de recepción;
La Fig. 6 es una representación esquemática del ciclo de medida;
La Fig. 7 es un diagrama de flujo del software de control;
La Fig. 8 es un ejemplo de una traza como se visualiza en un PC; y La Fig. 9 muestra un subpaquete de datos.
Descripción detallada de la invención
De acuerdo con la invención, la teoría del pico de absorción del agua se adoptó en el estudio de la oxigenación de un tejido, llevada a cabo mediante un instrumento optoelectrónico, que, en asociación con una parte de hardware y software de procesamiento de datos y pilotaje relativo puede medir la absorción óptica característica de un material a determinadas longitudes de onda que pertenecen al espectro de infrarrojo cercano (NIR). A partir de estas medidas y en el campo de aplicación particular de tejido biológico (muscular y cerebral), por medio de un procesamiento oportuno de los datos recibidos, se pude obtener un nivel absoluto de la concentración de oxihemoglobina (HbCh) y desoxihemoglobina (Hb), que posibilita establecer y visualizar en tiempo real la oxigenación/saturación de un tejido.
En un ejemplo de una ejecución, tal como la mostrada en la Fig. 2, el instrumento está compuesto básicamente de:
una fuente óptica que genera radiación NIR a una intensidad continua necesaria para la medida;
una sonda óptica que dirige, por medio de una fibra de inyección óptica, la luz generada por la fuente en el tejido
y recibe, por medio de una guía de luz, la luz que abandona el tejido que se está midiendo
Una unidad receptora óptica que convierte la luz procedente del tejido en una señal eléctrica y la amplifica correctamente;
una... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para la medida no invasiva del estado de la oxigenación/saturación de un tejido humano o animal (TS) que tiene una concentración de agua dada, tal como, el cerebro o un músculo, que comprende, tras la elección del tejido a analizar, las etapas:
-proporcionar un instrumento para la medición no invasiva de la oxigenación/saturación de tejido biológico que comprende al menos una fuente óptica (OS) que genera radiaciones luminosas de intensidad continua, una sonda óptica (OP) que comprende un emisor (E) para llevar las radiaciones de luz generadas por al menos una fuente óptica (OS) en una parte del tejido (TS) y un receptor (R) para recibir las radiaciones retrodispersadas del tejido, una unidad receptora (RU) usada para convertir y amplificar una señal óptica procedente de dicho receptor (R) en una señal eléctrica de salida (MIS), en el que la unidad receptora (RU) es un subsistema electrónico para detectar señales ópticas de bajo nivel y comprende un fotodetector (PD) para la conversión de radiaciones ópticas que proceden del tejido al receptor (R) en una señal de corriente proporcional a ellas, un preamplificador (PREAMPLI) para convertir y amplificar la corriente en una señal de tensión, y un bloque de procesamiento analógico (SHAPER) adaptado para filtrar y maximizar la proporción de señal frente a ruido y suministrar una señal de salida proporcional a la intensidad óptica retrodispersada del tejido y que comprende un circuito de ajuste de ganancia para el ajuste automático de la ganancia para adaptar el instrumento para medir tejidos con diferentes niveles de absorción, y un circuito de compensación adaptado para minimizar el efecto de luz externa en tiempo real añadiendo una señal igual a ella, pero de signo opuesto, y una etapa de integración sincronizada con la propia señal, una unidad de control electrónica (CU) adaptada para gestionar las temporizaciones, señales medidas y una interfaz de un ordenador personal externo (PC) a través de un software para el procesamiento de las señales eléctricas recibidas
para obtener niveles absolutos de la oxigenación del tejido;
-configurar y ajustar el instrumento de acuerdo con el tipo de tejido:
- poner el emisor (E) y receptor (R) de la sonda óptica (OP) en contacto con el tejido (TS);
-comenzar el ciclo de medida usando una señal apropiada;
-el emisor (E) que emite radiaciones luminosas a una intensidad óptica dada y al menos a tres diferentes longitudes de onda en el espectro de infrarrojo cercano, donde al menos una es 98 nm, correspondiente a un pico de absorción de agua para una iluminación localizada del tejido;
-el circuito de ajuste de ganancia que ajusta automáticamente la ganancia electrónica por medio de un potenciómetro digital, para adaptar la sensibilidad del instrumento al nivel de absorción del tejido examinado, y compensar el desplazamiento por medio de dicho circuito de compensación, para minimizarla intensidad de luz externa añadiendo una señal igual a esta, pero de signo opuesto,
-el receptor (R) que recibe las radiaciones luminosas retrodispersadas del tejido a una distancia establecida de la zona iluminada;
-transformarla radiación retrodispersada detectada en una señal eléctrica por medio de dicho fotodetector (PD) y amplificar la señal eléctrica por medio de dicho preamplificador de bajo nivel de ruido (PREAMPLI); la unidad de control electrónica (CU):
-calcular la absorción óptica, expresada en densidad óptica, para cada longitud de onda dependiendo de la intensidad óptica incidente sobre el tejido y
retrodispersar la intensidad óptica;
-calcular la reflectancia para cada longitud de onda de la radiaciones emitidas;
- multiplicar cada reflectancia por una constante dependiendo del tipo de receptor;
-calcular el coeficiente de absorción a los 98 nm de longitud de onda, de acuerdo con la concentración y coeficiente de absorción específicos del agua;
-calcular el nivel de reflectancia de acuerdo con la teoría migración de fotones en tejidos y con dependencia de su dispersión en el interior del tejido;
-invertir el procedimiento de calcular la reflectancia en base al coeficiente y la reflectancia medida a la longitud de onda de 98 nm para recuperar el coeficiente de difusión (dispersión) en el tejido a dicha longitud de onda;
-usar el coeficiente de dispersión calculado para deducir el coeficiente de dispersión de las demás longitudes de onda también;
-invertir el procedimiento de cálculo de la reflectancia sobre la base del coeficiente de dispersión calculado y la reflectancia medida para cada longitud de onda para recuperar el coeficiente de absorción para cada longitud de onda;
-calcular las concentraciones absolutas de oxihemoglobina y desoxihemoglobina, de acuerdo con la ley de Lambert-Beer usando el coeficiente de absorción calculado previamente;
-calcular la concentración absoluta de hemoglobina total como una suma de las concentraciones de oxigeno en hemoglobina y desoxihemoglobina y el índice de oxigenación del tejido como la proporción de la concentración de oxihemoglobina frente a la concentración de hemoglobina total;
-memorizar y posiblemente visualizar en tiempo real en la pantalla de un ordenador personal (PC) las concentraciones calculadas.
2. Un instrumento para la medición no invasiva del estado de la oxigenación/ saturación de tejido biológico bien de un tejido humano o animal, tal como, el cerebro o un músculo, mediante el procedimiento de acuerdo con la reivindicación 1, que comprende al menos una fuente óptica (OS) que genera radiaciones luminosas de intensidad continua, una sonda óptica (OP) que comprende un emisor (E) para llevar las radiaciones de luz generadas por al menos una fuente óptica (OS) en una parte del tejido y un receptor (R) para recibir las radiaciones retrodispersadas del tejido, una unidad receptora (RU) usada para convertir y amplificar la señal óptica procedente de dicho receptor (R) en una señal eléctrica de salida (MIS), en el que la unidad receptora (RU) es un subsistema electrónico para detectar señales ópticas de bajo nivel y comprende un fotodetector (PD) para la conversión de radiaciones ópticas que proceden del tejido al receptor (R) en una señal de corriente proporcional a ellas, un preamplificador (PREAMPLI) para convertir y amplificar la corriente en una señal de tensión, y un bloque de procesamiento analógico (SHAPER) adaptado para filtrar y maximizar la proporción de señal frente a ruido y suministrar una señal de salida proporcional a la intensidad óptica retrodispersada del tejido y que comprende un circuito de ajuste de ganancia para el ajuste automático de la ganancia para adaptar el instrumento para medir tejidos con diferentes niveles de absorción, y un circuito de compensación adaptado para minimizar el efecto de luz externa en tiempo real añadiendo una señal igual a ella, pero de signo opuesto, y una etapa de integración sincronizada con la propia señal, una unidad de control electrónica (CU) adaptada para gestionar las temporizaciones, señales medidas y una interfaz de un ordenador personal externo (PC) a través de un software para el procesamiento de las señales eléctricas recibidas para obtener niveles absolutos de la oxigenación del tejido para visualizar en tiempo real los niveles absolutos obtenidos, en el que la fuente óptica (OS) está compuesta de al menos tres módulos ópticos independientes (LD1 +C1, LD2+C2,...,LDn+Cn) para la emisión de diferentes radiaciones luminosas respectivas con longitudes de onda que pertencen al espectro de infrarrojo cercano, donde al menos una de dichas radiaciones se corresponde con un pico de absorción de agua a 98 nm, y donde el emisor (E) y receptor (R) están a una distancia fijada de acuerdo con el nivel de potencia de la fuente óptica.
3. Un instrumento de acuerdo con la reivindicación 2, en el que la fuente óptica (OS) comprende cuatro módulos ópticos independientes, siendo dos de los cuales para emisión de radiaciones luminosas con longitudes de onda correspondientes con picos de absorción de agua respectivos y siendo dos de los cuales para una emisión de radiación de luz respectiva con longitudes de onda no correspondientes con los picos de absorción de agua.
4. Un instrumento de acuerdo con las reivindicaciones 2 o 3, en el que cada módulo óptico de la fuente óptica (OS) comprende un diodo láser (LD), controlado por una seña digital, un acoplador óptico (C) para acoplar las señales ópticas generadas en una fibra óptica (OF), para enviar todas las señales que abandonan cada módulo a un único punto, y un sistema para medir la potencia óptica generada para suministrar una señal de tensión de salida proporcional a la unidad de control electrónica (CU).
5. Un instrumento de acuerdo con una cualquiera de las reivindicaciones 2 a 4, en el que el receptor (R) incluye una guía de luz líquida (LG) para incrementar el área de recepción y sensibilidad del instrumento.
6. Un instrumento de acuerdo con cualquiera de las reivindicaciones 2 a 5, en el que el emisor y receptor ópticos están sobre el mismo soporte y la fuente óptica y la unidad receptora están colocadas en el interior de la sonda óptica, comunicándose la unidad receptora con la unidad de control electrónica por medio de una conexión alámbrica o inalámbrica.
7. Un instrumento de acuerdo con una cualquiera de las reivindicaciones 2 a 6, para su uso, en combinación con dispositivos de visualización y/o dispositivos de alarma acústicos y/o visuales indicativos de niveles extremos de la evolución de oxigenación, en el seguimiento de la evolución de oxigenación incluso en tiempo real durante una actividad deportiva.
Patentes similares o relacionadas:
Sistema y procedimiento para evaluar el riesgo asociado con un estado de glucosa, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un dispositivo informático configurado para realizar un procedimiento de análisis de un estado de glucosa, comprendiendo el procedimiento: identificar, […]
Procedimiento y aparato para proporcionar el procesamiento y control de datos en un sistema de comunicación médica, del 29 de Julio de 2020, de ABBOTT DIABETES CARE INC: U procedimiento, que comprende: ejecutar, en una unidad receptora , una rutina predeterminada asociada con una operación de un dispositivo de monitorización […]
 Dispositivo sensor para detección de señales bioeléctricas, del 29 de Julio de 2020, de CorTec GmbH: Dispositivo sensor para detectar senales bioelectricas y para implantar dentro o fuera de un cerebro, el dispositivo sensor que comprende […]
Dispositivo sensor para detección de señales bioeléctricas, del 29 de Julio de 2020, de CorTec GmbH: Dispositivo sensor para detectar senales bioelectricas y para implantar dentro o fuera de un cerebro, el dispositivo sensor que comprende […]
FUNDA ELECTRÓNICA PARA ADAPTACIÓN DE DISPOSITIVOS MÓVILES CON INSTRUMENTOS DE DIAGNÓSTICO MÉDICO MULTIDISCIPLINAR, del 27 de Julio de 2020, de RUESGA DELGADO,OSCAR: Funda electrónica para adaptación de dispositivos móviles con instrumentos de diagnóstico médico multidisciplinar que comprende una funda de uso electrónico […]
Cama eléctrica, del 8 de Julio de 2020, de Keeson Technology Corporation Limited: Una cama eléctrica, que comprende una estructura de cama, una pluralidad de láminas de cama, un dispositivo de despertador, un reloj y una caja de control […]
SÍSTEMA Y MÉTODO PARA EL TRATAMIENTO DE ADICCIONES DE UN INDIVIDUO QUE LO NECESITE, CON BAJAS TASAS DE RELAPSO, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención corresponde a un sistema, más particularmente a un sistema NFB, y método, que permite el tratamiento de adicciones en las que está […]
Aparato y método de algometría humana, del 1 de Julio de 2020, de The Children's Research Institute: Un método implementado por el procesador para medir objetivamente el dolor que comprende: aplicar estimulación eléctrica de una intensidad específica […]
MAMÓGRAFO ÓPTICO QUE UTILIZA INFRARROJO CERCANO EN GEOMETRÍA DE REFLECTANCIA DIFUSA, del 25 de Junio de 2020, de CONSEJO NACIONAL DE INVESTIGACIONES CIENTIFICAS Y TECNICAS (CONICET) (33.3%): Un dispositivo formador de imágenes mamográficas para análisis y detección de posibles inhomogeneidades en el tejido mamario de una paciente usando […]