EVALUACIÓN EN TIEMPO REAL DE DOSIS DE NEUTRONES EN PACIENTES EN TRATAMIENTO CON RADIOTERAPIA Y DETECTOR PARA LLEVAR A CABO EL PROCEDIMIENTO.
Evaluación en tiempo real de dosis de neutrones en pacientes en tratamiento con radioterapia y detector para llevar a cabo el procedimiento.
Procedimiento y detector para calcular las dosis equivalentes de neutrones en órganos de un paciente y el riesgo asociado de inducción de cánceres secundarios mediante neutrones en radioterapia con fotones. El cálculo se realiza relacionando dosis en detectores colocados en diferentes posiciones en un maniquí antropomorfo y los eventos de efecto único en un dispositivo semiconductor colocado en la sala de tratamiento. El método permite un procedimiento sencillo y universal de estimación del riesgo de cáncer secundario a partir de las lecturas en tiempo real de un dispositivo electrónico.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201130932.
Solicitante: UNIVERSIDAD DE SEVILLA.
Nacionalidad solicitante: España.
Inventor/es: GOMEZ RODRIGUEZ,FAUSTINO, SÁNCHEZ DOBLADO,Francisco, DOMINGO MIRALLES,Carlos, MARIN MUÑOZ,Jesus.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61N5/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61N ELECTROTERAPIA; MAGNETOTERAPIA; RADIOTERAPIA; TERAPIA POR ULTRASONIDOS (medida de corrientes bioeléctricas A61B; instrumentos quirúrgicos, dispositivos o métodos para transferir formas no mecánicas de energía hacia o desde el cuerpo A61B 18/00; aparatos de anestesia en general A61M; lámparas incandescentes H01K; radiadores de infrarrojos utilizados como calefactores H05B). › Radioterapia (dispositivos o aparatos aplicables a la vez a la terapia y al diagnóstico A61B 6/00; aplicación de material radiactivo al cuerpo A61M 36/00).
Fragmento de la descripción:
EVALUACIÓN EN TIEMPO REAL DE DOSIS DE NEUTRONES EN PACIENTES EN TRATAMIENTO CON RADIOTERAPIA Y DETECTOR PARA LLEVAR A CABO EL PROCEDIMIENTO
CAMPO DE LA INVENCIÓN La presente invención se refiere a la metodología de la radioterapia, en particular a métodos para evaluar las dosis de radiación de un paciente durante el tratamiento.
ESTADO DE LA TÉCNICA La radioterapia representa una de las herramientas más útiles disponibles para curar el cáncer, junto con la cirugía y la quimioterapia.
En muchos de los procedimientos de terapia con radiación, la dosis periférica no deseada se debe a fotones y neutrones. Aunque las dosis de fotones se han estudiado en profundidad, la contaminación con neutrones de haces de fotones de alta energía todavía es objeto de investigación y discusión.
La emisión de neutrones se produce esencialmente en materiales de alta Z (W, Pb, Fe, Cu, etc.) en los componentes de cabezal de acelerador (blanco, filtro de aplanador, mordazas, colimadores, imán de desviación, blindaje, etc.) mediante reacción electronuclear (e, e', n) y fotonuclear (y, n) como consecuencia de la presencia de fotones en el haz con mayor energía que el umbral de reacción fotonuclear.
La medición de la fluencia de neutrones dentro de una sala de radioterapia es una tarea difícil. Por tanto, no resulta fácil cuantificar la producción de neutrones en radioterapia: los detectores pasivos (es decir, activación de oro, TLD, detectores de trazas, etc.) requieren un tiempo considerable para el procesamiento, el análisis y la evaluación, mientras que para los contadores activos (es decir, centelleadores de BF3, 3 He, 6 Lil) , la acumulación y saturación de la señal debido a la radiación pulsada de los aceleradores médicos dificulta la separación de la contribución de neutrones inmersos en un campo de fotones pulsado de elevada fluencia. Por tanto, el riesgo radiológico asociado con los neutrones producidos durante el tratamiento no se evalúa habitualmente cuando se elige la mejor estrategia que implica la menor cantidad de riesgo para el paciente. Por tanto, existe una necesidad de nuevos métodos de determinación de las dosis equivalentes de neutrones recibidas en órganos relevantes en tiempo real.
RESUMEN DE LA INVENCIÓN
El procedimiento y dispositivo de la invención permite una estimación de las dosis equivalentes de neutrones en órganos de un paciente y el riesgo asociado de inducción de cánceres secundarios mediante neutrones en radioterapia con fotones. El detector usado no provoca interferencia con los pacientes y puede usarse fácilmente en la práctica diaria. A pesar de la complejidad del problema, el procedimiento es sencillo y universal. En consecuencia, las dosis equivalentes de neutrones en órganos de pacientes que se someten a tratamientos con radioterapia pueden estimarse en cualquier instalación, a partir de las lecturas del dispositivo digital y usando el modelo desarrollado, sin ninguna medición adicional de la radiación. El procedimiento para calcular las dosis equivalentes sigue las etapas de:
a. colocar un maniquí antropomorfo enfrente de un dispositivo de radiación, estando dotado el maniquí de dosímetros de neutrones pasivos en ubicaciones predeterminadas,
b. calcular las dosis en los detectores teniendo en cuenta la distribución de energía de fluencia de neutrones mediante una simulación de Monte Cario,
c. interpolar las dosis usando el modelo de Christy-Eckermann a las posiciones reales de los órganos.
El dispositivo comprende una pluralidad de celdas de memoria que tienen una capa dieléctrica de vidrio de borofosfosilicato (BPSG) en la disposición del chip adaptadas para que cada memoria almacene un nivel lógico que cambia debido a la interacción de un neutrón térmico.
Pueden encontrarse ventajas adicionales de la invención en las reivindicaciones dependientes.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
Para completar la descripción y con el fin de proporcionar una mejor comprensión de la invención, se proporciona un conjunto de dibujos. Dichos dibujos ilustran una realización preferida de la invención, que no debe interpretarse como restrictiva del alcance de la invención sino tan sólo como un ejemplo de cómo puede llevarse a cabo la invención. Los dibujos comprenden las siguientes figuras:
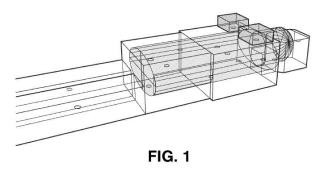
Figura 1. es un modelo de un maniquí antropomorfo usado en la medida y cálculo de la dosis de neutrones Figuras 2a y 2b. muestran las posiciones de los detectores con respecto a un modelo de los órganos. Figura 3. es un gráfico que muestra los cálculos para determinar un factor de corrección para el tamaño de búnker (sala de tratamiento) .DESCRIPCIÓN DE LA INVENCIÓN
El detector de la invención es realmente una pluralidad de detectores que corresponden a cada celda de memoria de un dispositivo semiconductor digital. Cada celda de la memoria almacena un nivel lógico (bit) que puede cambiar debido a la interacción de una partícula con los materiales del componente semiconductor, produciendo suficiente ionización a partir de los procesos posteriores. Este proceso se conoce como efecto de un único evento (SEE, "Single Event Effecf') .
El detector consiste en una pluralidad de chips, por ejemplo 128 con una memoria total de 64 MiB. Los componentes de memoria se seleccionan para que tengan una capa dieléctrica de vidrio de borofosfosilicato (BPSG) en la disposición del chip de manera que sean sensibles a neutrones térmicos. Preferiblemente, deben considerarse dispositivos que muestran BPSG en proximidad estrecha al sustrato de silicio. El mecanismo responsable es la captura de neutrones a partir del isótopo 10B que constituye el 20% del boro natural. El boro se usa comúnmente en semiconductores como dopante de tipo p y especie de implante en silicio, y también en la composición de la capa dieléctrica de vidrio de borofosfosilicato (BPSG) (2-8% en peso) . La sección eficaz de la captura de neutrones de 10B se comporta como 1/v, donde v representa la velocidad de los neutrones. Por tanto, no es necesario considerar neutrones rápidos.
El detector se coloca dentro de la sala de radioterapia y se controla con un ordenador a través de una conexión en serie. Antes de cada irradiación, se ajusta el contenido de la memoria a un patrón fijado. Después de eso, se lee el contenido de la memoria y se calcula la cantidad de SEE. El dispositivo digital se ubica próximo al eje de giro principal del acelerador (gantr y en inglés) enfrente del acelerador lineal, normalmente cerca de la pared de la sala. De este modo, no interfiere con los tratamientos de radioterapia y resulta independiente del ángulo con el eje de giro principal. El sistema muestra que el número de eventos tiene una repetibilidad (desviación estándar relativa) de aproximadamente el 2% para irradiaciones de 1000 unidades monitor (UM a 15 MV con un campo de (1 O x 1O) cm2) . También presenta una excelente linealidad, ya que las lecturas promedio presentan una desviación relativa a partir de una regresión lineal con UM del acelerador lineal menor del 1%. El dispositivo es básicamente insensible a los fotones mientras que el tamaño de memoria y funcionamiento produce una sensibilidad a neutrones del sistema suficiente para medir la intensidad de producción de neutrones del acelerador mediante disparos de 1000-2000 UM con baja incertidumbre estadística que garantiza la linealidad y el funcionamiento fiable.Un maniquí antropomorfico (figura 1) permite adquirir un conjunto de mediciones que se asemejan a la dosis en el paciente. La mejor elección del material (madera de baja densidad para los pulmones y polietileno para el resto del cuerpo) se basa en los ensayos llevados a cabo con otros maniquíes (construidos en nylon, inyectando urea al polietileno, tejidos y órganos reales procedente de porcino, etc.) para conocer la repercusión de elementos, tales como el nitrógeno o la proporción de hidrógeno respecto a los tejidos humanos. Se eligen dieciséis ubicaciones estratégicas en el maniquí para realizar las mediciones de la fluencia de neutrones con dosímetros de neutrones pasivos, que permiten evaluar los valores equivalentes de dosis en esos puntos, ubicados a profundidades variables. Se construye una cavidad adecuada para los detectores pasivos en cada ubicación.
La evaluación de los equivalentes de dosis de neutrones en todos los puntos especificados permite estimar las dosis equivalentes de neutrones en todos los órganos o tejidos de relevancia del paciente, seleccionados para su radioprotección: cerebro, tiroides, mamas, pulmones, esófago, estómago, hígado, vesícula biliar, colon (ascendente, descendente, transversal y sigmoide) , ovarios, testículos, así como huesos y médula ósea roja. Puesto...
Reivindicaciones:
1. Procedimiento de evaluación del riesgo de adquirir un segundo tumor maligno tras un tratamiento con radioterapia debido a la radiación de neutrones, en el que la evaluación se realiza mediante la fórmula
R (Oi) = E · C · B · DE (Oi) · S · RN (Oi)
en la que E es un número de efectos de un único evento en un dispositivo semiconductor, C es un factor de calibración, B es un factor de corrección debido al tamaño de búnker facilitado por la fórmula 10
B = 1/F
F=P1+P2/s
siendo P1 = 0, 396 ± 0, 027m2, P2 = 37, 3 ± 1, 1m2, F la fluencia de neutrones térmicos 15 normalizada y s la superficie del suelo de la sala, RN es un coeficiente de riesgo normalizado, S es el número de sesiones de tratamiento y en la que DE es una dosis equivalente por evento en un órgano determinado (Oi) calculada según el siguiente procedimiento:
a. colocar un maniquí antropomórfico de polietileno y madera enfrente de un dispositivo 20 de radiación con acelerador lineal, estando dotado el maniquí de dosímetros de neutrones pasivos en ubicaciones predeterminadas, b. calcular las dosis en los detectores teniendo en cuenta la distribución de energía de fluencia de neutrones mediante una simulación de Monte Carlo,
c. interpolar las dosis usando el modelo de Christy-Eckermann a las posiciones reales 25 de los órganos.
2. Procedimiento según la reivindicación 1, caracterizado porque el tratamiento es un tratamiento en el abdomen o un tratamiento en la cabeza y las dosis equivalentes para cada órgano son: 30
3. Dispositivo semiconductor digital especialmente adaptado para usarse en el método según la reivindicación 1, que comprende una pluralidad de celdas de memoria que comprenden a su vez una capa dieléctrica de vidrio de borofosfosilicato (BPSG) en la disposición del chip adaptadas para que cada memoria almacene un nivel lógico que 5 cambia debido a la interacción de un neutrón térmico (E) .
Patentes similares o relacionadas:
Dispositivo de tratamiento con láser VCSEL de alta potencia con función de enfriamiento de la piel y su estructura de empaquetado, del 6 de Mayo de 2020, de Sanhe Laserconn Tech Co., Ltd: Un dispositivo de tratamiento con láser VCSEL de alta potencia que tiene una función de enfriamiento de la piel, que comprende un disipador […]
DISPOSITIVO ADAPTABLE A EQUIPOS DE RADIOTERAPIA EXTERNA QUE CONCENTRA LA DOSIS EN EL BLANCO CON FOCO VARIABLE, del 30 de Enero de 2020, de UNIVERSIDAD DE LA FRONTERA: Un dispositivo concentrador de fluencia de radiación ionizante de foco variable adaptable a una fuente de electrones de alta energía de un dispositivo […]
DISPOSITIVO CONCENTRADOR DE FLUENCIA DE RADIACIÓN IONIZANTE, QUE FOCALIZA ELECTRONES Y FOTONES X ADAPTABLE, del 30 de Enero de 2020, de UNIVERSIDAD DE LA FRONTERA: Un dispositivo concentrador de fluencia de radiación ionizante de foco variable adaptable a una fuente de electrones de alta energía de un dispositivo […]
Balón de fijación resistente a formación de manguito para dispositivo médico, del 15 de Enero de 2020, de Hologic Inc: Un dispositivo médico , incluyendo: una estructura de soporte alargada ; y un balón inflable , incluyendo el balón una parte de primer […]
Método de aplicación de una composición y composición farmacéutica con una pauta terapéutica para su administración, del 20 de Noviembre de 2019, de Hafezi, Farhad: Composición farmacéutica que comprende un principio activo que destruye o retarda la proliferación de células diana, en donde las células diana habían adquirido […]
Cabina en forma de domo geodésico que sirve para equilibrar y armonizar la bioenergía de los seres vivos, favoreciendo el bienestar energético y físico., del 25 de Septiembre de 2019, de GIL SÁNCHEZ, Mario: 1. Cabina en forma de domo geodésico que sirve para equilibrar y armonizar la bioenergía de los seres vivos, favoreciendo el bienestar energético […]
DISPOSITIVO DE ESTIMULACIÓN DE TEJIDOS CON DEMULTEPLEXOR DE SALIDA, del 27 de Junio de 2019, de PANACEA QUANTUM LEAP TECHNOLOGY LLC: Un dispositivo de estimulación de tejidos que comprende: una fuente; una unidad de control; un circuito de etapa de salida desacoplado conectado […]
Métodos para controlar la respuesta a las radioterapias en cáncer, del 6 de Febrero de 2019, de RNA Diagnostics Inc: Un método in vitro para determinar la respuesta de un cáncer a la radiación que comprende: i. aislar ARN de una biopsia de cáncer obtenida […]