DISPOSITIVO PARA LA DETECCIÓN DE UNA ÚNICA MOLÉCULA EN SITUACIÓN DE NANOCONFINAMIENTO Y EN RÉGIMEN DINÁMICO, PROCEDIMIENTO DE FABRICACIÓN Y USO.
Dispositivo para la detección de una única molécula en situación de nanoconfinamiento y en régimen dinámico,
procedimiento de fabricación y uso.
El objeto de la presente invención está relacionado con un dispositivo que integra estructuras de cristal fotónico y micro-nanocanales para la manipulación y detección de moléculas de ADN y otras moléculas con marcadores luminiscentes. El dispositivo, basado en la capacidad de las guías fotónicas de direccionar las ondas electromagnéticas, concentra la señal de emisión de la molécula en respuesta a una señal de excitación en una dirección dada. Son igualmente objetos de la presente invención el procedimiento de fabricación del dispositivo y el uso del mismo para la detección de una única molécula en situación de nanoconfinamiento y en régimen dinámico.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201330922.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Inventor/es: POSTIGO RESA,PABLO AITOR, ORTIZ DE ELGUEA,Aratz, JUARROS LASKURAIN,Aritz, MERINO ÁLVAREZ,Santos.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B82Y15/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B82 NANOTECNOLOGIA. › B82Y USOS O APLICACIONES ESPECIFICOS DE NANOESTRUCTURAS; MEDIDA O ANALISIS DE NANOESTRUCTURAS; FABRICACION O TRATAMIENTO DE NANOESTRUCTURAS. › Nano tecnología para interactuar, detectar o actuar, p. ej. puntos cuánticos como marcadores en ensayos de proteínas o motores moleculares.
Fragmento de la descripción:
SECTOR Y OBJETO DE LA INVENCION
El objeto de la presente invención se enmarca en el sector de la nanofotónica y micro- nanofluídica y está relacionado con un dispositivo que integra estructuras de cristal fotónico y micro-nanocanales para la manipulación y detección de moléculas de ADN y otras moléculas con marcadores luminiscentes. El dispositivo, basado en la capacidad de las guías fotónicas de direccionar las ondas electromagnéticas, concentra la señal de emisión de la molécula en respuesta a una señal de excitación en una dirección dada. Respecto a la invención, hay que destacar su gran nivel de miniaturización que permite diseños con tamaño reducido, la gran capacidad de concentración de la señal que permite su medida con detectores convencionales y su facilidad de fabricación mediante técnicas de alto rendimiento.
ESTADO DE LA TÉCNICA
Existen múltiples dispositivos o métodos de sensado para medir de manera rápida y fiable un gran número de parámetros, como por ejemplo, temperatura, presión, intensidad de campo eléctrico, etc. El interés se centra actualmente en el desarrollo de dispositivos o métodos de sensado para la detección, identificación y cuantificación de sustancias, como pueden ser gases, líquidos, proteínas, hormonas, bacterias o ADN, entre muchas otras. Estos dispositivos y métodos de sensado tienen aplicación en infinidad de campos, como por ejemplo, la investigación farmacéutica, el diagnóstico de enfermedades, la detección de contaminantes, o la guerra bacteriológica.
El interés en reducir el volumen de los procesos analíticos, combinado con los avances en micro y nanofluídica, están motivando el desarrollo de nuevos chips en los cuales los análisis pueden ser desarrollados más rápidamente y a un coste mucho menor que los tradicionalmente usados en laboratorios de biología molecular. Las nuevas aproximaciones en investigación están motivadas por la posibilidad de observar nuevos fenómenos u obtener información más detallada de sistemas activos biológicamente. Por este motivo, durante los últimos años la comunidad científica ha promovido una clase de investigación centrada en nuevas aproximaciones físicas y químicas al análisis biomolecular. La
complejidad de los procesos de la vida y la riqueza de la biología molecular proporcionan un amplio camino con el estudio de estos nuevos dispositivos. El desarrollo de estos nuevos chips está cambiando la naturaleza de las cuestiones de las que podemos obtener respuestas experimentales a nivel molecular. Estos nuevos chips integran medidas eléctricas, ópticas y físicas combinadas con el guiado de fluidos para crear un nuevo concepto de biochips denominados dispositivos para el análisis de una única molécula (single molecule devices). En general, estos chips pueden permitir un análisis menos invasivo de fluidos biológicos complejos para diagnóstico médico y terapias avanzadas. Un amplio rango de tecnologías, incluida la fabricación, están siendo direccionadas hacia estos objetivos. El conjunto de herramientas denominadas lab-on-a-chip (dispositivo que integra funciones de un laboratorio en un chip), y particularmente, los chips para detección de una única molécula, pueden en el medio y largo plazo proporcionar sistemas funcionales para el diagnóstico de determinadas enfermedades diana y proporcionar sistemas eficientes en el avance de terapias asociadas a enfermedades crónicas.
El desarrollo de chips moleculares en los que interaccionar con las moléculas requiere no únicamente de técnicas de detección ultrasensibles sino que es necesario el control micro y nanofluídico a nivel de chip, integrando canales, celdas, válvulas, electrodos y funcionalización superficial que permita la interacción con moléculas específicas. No menos importante, es el desarrollo de procesos de fabricación que permitan la formación de canales, agujeros o rendijas de dimensiones en la escala de las moléculas que queremos detectar, es decir, en el orden de unos pocos nanómetros. Sin embargo, aunque necesario, esto no es suficiente, y el desarrollo de tecnologías maduras que permitan la fabricación de dispositivos con motivos en esta escala de una forma fiable y económica resulta fundamental para el éxito y llegada a la industria de este nuevo concepto de chip. La combinación exitosa de todos estos factores crea un rango de oportunidades enorme en el campo del análisis molecular.
Los métodos usados en la actualidad para el análisis de ADN son costosos y lentos. Requieren cortar cada molécula en millones de fragmentos, replicar cada segmento, clasificarlos por tamaño y reconstruir la cadena de ADN original. Por el contrario, los métodos basados en información obtenida de una única molécula, como en el estiramiento de ADN, consisten en el estiramiento de moléculas individuales por confinamiento en los canales nanofluídicos, abriendo nuevas posibilidades para el análisis de ADN [F. Persson et al., Chem. Soc. Rev. 39 (2010) 985-999] y la detección bioquímica, lo que acelera el
proceso y reduce el coste. Paralelamente, M. Wanunu et al. [M. Wanunu et al.. Nature Nanotechnology 5 (2010) 160-165.] detectaron concentraciones de ADN en el rango picomolar, capturando moléculas a través de nanoporos y un gradiente salino, mostrando la posibilidad de detectar ADN sin amplificarlo previamente y con un gran rendimiento en función del tiempo.
El estiramiento de moléculas individuales de ADN en canales nanofluídicos se puede utilizar para el estudio de las propiedades físicas y biológicas de estas moléculas. Estos dispositivos nanofluídicos se han utilizado para mediciones en tiempo real del contorno de las moléculas de ADN estiradas [E. Abad et al.. Microelectronic Engineering 88 (2011) 300304], estudios de interacción entre proteína y ADN, la organización ordenada usando endonucleasas, la identificación de moléculas individuales de ADN usando nanoranuras, estudios biológicos de conformación, movimiento entrópico y velocidad de moléculas de ADN estiradas en nanocanales [J.T. Mannion et al. Biophys. J. 90 (2006) 45384545], y espectroscopia de confinamiento de moléculas individuales de ADN en nanocanales [F. Persson et al., Nano Lett. 9 (4) (2009) 1382-1385].
Por otro lado, la caracterización a gran escala de complejos proteicos requiere generalmente de la separación de complejas muestras de proteínas y la identificación de cada proteína de manera individual. Entre los métodos más utilizados para el análisis de proteínas se encuentra la electroforesis, la espectroscopía de masas y la secuenciación peptídica. Esta metodología es difícil de automatizar y por esta razón, las aproximaciones alternativas de identificación de proteínas como los microarrays, que evitan la necesidad de separación de las proteínas, han ganado popularidad en el campo de la proteómica [P. Bertone et al.. Febs J. 272, 21 (2005) 5400-5411]. Sin embargo, incluir proteínas en formato microarray supone un reto mucho mayor que incluir moléculas de ADN. La funcionalidad de las proteínas depende del estado de las proteínas, por ejemplo de las modificaciones conformacionales, formación de complejos con otras proteínas, localización subcelular y modificaciones covalente reversibles. Es también importante que en los chips de proteínas en los que se requiere plena funcionalidad de las proteínas sea posible mantenerlas en estado activo a altas densidades.
Paralelamente, los chips basados en detección de una única proteína están obteniendo resultados prometedores. De este modo, la combinación de un nanoporo (2-100 nm) acoplado a un campo eléctrico ha resultado ser una herramienta fundamental para estudiar
translocaciones de proteínas y cambios conformacionales de proteínas [C. Merstorf et al.. ACS Chem. Biol. 7, 652-658 (2012).], o más recientemente, estudiar la presencia de proteínas nativas unidas covalentemente a aptámeros en las proximidades del nanoporo [M. Soskine,et al. Nanolett 12, 4895-4900 (2012).]. El principio de detección se basa en aplicar un campo eléctrico a ambos extremos del nanoporo, el cual separa dos cámaras aisladas, induciendo una corriente iónica a través de un único agujero en la presencia de una solución salina. De este modo, cuando una proteína pasa a través del agujero, induce un decrecimiento en la corriente eléctrica, consecuencia del bloqueo al que da lugar en el paso de iones. Esta señal dependerá de la naturaleza de la proteína y de las características del nanoporo: tamaño, estructura conformacional, carga neta, geometría e interacciones.
En una gran parte de los dispositivos moleculares citados anteriormente se requiere el análisis de la señal de fluorescencia proveniente de una única molécula, bien sea como medida directa...
Reivindicaciones:
1.- Dispositivo para la detección de una única molécula en situación de nanoconfinamiento y en régimen dinámico a través de la excitación de un emisor unido a la molécula o que forma parte de la misma y que comprende los siguientes elementos:
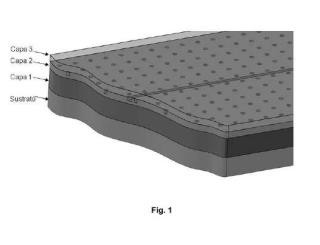
un sustrato,
una capa inferior de aislamiento óptico y baja absorción óptica a la longitud de onda de emisión del fluoróforo,
una capa central formada por un material dieléctrico y baja absorción óptica a la longitud de onda de emisión del fluoróforo caracterizado porque la capa central presenta al menos una estructura de cristal fotónico y al menos un nanocanal en el cual se confina la molécula a detectar y porque la capa central está cubierta por una capa superior de aislamiento óptico que actúa como sello del nanocanal.
2.- Dispositivo según la reivindicación 2, caracterizado porque el emisor es un fluoróforo, punto cuántico, o molécula fluorescente.
3.- Dispositivo según una cualquiera de las reivindicaciones 1 o 2, caracterizado porque la excitación se produce por iluminación mediante una lámpara de luz blanca o monocromática.
4.- Dispositivo según una cualquiera de las reivindicaciones 1 o 2, caracterizado porque la excitación se produce mediante láser.
5.- Dispositivo según una cualquiera de las reivindicaciones 1 a 4, caracterizado porque el sustrato que otorga rigidez mecánica al dispositivo se fabrica en un material que se selecciona entre silicio, vidrio o polímero y tiene un grosor comprendido entre 50 pm y 3 mm.
6.- Dispositivo según una cualquiera de las reivindicaciones 1 a 5, caracterizado porque la capa inferior de aislamiento óptico se fabrica en un material que se selecciona entre sílice o polímero y tiene un grosor comprendido entre 50 nm y 1500 pm.
7.- Dispositivo según una cualquiera de las reivindicaciones 1 a 6, caracterizado porque la capa central de material dieléctrico se fabrica en un material que se selecciona entre nitruro de silicio, y óxido de titanio y tiene un grosor comprendido entre 30 y 1000 nm.
8.- Dispositivo según la reivindicación 7, caracterizado porque la capa central presenta entre 1 y 5000 nanocanales que tienen entre 5 y 2000 pm de longitud, entre 20 y 1000 nm de anchura y entre 20 y 1000 nm de profundidad.
9.- Dispositivo según la reivindicación 8, caracterizado porque la capa central presenta entre 1 y 5000 estructuras de cristal fotónico formadas por una red periódica de cavidades de tamaño submicrónico ubicadas en ambos lados de al menos uno de los nanocanales con:
una simetría que se selecciona entre triangular, cuadrada o mezcla de ambas,
un parámetro de red de separación entre las cavidades (a) comprendido entre 10nm y 1000 pm.
10.- Dispositivo según la reivindicación 9, caracterizado porque las cavidades presentan geometría cilindrica coaxial perpendicular a la superficie plana de la capa con un tamaño de radio comprendido entre 10nm y 1000 pm.
11.- Dispositivo según la reivindicación 9, caracterizado porque las cavidades presentan geometría semiesférica con un tamaño de radio comprendido entre 10nm y 1000 pm.
12.- Dispositivo según la reivindicación 9, caracterizado porque las cavidades presentan geometría prismática coaxial perpendicular a la superficie plana de la capa con un tamaño de radio de la circunferencia circunscrita a la base comprendido entre 10nm y 1000 pm.
13.- Dispositivo según una cualquiera de las reivindicaciones 1 a 13, caracterizado porque la capa superior sellante de aislamiento óptico se fabrica en un material que se selecciona entre vidrio y polímero y tiene un espesor comprendido entre 100 y 1000 pm.
14.- Dispositivo según la reivindicación 13, caracterizado porque la capa superior incluye una capa de un óxido conductor eléctrico transparente.
15.- Dispositivo según la reivindicación 13, caracterizado porque la capa superior incluye un electrodo metálico.
16.- Dispositivo según una cualquiera de las reivindicaciones 1 a 15, caracterizado porque presenta entre 1 y 100 puertos de entrada y salida para la inyección de fluidos.
17.- Dispositivo según una cualquiera de las reivindicaciones 1 a 16, caracterizado porque presenta entre 1 y 100 microcanales en forma de V para el transporte de fluidos hasta la entrada de los nanocanales.
18.- Dispositivo según la reivindicación 17, caracterizado porque los microcanales tienen una anchura comprendida entre 1 y 500 pm y una profundidad comprendida entre 0,5 y 50 pm.
19.- Dispositivo según una cualquiera de las reivindicaciones 1 a 18, caracterizado porque los materiales de las distintas capas que lo conforman se seleccionan en función de la longitud de onda del emisor de forma que:
el índice de refracción del material utilizado para el sustrato es arbitrario por estar minimizada su influencia sobre la luz emitida.
el índice de refracción del material utilizado para la capa inferior es < 1, 5 para la longitud de onda del emisor.
el índice de refracción del material utilizado para la capa central es > 1, 5 para la longitud de onda del emisor.
20.- Dispositivo según la reivindicación 19, caracterizado porque el material de la capa central presenta en la región espectral del emisor un coeficiente de absorción k en el índice de refracción complejo n = n + ik cuyo valor está comprendido entre 0 y 1.
21.- Dispositivo según una cualquiera de la las reivindicaciones 1 a 20, caracterizado porque se elimina el sustrato que otorga rigidez mecánica al dispositivo.
22.- Procedimiento de fabricación de un dispositivo según las reivindicaciones 1 a 21, caracterizado porque comprende:
una etapa en la que se proporciona un sustrato plano a escala submicrónica con una capa de un material que presenta un coeficiente de absorción k comprendido entre 0 y 1 y un índice de refracción inferior a 1,5 en el rango de longitud de onda del fluoróforo empleado,
una etapa en la que se proporciona una capa con un coeficiente de absorción k comprendido entre 0 y 1 y un índice de refracción superior a 1,5 en el rango de longitud de onda del fluoróforo empleado,
una etapa de formación mediante litografía de nanoimpresión de una red periódica de cavidades de tamaño inferior a la miera sobre la superficie de dicho sustrato y de uno o varios canales para transportar un fluido también de dimensiones submicrónicas,
una etapa de deposición de un material transparente sobre dichas cavidades con el 5 fin de sellarlas por su parte superior.
23.- Uso de un dispositivo según las reivindicaciones 1 a 21 para la detección de una única molécula en situación de nanoconfinamiento y en régimen dinámico que comprende las siguientes etapas:
introducción del fluido que contiene las moléculas a través de los puertos de entrada
del dispositivo.
circulación de las moléculas a través de los microcanales mediante presión o campo eléctrico hasta llegar a la zona de entrada a los nanocanales.
penetración y difusión de las moléculas en los nanocanales en ausencia de excitación 15 externa
excitación del fluoróforo ligado a las moléculas a través de la iluminación con fuente de luz monocromática o policromática.
detección de la emisión del fluoróforo a través de una cámara CCD.
Patentes similares o relacionadas:
Nanoparticulas de AG2S súper fluorescentes en la región del infrarrojo cercano y metódo de obtención, del 15 de Julio de 2020, de UNIVERSIDAD COMPLUTENSE DE MADRID: Nanopartículas de Ag2S súper fluorescentes en la región del infrarrojo cercano y método de obtención. El marcaje con sondas fluorescentes […]
Método para la detección rápida de Candida auris y el diagnóstico de la infección causada por este patógeno, del 26 de Mayo de 2020, de FUNDACIÓN PARA LA INVESTIGACIÓN DEL HOSPITAL UNIVERSITARIO LA FE: Método para la detección rápida de Candida aurisy el diagnóstico de la infección causada por este patógeno. La presente invención se relaciona con […]
Clústeres cuánticos atómicos estables, su método de obtención y uso de los mismos, del 6 de Mayo de 2020, de UNIVERSIDADE DE SANTIAGO DE COMPOSTELA: Clústeres cuánticos atómicos, AQCs, estables caracterizados por estar compuestos por menos de 500 átomos de metal, su procedimiento de obtención caracterizado […]
Generación de una secuencia de control para control cuántico, del 12 de Febrero de 2020, de Quantum Valley Investment Fund LP: Un método de control para controlar un sistema de espines, comprendiendo el método de control: acceder a un modelo de sistema de espines que representa un sistema […]
SENSOR DE HUMEDAD, del 30 de Enero de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Sensor de humedad basado en la respuesta óptica de un ópalo artificial a la adsorción de agua. El diseño básico precisa únicamente de la lectura de la banda de difracción […]
SENSOR DE HUMEDAD, del 27 de Enero de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Sensor de humedad basado en la respuesta óptica de un ópalo artificial a la adsorción de agua. El diseño básico precisa únicamente de la lectura de la banda de difracción […]
 Nanoestructuras que comprenden manganeso, del 25 de Diciembre de 2019, de Spago Nanomedical AB (publ): Nanoestructura que comprende iones de manganeso incorporados en un marco polimérico que comprende por lo menos cinco grupos bisfosfonato geminales, […]
Nanoestructuras que comprenden manganeso, del 25 de Diciembre de 2019, de Spago Nanomedical AB (publ): Nanoestructura que comprende iones de manganeso incorporados en un marco polimérico que comprende por lo menos cinco grupos bisfosfonato geminales, […]
Cuantificación rápida de biomoléculas en un biosensor nanofluídico selectivamente funcionalizado y método de la misma, del 11 de Diciembre de 2019, de Abionic SA: Un biosensor para detectar y cuantificar biomoléculas marcadas por fluorescencia ; comprendiendo dicho biosensor un nanocanal definido […]