Anomalías de la expresión de microARN en tumores pancreáticos endocrinos y acinares.
Un método para determinar el pronóstico de un sujeto con cáncer pancrático,
que comprende la medición del nivel de al menos un producto génico miR en una muestra de ensayo de dicho sujeto, en donde:
el producto génico miR se asocia con un pronóstico adverso en el cáncer pancreático; y un aumento en el nivel del al menos un producto génico miR en la muestra de ensayo, con respecto al nivel de un producto génico miR correspondiente en una muestra de control, es indicativo de un pronóstico adverso en donde el al menos un producto génico miR es miR-21.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/000024.
Solicitante: THE OHIO STATE UNIVERSITY RESEARCH FOUNDATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1524 North High Street Columbus, OH 43201 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CROCE,Carlo,M, CALIN,GEORGE A.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61N1/30 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61N ELECTROTERAPIA; MAGNETOTERAPIA; RADIOTERAPIA; TERAPIA POR ULTRASONIDOS (medida de corrientes bioeléctricas A61B; instrumentos quirúrgicos, dispositivos o métodos para transferir formas no mecánicas de energía hacia o desde el cuerpo A61B 18/00; aparatos de anestesia en general A61M; lámparas incandescentes H01K; radiadores de infrarrojos utilizados como calefactores H05B). › A61N 1/00 Electroterapia; Circuitos correspondientes (A61N 2/00 tiene prioridad; preparaciones conductoras de la electricidad que se utilizan en terapia o en examen in vivo A61K 50/00). › Aparatos de iontoforesis o de electroforesis.
PDF original: ES-2524018_T3.pdf



Fragmento de la descripción:
Anomalías de la expresión de microARN en tumores pancreáticos endocrinos y acinares
Apoyo gubernamental
La invención fue subvencionada, en todo o en parte, por los Proyectos Programados de Subvenciones P01CA76259 y P01CA81534 del Instituto Nacional del Cáncer. El Gobierno tiene ciertos derechos sobre la invención.
Antecedentes de la Invención Los cánceres pancreáticos se pueden clasificar según el sitio donde se encuentre el cáncer en el páncreas o según el tipo de célula a partir del que se ha generado el cáncer. El cáncer pancreático puede producirse en la cabeza, cuerpo o cola del páncreas y los síntomas pueden variar dependiendo de dónde se localice el tumor en el páncreas. 15 El 70-80 % de los cánceres pancreáticos se producen en la cabeza del páncreas. La mayoría de los cánceres del páncreas son de tipo exocrino, y más del 90 % de estos cánceres pancreáticos exocrinos son adenocarcinomas. Casi todos de estos son adenocarcinomas ductales, en los que el cáncer se produce en las células del revestimiento de los conductos del páncreas. Además, hay tipos más raros de cáncer pancreático, tales como los tumores quísticos, el cáncer de células acinares y los sarcomas. Los tumores quísticos son tumores que producen un quiste o saco lleno de fluido en el páncreas. Los sarcomas, cánceres del tejido conjuntivo que mantiene juntas las células del páncreas, son raros y a menudo se producen en niños.
Además de los cánceres exocrinos, se pueden producir cánceres endocrinos. Los cánceres endocrinos se pueden denominar en referencia a la hormona que producen, por ejemplo gastrinomas (que producen gastrina) , insulinomas (que producen insulina) , somatostatinomas (que producen somatostatina) , VIPomas (que producen VIP) y glucagonomas (que producen glucagón) . Además, pueden producirse linfomas en el páncreas, aunque son raros.
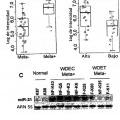
Los tumores pancreáticos endocrinos (PET) se pueden producir esporádicamente o como parte de un síndrome neoplásico endocrino múltiple tipo 1 (MEN1) (Kloppel, G., y col., Ann. N.Y. Acad. Sci. 1014:13-27 (2004) ) . Estas neoplasias se clasifican clínicamente como funcionales (F-PET) o no funcionales (NF-PET) , según la presencia de síntomas debidos a la hipersecreción hormonal. Los F-PET están representados mayoritariamente por insulinomas. En cuanto al diagnóstico; se observa enfermedad metastática en solo el 10 % de los insulinomas pero hasta el 60 % en NF-PET, y la mayoría de las muertes relacionadas con PET se producen por metástasis hepáticas (Kloppel, G., y col., Ann. N.Y. Acad. Sci. 1014:13-27 (2004) ) . El potencial de malignidad entre los PET varía mucho y no se puede predecir basándose en la apariencia histológica. De hecho, la inmensa mayoría de los PET son tumores endocrinos bien diferenciados (WDET) y se definen como carcinomas endocrinos bien diferenciados (WDEC) solo cuando se identifica la invasión o metástasis (Kloppel, G., y col., Ann. N.Y. Acad. Sci. 1014:13-27 (2004) ) .
El carcinoma pancreático celular acinar (PACC) es un tipo de tumor extremadamente raro, distinto del adenocarcinoma ductal y PET, aunque se observa cierto solapamiento con PET por la expresión de ambos marcadores neuroendocrinos en un tercio de los casos y la existencia de carcinomas mixtos acinares-endocrinos (Ohike, N., y col., Virchows Arch. 445:231-35 (2004) ) . El PACC siempre es maligno con una supervivencia media de 18 meses, que lo sitúa entre la del adenocarcinoma pancreático ductal y las neoplasias endocrinas (6 meses y 40 meses, respectivamente) (Holen, K.D., y col., J. Clin. Oncol. 20:4673-78 (2002) ) .
Se sabe poco sobre la patogénesis molecular de los PET (Kloppel, G., y col., Ann. N.Y. Acad. Sci. 1014:13-27 (2004) ) . La inactivación del gen MEN1 es el acontecimiento génico más frecuente que se identifica en el PET esporádico, mientras que son poco comunes las mutaciones en los genes normalmente implicados en el adenocarcinoma pancreático (Perren, A., y col., Ann. N.Y. Acad. Sci. 1014:199-208 (2004) ) . Se sabe incluso menos con respecto a las anomalías moleculares del PACC (Abraham, S.C., y col., Am. J. Pathol. 160:953-62 (2002) ) . No está disponible ningún dato del perfil de expresión para el PACC y la comprensión de los cambios de expresión génica que se producen en el PET aún está en una fase inicial (Hansel, D.E., y col., Clin. Cancer Res. 10:6152-58 (2004) ) . Los microARN son productos génicos pequeños (20-24 nucleótidos) no codificantes ARN que tienen funciones críticas en muchos procesos biológicos, tales como la proliferación celular, apoptosis y ritmo de desarrollo. Para 55 llevar a cabo estas funciones, los microARN regulan negativamente la estabilidad y/o la eficacia traduccional de sus ARNm dianas (Ambros, V., Nature 431:350-55 (2004) ) . Actualmente, se conocen 313 microARN maduros únicos humanos, de los cuales 223 se han verificado experimentalmente en seres humanos (www.microrna.sanger.ac.uk) . Estudios recientes sugieren que la expresión aberrante de ARNm particulares puede estar implicada en enfermedades humanas, tales como trastornos neurológicos (Ishizuka, A., y col., Genes Dev. 16:2497-2508 (2002) ) y cáncer. En particular, se ha descubierto una expresión alterada de miR-16-1 y/o miR-15a en las leucemias linfocíticas crónicas (CLL) (Cahn, G.A., y col., Proc. Natl. Acad. Sci. US.A. 99:15524-15529 (2002) ) . Se ha relacionado la expresión aberrante de 5 microARN con cánceres y se pueden distinguir características diagnósticas/pronósticas de tipos específicos de cáncer basándose en sus perfiles de microARN (Caldas, C., and
J.D. Brenton, Nature Med. 11:712-14 (2005) ; Croce, C.M., y G.A. Calin, Cell 122:6-7 (2005) ) . Los estudios 65 funcionales también han relacionado la expresión aberrante de microARN con carcinogénesis (Chan, J.A., y col., Cancer Res. 65:6029-33 (2005) ; Cheng, A.M., y col., 10 Nucleic Acids Res. 33:1290-97 (2005) ; He, L., y col., Nature
435:828-33 (2005) ; y Johnson, S.M., y col., Cell 120:635-47 (2005) ) .
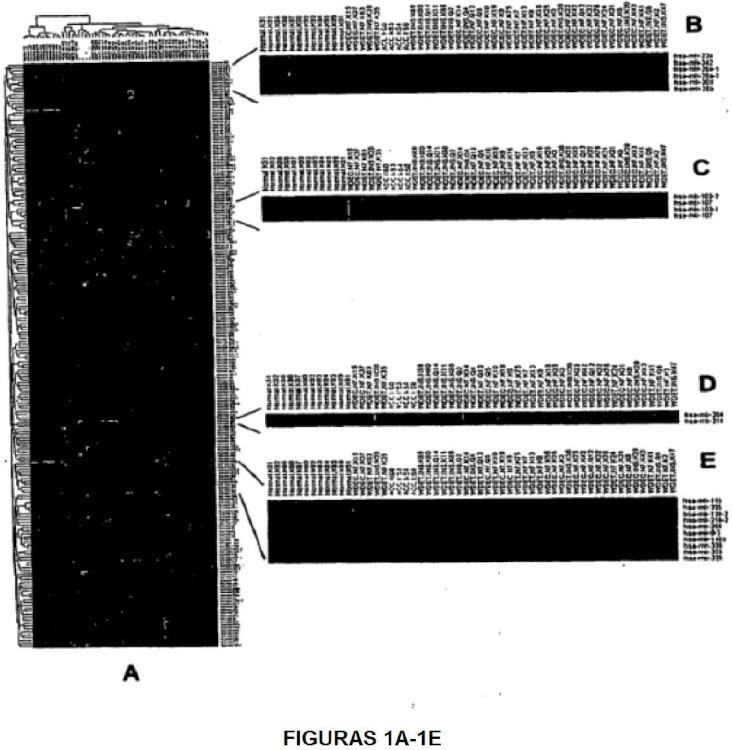
El desarrollo y uso de micromatrices que contienen todos los microARN humanos conocidos ha permitido un análisis simultáneo de la expresión de cada miARN en una muestra (Liu, C.G., y col., Proc Natl. Acad. Sci. U.S.A. 101:9740
9744 (2004) ) . Estas micromatrices de microARN15 no solo se han utilizado para confirmar que el miR-16-1 está mal regulado en las células de CLL humana, sino también para generar firmas de expresión de miARN que se asocian con características clinicopatológicas bien definidas de la CLL humana (Calin, G.A., y col., Proc. Natl. Acad. Sci. USA. 101:1175-11760 (2004) ) .
El documento WO 2005/078139 se refiere a genes microARN y su asociación con las características cromosómicas implicadas en la etiología de diferentes cánceres. Este documento trata el posible uso de la evaluación de la expresión génica de miR para indicar la presencia de un cáncer que produce una lesión cromosómica en un sujeto.
En GUWEIDHI AHMED Y COL: "Enhanced expression of 1-3-3sigma in pancreatic cancer and its role in cell cycle regulation and apoptosis" CARCINOGENESIS (OXFORD) , vol. 25, nº 9, Septiembre 2004, páginas 1575-1585, se aborda un estudio dirigido a investigar la expresión y papel funcional del 14-3-3sigma en el adenocarcinoma pancreático ductal (PDAC) . En este estudio se concluyó que la marcada sobre-expresión de 14-3-3sigma en PDAC junto con alteraciones múltiples génicas y epigénicas conocidas de colaboradores potenciales que interactúan con 14-3-3sigma sugieren un papel importante de la señalización 14-3-3sigma corriente abajo en el cáncer pancreático.
En LU JUN Y COL: "MicroRNA expression profiles classify human cancers" NATURE, NATURE PUBLISHING GROUP, GB, vol. 435, nº 7043, 9 de junio de 2005, páginas 834-838, se trata un estudio dirigido al microARN y su uso potencial en el diagnóstico del cáncer.
La identificación de microARN que se expresen diferencialmente en las células de cáncer pancreático puede ayudar a localizar miARN específicos que estén implicados en el cáncer pancreático (por ejemplo, tumores pancreáticos endocrinos, carcinomas acinares) . Además, la identificación de supuestas dianas de estos miARN puede ayudar a desvelar su papel patogénico. La presente invención proporciona nuevos métodos y composiciones para el diagnóstico, pronóstico y tratamiento del cáncer pancreático.
Sumario de la invención La presente invención se basa, en parte, en la identificación de miARN específicos asociados con niveles de expresión alterados de las células de cáncer pancreático.
En consecuencia, la invención proporciona un método para determinar el pronóstico de un sujeto con un cáncer pancreático, que comprende la medición... [Seguir leyendo]
Reivindicaciones:
1. Un método para determinar el pronóstico de un sujeto con cáncer pancrático, que comprende la medición del nivel de al menos un producto génico miR en una muestra de ensayo de dicho sujeto, en donde:
el producto génico miR se asocia con un pronóstico adverso en el cáncer pancreático; y un aumento en el nivel del al menos un producto génico miR en la muestra de ensayo, con respecto al nivel de un producto génico miR correspondiente en una muestra de control, es indicativo de un pronóstico adverso en donde el al menos un producto génico miR es miR-21.
2. Un método de acuerdo con la reivindicación 1, en el que el cáncer pancrático se asocia con metástasis y/o un índice alto de proliferación.
3. Un método para determinar si un cáncer pancreático de un sujeto es metastático, que comprende la medición del nivel de al menos el producto génico miR-21 en una muestra de ensayo de dicho sujeto, en donde:
el producto génico miR se asocia con metástasis; y un aumento del nivel del al menos un producto génico miR en la muestra de ensayo, con respecto al nivel de un producto génico miR correspondiente en una muestra de control, es indicativo de metástasis.
4. Un método para determinar si un cáncer pancreático de un sujeto tiene un índice alto de proliferación, que comprende la medición del nivel de al menos un producto génico miR-21 en una muestra de ensayo de dicho sujeto, en donde:
el producto génico miR está asociado con un índice alto de proliferación; y un aumento del nivel del al menos un producto génico miR en la muestra de ensayo, con respecto al nivel de un producto génico miR correspondiente en la muestra de control, es indicativo de un índice alto de proliferación.
5. Un método para diagnosticar si un sujeto tiene un cáncer pancreático con un pronóstico adverso, que comprende:
(1) la transcripción inversa de ARN de una muestra de ensayo obtenida del sujeto para proporcionar un grupo de oligodesoxinucleótidos diana;
(2) la hibridación de los oligodesoxinucleótidos diana con una micromatriz que comprende oligonucleótidos sonda específicos de miARN para proporcionar un perfil de hibridación para dicha muestra de ensayo; y
(3) la comparación del perfil de hibridación de la muestra de ensayo con el perfil de hibridación generado a partir de una muestra de control.
en donde un incremento en la señal de miR-21 es indicativo de que el sujeto tiene un cáncer pancreático con un pronóstico adverso.
6. Un método para determinar el pronóstico de un sujeto con cáncer pancreático, que comprende la medición del nivel de PDCD4 en una muestra de ensayo he dicho sujeto, en donde una disminución del nivel de PDCD4 en la muestra de ensayo, con respecto al nivel de PDCD4 en una muestra de control, es indicativa de un pronóstico adverso.
7. El método de la reivindicación 6, en donde el cáncer pancreático se asocia con metástasis y/o un índice alto de proliferación.
Patentes similares o relacionadas:
DISPOSITIVO Y SISTEMA AUTÓNOMO DE MONITORIZACIÓN DE PACIENTES Y ADMINISTRACIÓN DE MEDICACIÓN POR VÍA TRANSDÉRMICA, del 23 de Julio de 2020, de UNIVERSIDAD CARLOS III DE MADRID: Dispositivo y sistema autónomo de monitorización de pacientes y administración de medicación por vía transdérmica. Se refiere a un dispositivo autónomo de gestión y administración […]
Matriz polimérica adhesiva para iontoforesis y dispositivo para iontoforesis que comprende dicha matriz, del 17 de Junio de 2020, de Feeligreen: Matriz polimérica adhesiva para el suministro de principio activo para iontoforesis que presenta una primera cara destinada a ser aplicada […]
Dispositivo de iontoforesis con pieza de extremo multi-electrodo, del 27 de Mayo de 2020, de L'OREAL: Pieza de extremo destinada a equipar un dispositivo para el tratamiento cosmético de materiales de queratina con una corriente eléctrica, comprendiendo […]
Dispositivo iontoforético con gestión de corriente independiente, del 22 de Enero de 2020, de L'OREAL: Dispositivo para el tratamiento cosmético de materiales de queratina con corriente eléctrica, que comprende: - una pieza terminal que comprende al […]
Dispositivo de aplicación de un producto aplicado sobre la piel de un usuario por iontoforesis, del 7 de Agosto de 2019, de SEB S.A.: Dispositivo de aplicación de un producto que se desea distribuir sobre una piel de un usuario mediante iontoforesis que incluye: -un cuerpo destinado a recibir el […]
Dispositivo y método para la transfección de grandes volúmenes, del 17 de Julio de 2019, de Lonza Cologne GmbH: Dispositivo para aplicar un campo eléctrico a una suspensión de células, derivados celulares, orgánulos, partículas subcelulares y/o vesículas, comprendiendo al menos […]
Un dispositivo electroquímico para la liberación de iones, del 2 de Abril de 2019, de NMR Technology AS: Un dispositivo electroquímico , que comprende una primera parte y una segunda parte, comprendiendo dicha primera parte: - un primer electrodo […]
Dispositivo iontoforético que tiene un depósito, del 20 de Marzo de 2019, de L'OREAL: Dispositivo para el tratamiento cosmético de materiales de queratina con una corriente eléctrica, que comprende al menos: - un sistema de suministro de energía […]