COMPUESTOS ÚTILES COMO INHIBIDORES DE PROTEÍNA QUINASAS.
Un compuesto de formula I: o una sal farmaceuticamente aceptable del mismo;
en la que: X1 es un enlace, O, NR8, S, SO o SO2; X2 es N o CH; R1 es H, alifatico C1-10, cicloalifatico C3-10, arilo C6-10, heteroarilo de 5 a 10 miembros o heterociclilo de 3 a 10 miembros; en la que dicho R1 esta opcionalmente sustituido con 0-5 J1; cada R2 y R3 es independientemente H, alifatico C1-10 o cicloalifatico C3-10; en la que cada R2 y R3 esta sustituido opcional e independientemente con 0-5 J2 y J3 respectivamente; y R2 y R3, junto con el atomo de carbono al que estan unidos, forman un anillo monociclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroatomos seleccionados cada uno de ellos independientemente entre O, N, y S; dicho anillo monociclico formado por R2 y R3 esta opcionalmente sustituido con 0-4 J23; R4 es H, C(O)R, C(O)OR o C(O)NRR', alifatico C1-10, cicloalifatico C3-10, arilo C6-10, heteroarilo de 5 a 10 miembros, heterociclilo de 3 a 10 miembros, -(alifatico C1-6)-(cicloalifatico C3-10), -(alifatico C1-6)-(arilo C6-10) o - (alifatico C1-6)-(heteroarilo de 5 a 10 miembros); y R4 esta opcionalmente sustituido con 0-5 J4; o R2 y R4, junto con los atomos de carbono a los que estan unidos, forman un anillo monociclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroatomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monociclico formado por R2 y R4 esta opcionalmente sustituido con 0-4 J24; R5 es H, CO2R, CH2OR, CONR2, CN, F o CF3; L es un enlace o -C(R6) (R7)-; cada R6 y R7 es independientemente H, alifatico C1-10 o cicloalifatico C3-10; en el que cada R6 y R7 esta sustituido opcional e independientemente con 0-5 J6 y J7 respectivamente; o R6 y R7, junto con el atomo de carbono al que estan unidos, forman un anillo monociclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroatomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monociclico formado por R6 y R7 esta opcionalmente sustituido con 0-4 J67 ; o R2 y R6, junto con el atomo de carbono al que estan unidos, forman un anillo monociclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroatomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monociclico formado por R2 y R6 esta opcionalmente sustituido con 0-4 J26 ; o R4 y R6, junto con el atomo de carbono al que estan unidos, forman un anillo saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroatomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monociclico formado por R4 y R6 esta opcionalmente sustituido con 0-4 J46; R8 es H, alifatico C1-6, cicloalifatico C3-8, C(O)R, C(O)OR o C(O)NRR' ; o cada J1 es independientemente haloalquilo C1-6, halo, NO2, CN, Q o -Z- Q; o dos J1 tomados juntos pueden formar opcionalmente =O; Z es alifatico C1-6 opcionalmente reemplazado con 0-3 apariciones de -NR-, -O-, -S-, -C(O)-, -C(=NR)-, - C(=NOR)-, -SO- o -SO2-; cada Z esta opcionalmente sustituido con 0-2 Jz; Q es H; alifatico C1-6; un anillo monociclico aromatico o no aromatico de 3 a 8 miembros que tiene 0-3 heteroatomos seleccionados independientemente entre O, N y S; o un sistema de anillos biciclico aromatico o no aromatico de 8-12 miembros, teniendo cada uno 0-5 heteroatomos seleccionados independientemente entre O, N y S; cada Q esta opcionalmente sustituido con 0-5 JQ; cada J2, J3, J6 y J7 es independientemente alifatico C1-6, cicloalifatico C3-6 o -(alquil C1-4)n-V1; en el que n es 0 o 1; V1 es halo (alifatico C1-4), -O(haloalifatico C1-4), halo, NO2, CN, OH, OR", SH, SR", NH2, NHR", N(R")2, COH, COR", CO2H, CO2R", CONH2, CONHR", CONR"2, OCOR", OCONH2, OCONHR", OCON(R")2, NHCOR", NR"COR", NHCO2R", NR"CO2R", NHCO2H, NR"CO2H, NHCONH2, NHCONHR", NHCON(R")2, SO2NH2, SO2NHR" SO2N(R")2, NHSO2R" o NR"SO2R"; o V1 es un grupo ciclico seleccionado entre cicloalifatico C3-6, fenilo, heteroarilo de 5 a 6 miembros o heterociclilo de 3 a 6 miembros; en el que dicho grupo ciclico esta opcionalmente sustituido con 0-3 JV; R" es alifatico C1-4 sin sustituir; o dos de J2, J3, J6 y J7 iguales, unidos al mismo atomo, juntos pueden formar opcionalmente =O; cada Jz y Jv es independientemente halo, alifatico C1-6, cicloalifatico C3-6, NO2, CN, -NH2, -NH(alifatico C1-4), - N(alifatico C1-4)2, -OH, -O(alifatico C1-4), -CO2H, -CO2(alifatico C1-4), -O(haloalifatico C1-4) o halo(alifatico C1-4); cada JQ, J4, J23, J24, J67, J26 y J46 es independientemente M o -Y-M; cada Y es independientemente un alifatico C1-6 opcionalmente reemplazado con 0-3 apariciones de -NR-, -O-, - S-, -C(O)-, -SO- o -SO2-; cada M es independientemente H, alifatico C1-6, cicloalifatico C3-6, halo(alifatico C1-4), -O(haloalifatico C1-4), heterociclilo de 3 a 6- miembros, halo, NO2, CN, OH, OR', SH, SR', NH2, NHR', N(R')2, COH, COR', CO2H, CO2R', CONH2, CONHR', CONR'2, OCOR', OCONH2, OCONHR', OCON (R')2, NHCOR', NR'COR', R NHCO2R', NR' CO2R', NHCO2H, NR'CO2H, NHCONH2, NHCONHR', NHCON(R')2, SO2NH2, SO2NHR', SO2N(R')2, NHSO2R' o NR'SO2R'; es H o alifatico C1-6 sin sustituir; y R' es alifatico C1-6 sin sustituir; o dos grupos R', junto con junto con el atomo de carbono al que estan unidos, forman un anillo monociclico saturado o parcialmente insaturado de 3 a 8 miembros que tiene 0-1 cada uno seleccionado independientemente entre O, N y S
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/025688.
Solicitante: VERTEX PHARMCEUTICALS INCORPORATED.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 130 WAVERLY STREET CAMBRIDGE, MA 02139-4242 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KNEGTEL, RONALD, KAY, DAVID, CHARRIER, JEAN-DAMIEN.
Fecha de Publicación: .
Fecha Solicitud PCT: 14 de Diciembre de 2007.
Clasificación Internacional de Patentes:
- C07D475/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › Compuestos heterocíclicos que contienen sistemas cíclicos de pteridina.
Clasificación PCT:
- C07D475/12 C07D […] › C07D 475/00 Compuestos heterocíclicos que contienen sistemas cíclicos de pteridina. › que contienen sistemas cíclicos de pteridina condensados con carbociclos o sistemas carbocíclicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2359467_T3.pdf
Fragmento de la descripción:
Campo técnico de la invención
La presente invención se refiere a compuestos útiles como inhibidores de proteína quinasas. La invención también proporciona composiciones farmacéuticamente aceptables que comprenden los compuestos de la invención y procedimientos para usar las composiciones en el tratamiento de diversos trastornos. La invención también proporciona procedimientos para preparar los compuestos de la invención.
Antecedentes de la invención
En los últimos años se ha ayudado a la búsqueda de nuevos agentes terapéuticos en gran medida por una mejor comprensión de la estructura de las enzimas y otras biomoléculas asociadas con enfermedades. Una clase importante de enzimas que ha sido el objeto de un estudio profundo es la proteína quinasas.
La proteína quinasas constituyen una gran familia de enzimas relacionadas estructuralmente que son responsables del control de una diversidad de procedimientos de transducción de señales dentro de la célula (véase Hardie, G y Hanks, S. The Protein Kinase Facts Book, I y II, Academic Press, San Diego, CA: 1995). Se cree que la proteína quinasas ha evolucionado desde un gen ancestral común debido a la conservación de su estructura y función catalítica. Casi todas las quinasas contienen un dominio catalítico similar de 250-300 aminoácidos. Las quinasas pueden clasificarse en familias por los sustratos que fosforilan (por ejemplo, proteína-tirosina, proteínaserina/treonina, lípidos, etc.). Se han identificado motivos de secuencia que corresponden, en general, a cada una de estas familias de quinasas (véase, por ejemplo, Hanks, S.K., Hunter, T., FASEB J. 1995, 9, 576-596; Knighton y col., Science 1991, 253, 407-414; Hiles y col, Cell 1992, 70, 419-429; Kunz y col, Cell 1993, 73, 585-596; Garcia-Bustos y col, EMBO J 1994, 13, 2352-2361).
En general, la proteína quinasas media la señalización intracelular realizando una transferencia de fosforilo desde un nucleósido trifosfato a un aceptor de proteínas que está implicado en una ruta de señalización. Estos acontecimientos de fosforilación actúan como interruptores moleculares de activación/desactivación que pueden modular o regular la función biológica de la proteína diana. Estos acontecimientos de fosforilación finalmente se inducen en respuesta a una diversidad de estímulos extracelulares y otros estímulos. Los ejemplos de dichos estímulos incluyen señales de estrés ambientales y químicas (por ejemplo, choque, choque térmico, radiación ultravioleta, endotoxinas bacterianas y H2O2), citocinas (por ejemplo, interleucina-1 (IL-1) y factor de necrosis tumoral alfa (TNF-a) y factores de crecimiento (por ejemplo, factor estimulador de colonias de granulocitos y macrófagos (GM-CSF), y factor de crecimiento de fibroblastos (FGF)). Un estímulo extracelular puede afectar a una o más respuestas celulares relacionadas con el crecimiento celular, migración, diferenciación, secreción de hormonas, activación de factores de transcripción, contracción muscular, metabolismo de glucosa, control de la síntesis de proteínas, supervivencia y regulación del ciclo celular.
Muchas enfermedades están asociadas con respuestas celulares anómalas inducidas por acontecimientos mediados por proteína quinasas como se ha descrito anteriormente. Esas enfermedades incluyen, pero sin limitación, cáncer, enfermedades autoinmunes, enfermedades inflamatorias, enfermedades óseas, enfermedades metabólicas, enfermedades neurológicas y neurodegenerativas, enfermedades cardiovasculares, alergias y asma, enfermedad de Alzheimer y enfermedades relacionadas con hormonas. Por consiguiente, ha habido un esfuerzo sustancial en la química médica para encontrar inhibidores de proteína quinasas que sean eficaces como agentes terapéuticos.
Las quinasas tipo Polo (PLK) pertenecen a una familia de serina/treonina quinasas que están muy conservadas entre las especies, que varían desde levaduras al ser humano (revisado en Lowery DM y col., Oncogene 2005, 24; 248-259). Las quinasas PLK tienen múltiples papeles en el ciclo celular, incluyendo control de la entrada y la progresión a través de la mitosis.
La PLK1 es la mejor caracterizada de los miembros de la familia PLK. PLK1 se expresa ampliamente y es la más abundante en tejidos con un alto índice mitótico. Los niveles de proteína PLK-1 se elevan y alcanzan un valor máximo en la mitosis (Hamanaka, R y col., J Biol Chem 1995, 270, 21086-21091). Todos los sustratos presentados de PLK1 son moléculas que se sabe que regulan la entrada y la progresión a través de la mitosis, e incluyen CDC25C, ciclina B, p53, APC, BRCA2 y el proteosoma. PLK1 está regulada positivamente en múltiples tipos de cáncer y los niveles de expresión se correlacionan con la gravedad de la enfermedad (Macmillan, JC y col., Ann Surg Oncol 2001, 8, 729-740). PLK1 es un oncogén y puede transformar células NIH-3T3 (Smith, MR y col., Biochem Biophys Res Commun 1997, 234, 397-405). La reducción o inhibición de PLK1 por ARNip, antisentido, microinyección de anticuerpos o transfección de una construcción dominante negativa de PLK1 en las células, reduce la proliferación y viabilidad de las células tumorales in vitro (Guan, R y col., Cancer Res 2005, 65, 2698-2704; Liu, X y col., Proc Natl Acad Sci U S A 2003, 100, 5789-5794, Fan, Y y col., World J Gastroenterol 2005, 11, 45964599; Lane, HA y col., J Cell Biol 1996, 135, 1701-1713). Las células tumorales en las que se ha reducido el nivel de
40
45
PLK1 tienen activados puntos de control del huso mitótico y defectos en la formación del huso mitótico, en el alineamiento de cromosomas y en la separación y citocinesis. Se ha notificado que la pérdida de viabilidad es el resultado de una inducción de apoptosis. Por el contrario, se ha notificado que las células normales mantienen la viabilidad tras la reducción de PLK1. La reducción de la expresión (knock down) in vivo de PLK1 por ARNip o el uso de construcciones dominantes negativas conduce a una inhibición del crecimiento o regresión de tumores en modelos de xenoinjerto.
PLK2 se expresa principalmente durante la fase G1 del ciclo celular y se localiza en el centrosoma en células en interfase. Los ratones knockout para PLK2 se desarrollan normalmente, son fértiles y tienen tasas de supervivencia normales, pero son aproximadamente un 20% más pequeños que los ratones de tipo silvestre. Las células de animales knockout progresan a través del ciclo celular más lentamente que en ratones normales (Ma, S y col., Mol Cell Biol 2003, 23, 6936-6943). La reducción de PLK2 por ARNip o introducción por transfección de mutantes con quinasa inactiva en las células bloquea la duplicación del centríolo. La regulación negativa de PLK2 también sensibiliza a las células tumorales al taxol y promueve la catástrofe mitótica, en parte por supresión de la respuesta de p53 (Burns TF y col., Mol Cell Biol 2003, 23, 5556-5571).
PLK3 se expresa a largo de todo el ciclo celular y aumenta desde la fase G1 a la mitosis. La expresión está regulada positivamente en tumores de ovario de alta proliferación y cáncer de mama y está asociada con un mal pronóstico (Weichert, W y col., Br J Cancer 2004, 90, 815-821; Weichert, W y col., Virchows Arch 2005, 446, 442-450). Además de la regulación de la mitosis, se cree que PLK3 está implicada en la fragmentación del aparato de Golgi durante el ciclo celular y en la respuesta a las lesiones del ADN. Se ha notificado que la inhibición de PLK3 por expresión dominante negativa promueve la apoptosis independiente de p53 después de las lesiones del ADN y reprime la formación de colonias por las células tumorales (Li, Z y col., J Biol Chem 2005, 280, 16843-16850).
PLK4 es estructuralmente más distinta de los otros miembros de la familia PLK. La reducción de esta quinasa produce apoptosis en células cancerosas (Li, J y col., Neoplasia 2005, 7, 312-323). Los ratones knockout para PLK4 se detienen en E7.5 con una alta fracción de células en mitosis y cromosomas segregados parcialmente (Hudson, JW y col., Current Biology 2001, 11, 491-946).
Se han implicado moléculas de la familia de proteína quinasas en el crecimiento, proliferación y supervivencia de células tumorales. Por consiguiente, existe una gran necesidad de desarrollar compuestos útiles como inhibidores de proteína quinasas. Las pruebas que implican a las quinasas PLK como esenciales para la división celular son firmes. El bloqueo del ciclo celular es un enfoque validado clínicamente para inhibir la proliferación y viabilidad de las células tumorales. Por lo tanto, sería deseable... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de fórmula I:
**(Ver fórmula)**
o una sal farmacéuticamente aceptable del mismo; en la que:
X1 es un enlace, O, NR8, S, SO o SO2; X2 es N o CH; R1 es H, alifático C1-10, cicloalifático C3-10, arilo C6-10, heteroarilo de 5 a 10 miembros o heterociclilo de 3 a 10 miembros; en la que dicho R1 está opcionalmente sustituido con 0-5 J1; cada R2 y R3 es independientemente H, alifático C1-10 o cicloalifático C3-10; en la que cada R2 y R3 está sustituido opcional e independientemente con 0-5 J2 y J3 respectivamente; y R2 y R3, junto con el átomo de carbono al que están unidos, forman un anillo monocíclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroátomos seleccionados cada uno de ellos independientemente entre O, N, y S; dicho anillo monocíclico formado por R2 y R3 está opcionalmente sustituido con 0-4 J23;
R4
es H, C(O)R, C(O)OR o C(O)NRR', alifático C1-10, cicloalifático C3-10, arilo C6-10, heteroarilo de 5 a 10 miembros, heterociclilo de 3 a 10 miembros, -(alifático C1-6)-(cicloalifático C3-10), -(alifático C1-6)-(arilo C6-10) o (alifático C1-6)-(heteroarilo de 5 a 10 miembros); y R4 está opcionalmente sustituido con 0-5 J4; o R2 y R4, junto con los átomos de carbono a los que están unidos, forman un anillo monocíclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroátomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monocíclico formado por R2 y R4 está opcionalmente sustituido con 0-4 J24; R5 es H, CO2R, CH2OR, CONR2, CN, F o CF3; L es un enlace o -C(R6) (R7)-; cada R6 y R7 es independientemente H, alifático C1-10 o cicloalifático C3-10; en el que cada R6 y R7 está sustituido opcional e independientemente con 0-5 J6 y J7 respectivamente; o R6 y R7, junto con el átomo de carbono al que están unidos, forman un anillo monocíclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroátomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monocíclico formado por R6 y R7 está opcionalmente sustituido con0-4 J67 ;o R2 y R6, junto con el átomo de carbono al que están unidos, forman un anillo monocíclico saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroátomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monocíclico formado por R2 y R6 está opcionalmente sustituido con0-4 J26 ;o R4 y R6, junto con el átomo de carbono al que están unidos, forman un anillo saturado o parcialmente insaturado de 3 a 8 miembros que contiene 0-4 heteroátomos seleccionados cada uno de ellos independientemente entre O, N y S; dicho anillo monocíclico formado por R4 y R6 está opcionalmente sustituido con 0-4 J46; R8 es H, alifático C1-6, cicloalifático C3-8, C(O)R, C(O)OR o C(O)NRR' ; o cada J1 es independientemente haloalquilo C1-6, halo, NO2, CN, Q o -Z-Q; o dos J1 tomados juntos pueden formar opcionalmente =O; Z es alifático C1-6 opcionalmente reemplazado con 0-3 apariciones de -NR-, -O-, -S-, -C(O)-, -C(=NR)-, C(=NOR)-, -SO-o -SO2-; cada Z está opcionalmente sustituido con 0-2 Jz; Q es H; alifático C1-6; un anillo monocíclico aromático o no aromático de 3 a 8 miembros que tiene 0-3 heteroátomos seleccionados independientemente entre O, N y S; o un sistema de anillos bicíclico aromático o no aromático de 8-12 miembros, teniendo cada uno 0-5 heteroátomos seleccionados independientemente entre O, N y S; cada Q está opcionalmente sustituido con 0-5 JQ; cada J2, J3, J6 y J7 es independientemente alifático C1-6, cicloalifático C3-6 o -(alquil C1-4)n-V1; en el que n es 0 ó 1; V1 es halo (alifático C1-4), -O(haloalifático C1-4), halo, NO2, CN, OH, OR", SH, SR", NH2, NHR", N(R")2, COH, COR", CO2H, CO2R", CONH2, CONHR", CONR"2, OCOR", OCONH2, OCONHR", OCON(R")2, NHCOR", NR"COR", NHCO2R", NR"CO2R", NHCO2H, NR"CO2H, NHCONH2, NHCONHR", NHCON(R")2, SO2NH2, SO2NHR" SO2N(R")2, NHSO2R" o NR"SO2R"; o V1 es un grupo cíclico seleccionado entre cicloalifático C3-6, fenilo, heteroarilo de 5 a 6 miembros o heterociclilo de 3 a 6 miembros; en el que dicho grupo cíclico está opcionalmente sustituido con 0-3 JV; R" es alifático C1-4 sin
40
sustituir; o dos de J2, J3, J6 y J7 iguales, unidos al mismo átomo, juntos pueden formar opcionalmente =O; cada Jz y Jv es independientemente halo, alifático C1-6, cicloalifático C3-6, NO2, CN, -NH2, -NH(alifático C1-4), N(alifático C1-4)2, -OH, -O(alifático C1-4), -CO2H, -CO2(alifático C1-4), -O(haloalifático C1-4) o halo(alifático C1-4); cada JQ, J4, J23, J24, J67, J26 y J46 es independientemente M o -Y-M; cada Y es independientemente un alifático C1-6 opcionalmente reemplazado con 0-3 apariciones de -NR-, -O-, S-, -C(O)-, -SO-o -SO2-; cada M es independientemente H, alifático C1-6, cicloalifático C3-6, halo(alifático C1-4), -O(haloalifático C1-4), heterociclilo de 3 a 6-miembros, halo, NO2, CN, OH, OR', SH, SR', NH2, NHR', N(R')2, COH, COR', CO2H, CO2R', CONH2, CONHR', CONR'2, OCOR', OCONH2, OCONHR', OCON (R')2, NHCOR', NR'COR', R NHCO2R', NR' CO2R', NHCO2H, NR'CO2H, NHCONH2, NHCONHR', NHCON(R')2, SO2NH2, SO2NHR', SO2N(R')2, NHSO2R' o NR'SO2R'; es H o alifático C1-6 sin sustituir; y R' es alifático C1-6 sin sustituir; o dos grupos R', junto con junto con el átomo de carbono al que están unidos, forman un anillo monocíclico saturado o parcialmente insaturado de 3 a 8 miembros que tiene 0-1 cada uno seleccionado independientemente entre O, N y S.
2. El compuesto de la reivindicación 1, en el que X1 es O, NR8, o S.
3. El compuesto de la reivindicación 1, en el que X1 es NR8.
4. El compuesto una cualquiera de las reivindicaciones 1-3, en el que X2 es N.
5. El compuesto de una cualquiera de las reivindicaciones 1-4, en el que R1 es arilo C6-10 opcionalmente sustituido arilo o heteroarilo opcionalmente sustituido de 5 a 10 miembros.
6. El compuesto de la reivindicación 5, en el que cada R1 es arilo C6-10 opcionalmente sustituido.
7. El compuesto de una cualquiera de las reivindicaciones 1-6, en el que R4 es cicloalifático C3-10.
8. El compuesto de las reivindicaciones 1-7, en el que R5 es H o CO2R.
9. El compuesto de una cualquiera de las reivindicaciones 1-8, en el que uno de R2 y R3 es H y el otro es alifático C16 opcionalmente sustituido o cicloalifático C3-8 opcionalmente sustituido.
10. El compuesto de una cualquiera de las reivindicaciones 1-9, en el que R8 es H.
11. El compuesto de la reivindicación 1, en el que:
L es un enlace; X2 es N; R1 es arilo C6-10 opcionalmente sustituido o heteroarilo opcionalmente sustituido de 5-10 miembros; y cada R2 y R3 es independientemente H, alifático C1-10 o ciclcoalifático C3-10; en los que cada R2 y R3 está opcionalmente sustituido con 0-5 J2 y J3 respectivamente; o R2 y R3, junto con el átomo de carbono al que están unidos, pueden formar un anillo monocíclico saturado o parcialmente insaturado de 3 a 6 miembros.
12. El compuesto de acuerdo con una cualquiera de las reivindicaciones 1-11, en el que:
cada J2 y J3 es independientemente alifático C1-6, cicloalifático C3-6 o -(alquil C1-4)n-V1; en el que n es 0 ó 1; V1 es halo (alifático C1-4), -O(haloalifático C1-4), halo, NO2, CN, OH, OR", SH, SR", NH2, NHR", N(R")2, COH, COR", CO2H, CO2R", CONH2, CONHR", CONR"2, OCOR", OCONH2, OCONHR", OCON(R")2, NHCOR", NR"COR", NHCO2R", NR"CO2R", NHCO2H, NR"CO2H, NHCONH2, NHCONHR", NHCON(R")2, SO2NH2, SO2NHR", SO2N(R")2, NHSO2R", o NR"SO2R"; R" es alifático C1-4 sin sustituir;
o dos de J3, J4, J5 o J6 iguales, unidos al mismo átomo, pueden formar juntos opcionalmente =O.
13. El compuesto de acuerdo con la reivindicación 1 seleccionado entre los siguientes: o una de sus sales farmacéuticamente aceptable.
**(Ver fórmula)**
14. Una composición que comprende un compuesto de una cualquiera de las reivindicaciones 1-13 y un transportador, adyuvante o vehículo farmacéuticamente aceptable.
15. El uso de un compuesto de una cualquiera de las reivindicaciones 1-13 en la fabricación de un medicamento para inhibir la actividad proteína quinasa en un paciente.
5 16. Un procedimiento para inhibir la actividad proteína quinasa en una muestra biológica in vitro, que comprende poner en contacto dicha muestra biológica con un compuesto de una cualquiera de las reivindicaciones 1-13.
17. El uso de la reivindicación 15 o el procedimiento de la reivindicación 16, en el que dicha proteína quinasa es PLK1.
18. El uso de un compuesto de una cualquiera de las reivindicaciones 1-13 en la fabricación de un medicamento
10 para tratar un trastorno proliferativo, un trastorno neurodegenerativo, un trastorno autoinmune, un trastorno inflamatorio o un trastorno mediado inmunológicamente en un paciente.
19. El uso de un compuesto de una cualquiera de las reivindicaciones 1-13 en la fabricación de un medicamento para tratar melanoma, mieloma, leucemia, linfoma, neuroblastoma o un cáncer seleccionado de cáncer de colon, mama, gástrico, ovárico, cervical, pulmonar, del sistema nervioso central (SNC), renal, de próstata, de vejiga o pancreático, en un paciente que lo necesita.
20. El uso de un compuesto de una cualquiera de las reivindicaciones 1-13 en la fabricación de un medicamento para tratar cáncer en un paciente que lo necesita.
Patentes similares o relacionadas:
Pteridinas como inhibidores del FGFR, del 26 de Junio de 2019, de Astex Therapeutics Ltd: Un compuesto de fórmula (I) :**Fórmula** que incluye cualquier forma tautomérica o estereoquímicamente isomérica del mismo, en el que W es -N(R3)-; cada […]
Compuestos como moduladores de ror gamma, del 12 de Junio de 2019, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I) **Fórmula** en la que: R1 es: -CN; -S(O)nR6; -S(O)nNR7R8; -S(O)(NR9)R 6; -N(R9)C(O)R6; -N(R9)C(O)OR6; […]
Métodos para preparar derivados de pirimidina útiles como inhibidores de proteína quinasa, del 10 de Febrero de 2016, de VERTEX PHARMACEUTICALS INCORPORATED: Un método de preparación de un compuesto representado por la Fórmula Estructural (I), o una sal farmacéuticamente aceptable del mismo: en la que: […]
Productos intermedios para preparar derivados condensados de piperazin-2-ona, del 1 de Julio de 2015, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Compuestos de fórmula (III) general I**Fórmula** en la cual R1 significa un radical seleccionado del grupo compuesto por cloro, R2 significa hidrógeno, R3 […]
Proceso para preparar dihidropteridinonas y productos intermedios de las mismas, del 20 de Agosto de 2014, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Proceso para preparar un compuesto de fórmula donde R5 representa alquilo C1-C6, alquil-C1-C4-cicloalquilo C3-C10 o cicloalquilo C3-C10, R4 representa […]
Procedimiento para preparar derivados condensados de piperazin-2-ona, así como productos intermedios del procedimiento, del 19 de Septiembre de 2012, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Procedimiento para preparar compuestos de fórmula general I en la cual R1 significa un radical seleccionado del grupo compuesto por cloro, fluoro, bromo, metansulfonilo, […]
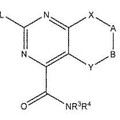 Compuestos de heteroarilo, sus composiciones y uso de los mismos como inhibidores de proteína quinasa, del 14 de Marzo de 2012, de SIGNAL PHARMACEUTICALS LLC: Un compuesto que tiene la siguiente fórmula:
y sus sales farmacéuticamente aceptables, donde:
R1 es alquiloC1-8 sustituido o no sustituido, arilo s ustituido o no sustituido, […]
Compuestos de heteroarilo, sus composiciones y uso de los mismos como inhibidores de proteína quinasa, del 14 de Marzo de 2012, de SIGNAL PHARMACEUTICALS LLC: Un compuesto que tiene la siguiente fórmula:
y sus sales farmacéuticamente aceptables, donde:
R1 es alquiloC1-8 sustituido o no sustituido, arilo s ustituido o no sustituido, […]
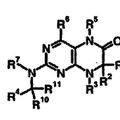 NUEVAS 2-BENCILAMINODIHIDROPTERIDINONAS, PROCEDIMIENTO PARA SU OBTENCION Y SU EMPLEO COMO MEDICAMENTOS, del 1 de Mayo de 2008, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH
BOEHRINGER INGELHEIM PHARMA GMBH & CO.KG: 13) Empleo de un compuesto de fórmula (I) para la obtención de un medicamento para el tratamiento y/o prevención de enfermedades tumorales que se deben a la superexpresión […]
NUEVAS 2-BENCILAMINODIHIDROPTERIDINONAS, PROCEDIMIENTO PARA SU OBTENCION Y SU EMPLEO COMO MEDICAMENTOS, del 1 de Mayo de 2008, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH
BOEHRINGER INGELHEIM PHARMA GMBH & CO.KG: 13) Empleo de un compuesto de fórmula (I) para la obtención de un medicamento para el tratamiento y/o prevención de enfermedades tumorales que se deben a la superexpresión […]