Uso de lacasas para la separación electrolítica del agua.
El uso de lacasas para la separación electrolítica de agua o para la generación electrocatalítica de oxígeno a partir de agua,
un electrodo enzimático para tal aplicación, un método para la generación electrolítica de oxígeno a partir de agua, y una celda electrolítica y un aparato para la separación de agua, conteniendo el electrodo enzimático de la invención.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201430538.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Inventor/es: ALCALDE GALEOTE,MIGUEL, PITA MARTINEZ,MARCOS, LOPEZ DE LACEY,ANTONIO, MATE MATE,Diana, GONZÁLEZ PÉREZ,David, SHELEEV,Sergey.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N9/02 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Oxidorreductasas (1.), p. ej. luciferasa.
- C25B1/04 C […] › C25 PROCESOS ELECTROLITICOS O ELECTROFORETICOS; SUS APARATOS. › C25B PROCESOS ELECTROLITICOS O ELECTROFORETICOS PARA LA PRODUCCION DE COMPUESTOS ORGANICOS O INORGANICOS, O DE NO METALES; SUS APARATOS (protección anódica o catódica C23F 13/00; crecimiento de monocristales C30B). › C25B 1/00 Producción electrolítica de compuestos inorgánicos o no metales. › por electrólisis del agua.
- C25B11/06
PDF original: ES-2550877_A1.pdf

Fragmento de la descripción:
Uso de Lacasas para la separación electrolítica del agua Estado de la técnica
La electrólisis del agua para la generación de oxígeno e hidrógeno
La electrólisis del agua es la descomposición del agua (H20) en oxígeno 02 y gas hidrógeno H2 gracias a una corriente eléctrica que pasa a través del agua. Es una ruta muy accesible para sintetizar 02 y H2.
Para separar el agua en sus componentes elementales 02 y H2, se conecta una fuente eléctrica a dos electrodos o placas que se sitúan dentro del agua. El H2 se genera en el cátodo (reducción a H2 molecular) y el oxígeno se genera en el ánodo (oxidación a oxígeno molecular). La principal dificultad para acometer la electrólisis del agua es encontrar catalizadores apropiados para llevar a cabo ambas reacciones redox a una alta velocidad y a bajos sobrepotenciales aplicados.
La descomposición del agua pura en hidrógeno y oxígeno a temperatura y presión estándares no es favorable en términos termodinámicos. De este modo, la electrólisis del agua requiere un exceso de energía en la forma de sobrepotencial para superar varias barreras de activación. Sin el exceso de energía la electrólisis del agua sucede muy despacio, o no sucede. Ésto se debe en parte a la limitada auto-ionización del agua. La conductividad eléctrica del agua pura es mucho menor que, por ejemplo, el agua de mar, debido a su alto contenido en electrolitos. La eficiencia de la electrólisis del agua puede, entonces, incrementarse por la adición de un electrolito (tales como una sal soluble, un ácido o una base) y su uso en electrocatálisis. Actualmente el proceso electrolítico prácticamente no se usa en aplicaciones industriales ya que el hidrógeno puede producirse de manera más económica desde combustibles fósiles.
La electrólisis del agua en condiciones estándar requiere un mínimo teórico de 237 kJ de energía eléctrica aplicada para disociar un mol de agua, que es la energía libre de Gibbs estándar para la formación del agua. En muchas ocasiones, aunque de modo incorrecto, la entalpia estándar de formación del agua líquida se usa como referencia (286 kJ/mol), o posiblemente la del agua vapor (242 kJ/mol). Éstos también se indican habitualmente como los valores de caloríficos superior (Higher Heating Valué, HHV) e inferior (Lower Heating Valué, LHV) del hidrógeno.
Ya que cada mol de agua necesita dos moles de electrones, y dado que la constante de Faraday, F, representa la carga de un mol de electrones (96485 C/mol), se deduce que el
potencial mínimo para la electrólisis es aproximadamente 1,23 V [Werner Zittel; Reinhold Wurster (1996-07-08) "Chapter 3: Production of Hydrogen. Part 4: Production from electricity by means of electmlysis]. Si se usa el HHV como referencia, el potencial obtenido es 1,48 eV, el potencial termoneutral.
En el caso de la electrólisis del agua, la energía libre de Gibbs representa el trabajo mínimo necesario para que suceda la reacción, y la entalpía de reacción es la cantidad de energía (trabajo y calor juntas) que tiene que suministrarse de modo que los productos de reacción están a la misma temperatura que los reactivos (por ejemplo, la temperatura estándar para los valores dados anteriormente). Esto implica que un electrolizador ideal, 100% eficiente produciría hidrógeno y oxígeno a temperatura más baja que el agua suministrada. Un electrolizador operando a 1,48 V únicamente presentaría una eficiencia del 83%, y produciría hidrógeno y oxígeno a la misma temperatura que el agua suministrada.
De esta manera, los electrolizadores de agua reales requieren potenciales mayores para que suceda la reacción. La parte que excede 1,23 V se llama sobrepotencial, y representa cualquier tipo de pérdida y condición no ideal del proceso electroquímico.
Para una celda bien diseñada el potencial mayor es el sobrepotencial de reacción para el proceso de oxidación de 4 electrones de agua a oxígeno en el ánodo; existen electrocatalizadores que pueden facilitar esta reacción, y las aleaciones de platino son el actual estado de la técnica para esta oxidación. El desarrollo de un electrocatalizador barato y eficaz para esta reacción sería un gran avance, y es un campo de investigación activo. La reacción de dos electrones para producir hidrógeno en el cátodo, que es más sencilla, puede ser electrocatalizada prácticamente sin sobrepotencial por un electrodo de platino, o en teoría con una enzima hidrogenasa. En el caso de emplear otros materiales, menos efectivos, para el cátodo (por ejemplo, grafito), aparecerán sobrepotenciales significativos.
Hasta la fecha, únicamente se ha utilizado un catalizador enzimático para la producción de O2 en la electrólisis del agua, en particular el Fotosistema II (Photosystem II, PSII), mientras que el electrodo de O2 tiene un efecto substancial en la actuación y durabilidad de los electrolizadores de agua, dada su cinética intrínsecamente lenta y su pobre durabilidad. Además, es posible enlazar el PSII a un electrodo y oxidar H2O a O2 con la ayuda de la luz solar, pero su tamaño, la falta de estabilidad y su complejidad hacen que la tarea sea inabordable. El sistema tiene al menos dos inconvenientes: las dificultades para inmovilizar el complejo enzimático sobre los electrodos y que la electrólisis del agua tiene que
acarrearse bajo la acción de la luz visible, la cual si falta priva al PSII de llevar a cabo su actividad [Kato, Metal., JACS(2013), 135, 10610-3],
Las hidrogenasas tolerantes al 02 son consideradas como bioelectrocatalizadores eficientes para la producción de H2 [Armstrong, FA et al., Chem. Soc. Rev. (2009), 38 (1), 36-51; Shafaat, HS etal., Biochim. Biophys. Acta (2013), 1827 (8-9), 986-1002].
Hasta la fecha, no se han descrito otros catalizadores enzimáticos para la electrólisis del agua.
Oxígeno: producción y usos
El oxígeno generalmente se produce industrialmente por destilación fraccionada de aire licuado, usando zeolitas con ciclos de presión para concentrar el oxígeno del aire, por electrólisis de agua y por otros medios. Los usos del oxígeno elemental incluyen la producción de acero, plásticos y materiales textiles, soldaduras, juntas, corte de aceros y otros metales, propulsores de cohetes, terapia de oxígeno, y sistemas de soporte vital en aeronaves, submarinos, vuelos espaciales y buceo.
La toma de oxígeno del aire es el propósito esencial de la respiración, por lo que la suplementación con oxígeno se utiliza en medicina. La terapia con oxígeno se usa para tratar varias enfermedades y condiciones como el enfisema, neumonía, algunos desórdenes cardíacos (fallo cardíaco congestivo), algunos desórdenes que causan un incremento en la presión arterial pulmonar, y cualquier enfermedad que limita la capacidad del cuerpo para tomar y usar oxígeno gaseoso. Otros usos son: el tratamiento de agua; trajes espaciales; suplementos de oxígeno adicionales para gente que escala montañas o vuela en aviones no presurizados de ala fija; suplementos de emergencia de oxígeno en aviones comerciales presurizados para los casos de despresurización de la cabina; usos industriales como el corte y soldadura de metales y la transformación del hierro en acero; en industria química para, por ejemplo, hacer reaccionar el etileno para crear el óxido de etileno, que, posteriormente, se puede convertir en etilenglicol, usado en, por ejemplo, la fabricación de anticongelantes y polímeros como el poliéster (precursor de muchos plásticos y tejidos).
Hidrógeno
Actualmente sólo el 5% del gas hidrógeno producido en el mundo se genera por electrólisis del agua. El hidrógeno se obtiene fundamentalmente de recursos fósiles (como el metano), pero estos recursos no son sostenibles. La mayoría del hidrógeno se usa cercano al sitio donde se produce, siendo los dos usos mayoritarios el procesado de combustibles fósiles (craqueo de petróleo en presencia de hidrógeno, hidrocraqueo) y la producción de amoníaco, sobre todo para el mercado de fertilizantes.
Lacasas
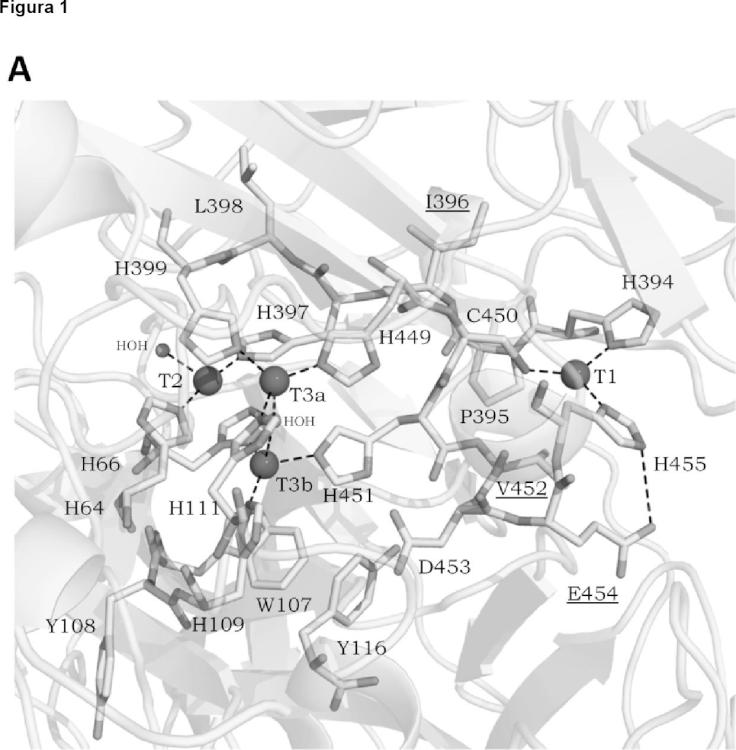
Las lacasas son enzimas oxidasas que contienen cobre y se encuentran en muchas plantas, hongos, microorganismos e insectos. Las oxidasas multicobre azules se componen de un centro activo poblado por cuatro cationes de cobre que catalizan la oxidación de muchos compuestos orgánicos e inorgánicos, tales como orto- y paradifenoles, aminofenoles, polifenoles, poliaminas, ligninas y arildiaminas usando 02 como el único aceptar de electrones, generalmente a valores ácidos de pH [Morozova, OV et al., Biochemistry (2007), 72 (10), 1136-50\. El mecanismo general de la lacasa incluye la oxidación de un substrato reductor en el sitio de cobre T1 con la consecuente reducción de 02 a agua en el cluster trinuclear de cobre... [Seguir leyendo]
Reivindicaciones:
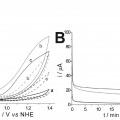
1. Uso de una lacasa para catalizar la generación electrocatalítica de 02 molecular a partir de agua.
2. Uso de una lacasa de acuerdo a la reivindicación 1, donde la lacasa se inmoviliza en el ánodo.
3. Uso de una lacasa de acuerdo con la reivindicación 2, donde la lacasa está unida covalentemente al ánodo, adsorbida sobre el ánodo, inmovilizada electrostáticamente sobre el ánodo, unida por medio de quelatos al ánodo, unida por monocapas autoensambladas, inmovilizada sobre el ánodo por diazotación, inmovilizada sobre el ánodo por procesos de click-chemistry, unida por avidina-biotina, mediante la formación de enlaces maleimida, mediante la formación de un recubrimiento sobre el ánodo, secada sobre el ánodo, inclusa en un liposoma que se inmoviliza sobre el ánodo, o por medio de un polímero y/o un agente de entrecruzamiento.
4. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 3, donde la lacasa se une covalentemente al ánodo.
5. Uso de una lacasa de acuerdo con la reivindicación 4, donde el electrodo incluye grafito de baja densidad modificado con grupos aminoarilo.
6. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 2 a la 5, donde la lacasa está provista de residuos aldehido sobre su superficie antes de la inmovilización sobre el ánodo.
7. Uso de una lacasa de acuerdo a cualquiera de las reivindicaciones de la 1 a la 6, donde la lacasa es una lacasa fúngica.
8. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 7, donde la lacasa tiene un potencial para el sitio T1 entre 730 y 780 mV.
9. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 8, donde la lacasa es resistente a aniones.
10. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 2 a la 9, donde el cluster T2/T3 de la lacasa inmovilizada está orientado hacia el electrodo.
11. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 10,
donde la lacasa comprende:
a) la secuencia SEQ ID NO 1; o
b) una vanante de la secuencia de a) que tiene al menos un 70% de identidad de secuencia a la SEQ ID NO 1, basándose en la identidad de la totalidad de los aminoácidos de dicha secuencia.
12. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 11, donde la lacasa comprende la secuencia SEQ ID NO 1.
13. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 10, donde la lacasa comprende:
a) la SEQ ID NO 2; o
b) una variante de la secuencia de a) que tiene al menos un 70% de identidad de secuencia con la SEQ ID NO 2, basándose en la identidad de la totalidad de los aminoácidos de dicha secuencia.
14. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 10 y la 13, donde la lacasa comprende la secuencia SEQ ID NO 2.
15. Uso de una lacasa de acuerdo con cualquiera de las reivindicaciones de la 1 a la 10, donde la lacasa comprende:
a) cualquiera de las secuencias SEQ ID NO 3, SEQ ID NO 4, SEQ ID NO 5, SEQ ID NO 6, SEQ ID NO 7, SEQ ID NO 8, SEQ ID NO 9, SEQ ID NO 10, SEQ ID NO 11, SEQ ID NO 12, SEQ ID NO 13, SEQ ID NO 14, SEQ ID NO 15, SEQ ID NO 16, SEQ ID NO 17; o
b) una variante de cualquiera de las secuencias de la SEQ ID NO 3 a la SEQ ID NO 17 de a), que tiene al menos un 70% de identidad de secuencia con la SEQ ID NO 3 a la SEQ ID NO 17, basándose en la identidad de la totalidad de los aminoácidos de dicha secuencia.
16. Un electrodo enzimático adecuado para la generación electrolítica de oxígeno molecular O2 a partir de agua, caracterizado por comprender un soporte electroconductor y, al menos, una enzima inmovilizada, seleccionada de la familia de enzimas de las lacasas, tal y como se define en cualquiera de las reivindicaciones de la 5 a la 7 y de la 9 a la 13.
17. Un electrodo de acuerdo con la reivindicación 16, donde la lacasa está unida
covalentemente al electrodo, adsorbida sobre el electrodo, inmovilizada electrostáticamente sobre el electrodo, unida por medio de quelatos al electrodo, unida por monocapas autoensambladas, inmovilizada sobre el electrodo por diazotación, inmovilizada sobre el electrodo por procesos de click-chemistry, unida por avidina-biotina, unida mediante la formación de enlaces maleimida, formando un recubrimiento sobre el electrodo, secada sobre el electrodo, inclusa en un liposoma que se inmoviliza sobre el ánodo, o por medio de un polímero y/o un agente de entrecruzamiento.
18. Un electrodo de acuerdo con las reivindicaciones 16 y 17, donde la lacasa está unida covalentemente al miembro soporte electroconductor.
19. Un electrodo de acuerdo con las reivindicaciones de la 16 a la 18, donde el electrodo incluye grafito de baja densidad con grupos aminoarilo.
20. Un electrodo de acuerdo con cualquiera de las reivindicaciones de la 16 a la 19, el cual contiene al menos un catalizador adicional, seleccionado del fotosistema II inmovilizado, peroxidasas, superoxidasas, microperoxidasas, catalasa, oxidasas, complejos organometálicos, de rutenio, cobalto, y/o hierro, y partículas metálicas tales como platino, oro o paladio.
21. Un método para la generación electrolítica de oxígeno a partir de agua, que comprenda un paso en el que se ponga el agua en contacto con el cátodo y el ánodo, donde una enzima, seleccionada de la familia de enzimas de las lacasas, se inmoviliza sobre el ánodo tal y como se define en cualquiera de las reivindicaciones 3 a la 6.
22. Un método de acuerdo con la reivindicación 21, donde la lacasa se une covalentemente al ánodo.
23. Una celda electrolítica que comprenda:
- un contenedor para contener o recibir agua, y
- al menos un electrodo tal y como se definen en cualquiera de las reivindicaciones de la 16 a la 20.
24. Una celda electrolítica de acuerdo con la reivindicación 23, donde se aplica un potencial eléctrico entre +1,23 V y +1,45 V.
25. Un aparato para la separación electrocatalítica del agua, donde el aparato contenga:
- una o una pluralidad de celdas tal y como se define en cualquiera de las reivindicaciones 23 y 24.
Patentes similares o relacionadas:
Métodos para controlar la producción de proteasas, del 1 de Julio de 2020, de ROAL OY: Una célula hospedadora que comprende al menos un gen cromosómico inactivado en donde el gen cromosómico inactivado comprende una secuencia de ácido nucleico que codifica un […]
Productos y métodos para el tratamiento de la esclerosis lateral amiotrófica, del 27 de Mayo de 2020, de The Research Institute at Nationwide Children's Hospital: Un virus recombinante adenoasociado que comprende el ADN que codifica el ARNhc de la dismutasa de superóxido 1 (SOD1) CATGGATTCCATGTTCATGA (SEQ ID NO: […]
Reconocimiento de unión a diana celular mediante un agente bioactivo usando transferencia de energía de resonancia de bioluminiscencia intracelular, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un sistema de ensayo que comprende: (a) una biblioteca de agentes bioactivos, cada uno de los cuales está fijado a un fluoróforo; (b) una diana celular fusionada a […]
Luciferasas de Oplophorus sintéticas con mayor emisión de luz, del 15 de Abril de 2020, de PROMEGA CORPORATION: Método que comprende: (a) expresar un polipéptido de luciferasa en una célula, en el que el polipéptido de luciferasa es una luciferasa modificada […]
Métodos para ajustar los niveles de producción de carotenoides y composiciones en géneros de Rhodosporidium y Rhodotorula, del 15 de Abril de 2020, de TEMASEK LIFE SCIENCES LABORATORY LIMITED: Un método para ajustar el nivel de producción y la composición de carotenoides en un huésped fúngico que comprende: (a) manipular genéticamente […]
Péptido que muestra actividad que promueve la generación de melanina y uso del mismo, del 8 de Abril de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de la SEQ ID NO: 1.
Polipéptidos de fusión relacionados con omega-hidroxilasa con propiedades mejoradas, del 8 de Abril de 2020, de Genomatica, Inc: Una variante de polipéptido de fusión híbrida de CYP153A-reductasa que comprende al menos el 90 % de identidad de secuencia con SEQ ID NO: 38 y que tiene […]
Expresión de polipéptido químico con receptores de linfocitos variables en células inmunes y usos para tratar el cáncer, del 8 de Abril de 2020, de EMORY UNIVERSITY: Un vector recombinante que comprende un ácido nucleico que codifica un polipéptido quimérico que comprende una secuencia de direccionamiento de un dominio de receptor […]